BRD4抑制剂JQ1对膀胱癌细胞增殖与凋亡的作用及其机制研究
谭益帆,刘修恒,王 磊,杜 洋,陈志远,刘 洋,沈 浩,刁长会
(武汉大学人民医院泌尿外科,湖北武汉 430060)
膀胱癌是泌尿系常见的恶性肿瘤,2017年美国新发膀胱癌患者数达79 030例,占所有新发癌症患者的4.6%。因膀胱癌死亡患者达16 870例,占所有因癌症死亡患者的2.8%[1]。在我国,膀胱癌是最常见的泌尿系肿瘤,其发病率及死亡率虽然低于美国等发达国家,但近年来也呈上升趋势[2]。膀胱癌的病理学类型有很多种,主要包括尿路上皮癌、鳞状细胞癌、腺癌以及小细胞癌等,其中最为常见的为尿路上皮癌[3]。膀胱癌的发病机制目前仍然不明确,涉及的生物学过程非常复杂,包括众多基因突变、染色质重组、激酶信号通路的改变等[4]。膀胱癌给人们带来了巨大的经济负担,威胁到人类健康,因此不断加深膀胱癌发病机制的认识,并寻找一种行之有效治疗方式已成为当务之急。
布罗莫结构域(bromodomains,BRDs)是一组包含110个氨基酸的蛋白分子,通过其特殊结构可以识别组蛋白末端乙酰化的赖氨酸位点。到目前为止已报道的溴结构域蛋白有61种,根据结构及功能的特点划分为8大BRD蛋白家族,溴结构域和超末端结构(bromodomain and extraterminal domain,BET)家族作为BRD家族中一员包含BRD2、BRD3、BRD4及BRDT蛋白[5]。BD1和BD2是BET蛋白家族氮末端都包含的2种保守的溴结构域,正是BD1和BD2这2种结构域起着识别并结合组蛋白尾部赖氨酸的作用[6]。溴化结构蛋白4(bromodomain-containing protein 4,BRD4)通过与组蛋白末端乙酰化赖氨酸结合可以促使染色质重塑因子和转录因子等相关蛋白富集于特定的基因转录位点,改变RNA聚合酶Ⅱ的活性,调控基因的表达,参与一系列重要生物活动过程,如细胞生长、细胞周期、炎症等[7-9]。BET蛋白家族的致癌功能首次在睾丸核蛋白中线癌中证实,通过染色质移位使BRD4基因突变,BRD4与睾丸核蛋白结合形成致癌蛋白,导致恶性睾丸核蛋白中线癌的发生[10]。随后很多的研究证实,BRD4在肝癌、乳腺癌、肺癌、及结直肠癌等肿瘤组织及癌细胞中高表达,而癌旁正常组织中低表达,并且BRD4通过抑制促凋亡基因BIM的表达及促进下游癌基因C-MYC的表达,促进肿瘤的发生和发展[11-14]。
到目前为止多种BET蛋白家族小分子抑制剂已被报道,包括JQ1与I-BET762等。与所有的BET抑制剂一样,JQ1可以竞争性地与BRD4溴结构域相结合,使BRD4蛋白从染色质的乙酰化赖氨酸上置换下来,从而干扰BRD4在机体中发挥生物学作用[15-16]。在与多种癌症细胞的研究中表明,JQ1都能有效抑制BET溴结构域,从而产生显著的抗癌作用[17]。众多文献证实JQ1在治疗膀胱癌具有广阔的应用前景。本文旨在探讨JQ1对膀胱癌细胞的影响及其可能的机制。
1 材料与方法
1.1细胞与材料人膀胱癌细胞株EJ细胞购于上海生命科学院细胞库,RPMI1640培养基、胎牛血清、胰蛋白酶购于美国Gibco公司;JQ1购于Selleck,用二甲基亚砜(dimethyl sulfoxide,DMSO)溶解后,配成溶度为50 mmol/L的储存浓度,储存于-80 ℃冰箱;CCK8试剂盒(cell counting kit-8)购于于同仁化工上海双达生物有限公司;磷脂结合蛋白-异硫氰酸荧光素/碘化丙啶(annexin V-fluorescein isothiocyanate/propidium iodide,Annexin V-FITC /PI)凋亡试剂盒、PI周期试剂盒购于联科公司;反转录试剂盒购于TaKaRa公司。
1.2方法
1.2.1细胞培养 膀胱癌细胞株EJ细胞用含10%的胎牛血清的RPMI1640培养基,置于含5%、37 ℃的CO2饱和湿度培养箱中培养。2~3 d换液传代1次,取对数生长期细胞用于实验。
1.2.2CCK8法检测JQ1对膀胱癌细胞株的活性影响 待细胞生长融合度达70%~80%时,用0.25%胰酶消化下细胞并进行计数,离心细胞重新加入培养基,调整细胞浓度至5×103个/100 μL,以每孔100 μL将细胞接种于96孔板中。待24 h后细胞贴壁,弃去培养基,分别加入不同浓度的 JQ1,处理24、48、72 h,并设立不加药物只加细胞及培养基的对照组及只加药物和培养基的空白对照组。弃去培养基,每孔加入含100 μL培养基和10 μL的CCK8试剂,2 h后用酶标仪测,于450 nm波长处读取吸光度值(A值)。JQ1对细胞存活率的影响(%)=[(实验孔A值-空白孔A值)/(对照孔A值-空白孔A值)],上述实验重复3次(实验孔含JQ1、细胞、培养基、CCK8试剂;对照孔含细胞、培养基、CCK8试剂;空白孔含培养基、CCK8试剂)。
1.2.3流式细胞术检测细胞凋亡 EJ细胞分为3组,DMSO组、JQ1(0.5 μmol/L)组、JQ1(1 μmol/L)组。细胞接种于6孔板中,待细胞生长融合度达70%~80%,加入DMSO、0.5、1 μmol/L的JQ1,48 h后收集各组细胞悬液,细胞悬液经预冷的磷酸盐(phosphate buffered solution,PBS)缓冲液洗涤2遍,加入250 μL 结合液(Binding Buffer)重悬细胞,调整其浓度为1×106个/ mL。取100 μL的细胞悬液于5 mL流式管中,加入5 μL Annexin V-FITC和10 μL的PI溶液。混匀后室温避光孵育15 min,最后在反应管中加入400 μL PBS,流式细胞仪分析,上述实验重复3次。
1.2.4流式细胞术检测细胞周期 EJ细胞分为3组,DMSO组、JQ1(0.5 μmol/L)组、JQ1(1 μmol/L)组。细胞接种于6孔板中,待细胞生长融合度达70~80%,加入0.5、1 μmol/L的JQ1,48 h后0.25%胰酶消化并收集各组细胞悬液,加入70%的乙醇溶液4 mL过夜,之后PBS缓冲液洗涤细胞,加入PI溶液和RNaseA(核糖核酸酶)室温避光孵育30 min,流式细胞仪分析,并用modfit LT2.0软件分析细胞周期,上述实验重复3次。
1.2.5Transwell侵袭实验检测JQ1对膀胱癌EJ细胞侵袭作用影响 EJ细胞接种在6孔板,完全培养基培养24 h后,分别加入含JQ1与DMSO的继续培养48 h,每个小室加入80 μL的基质胶。之后胰蛋白酶消化细胞,以细胞数量1×105个/100 μL接种于小室,下室加入500 μL含10%血清培养基,24 h后,使用0.5%结晶紫染色。倒置显微镜观察并拍照穿膜的细胞。
1.2.6qRT-PCR法检测JQ1对EJ细胞C-MYC及Bcl-XL基因表达的影响 EJ细胞接种于6 孔板,待细胞生长融合度达70%~80%,加入DMSO、0.5、1 μmol/L的JQ1,48 h后,分别加入Trizol试剂提取RNA。用紫外线分光光度计检测RNA的浓度和纯度。将提取的总RNA取等量按反转录试剂盒说明逆转录成cDNA,使用实时定量荧光PCR仪(美国ABI公司)按照试剂盒说明书以cDNA为模板,使用C-MYC及Bcl-Xl的特定引物(上海生工生物有限公司合成),进行聚合酶链式反应(polymerase chain reaction,PCR)扩增,以GAPDH为内参。依据各组循环阈值Ct采用2-△△ct结果作为测定mRNA的相对表达量。所有引物均参照相关文献设计,由Invitrogen公司合成。序列如下:C-MYC,上游5′-AGGGATCGCGCTGAGTATAA-3′和下游5′-TGCCTCTCGCTGGAATTACT-3′;Bcl-2,上游5′-AGTACCTGAACCGGCACCT-3′和下游5′CAGCCAGGAGAAATCAAACAG-3′;GAPDH,上游5′-TCAAGAAGGTGGTGAAGCAG-3′和下游5′-CGTCAAAGGTGGAGGAGTG-3′。
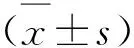
2 结 果
2.1JQ1抑制EJ细胞株的增殖JQ1抑制膀胱癌细胞的增殖,我们首先分别采用浓度为0.0032、0.016、0.08、0.4、2、10 μmol/L的JQ1处理膀胱癌EJ细胞,72 h后加入CCK8试剂,2 h后用酶标仪,于450 nm波长处读取吸光度值(A值),计算各组的增殖率,得出JQ1在EJ细胞株的IC50值为0.79 μmol/L(图1A)。因此,之后的实验我们选取JQ1浓度为0.5、1 μmol/L进行。JQ1对EJ细胞的活性有明显的抑制作用,在浓度为0.5~1 μmol/L之间,随作用时间延长细胞活性逐渐降低(图1B)。因此,JQ1可呈时间和浓度依赖的方式抑制膀胱癌EJ细胞的增殖。
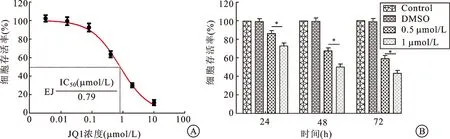
图1BRD4抑制剂JQ1抑制膀胱癌细胞的增殖
A:JQ1的浓度分别为0.0032、0.016、0.08、0.4、2、10 μmol/L处理膀胱癌EJ细胞后细胞存活率;B:浓度为0.5、1 μmol/L的JQ1处理EJ细胞24、48、72 h后细胞存活率;与对照组比较,*P<0.05(n=3)。
2.2JQ1促进EJ细胞株凋亡JQ1促进EJ的凋亡,我们采用了JQ1浓度为0.5、1 μmol/L处理EJ细胞,48 h后收集细胞并用流式细胞仪分析周期,结果显示与对照组相比,经JQ1处理过的EJ细胞株凋亡细胞明显增多,且随浓度增加而逐渐增多。差异有统计学意义(图2A、B)。
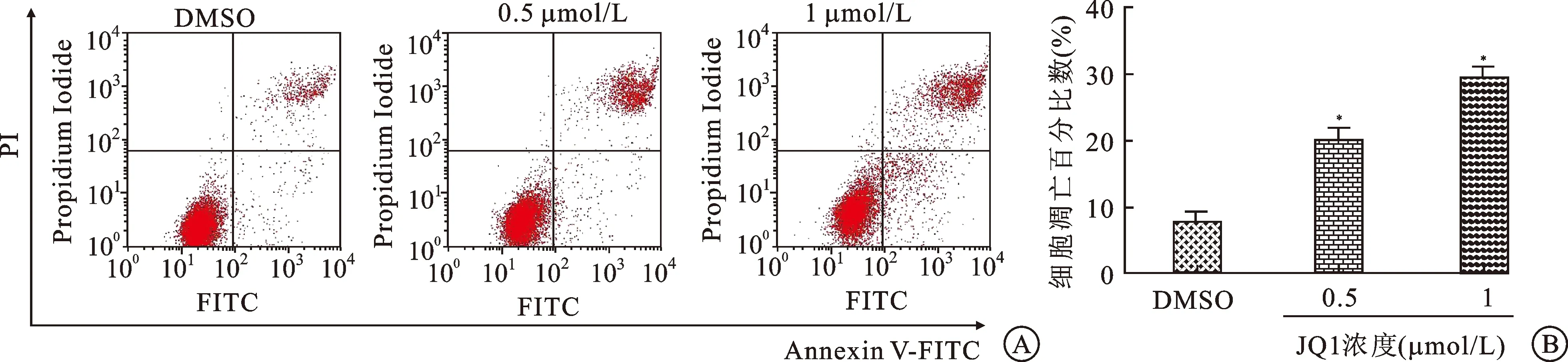
图2BRD4抑制剂JQ1诱导膀胱癌细胞凋亡
A:浓度为0.5、1 μmol/L的JQ1处理EJ细胞48 h后通过流式细胞技术测定细胞凋亡;B:浓度为0.5、1 μmol/L的JQ1处理EJ细胞48 h后计算细胞凋亡的百分比;与对照组比较:*P<0.05(n=3)。
2.3JQ1阻滞EJ细胞株于G0/G1期为了验证JQ1对EJ细胞周期的影响,我们采用JQ1浓度为0.5、1 μmol/L处理EJ细胞,48 h后收集细胞并用流式细胞仪分析周期,结果(图3A、B)显示与对照组相比,JQ1处理过的EJ细胞株G0/G1期细胞比例明显增多,且随浓度增加而增多,提示JQ1阻滞细胞于G0/G1期,差异有统计学意义(P<0.05)。

图3BRD4抑制剂JQ1阻滞膀胱癌细胞于G0/G1期
A:浓度为0.5、1 μmol/L的JQ1处理EJ细胞48 h后通过流式细胞技术测定细胞周期;B:浓度为0.5、1 μmol/L的JQ1处理EJ细胞48 h后计算细胞所处周期的百分比数;与对照组比较,*P<0.05(n=3)。
2.4JQ1抑制EJ细胞株侵袭验证JQ1是否对膀胱癌细胞的侵袭能力有影响,我们采用浓度为0.5、1 μmol/L的JQ1处理EJ细胞株,对照组采用DMSO处理,结果显示JQ1对EJ细胞的侵袭能力产生显著的抑制作用(图4)。
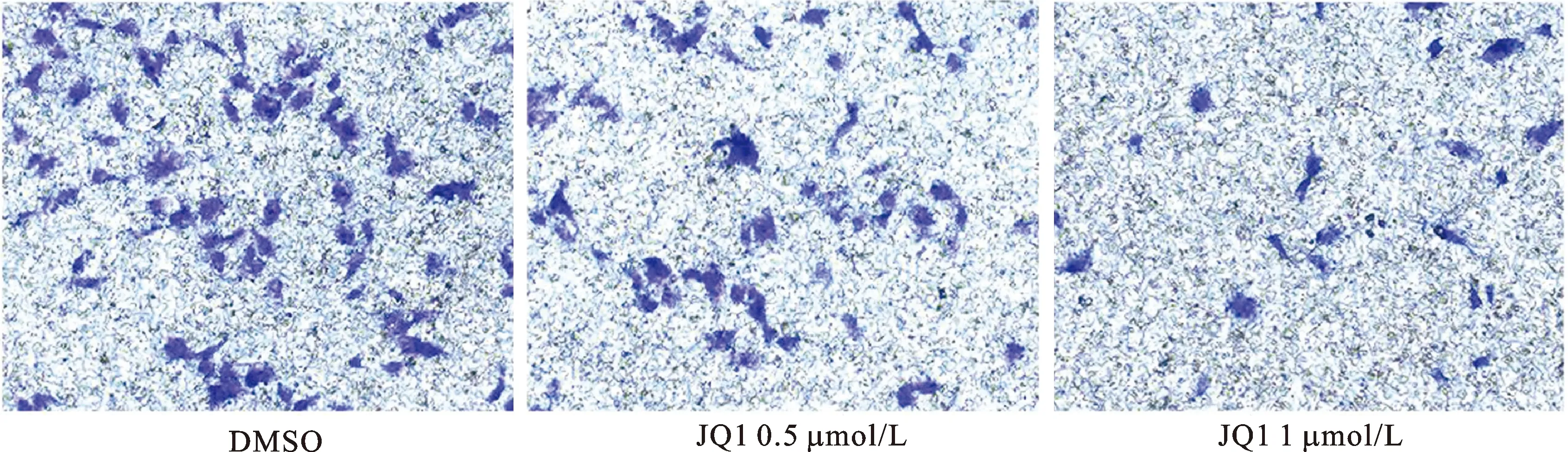
图4BRD4抑制剂JQ1降低膀胱癌细胞侵袭能力
2.5JQ1下调EJ细胞株中C-MYC及Bcl-2mRNA表达量分别用浓度为0.5 μmol/L、1 μmol/L的JQ1处理EJ细胞株,48 h后提取总RNA并用qRT-PCR法检测JQ1对C-MYC及Bcl-2表达量的影响。结果显示经JQ1处理后的EJ细胞C-MYC及Bcl-2表达量下降,并且随着JQ1浓度的增加mRNA表达量逐渐下降(图5)。
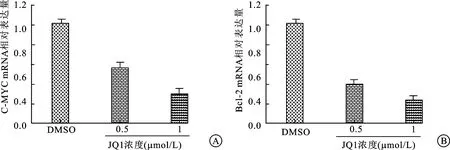
图5BRD4抑制剂JQ1下调EJ细胞株中C-MYC及Bcl-2mRNA表达量
A:C-MYC mRNA相对表达量;B:Bcl-2 mRNA相对表达量;与对照组比较,*P<0.05(n=3)。
3 讨 论
膀胱癌是一种异质性的肿瘤,在男性中高发,是造成男性因癌症死亡的第4大原因,研究证实大量饮酒及吸烟是膀胱癌的发病风险因素[18]。其治疗方式选择取决于肿瘤的病理分期和分级,对于早期非肌层浸润的膀胱癌主要采取原发肿瘤切除术或者联合膀胱灌注化疗药物,而对于肌层浸润膀胱癌主要采取根治性膀胱切除术,随着新辅助全身化疗以及放疗的联合应用患者预后有明显改善[19]。然而膀胱癌有着很高的复发及转移率,目前对于复发性及转移性膀胱癌缺乏有效的治疗方法,因此开发出一种新的治疗方法尤为重要。许多文献证实BRD4抑制剂JQ1可以抑制肿瘤的发生发展,提示JQ1可能会成为膀胱癌的新治疗手段。
近年来,表观遗传调控逐渐成为肿瘤研究的热点,肿瘤存在表观遗传调控异常逐渐得到证实。针对表观遗传调控药物已在临床实验应用并且非常有前景[20-21]。BET家族作为表观遗传识别蛋白通过结合组蛋白尾部赖氨酸,调控基因的表达,参与细胞周期、细胞生长、凋亡、炎症等一系列重要生物活动过程,并且与肿瘤的发生发展有关。JQ1作为第一种BET蛋白家族抑制剂,在多种肿瘤中证实其可以与BRD4溴结构域相结合,使BRD4蛋白从染色质的乙酰化赖氨酸上置换下来,从而干扰BET蛋白发挥生物学作用。另外在体外细胞实验及体内动物实验中都证实JQ1还可以通过C-MYC依赖途径和非C-MYC依赖途径产生抗肿瘤效应[22]。在我们的研究中,通过设立不同浓度JQ1组作用于膀胱癌细胞,我们发现随着浓度的增加,JQ1逐渐抑制膀胱癌细胞的增殖,随后延长作用时间,膀胱癌细胞的活性逐渐降低,证实JQ1可呈时间和浓度依赖的方式抑制膀胱癌细胞增殖。接着我们通过流式细胞仪检测JQ1对膀胱癌的作用,结果显示JQ1通过促进膀胱癌细胞凋亡,阻滞细胞于G0/G1期产生抗癌作用。
BET蛋白抑制剂抗癌效应的具体机制尚未完全揭示,目前较为明确的机制是JQ1可以调节C-MYC的表达。C-MYC影响着许多细胞生物学功能,包括细胞增殖、凋亡等。C-MYC表达的下调导致细胞增殖受到抑制,甚至诱导抗凋亡基因如Bcl-XL和Bcl-2表达的降低从而导致细胞凋亡增多[23-24]。然而在有些肿瘤细胞中,JQ1通过非C-MYC途径产生抗癌效应[25]。我们通过qRT-PCR实验证实,JQ1通过作用C-MYC及Bcl-2达到抗癌的效应。随着JQ1浓度的增加,癌基因C-MYC及抗凋亡基因Bcl-2表达逐渐下降,提示JQ1在膀胱癌中抗癌效应可能与C-MYC及Bcl-2基因表达减少有关。
综上所述,BRD4抑制剂JQ1抑制膀胱癌细胞增殖,促进膀胱癌细胞凋亡,阻滞细胞于G0/G1期,其可能机制与降低癌基因C-MYC及抗凋亡基因Bcl-2的表达有关。我们研究结果可能对未来膀胱癌治疗提供了一种新的思路。
参考文献:
[1] SIEGEL RL,MILLER KD,JEMAL A.Cancer statistics,2017[J].CA Cancer J Clin,2017,67(1):7-30.
[2] CHEN W,ZHENG R,BAADE PD,et al.Cancer statistics in China,2015[J].CA Cancer J Clin,2016,66(2):115-132.
[3] WANG Z,WANG X,ZHANG D,et al.Long non-coding RNA urothelial carcinoma-associated 1 as a tumor biomarker for the diagnosis of urinary bladder cancer[J].Tumour Biol,2017,39(6):13933796741010428317709990
[4] RENTSH CA,MULLER DC,RUIZ C,et al.Comprehensive molecular characterization of urothelial bladder carcinoma:a step closer to clinical translation?[J].Eur Urol,2017,72(6):960-961.
[5] HU Y,ZHOU J,YE F,et al.BRD4 inhibitor inhibits colorectal cancer growth and metastasis[J].Int J Mol Sci,2015,16(1):1928-1948.
[6] DHALLUIN C,CARLSON JE,ZENG L,et al.Structure and ligand of a histone acetyltransferase bromodomain[J].Nature,1999,399(6735):491-496.
[7] CHENG Z,GONG Y,MA Y,et al.Inhibition of BET bromodomain targets genetically diverse glioblastoma[J].Clin Cancer Res,2013,19(7):1748-1759.
[8] FILIPPAKOPOULOS P,KNAPP S.Targeting bromodomains:epigenetic readers of lysine acetylation[J].Nat Rev Drug Discov,2014,13(5):337-356.
[9] FILIPPAKOPOULOS P,PICAUD S,MANGOS M,et al.Histone recognition and large-scale structural analysis of the human bromodomain family[J].Cell,2012,149(1):214-231.
[10] MATZUK MM,MCKEOWN MR,FILIPPAKOPOULOS P,et al.Small-molecule inhibition of BRDT for male contraception[J].Cell,2012,150(4):673-684.
[11] LI GQ,GUO WZ,ZHANG Y,et al.Suppression of BRD4 inhibits human hepatocellular carcinoma by repressing MYC and enhancing BIM expression[J].Oncotarget,2016,7(3):2462-2474.
[12] ANDRIEU G,TRAN AH,STRISSEL KJ,et al.BRD4 regulates breast cancer dissemination through Jagged1/Notch1 signaling[J].Cancer Res,2016,76(22):6555-6567.
[13] LIAO YF,WU YB,LONG X,et al.High level of BRD4 promotes non-small cell lung cancer progression[J].Oncotarget,2016,7(8):9491-9500.
[14] TOGEL L,NIGHTINGALE R,CHUEH AC,et al.Dual targeting of bromodomain and extraterminal domain proteins,and WNT or MAPK signaling,inhibits c-MYC expression and proliferation of colorectal cancer cells[J].Mol Cancer Ther,2016,15(6):1217-1226.
[15] GAO X,WU X,ZHANG X,et al.Inhibition of BRD4 suppresses tumor growth and enhances iodine uptake in thyroid cancer[J].Biochem Biophys Res Commun,2016,469(3):679-685.
[16] FERRI E,PETOSA C,MCKENNA CE.Bromodomains:Structure,function and pharmacology of inhibition[J].Biochem Pharmacol,2016,106:1-18.
[17] JUNG M,GELATO KA,FERNANDEZ-MONTALVAN A,et al.Targeting BET bromodomains for cancer treatment[J].Epigenomics,2015,7(3):487-501.
[18] MASAOKA H,MATSUO K,SAWADA N,et al.Alcohol consumption and bladder cancer risk with or without the flushing response:The Japan Public Health Center-based Prospective Study[J].Int J Cancer,2017,141(12):2480-2488.
[19] SOLOMON JP,HANSEL DE.Morphologic and molecular characteristics of bladder cancer[J].Surg Pathol Clin,2015,8(4):663-676.
[20] GADDIS M,GERRARD D,FRIETZE S,et al.Altering cancer transcriptomes using epigenomic inhibitors[J].Epigenetics Chromatin,2015,8:9.
[21] BENEDETTI R,CONTE M,ALTUCCI L.Targeting histone deacetylases in diseases:where are we?[J].Antioxid Redox Signal,2015,23(1):99-126.
[22] KANNO T,KANNO Y,LEROY G,et al.BRD4 assists elongation of both coding and enhancer RNAs by interacting with acetylated histones[J].Nat Struct Mol Biol,2014,21(12):1047-1057.
[23] MERTZ JA,CONERY AR,BRYANT BM,et al.Targeting MYC dependence in cancer by inhibiting BET bromodomains[J].Proc Natl Acad Sci U S A,2011,108(40):16669-16674.
[24] KELLY PN,GRABOW S,DELBRIDGE AR,et al.Endogenous Bcl-xL is essential for Myc-driven lymphomagenesis in mice[J].Blood,2011,118(24):6380-6386.
[25] BAKER EK,TAYLOR S,GUPTE A,et al.BET inhibitors induce apoptosis through a MYC independent mechanism and synergise with CDK inhibitors to kill osteosarcoma cells[J].Sci Rep,2015,5:10120.

