两种微量肉汤稀释法药敏板用于沙门菌药敏检测结果比较
张晓嫒 崔霞 王迪 陆峥 陈倩
沙门菌是一种重要的肠道致病菌,广泛存在于自然环境中,通过粪-口途径传播,可引起肠胃炎症状,严重者导致死亡[1]。沙门菌可引起食物中毒散发甚至暴发流行,也能引起院内交叉感染[1]。据WHO统计数据,全球每年有约1 600万例沙门菌感染病例,其中60万例死亡[2]。对沙门菌开展耐药性监测,可以掌握其耐药性现状和变化趋势,进而为临床用药策略的调整提供科学依据[3-4]。沙门菌耐药性监测要求长期监测数据具有稳定性和可比较性,因此,对检测方法和实验试剂的重复性、不同品牌试剂检测结果的一致性要求高,但是目前还没有关于不同品牌的微量肉汤稀释药敏板重复性和一致性的报道。2016年,针对目前我国沙门菌耐药性监测中使用最广泛的2种微量肉汤检测药敏板,进行结果评价和比较。
1 材料与方法
1.1 实验菌株 选择6株不同血清型的沙门菌作为测试菌株进行耐药性检测,质控菌株使用大肠杆菌ATCCTM25922。所有菌株均经过生化和血清鉴定,6株沙门菌编号和血清型分别为1阿贡纳沙门菌、2山夫登保沙门菌、3肠炎沙门菌、4鼠伤寒沙门菌、5黄金海岸沙门菌、6猪霍乱沙门菌。
1.2 药敏检测方法 药敏试验采用微量肉汤法(依据2016食源性疾病监测工作手册),2种微量肉汤药敏板分别为上海星佰生物技术有限公司和美国赛默飞世尔科技公司(以下简称Thermo)产品,均为革兰阴性需氧菌药敏检测板,检测药物包括氨苄西林(ampicillin,AMP)、氨苄西林/舒巴坦(ampicillin/sulbactam,AMS)、四环素(tetracycline,TET)、氯霉素(chloramphenicol,CHL)、头孢唑啉(cefazlin,CFZ)、甲氧苄胺嘧啶/磺胺甲噁唑(trimethoprim/sulfamethoxazole,SXT)、环丙沙星(ciprofloxacin,CIP)、头孢他啶 (ceftazidime,TAZ)、亚胺培南(lmipenem,IMP)、萘啶酸(nalidixic acid,NAL)、头孢西丁(cefoxitin,CFX)、头孢噻肟(cefotaxime,CTX)和庆大霉素(gentamicin,GEN),其结果与美国临床实验室标准化协会(CLSI)2015年标准比较[5],以大肠杆菌ATCCTM25922做为质控菌株。
2 结果
2.1 上海星佰药敏板MIC定量结果和药物敏感性结果可重复性评价 质控菌株ATCCTM25922除在TET上2次结果存在一个浓度梯度的差异外,其他抗生素2次实验结果的MIC值完全一致。质控菌株ATCCTM25922的MIC值都在质控范围内。6株菌的2次实验结果比较发现有14个孔[14/(13×6)=17.95%]MIC值不一致,均只相差一个浓度梯度。7种抗生素出现了两次实验MIC值不相同的现象。这7种抗生素是 TET、TET、CFZ、CIP、CFX、CTX、GEN,分别有 4、3、2、2、1、1、1 株菌出现差异。在药物敏感性判断上,菌株1和2的CFZ药敏性分别出现不一致结果,2次实验结果分别判断为耐药和中介;其余MIC出现差异的实验孔在药敏判断上没有差异。
2.2 Thermo药敏板MIC定量结果和药物敏感性定性结果可重复性评价 质控菌株ATCCTM25922除在TET上2次结果存在一个浓度梯度的差异外,其他抗生素2次实验结果的MIC值完全一致。质控菌株ATCCTM25922的MIC值都在质控允许范围内。6株菌的2次实验结果比较发现有4孔的[4/(13×6)=5.12%]MIC值不一致,均只相差一个浓度梯度。13种抗生素中,有3种出现了2次实验MIC不相同的现象。这3 种抗生素是 AMS、NAL、CFX,分别有 1、2、1株菌出现差异。MIC出现差异的实验孔在定性判断上没有差异。
2.3 两种药敏板检测结果一致性评价 2种药敏板对6株沙门菌和质控菌株大肠埃希菌ATCCTM25 922分别开展2次重复实验,AMP、SXT、CIP、TAZ的2次实验结果均一致,其余9种抗生素的实验结果存在差异。质控菌株ATCCTM25 922的AMS MIC值在2种药敏板的2次重复结果中存在差异。6株沙门菌2种药敏板的MIC值结果存在差异的孔有26个[26/(13×6×2)=16.67%],其中2次重复实验结果均存在差异的实验孔有15个,一次实验结果存在差异的实验孔有11个(表1)。
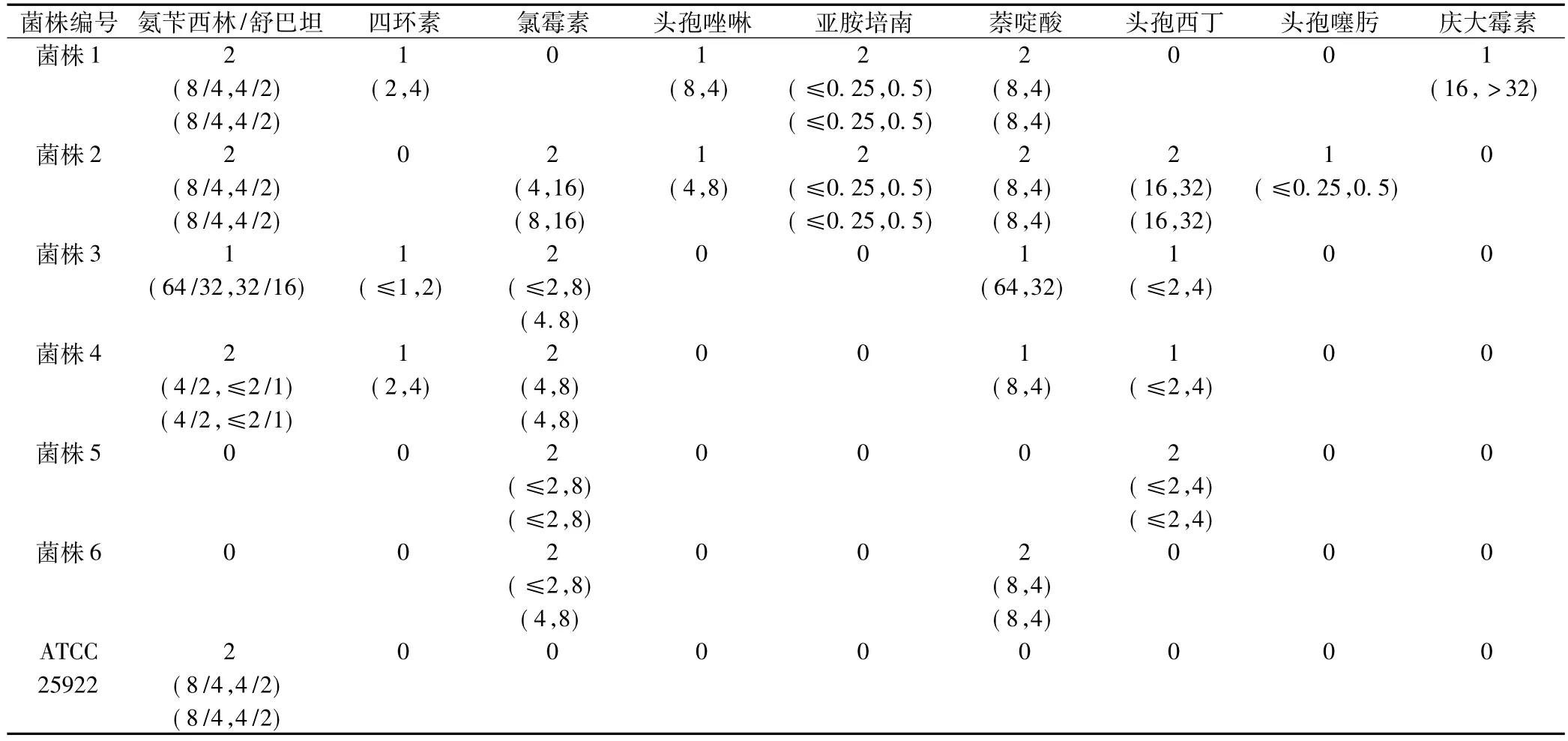
表1 2种药敏板MIC值存在差异的抗生素
15个2次重复实验结果均存在差异的实验孔一共涉及5种抗生素:AMS(3株)、CHL(5株)、IMP(2株)、NAL(3株)、CFX(2株)。11个一次结果存在差异的实验孔涉及7种抗生素:AMS、TET、CFZ、NAL、CFX、CTX、GEN。氨苄西林/舒巴坦AMS、NAL 的差异结果中,上海星佰药敏板比Thermo药敏板均高1个梯度值;TET、CHL、IMP、CFX、CTX、GEN 的差异结果中,星佰药敏板比Thermo药敏板均低1个或者2个梯度值(表1)。在定性判断上,菌株2的CHL用上海星佰药敏板两次实验均判断为敏感,用Thermo药敏板两次实验均判断为中介;菌株2的CFX用上海星佰药敏板两次实验均判断为中介,用Thermo药敏板两次实验均判断为敏感(表1)。
3 讨论
3.1 国内相关报道显示,近年沙门菌已成为婴幼儿细菌性腹泻的首要病原菌[6,7]。同时,沙门菌耐药现状严峻,有报道显示,腹泻患者分离的沙门菌对氨苄西林、萘啶酸、四环素、哌拉西林三代头孢类抗生素广泛耐药[3-4,8],而且还出现了耐氨基糖苷类和耐碳青霉烯类抗生素的沙门菌[9,10]。所以,有必要长期连续地开展沙门菌的耐药监测,一是为临床检验性用药提供数据支持,其次是可以监测耐药菌的流行传播现状和新耐药菌的出现。
3.2 纸片扩散法、自动化商业仪器药敏检测法、微量肉汤稀释法是目前广泛用于耐药性检测和监测的药敏检测方法。纸片扩散法检测成本低,但是其检测结果受到琼脂、纸片的质量影响较大,结果稳定性和重复性差,准确性低[11]。VITEK 2 Compact仪器药敏检测法操作简单,适用于临床批量检测,快速获得药敏结果,但是其配套的商业药敏卡中的药物浓度梯度范围小,不利于长期监测耐药性变化状况。与其他方法相比,微量肉汤稀释法检测结果准确[12]。商业化的微量肉汤稀释药敏板实验操作简单,既能够应用于临床一线检测,又适用于监测机构开展长期耐药监测。
3.3 在本研究中,评价了2种常见的微量肉汤稀释药敏板。上海星佰药敏板和Thermo药敏板的重复性好,但在检测和监测中应该考虑MIC测定结果存在一个梯度的实验误差。2种药敏板的结果可以综合在一起分析,但需考虑MIC测定结果一个梯度的实验误差。综上所述,使用这2种药敏板开展药敏检测和监测重复性好,不同批次实验结果可以进行综合分析。
[1]Voetsch A C,Van Gilder T J,Angulo F,et al.Food net estimate of the burden of illness caused by nontyphoidal Salmonella infections in the United States[J].Clin Infect Dis,2004,38(Suppl):S127 -134.
[2]Majowicz S E,Musto J,Scallan E,et al.The global burden of nontyphoidal Salmonella gastroenteritis[J].Clin Infect Dis,2010,50(6):882 -889.
[3]张晓嫒,王迪,陈倩.北京市食源性非伤寒沙门菌的分子分型和耐药性研究[J].中国食品卫生杂志,2015,27(3):232-237.
[4]崔志刚,王爱敏,王鸣柳,等.婴幼儿腹泻感染的非伤寒沙门菌分子分型和耐药情况研究[J].疾病监测,2014,29(6):428-431.
[5]CLSI. Performance standards for antimicrobial susceptibility testing: seventeenth informational supplement M100-S22[S].Wayne,PA:Clinical and Laboratory Standards Institute,2012.
[6]杨小蓉,谢晓英,任敏,等.四川省成都市433例婴幼儿腹泻病原微生物监测分析[J].疾病监测,2012,27(2):97-100.
[7]焦继光,刘会霞.婴幼儿腹泻病原微生物的感染特点分析[J].中国医药指南,2013,11(20):44-45.
[8]沈美萍,吴晓燕,王良平.2009-2013年浙江省平湖市沙门菌临床感染血清型及耐药性分析[J].疾病监测,2014,29(7):560-563.
[9]Folster J P,Rickert R,Barzilay E J,et al.Identification of the aminoglycoside resistance determinants armA and rmtC among non-Typhi Salmonella isolates from humans in the United States[J].Antimicrob Agents Chemother,2009,53(10):4563-4564.
[10]DayMR,MeunierD,DoumithM,et al.Carbapenemaseproducing Salmonella enterica isolates in the UK[J].J Antimicrob Chemother,2015,70(7):2165 -2167.
[11]崔俊昌,宋秀杰.不同MH琼脂对于替加环素对鲍曼不动杆菌药敏结果的影响[J].中国药物应用监测,2012,9(1):84-86.
[12]邹自英,雷启丽,刘媛,等.鲍曼不动杆菌替加环素不同药敏检测方法敏感性对比分析[J].国际检验医学杂志,2015,36(7):880-881.

