注射用黄芪多糖辅助治疗非小细胞肺癌的Meta分析
于海艳,陈高峰
(广州中医药大学,广州 510405)
WHO根据肺癌生物学、治疗和预后将肺癌分为2大类:非小细胞肺癌和小细胞肺癌2大类,其中非小细胞肺癌(NSCLC)所占比例超过85%[1-3],手术治疗是目前治疗非小细胞肺癌最有效的方法,但约1/3的患者在初次确诊肺癌时就已处于中晚期[4],这些患者大多已无明确的手术指征,故化疗在非小细胞肺癌治疗中占据重要地位,是非小细胞肺癌患者治疗的基石[5-6]。黄芪多糖(Astragalan)是从黄芪中提取的有效活性成分,在辅助治疗恶性肿瘤、减轻放化疗毒副作用方面有一定疗效。为此,笔者根据Cochrane系统评价方法,对黄芪多糖注射液辅助治疗非小细胞肺癌的临床有效性和安全性进行系统评价,以期为临床决策提供证据。
1 资料与方法
1.1 检索策略 通过计算机检索,中文数据库包括中国知网(CNKI)、中国科技期刊全文数据库(VIP)、万方数据库,英文数据库包括PubMed、Cochrane图书馆和EMbase数据库。检索起止时间为该数据库建库时至2017年4月。中文检索词为“非小细胞肺癌”“非小细胞型肺癌”“非小细胞性肺癌”“非小细胞癌”“肺癌”“NSCLC”“黄芪多糖”;英文检索词为“non-small-cell lung cancer”“non-small-cell lung carcinoma”“lung cancer”“lung tumor”“NS CLC”“astragalan”“astragalus polysaccharides”。根据情况采取主题词和自由词检索相结合的方式。
1.2 纳入标准 研究类型:黄芪多糖注射液辅助治疗非小细胞肺癌的随机对照试验。研究对象:经病理学或细胞学检查确诊的Ⅰ到Ⅳ期的非小细胞型肺癌。干预措施:对照组为所有以放疗或化疗为基础的西医治疗方案,治疗组是在对照组基础上予以注射用黄芪多糖静脉输注。结局指标:1)WHO关于肿瘤病灶客观疗效评价标准[7];2)治疗前后的χ2评分及以卡氏评分为基础的生活质量改善程度的评估;348WBC、NEU、HGB等实验室检查指标。
1.3 排除标准 重复发表的文献,数据不全的文献,动物实验研究文献,综述类文献。
1.4 文献筛查 由2位研究者按照制定好的检索词独立检索文献、筛选文献,并进行文献资料提取,交叉核对,有分歧时讨论解决,未达成统一时与第三方讨论确定。若需要用到原始文献中未明确的数据时,可通过电话或电子邮件与作者联系后获取相关数据。最终纳入的研究信息提取包括:1)研究基本信息;2)干预措施;3)结局指标;4)不良反应。
1.5 文献质量评价 按照Cochrane干预措施系统评价手册5.1.0 偏倚风险评估工具对纳入文献进行质量评价和偏倚风险评估:1)随机方案方法;2)分配方案隐藏;3)受试者及实验人员盲法的设置;4)评估者盲法设置;5)结果数据的完整性;6)选择性报告结果;7)其他偏倚。
1.6 统计学方法 应用RevMan 5.3版本对资料进行数据统计分析。首先对各研究进行异质性检验评价。若P≥0.1,I2≤50%,说明研究间具有同质性,使用固定效应模型。若P<0.1,I2>50%,则认为研究间存在异质性,可进一步亚组分析。计数资料使用相对危险度(RR)作为统计量,连续资料使用标准化均数差(SMD)进行分析。若连续型数据研究只给出治疗前后的均数及标准差,且治疗前数据有统计学差异,可按照Cochrane干预措施系统评价手册5.1.0第16章中所给出公式计算差值标准差。对于等级资料根据Cochrane干预措施系统评价手册5.1.0第9章将较短的有序量表常通过将相邻分类合并在一起而转换成二分类资料。采用漏斗图进行发表偏倚的分析,若异质性较大则采用敏感性分析以明确结果是否稳健可信。
2 结果
2.1 文献检索筛选结果 共计检索文献143篇。首先剔除重复文献71篇;进一步阅读文题与摘要排除48篇文献,其中综述8篇、干预措施不符合29篇、干预对象不符合6篇、动物实验5篇;进行全文阅读后排除文献15篇,其中结局指标不符合9篇,文献数据不完整4篇,对照不符合要求2篇。最后共纳入9篇随机对照试验[8-16],共783例患者,其中治疗组393例,对照组390例。纳入研究的基本情况资料见表1。

表1 纳入研究的基本情况资料
2.2 偏倚风险评估 在随机分组方面,2个研究[8,10]采用随机数字表法分组,1个研究[9]采用住院序号分组,其余6个研究[11-16]仅描述“随机分组”,但具体的随机方法无详细描述,评价为“不清楚”。所有研究均未提及盲法及分配方案隐藏情况,评价为“不清楚”。所有研究中的患者均无失访报道,其中2篇研究[9,14]预先确定的结局指标未完全报道,评价为“高风险”。方法学质量评价按照Cochrane干预措施系统评价手册5.1.0第8章Cochrane 协作网偏倚风险评估工具进行评估。
2.3 结果分析
2.3.1 总有效率 较短的有序量通过将相邻分类合并在一起而转换成二分类资料。根据WHO关于有效率定义标准,将完全缓解(CR)和部分缓解(PR)、稳定(SD)和恶化(PD)分别合并为有效和无效的二分类变量。有5个研究[9-10,12,14,16]报道了WHO肿瘤疗效标准。异质性检验结果示P = 0.77,I2 = 0%,各研究间无统计学异质性,故采用固定效应模型进行Meta分析。Meta分析结果显示试验组与对照组相比,治疗有效率明显提高,差异有统计学意义[OR=1.93,95%CI(1.24,3.00),P=0.003]。
2.3.2 KPS评分 有2个研究[10-11]报道了治疗后KPS评分情况。异质性检验结果示P =0.62,I2 = 0%,各研究间统计学无异质性,故采用固定效应模型进行Meta分析。Meta分析结果显示治疗组与对照组相比,KPS评分分值显著提高,差异有统计学意义[MD=9.33,95%CI(7.26,11.40),P< 0.000 01]。
2.3.3 CD3+水平 有5个研究[8-9,12,15-16]报道了治疗后情况。异质性检验结果示P = 0.44,I2 = 0%,各研究间统计学无异质性,故采用固定效应模型进行Meta分析。Meta分析结果显示治疗组与对照组相比,可显著提高CD3+水平,其差异有统计学意义[MD=11.26,95% CI(10.40,12.11),P<0.000 01]。
2.3.6 白细胞计数 有4个研究[8,10,14,16]报道了治疗后WBC情况。异质性检验结果示P=0.21,I2 = 34%,各研究间统计学异质性不显著,故采用固定效应模型进行Meta分析。Meta分析结果显示治疗组与对照组相比,WBC水平明显提高,其差异有统计学意义[MD=1.81,95%CI(1.49,2.13),P<0.000 01]。
2.3.7 中性粒细胞计数 有3个研究[8,14,16]报道了治疗后NEU情况。异质性检验结果示P=0.93,I2=0%,各研究间统计学无异质性,故采用固定效应模型进行Meta分析。结果显示治疗组与对照组相比,NEU水平明显提高,其差异有统计学意义[MD=2.23,95% CI(1.84,2.61),P<0.000 01]。
2.4 偏倚方面 运用 RevMan 5.3 制作漏斗图,对以上指标进行漏斗图分析,结果都呈对称的倒置漏斗图,且呈现倒漏斗状,表明发表偏倚较小。见图1。
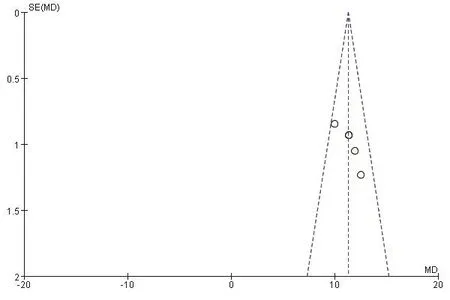
图1 治疗后2组水平比较漏斗图
3 讨论
本研究共纳入9项近年来黄芪多糖联合放疗化疗应用于非小细胞肺癌治疗的相关随机对照试验,对其进行汇总和分析。结果显示:1)在疗效方面,黄芪多糖联合放疗化疗应用于非小细胞肺癌,患者总有效率、生活质量改善、KPS评分、等指标均优于单纯应用放化疗治疗,具有显著的统计学差异,说明黄芪多糖应用于NSCLC辅助治疗具有提高疗效,增强患者免疫力的作用;2)在安全性方面,治疗组在抑制放化疗后白细胞计数、中性粒细胞计数减少等不良反应方面优于对照组,说明黄芪多糖作为辅助治疗手段能降低放化疗的主要毒副作用。但只有1篇研究[14]提及无不良反应,其余研究均未描述。
本研究在纳入文献中尚无多中心大型RCT,大部分试验未详细描述随机方法,是否实施分配隐藏和盲法等不足,在一定程度上导致选择性、实施、测量等各方面的偏倚。故目前尚需要多中心、大样本、高质量设计的随机对照试验来支持和印证本研究所得出的结果。
综上所述,注射用黄芪多糖联合放疗化疗作为NSCLC的辅助治疗,在增强疗效及免疫力,减少不良反应等方面,优于单纯放化疗方案。但本系统评价部分试验方案设计不严谨,样本量较少,导致上述结论存在一定偏倚。故还需设计严谨的多中心大样本量研究,为指导临床用药提供循证医学证据。
参考文献:
[1] ETTINGER D S, WOOD D E, AISNER D L, et al. Non-Small cell lung cancer, version 5.2017 clinical practice guidelines in oncology[J]. Journal of the National Comprehensive Cancer Network, 2017, 15(4):504-535.
[2]田晓刚,王小虎.非小细胞肺癌放疗的研究进展[J].甘肃医药, 2012, 31(9):673-675.
[3]TORRE L A, SIEGEL R L, JEMAL A. Lung cancer statistics[J]. Advances in Experimental Medicine and Biology,2016, (893):1-19.
[4]DE M-f, MIGLIORINO M R, MANCUSO A, et al.Neoadjuvant strategies for non-small cell lung cancer[J]. I Supplementi di Tumori: Offi cial Journal of Società Italiana di Cancerologia...[et al.], 2004, 3(2):S49.
[5]胡毅,陶海涛.晚期非小细胞肺癌的药物治疗进展[J].中国药物应用与监测,2014,11(6):329-333.
[6] ISHIKURA S. Optimal radiotherapy for non-small-cell lung cancer: current progress and future challenges[J]. General Thoracic and Cardiovascular Surgery, 2012, 60(3):127-131.
[7]中国抗癌协会.新编常见恶性肿瘤诊治规范[M].北京:中国协和医科大学出版社,1999.
[8]吕行,赵强,宁鹏,等.黄芪多糖对非小细胞肺癌放疗期细胞免疫及血常规的影响[J].中医药导报, 2014, 20(9):35-37.
[9]孙芳,宋波,王燕虎,等.黄芪多糖联合碘-125治疗中晚期非小细胞肺癌的临床研究[J].中国实验方剂学杂志,2014, 20(1):189-192.
[10]李小江,贾英杰,孙一予,等.注射用黄芪多糖联合化疗治疗晚期非小细胞肺癌临床疗效观察[J].中国肿瘤临床,2008, 35(16):919-921.
[11]李穗华.黄芪多糖注射液对Ⅱ-Ⅲ期非小细胞肺癌放疗患者免疫功能影响研究[J].实用中医药杂志, 2016,32(4):296-297.
[12]王永海,邢建群,寇丽春.黄芪多糖对非小细胞肺癌放疗患者免疫功能的影响[J].长春中医药大学学报, 2015,31(3):554-555, 634.
[13]王美阁.黄芪多糖对非小细胞肺癌患者免疫功能的影响[J].光明中医, 2017, 32(3):335-337.
[14]秦海燕,牛道立,蒋昌斌,等.注射用黄芪多糖联合三维适形放疗治疗老年肺癌临床观察[J].中国肿瘤临床,2009, 36(24):1401-1403.
[15]袁力.黄芪多糖注射液对非小细胞肺癌患者免疫功能的影响[J].海峡药学, 2015, 27(8):134-135.
[16]陈卓,于卫江.注射用黄芪多糖对非小细胞肺癌放疗的作用及对机体免疫的影响[J].中国实验方剂学杂志, 2013,19(6):309-313.

