老年患者脑萎缩的影响因素研究
高智玉,刁加桂,杨团峰,高旭光
脑萎缩(BA)分为广泛性BA和局限性BA,局限性BA多继发于某些脑部疾病,各年龄段均可出现。广泛性BA(以下简称BA)起病隐匿,原因不明,主要见于老年人群,也是老年人群脑功能障碍的重要原因。BA是老年人阿尔茨海默病、帕金森病、多系统萎缩等疾病的共同基础,防治BA有利于防治各种老年神经变性疾病[1-3]。然而BA的具体病因不明,缺乏防范措施。本研究旨在寻找BA的具体致病因素,从而为BA及各种神经变性疾病的防治提供依据。
1 资料与方法
1.1 纳入、排除标准 纳入标准:年龄≥60岁,入院后颅脑MRI检查显示不存在影响BA评分的急性或慢性占位性病变,入院前1个月内未服用降糖、降脂药物。排除标准:颅脑MRI检查显示有明显的急性或慢性占位效应的颅内病变,如脑出血、蛛网膜下腔出血、大面积脑梗死(面积>大脑中动脉1/3供血区)、脑积水、脑瘤等,急慢性中毒及颅内感染。
1.2 临床资料 选取2013年10月—2014年10月淄博市淄川区医院神经内科收治的符合研究标准的331例老年患者为研究对象。其中缺血性卒中236例,眩晕68例,其他疾病27例(包括头痛10例、面神经炎7例、抑郁障碍4例、癫痫4例、脊髓炎1例、癔症1例)。入选患者均为当地汉族居民。
1.3 研究方法 在患者尚未接受降糖、降脂药物的情况下,于入院当日或次日清晨采空腹静脉血,检测血糖(Glu)、三酰甘油(TG)、总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)水平。同时对入选患者进行颅脑MRI检查,由1位富有阅片经验的临床医师对每位患者进行BA评分,评分时只考察BA整体的程度,对各种原因所致的局限性BA不做评价。
BA评分标准:0分为无BA,1分为最轻度的BA表现,2分为较轻度的BA表现,3分为中度的BA表现,4分为较重度的BA表现,5分为最重度的BA表现。
1.4 观察指标 依据BA评分结果分为无BA组和BA组,比较无BA组和BA组患者的一般资料(性别、年龄、诊断)及实验室检查指标,采用有序Logistic回归分析分析BA评分的影响因素。
1.5 统计学方法 采用SPSS 18.0统计软件进行数据分析。计数资料比较采用χ2检验;计量资料以(x ±s)表示,两组间比较采用成组t检验;以BA评分为因变量,以性别、诊断分类为自变量,年龄、Glu、TG、TC、HDL-C及LDL-C水平作为协变量行有序Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 BA评分结果 BA评分结果为无BA患者131例,BA患者200例(BA评分1分88例、BA评分2分52例、BA评分3分49例、BA评分4分9例、BA评分5分2例)。
2.2 一般资料及实验室检查指标比较 除TG和HDL-C外,无BA组和BA组患者一般资料及其他实验室检查指标比较,差异均有统计学意义(P<0.05,见表1)。
2.3 有序Logistic回归分析结果 BA评分影响因素的有序Logistic回归分析各变量的赋值见表2。有序Logistic回归分析显示,年龄、性别、诊断及LDL-C水平是老年患者BA评分的影响因素(P<0.05,见表3)。
2.4 70~75岁无BA患者与BA患者实验室检查指标比较 均衡年龄和性别后,将70~75岁患者按照有、无BA分为无BA亚组(n=23)和BA(n=41)亚组。两亚组间Glu、TG、TC、HDL-C水平比较,差异均无统计学意义(P>0.05);BA亚组LDL-C水平低于无BA亚组,差异有统计学意义(P<0.05,见表4)。
2.5 缺血性卒中患者与非缺血性卒中患者BA评分比较均衡年龄和性别后,将年龄≥70岁的患者按照有无缺血性卒中分为缺血性卒中亚组(n=151)和非缺血性卒中亚组(n=58)。缺血性卒中亚组BA评分高于非缺血性卒中亚组,差异有统计学意义(P<0.05,见表5)。
3 讨论
BA的具体诱发因素尚不明确,可能与遗传、代谢、营养、内分泌、中毒、缺血、缺氧及伴发疾病等多方面因素有关。本研究Logistic回归分析显示,高龄、男性、缺血性卒中及低LDL-C水平可能是BA加重的危险因素,年龄作为BA的危险因素众所周知,本研究结合有关文献,重点对性别、缺血性卒中及LDL-C水平与BA严重程度的关系进行探讨。
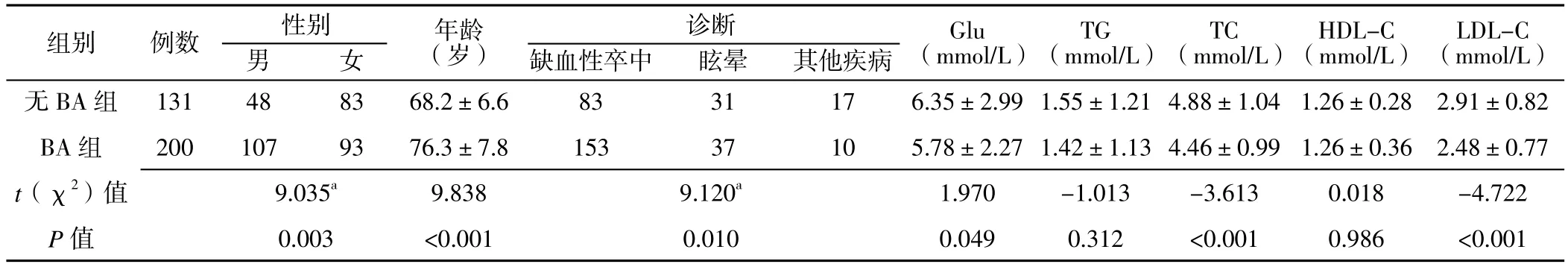
表1 无BA组和BA组患者一般资料及实验室检查指标比较Table 1 Comparison of the baseline characteristics between BA and non-BA groups

表2 BA评分影响因素的有序Logistic回归分析变量赋值Table 2 Assignment for the variables associated with BA score included in ordinal Logistic regression model

表3 老年患者BA评分影响因素的有序Logistic回归分析Table 3 Ordinal Logistic regression analysis of the associated factors for BA score in elderly patients
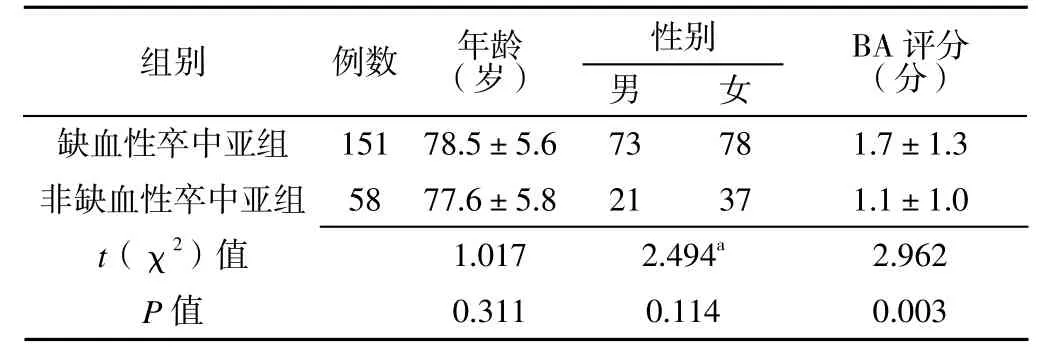
表5 缺血性卒中亚组与非缺血性卒中亚组间年龄、性别及BA评分比较Table 5 Comparison of age, sex, and BA scores between ischemic stroke subgroup and non-ischemic stroke subgroup
性别与BA的关系已有较多报道[4-5],均提示老年男性人群BA程度重于女性,但具体机制不明确,可能与内分泌激素差异有关。有报道雌性激素有多方面的神经保护作用[6],在阿尔茨海默病的研究中认为雌激素能抑制或减少β-淀粉样蛋白沉积,增加淀粉样肽前体蛋白(APP)向可溶性APP转化,从而抑制阿尔茨海默病的病情进展[7];国内李桃等[8]研究认为1个月的雌激素替代治疗对中年卵巢切除大鼠的认知功能及大脑白质和海马内的髓鞘具有明显的保护作用,这种保护作用可能与雌激素下调大脑白质和海马内Lingo-1蛋白的表达有关。流行病学调查认为女性焦虑障碍发生率明显高于男性[9-10],而慢性焦虑障碍对老年缺血性脑血管病有保护性作用[11],缺血性脑血管病则是导致BA的因素之一。
单次缺血性卒中并不会引发BA,但缺血性卒中反复发作(包括多发腔隙性梗死)则可引发BA[12]。另外,缺血性卒中多由动脉粥样硬化或各种小动脉病变引起,广泛脑动脉粥样硬化或小动脉病变除了引起急性缺血性卒中外,尚可引起脑组织慢性缺血缺氧,进而引发缺血缺氧性脑白质病变及BA[13-16]。皮质下动脉硬化性脑病是缺血性脑血管病的一种特殊类型,在临床上非常常见,BA也是其常伴发的重要影像学表现之一[17-18]。由此可见,积极防治缺血性卒中,改善动脉供血,也是防治BA的重要方面。
关于LDL-C水平与BA的相互关系当前报道不多,本研究结合有关文献从基础和临床两方面进行探讨。人体内胆固醇分内源性和外源性,内源性胆固醇是指由人体自身细胞合成的胆固醇,是人体内胆固醇的主要来源,约占3/4。肝脏是合成胆固醇最主要的器官,其次是肾上腺、性腺及皮肤等。外源性胆固醇即指来源于食物的天然胆固醇,约占总量的1/4[19]。来源于食物的胆固醇需要在肝脏代谢转化,然后与在肝脏合成的胆固醇一起与脂蛋白结合形成LDL-C,LDL-C随血流输送至全身各部以供组织利用,全身各组织细胞表面存在丰富的LDL-C受体,可与LDL-C结合,与受体结合的LDL-C通过细胞内吞作用进入细胞内,然后通过各种酶促反应,解离出胆固醇各组织细胞利用。全身各组织细胞虽然有自身合成胆固醇的能力,但由于胆固醇合成过程的复杂性及高耗能性,各组织细胞倾向于优先利用经LDL-C转运来的胆固醇。当血源胆固醇不足时,细胞即增加自身胆固醇合成,以满足自身需要[20]。细胞内胆固醇供应的这种双重途径是生物进化过程中形成的保证胆固醇供应不会中断的重要方式,这也充分说明胆固醇对细胞功能的重要性。另外,胆固醇在细胞内的水平保持相对稳定并受到严格调控,过低或过高均会影响细胞功能并引发疾病[21-22]。

表4 无BA亚组和BA亚组年龄、性别及实验室检查指标比较Table 4 Comparison of age, sex, and laboratory findings between BA and non-BA subgroups
胆固醇在人体各组织中分布广泛,但以脑和神经组织最为丰富,占全身总量的23%~25%。在脑和神经系统中,胆固醇是构成细胞膜和神经髓鞘的重要成分,对维持细胞膜的正常功能及神经兴奋传导有重要作用[23]。在婴幼儿及青少年期,胆固醇对脑的发育有重要作用,其是突触和树突形成不可缺少的物质,能促进轴突的生长[24-26]。给动物进行胆固醇耗竭可引起突触和树突的退化、神经传导障碍及突触的可塑性下降[27]。成年人脑胆固醇代谢相对缓慢,但也有研究认为成年人脑中胆固醇的合成与降解仍然很活跃,并且在这方面的任何变化均会对脑的高级功能产生深刻影响[28]。尽管目前认为脑中的胆固醇主要由星型胶质细胞合成,少部分来源于LDL-C提供的胆固醇,但LDL-C水平长期下降肯定也会影响脑内胆固醇水平[29]。所以长期LDL-C水平过低,不排除有引发脑部疾病的可能。
国内黄常洪等[30]研究认为阿尔茨海默病组患者血浆TC、HDL-C及LDL-C较正常对照组均明显下降。有研究认为老年高TC水平与痴呆风险降低相关[31]。有研究认为帕金森病患者的血清TC、TG、LDL-C、HDL-C、载脂蛋白B水平有所降低,以男性帕金森病患者的血脂水平降低更明显[32-34]。毕崇凤等[35]通过病例回顾性分析认为多系统萎缩(MSA)患者的血清TC、LDL-C、HDL-C、载脂蛋白A、载脂蛋白B水平较正常人降低,并认为低血脂水平可能与MSA的发病机制有关。提示上述疾病与BA同属于神经退行性疾病,有一定相关性。不排除长期的低LDL-C水平是引发BA及各种神经变性疾病的共同因素。
另一方面,胆固醇除了是细胞膜及神经髓鞘的组成成分外,尚是合成人体类固醇激素、胆汁酸及维生素D3的原料。血浆胆固醇水平低下也可能造成上述物质的合成减少。类固醇激素是人体生长发育的重要物质,其合成不足,也可能引发疾病。已有研究认为性激素水平低下的老年人群较性激素水平正常者有更突出的BA表现[36]。胆汁酸是由肝脏合成分泌的消化液,经胆管排入肠道,对脂肪类食物的消化吸收有重要作用,胆汁酸分泌减少会引起脂类物质包括胆固醇吸收减少,胆固醇吸收减少又会进一步引发胆汁酸的合成下降,这种胆汁酸与胆固醇之间的恶性循环会引发血胆固醇水平的整体下降。阻塞性黄疸的患者血清LDL-C水平下降也支持这一观点[37-38]。
综上,长期低胆固醇血症与BA有相关性,可能是诱发各种神经退行性疾病的独立危险因素。又由于LDL-C是引发动脉粥样硬化的主要原因,降低LDL-C是心、脑血管疾病一级和二级预防的重要基石。当前在医疗界推行强化降脂,也诱发不少盲目降脂和滥用他汀类药物的现象。如何才能做到合理降脂,既保护心、脑血管,又不损伤神经系统,是未来临床研究的重要课题。
本研究探讨了BA部分可能的危险因素,得出LDL-C水平降低可能与BA有关。这对心脑血管疾病的长期他汀类药物治疗及BA的防治均有重要意义。本研究中LDL-C水平与BA的关系尚只是一种临床推断,不能完全断定其因果关系,要明确长期低LDL-C水平与BA之间的关系,还需大样本前瞻性队列研究及分子机制方面的研究来证实。另外,本研究由于条件限制,纳入因素尚不够多,还有许多其他的BA诱发因素需进一步研究揭示。
作者贡献:高智玉负责本研究的构思、设计、可行性分析,部分临床资料的搜集整理、文献查找及论文撰写;刁加桂负责部分临床资料的搜集整理;杨团峰协助进行论文的统计分析和英文修订;高旭光对本研究的构思设计给予指导,并负责文章的修订和质量把控。
本文无利益冲突。
[1]姚胜旗,陆学胜,许敏,等.阿尔茨海默病患者脑萎缩与认知功能障碍的相关性[J].中国老年学杂志,2014,34(3):581-583.DOI:10.3969/j.issn.1005-9202.2014.03.003.
YAO S Q,LU X S,XU M,et al.The correlation between brain atrophy and cognitive dysfunction in patients with Alzheimer Disease[J].Chinese Journal of Gerontology,2014,34(3):581-583.DOI:10.3969/j.issn.1005-9202.2014.03.003.
[2]龚晓慧,赵珉珉,赵政凯,等.帕金森病影像学改变与临床表现相关性23例分析[J].中国误诊学杂志,2007,7(21):5148-5149.DOI:10.3969/j.issn.1009-6647.2007.21.189.
GONG X H,ZHAO M M,ZHAO Z K,et al.Correlation analysis of 23 cases Parkinson's disease imaging changes and clinical manifestations[J].Chinese Journal of Misdiagnostics,2007,7(21):5148-5149.DOI:10.3969/j.issn.1009-6647.2007.21.189.
[3]卢明鸥,张昱,朱辉,等.多系统萎缩的临床与病理特点及诊断[J].中华神经科杂志,2011,44(5):335-338.DOI:10.3760/cma.j.issn.1006-7876.2011.05.011.
LU M O,ZHANG Y,ZHU H,et al.Clinical and pathological characteristics of multiple system atrophy[J].Chin J Neurol,2011,44(5):335-338.DOI:10.3760/cma.j.issn.1006-7876.2011.05.011.
[4]GUR R C,MOZLEY P D,RESNICK S M,et al.Gender differences in age effect on brain atrophy measured by magnetic resonance imaging[J].Proc Natl Acad Sci U S A,1991,88(7):2845-2849.
[5]XU J,KOBAYASHI S,YAMAGUCHI S,et al.Gender effects on age-related changes in brain structure[J].AJNR Am J Neuroradiol,2000,21(1):112-118.
[6]沈丽霞,张力.雌激素神经保护作用研究进展[J].神经药理学报,2012(3):29-36.
SHEN L X,ZHANG L.Progress on the neuroprotective effects of estrogen[J].Acta Neuropharmacologica,2012(3):29-36.
[7]王澎伟,梁庆成,吴云.雌激素在阿尔茨海默病中神经保护作用机制的研究进展[J].卒中与神经疾病,2013,20(1):59-61.DOI:10.3969/j.issn.1007-0478.2013.01.020.
WANG P W,LIANG Q C,WU Y.Advances in neuroprotective mechanisms of estrogen in Alzheimer's disease[J].Stroke and Nervous Disease,2013,20(1):59-61.DOI:10.3969/j.issn.1007-0478.2013.01.020.
[8]李桃,罗艳敏,肖倩,等.雌激素替代治疗对中年卵巢切除大鼠大脑白质、海马内髓鞘及Lingo-1蛋白的影响[J].基础 医 学 与 临 床,2017,37(7):982-987.DOI:10.3969/j.issn.1001-6325.2017.07.016.
LI T,LUO Y M,XIAO Q,et al.Effects of estrogen replacement therapy on the myelin sheath of cerebral white matter and hippocampus and Lingo-1 expression in middle-aged ovariectomized rats[J].Basic & Clinical Medicine,2017,37(7):982-987.DOI:10.3969/j.issn.1001-6325.2017.07.016.
[9]杨秀成,何呈刚,苏静,等.山东省莱芜市15岁及以上人群精神障碍流行病学调查[J].临床精神医学杂志,2017,27(1):56-58.DOI:10.3969/j.issn.1005-3220.2017.01.022.
YANG X C,HE C G,SU J,et al.Epidemiological survey of mental disorders among people aged 15 and over in Laiwu city of Shandong Province[J].Chinese Mental Health Journal,2017,27(1):56-58.DOI:10.3969/j.issn.1005-3220.2017.01.022
[10]余灿清,吕筠,陈怡平,等.中国10地区30~79岁成人广泛性焦虑障碍的相关因素[J].中国心理卫生杂志,2015,29(8):581-586.DOI:10.3969/j.issn.1000-6729.2015.08.005.
YU C Q,LYU J,CHEN Y P,et al.Related factors to generalized anxiety disorder among adults aged 30-79 years from 10 China regions[J].Chinese Mental Health Journal,2015,29(8):581-586.DOI:10.3969/j.issn.1000-6729.2015.08.005.
[11]高智玉,王维宝.慢性焦虑抑郁与缺血性脑血管病的相关性[J].中华老年心脑血管病杂志,2014,16(7):694-697.DOI:10.3969/j.issn.1009-0126.2014.07.006.
GAO Z Y,WANG W B.Correlation between chronic anxiety depression and ischemic cerebrovascular disease[J].Chinese Journal of Geriatric Heart Brain & Vessel Diseases,2014,16(7):694-697.DOI:10.3969/j.issn.1009-0126.2014.07.006.
[12]杨洁,区腾飞,蒲蜀湘,等.卒中及短暂性脑缺血发作患者不同部位脑萎缩的危险因素[J].中国神经精神疾病杂志,2016,42(10):609-615.DOI:10.3969/j.issn.1002-0152.2016.10.008.
YANG J,QU T F,PU S X,et al.Risk factors for different brain region atrophy among stroke and transient ischemic attack patients[J].Chinese Journal of Nervous and Mental Diseases,2016,42(10):609-615.DOI:10.3969/j.issn.1002-0152.2016.10.008.
[13]葛海洋.脑皮质下小血管病变与脑萎缩的相关性分析[J].中国实用神经疾病杂志,2011,14(15):33-34.DOI:10.3969/j.issn.1673-5110.2011.15.015.
GE H Y.Discussion on the association between cerebral subcortieal small-vessel disease and brain atrophy[J].Chinese Journal of Practical Nervous Diseases,2011,14(15):33-34.DOI:10.3969/j.issn.1673-5110.2011.15.015.
[14]NITKUNAN A,LANFRANCONI S,CHARLTON R A,et al.Brain atrophy and cerebral small vessel disease:a prospective followup study[J].Stroke,2011,42(1):133.DOI:10.1161/STROKEAHA.110.594267.
[15]钟婷婷,郁可,霍颖超,等.颅内外动脉粥样硬化性狭窄与脑白质高信号的关系[J].中华老年心脑血管病杂志,2015,17(12):1282-1285.DOI:10.3969/j.issn.1009-0126.2015.12.015.
ZHONG T T,YU K,HUO Y C,et al.Relation of extracranial and intracranial atherosclerotic stenosis with white matter hyperintensities[J].Chinese Journal of Geriatric Heart Brain &Vessel Diseases,2015,17(12):1282-1285.DOI:10.3969/j.issn.1009-0126.2015.12.015.
[16]王洪萍,闫福岭.无残障老年人脑白质疏松与脑萎缩的相关性研究[J].中华脑血管病杂志:电子版,2010,4(5):345-350.DOI:10.3969/j.issn.1672-9248.2010.05.003.
WANG H P,YAN F L.The relationship between leukoaraiosis and cerebral atrophy on magnetic resonance imaging in the elderly nondisaility people[J].Chinese Journal of Cerebrovascular Diseases(Electronic Version),2010,4(5):345-350.DOI:10.3969/j.issn.1672-9248.2010.05.003.
[17]李建华,赵晓燕,葛志亮.皮层下动脉硬化性脑病的CT和低场MRI诊断分析[J].医学影像学杂志,2015(5):921-923.
LI J H,ZHAO X Y,GE Z L.Diagnostic analysis of CT and low field MRI of subcortical arteriosclerotic encephalopathy[J].Journal of Medical Imaging,2015(5):921-923.
[18]罗青毅,邹习忠,冉强,等.皮层下动脉硬化性脑病100例临床CT分析[J].世界最新医学信息文摘:连续型电子期刊,2014(30):240,244.DOI:10.3969/j.issn.1671-3141.2014.30.191.
[19]左玉,冯丽霞,魏世芳.胆固醇的研究及应用[J].太原师范学院学报(自然科学版),2010(4):104-107.
ZUO Y,FENG L X,WEI S F.Research and application of Cholesterol[J].Journal of Taiyuan Normal University (Natural Science Edition),2010(4):104-107.
[20]李伯良,段治军.胆固醇代谢平衡调控的分子机理[J].中国生物工程杂志,1996,16(5):27-33.DOI:10.13523/j.cb.19960506.
LI B L,DUAN Z J.Molecular mechanism of balance regulation of cholesterol metabolism[J].Journal of Chinese Biotechnology,1996,16(5):27-33.DOI:10.13523/j.cb.19960506.
[21]廖雅成,宋保亮.胆固醇的代谢调控与细胞内运输机制[J].科技导报,2016,34(13):53-59.
LIAO Y C,SONG B L.Metabolic regulation and intracellular transport mechanism of cholesterol[J].Science & Technology Review,2016,34(13):53-59.
[22]CHEN J,COSTAL L G,GUIZZETTI M.Assessment of cholesterol homeostasis in astrocytes and neurons[J].Methods Mol Biol,2011,758:403-414.DOI:10.1007/978-1-61779-170-3-27.
[23]DIETSCHY J M.Central nervous system:cholesterol turnover,brain development and neurodegeneration[J].Biol Chem,2009,390(4):287-293.DOI:10.1515/BC.2009.035.
[24]FESTER L,ZHOU L,BUTOW A,et al.Cholesterol-promoted synaptogenesis requires the conversion of cholesterol to estradiol in the hippocampus[J].Hippocampus,2009,19(8):692-705.DOI:10.1002/hipo.20548.
[25]GORITZ C,MAUCH D H,PFRIEGER F W.Multiple mechanisms mediate cholesterol-induced synaptogenesis in a CNS neuron[J].Mol Cell Neurosci,2005,29(2):190-201.DOI:10.1016/j.mcn.2005.02.006.
[26]DE CHAVES E I,RUSINOL A E,VANCE D E,et al.Role of lipoproteins in the delivery of lipids to axons during axonal regeneration[J].J Biol Chem,1997,272(49):30766-30773.
[27]KOUDINOV A R,KOUDINOVA N V.Cholesterol homeostasis failure as a unifying cause of synaptic degeneration[J].J Neurol Sci,2005,229/230:233-240.DOI:10.1016/j.jns.2004.11.036.
[28]MARTIN M,DOTTI C G,LEDESMA M D.Brain cholesterol in normal and pathological aging[J].Biochim Biophys Acta,2010,1801(8):934-944.DOI:10.1016/j.bbalip.2010.03.011.
[29]LUTJOHANN D,STROICK M,BERTSCH T,et al.High doses of simvastatin,pravastatin,and cholesterol reduce brain cholesterol synthesis in guinea pigs[J].Steroids,2004,69(6):431-438.DOI:10.1016/j.steroids.2004.03.012.
[30]黄常洪,李光清,唐珂.老年痴呆患者的血脂水平分析[J].检验医学与临床,2011,8(16):1925-1926.DOI:10.3969/j.issn.1672-9455.2011.16.003.
HUANG C H,LI G Q,TANG K.Analysis of blood lipid level of elder patients with Alzheimer disease[J].Laboratory Medicine& Clinic,2011,8(16):1925-1926.DOI:10.3969/j.issn.1672-9455.2011.16.003.
[31]MMZANDI M.High total cholesterol levels in late life associated with a reduced risk of dementia[J].Neurology,2005,64(10):1689-1695.DOI:10.1212/01.WNL.0000161870.78572.A5.
[32]戚志强,张克忠,王圣龙,等.帕金森病患者血脂水平的变化及其临床相关性研究[J].中华老年心脑血管病杂志,2016,18(2):119-121.DOI:10.3969/j.issn.1009-0126.2016.02.003.
QI Z Q,ZHANG K Z,WANG S L,et al.Relationship between blood lipid level in Parkinson's disease patients and their clinical characteristics[J].Chinese Journal of Geriatric Heart Brain &Vessel Diseases,2016,18(2):119-121.DOI:10.3969/j.issn.1009-0126.2016.02.003.
[33]秦晓凌,刘春风,罗蔚锋,等.帕金森病患者血脂水平回顾性分析[J].中华神经科杂志,2013,46(8):541-543.DOI:10.3760/cma.j.issn.1006-7876.2013.08.011.
QIN X L,LIU C F,LUO W F,et al.A retrospective analysis of blood lipid levels in patients with Parkinson's disease[J].Chin J Neurol,2013,46(8):541-543.DOI:10.3760/cma.j.issn.1006-7876.2013.08.011.
[34]HUANG X,CHEN H,MILLER W C,et al.Lower low-density lipoprotein cholesterol levels are associated with Parkinson's disease[J].Mov Disord,2007,22(3):377-381.DOI:10.1002/mds.21290.
[35]毕崇凤,钱海蓉,彭丽君,等.多系统萎缩患者的血脂水平分析[J].中华医学杂志,2015,95(41):3361-3365.DOI:10.3760/cma.j.issn.0376-2491.2015.41.010.
BI C F,QIAN H R,PENG L J,et al.Analysis of serum lipid level in patients with multiple system atrophy[J].Zhonghua Yi Xue Za Zhi,2015,95(41):3361-3365.DOI:10.3760/cma.j.issn.0376-2491.2015.41.010.
[36]RYAN J,ARTERO S,CARRIERE I,et al.Brain volumes in late life:gender,hormone treatment,and estrogen receptor variants[J].Neurobiology of Aging,2013,35(3):645-654.DOI:10.1016/j.neurobiolaging.2013.09.026.
[37]高伟芳,李晓,桑荣霞,等.阻塞性黄疸患者总胆汁酸的表达及与血脂水平的关系研究[J].现代生物医学进展,2017,17(15):2910-2912.DOI:10.13241/j.cnki.pmb.2017.15.028.
GAO W F,LI X,SANG R X,et al.Study of total bile acid and blood lipid levels in patients with obstructive jaundice[J].Progress in modern biomedicine,2017(15):2910-2912.DOI:10.13241/j.cnki.pmb.2017.15.028.
[38]汤建军,孙权.乌司他丁对梗阻性黄疸患者围术期肠黏膜屏障功能的影响[J].疑难病杂志,2014,13(10):1025-1027,1030.DOI:10.3969/j.issn.1671-6450.2014.10.011.

