酪氨酸激酶抑制剂相关皮肤不良反应30例分析
朱慧玲 程喜平 黄卫宁 王霞 温柳演 凡慧张阳冰 张德华 何嘉曦 熊春萍 韩建德
510120广州医科大学附属第一医院皮肤科(朱慧玲、程喜平、黄卫宁、王霞、温柳演、凡慧、张阳冰、熊春萍),呼吸内科(张德华),胸外科(何嘉曦);中山大学附属第一医院皮肤科(韩建德)
酪氨酸激酶抑制剂常见的不良反应为皮肤不良反应(adverse cutaneous reactions,ACR)。皮疹的出现可能是酪氨酸激酶抑制剂抗肿瘤有效的标志,与肿瘤患者的生存率密切相关[1⁃2]。但皮肤不良反应可影响患者的生活质量,严重时影响酪氨酸激酶抑制剂的继续使用。因此,及时发现、识别酪氨酸激酶抑制剂相关皮肤不良反应并尽早对其进行有效干预,对确保靶向抗肿瘤治疗的持续进行十分重要。我们分析收集的酪氨酸激酶抑制剂相关ACR病例的临床特征。
对象与方法
一、对象
收集2015年1月至2016年12月就诊于广州医科大学附属第一医院皮肤科门诊或在呼吸内科、胸外科病区住院,服用酪氨酸激酶抑制剂后出现皮疹患者30例,其中女16例,男14例,年龄22~79(58.0±14.0)岁,潜伏期2 d至6个月。30例中2例为急性淋巴细胞白血病,断裂点结集区-Abelson鼠白血病病毒原癌基因同源体的融合基因(break point cluster region⁃abelson murine leukemia viral oncogene homolog,BCR⁃ABL)均阳性,口服达沙替尼(100 mg/d)或伊马替尼(400 mg/d)。其余28例为肺腺癌Ⅲb期或Ⅳ期患者,其中26例肿瘤组织表皮生长因子受体(epidermal growth factor receptor,EGFR)19号或21号外显子发生突变,口服厄洛替尼(150 mg/d)19例,口服吉非替尼(250 mg/d)6例,口服埃克替尼(375 mg/d)1例;1例EGFR19号序列缺失突变和20号T790M突变,口服奥斯替尼(80 mg/d);1例无EGFR突变,口服安罗替尼(12 mg/d)。
二、一般情况
30例患者在接受酪氨酸激酶抑制剂治疗前肝肾功能均在正常范围内。2例急性淋巴细胞白血病患者接受靶向治疗前血常规检查显示三系减少,其余患者未见异常。
三、方法
总结皮疹的特点、实验室检查和病理检查结果特点、治疗经过、转归等临床资料,并进行分析。
结 果
一、皮疹分类
1.痤疮样皮疹:由厄洛替尼引起10例、吉非替尼4例、达沙替尼1例。15例中男8例,女7例,年龄28~79岁,中位年龄54.0岁,潜伏期2~180 d,中位潜伏期为21 d。皮疹表现为炎性丘疹、丘脓疱疹等,分布于面部、头皮、颈部(图1A)、躯干(图1B)、会阴部,少部分患者皮疹出现在四肢,伴疼痛,不伴瘙痒。根据美国JAAD皮疹严重程度分级标准[3],将患者按皮疹分为1级8例,2级3例,3级3例,4级1例。其中1级和2级各有1例患者肝酶水平轻度升高,分别为丙氨酸转氨酶(ALT)56.5 U/L、天冬氨酸转氨酶(AST)66.9 U/L和ALT 57 U/L、γ谷胺酰转移酶70 U/L。3例3级患者血超敏C反应蛋白(33.8~121.7 mg/L)轻度升高,白细胞10.21×109/L~12.93×109/L,中性粒细胞0.733~0.901,肝功能检查示ALT 49.2~88.1 U/L,γ谷胺酰转移酶107.6~188 U/L。1例4级患者伴高热,血超敏C反应蛋白465.8 mg/L,白细胞13.47×109/L,中性粒细胞0.792,肝功能检查AST 315 U/L,ALT63 U/L。15例患者的皮疹组织病理:表皮轻度增生,毛囊口扩张,角化过度,表皮层内、毛囊内、毛囊周围、皮脂腺和汗腺周围均可见以中性粒细胞为主的炎症细胞浸润,伴有少量淋巴细胞、组织细胞(图2A,2B)。治疗:8例1级、3例2级、3例3级皮疹患者予口服米诺环素(100 mg/d)治疗6周,皮疹可逐渐消退,但停药后复发;1例4级患者停用酪氨酸激酶抑制剂并静脉滴注注射用甲泼尼龙琥珀酸钠60 mg/d治疗3 d后改40 mg/d治疗4 d,皮疹明显减轻,改口服泼尼松40 mg/d共2 d,20 mg/d共3 d,10 mg/d共2 d,皮疹完全消退,护肝治疗(静脉滴注阿拓莫兰1 200 mg/d;口服易善复3次/d,每次2片)1周后肝酶恢复正常水平。
2.湿疹样皮疹:由厄洛替尼引起6例、吉非替尼2例、奥斯替尼1例、伊马替尼1例,共10例,其中男3例,女7例,年龄22~74岁,中位年龄为62.5岁,潜伏期7~120 d,中位发病间歇期潜伏期为56.5 d。皮疹表现为鲜红色或暗红色斑疹、斑片、丘疹、糜烂、鳞屑或苔藓样变等,形态似急性(图1C)或慢性湿疹(图1D),后期有色素沉着,全身皮肤均可受累。其中1例皮疹分布广泛,伴发高热,血超敏C反应蛋白1 160.2 mg/L;嗜酸性粒细胞比例0.057;肝功能检查示ALT 48.5 U/L,AST 54.9 U/L。另有1例嗜酸性粒细胞比例0.076。10例患者的皮疹组织病理:角化不全,角质层内可见浆液渗出,表皮出现不同程度的海绵水肿,棘层肥厚,上皮脚不规则延长(图2C),可见基底细胞液化、变性,真皮浅层、血管周围可见淋巴细胞及嗜酸性粒细胞浸润(图2D)。治疗:1例伴发热的患者暂停口服酪氨酸激酶抑制剂,静脉滴注注射用甲泼尼龙琥珀酸钠40 mg/d共5 d;口服泼尼松30 mg/d共3d,口服泼尼松10 mg/d共4 d;复方甘草酸苷3次/d每次2片,肌内注射苯海拉明每晚20 mg,口服依巴斯汀10 mg/d,酮替芬2 mg/d;护肝等对症治疗2周,皮疹消退、肝酶恢复正常水平。其余9例患者予2~3联抗过敏及外用糖皮质激素治疗3~4周有效,撤药后皮疹易反复。
3.麻疹样皮疹:由埃克替尼引起1例、达沙替尼1例共2例,均为男性患者,年龄28~52岁,中位年龄40岁,潜伏期38~95 d,中位潜伏期为66.5 d。皮疹表现为全身皮肤密集分布的鲜红色针尖大或粟粒大的斑疹或丘疹,有融合趋势(图1E和1F)。其中1例出现高热,嗜酸性粒细胞比例(0.303)升高。治疗:1例出现高热的患者暂停酪氨酸激酶抑制剂,静脉滴注甲泼尼龙琥珀酸钠40 mg/d共1周;口服泼尼松30 mg/d共3 d,10 mg/d共4 d),口服复方甘草酸苷3次/d每次2片;口服依巴斯汀10 mg/d;酮替芬2 mg/d,治疗2周后皮疹消退。另1例患者仅给予3联抗过敏药物口服,皮疹消退。撤药后皮疹易反复。
4.毛细血管扩张:由厄洛替尼引起1例,为女性患者,年龄60岁,潜伏期175 d,表现为面部对称性红斑基础上出现明显扩张的毛细血管,可见散在针尖大脓疱(图1G)。否认长期使用面膜或糖皮质激素软膏。予3%硼酸溶液湿敷(3次/d)以及外用鱼肝油软膏处理,10 d后脓疱与红斑消失,毛细血管扩张未见明显改善。
5.指/趾甲及甲周改变:由厄洛替尼引起6例、吉非替尼1例共7例,其中男2例,女5例,年龄47~79岁,中位年龄54岁。皮疹表现为甲板蚀损、裂隙、断裂、变黄、浑浊以及甲周红肿,出现甲旁肉芽肿或流脓液(图1H),双侧指/趾甲受累,伴疼痛。1级5例,2级2例。治疗:口服克林霉素600 mg/d或头孢呋辛500 mg/d,外用抗生素软膏2~3次/d或高锰酸钾溶液湿敷2~3次/d,治疗2周,甲周红肿或肉芽肿可减轻或消失,停药后复发。
6.手足皮肤反应:由安罗替尼引起1例,为女性患者,年龄75岁,潜伏期21 d,表现为掌、跖、指、趾黄色硬化性角化性斑疹和表皮剥脱(图1I),伴剧烈疼痛。服抗肿瘤药物间歇期上述症状自行减轻,服药期症状加重。皮疹发作期间予外用扶他林乳胶剂以及强效保湿乳剂(至少3次/d),可缓解局部疼痛。
7.毛发改变:由厄洛替尼引起4例,其中男女各2例,年龄61~74岁,中位年龄为65.5岁。表现为头发卷曲、变黑、变短,眉毛、睫毛卷曲、变黑、变长(图1J)。
8.皮肤干燥:由厄洛替尼引起7例、吉非替尼2例共9例,其中男4例,女5例,年龄39~74岁,中位年龄60岁。皮疹伴瘙痒。其中3级2例,表现为全身皮肤极度干燥,不合并其他类型皮疹;2级7例,合并其他类型的皮疹。予强效保湿乳剂处理可缓解皮肤干燥和紧绷感。
二、多种皮疹相继或同时发生
3例痤疮样皮疹与皮肤干燥、指/趾甲及甲周改变相继出现;1例痤疮样皮疹与皮肤干燥、毛发改变相继出现;2例痤疮样皮疹与指/趾甲改变相继出现;1例痤疮样皮疹与皮肤干燥相继出现;2例湿疹样皮疹与皮肤干燥相继出现;2例湿疹样皮疹与毛发改变、指/趾甲改变相继出现;2例麻疹样皮疹与痤疮样皮疹同时出现。
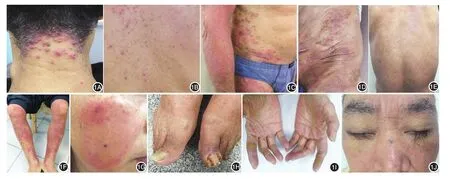
图1 酪氨酸激酶抑制剂相关皮肤不良反应患者的皮损表现 1A:头皮、颈后区多个丘脓疱疹;1B:背部散在分布红色丘疹、丘脓疱疹;1C:躯干、四肢鲜红色丘疹、鳞屑,融合成大片红斑、增厚;1D:腹部、下肢暗红色斑疹、斑丘疹,表面少许苔藓化,伴色素沉着;1E:躯干密集分布红色针尖大斑疹;1F:四肢密集分布针尖大红色丘疹、斑疹,部分融合;1G:面颊部红斑基础上可见毛细血管扩张及少许针尖大脓疱;1H:多个足趾甲板变脆、蚀损、裂隙以及变黄,甲周红肿、甲旁肉芽肿形成并结脓痂;1I:双手掌、手指黄色硬化性角化性斑疹和表皮剥脱;1J:眉毛、睫毛卷曲、变黑、变长

图3 湿疹样皮疹组织病理 角化不全,角质层内可见浆液渗出,棘层肥厚,上皮脚不规则延长,真皮浅层炎症细胞浸润,血管周围可见淋巴细胞及嗜酸性粒细胞浸润(箭头,3A:HE ×40;3B:HE× 400)
讨 论
EGFR抑制剂(EGFR inhibitors,EGFRI)是靶向抗肿瘤药物的第一大家族,常用于治疗非小细胞肺癌[4],包括EGFR酪氨酸激酶抑制剂(EGFR⁃tyrosine kinase inhibitors,EGFR⁃TKI)如厄洛替尼、吉非替尼、盐酸埃克以及奥斯替尼等。BCR⁃ABL酪氨酸激酶抑制剂包括伊马替尼和达沙替尼,应用于BCR⁃ABL阳性的白血病[5⁃6]。血管生成抑制剂如安罗替尼对某些实体瘤具有一定疗效[5⁃7]。以上酪氨酸激酶抑制剂在分子水平与致癌基因或蛋白特异性结合,选择性杀伤肿瘤细胞而不损伤正常细胞,因此较少引起骨髓抑制、心脏毒性、神经毒性等不良反应,但ACR却并不少见,如EGFRI引起的ACR发生率高达62%~91%[6,8]。
EGFRI引起的ACR表现基本一致,常见的包括痤疮样皮疹、指/趾甲及甲周改变、皮肤干燥、毛发异常,较少见的有毛细血管扩张等[6,9⁃11]。BCR⁃ABL 酪氨酸激酶抑制剂引起的ACR表现为麻疹样皮疹、痤疮、湿疹样皮疹、指甲改变和皮肤干燥等[5⁃6]。血管生成抑制剂常见的ACR包括手足综合征等[6⁃7]。本文对30例酪氨酸激酶抑制剂相关ACR进行分类、归纳和分析,发现痤疮样皮疹(15例)比例最高,其次为湿疹样皮疹(10例)、皮肤干燥(9例)和指/趾甲及甲周改变(7例),毛发改变(4例)、麻疹样皮疹(2例)的比例较低,而手足皮肤反应、毛细血管扩张这两种类型皮疹仅各1例。本文湿疹样皮疹见于口服厄洛替尼、吉非替尼、奥斯替尼和伊马替尼的患者,查阅目前国内外文献,BCR⁃ABL酪氨酸激酶抑制剂可引起湿疹样改变[12],尚未见文献报道厄洛替尼、吉非替尼和奥斯替尼等EGFR⁃TKI可引起类似改变。麻疹样皮疹分别出现于服用达沙替尼和埃克替尼的患者,文献报道伊马替尼和达沙替尼等BCR⁃ABL抑制剂可引起麻疹样皮疹[5⁃6],但未见埃克替尼等EGFRI引起该类型皮疹的报道。对于服用酪氨酸激酶抑制剂的患者,除了关注常见的ACR外,也需要警惕少见或罕见的ACR,以便及时作出相应的处理。以上结果及分析也说明,酪氨酸激酶抑制剂相关ACR皮疹形态各异,不同类型的酪氨酸激酶抑制剂可引起相同类别的ACR。
我们对痤疮样皮疹、血管水肿样皮疹和湿疹样皮疹这3种类型的ACR进行病理分析,发现痤疮样皮疹病理改变主要为毛囊口扩张、角化过度以及以中性粒细胞为主的炎症细胞浸润,与既往的研究基本一致。而血管性水肿样皮疹和湿疹样皮疹病理表现为具有嗜酸性粒细胞浸润的急、慢性过敏性改变,与传统的药疹或湿疹的病理改变相似。综合这两类皮疹的形态和病理特点,部分病例伴有外周血嗜酸性粒细胞比例升高,对糖皮质激素及抗过敏治疗敏感等,我们推测其发生机制与痤疮样皮疹的发病机制不同,可能与传统的药疹或湿疹的发病机制一致,涉及到迟发型变态反应。
[1]Fiala O,Pesek M,Finek J,et al.Skin rash as useful marker of erlotinib efficacy in NSCLC and its impact on clinical practice[J].Neoplasma,2013,60(1):26⁃32.doi:10.4149/neo_2013_004.
[2]Gridelli C,Maione P,Amoroso D,et al.Clinical significance and treatment of skin rash from erlotinib in non⁃small cell lung cancer patients:results of an Experts Panel Meeting[J].Crit Rev Oncol Hematol,2008,66(2):155 ⁃162.doi:10.1016/j.critrevonc.2007.10.004.
[3]Common Terminology Criteria for Adverse Events[CTCAE]v4.0.US DepartmentofHealth and Human Services.National Institutes of Health.National Cancer Institute[OL].May 28,2009.Available from: URL:http://evs.nci.nih.gov/ftp1/CTCAE/CTCAE_4.03_2010⁃06⁃14_QuickReference_5x7.pdf.
[4]Johnston JB,Navaratnam S,Pitz MW,et al.Targeting the EGFR pathway for cancer therapy[J].Curr Med Chem,2006,13(29):3483⁃3492.
[5]Macdonald JB,Macdonald B,Golitz LE,et al.Cutaneous adverse effects of targeted therapies.Part I:Inhibitors of the cellular membrane[J].J Am Acad Dermatol,2015,72(2):203⁃218;quiz 219⁃220.doi:10.1016/j.jaad.2014.07.032.
[6]Reyes⁃Habito CM,Roh EK.Cutaneous reactions to chemothera⁃peutic drugs and targeted therapy for cancer:Part II.Targeted therapy[J].J Am Acad Dermatol,2014,71(2):217.e1⁃217.e11;quiz 227⁃228.doi:10.1016/j.jaad.2014.04.013.
[7]Sun Y,Niu W,Du F,et al.Safety,pharmacokinetics,and antitumor properties of anlotinib,an oral multi⁃target tyrosine kinase inhibitor,in patients with advanced refractory solid tumors[J].J Hematol Oncol,2016,9(1):105.doi:10.1186/s13045⁃016⁃0332⁃8.
[8]Holcmann M,Sibilia M.Mechanisms underlying skin disorders induced by EGFR inhibitors[J].Mol Cell Oncol,2015,2(4):e1004969.doi:10.1080/23723556.2015.1004969.
[9]Segaert S,Van Cutsem E.Clinical signs,pathophysiology and management of skin toxicity during therapy with epidermal growth factor receptor inhibitors[J].Ann Oncol,2005,16(9):1425⁃1433.doi:10.1093/annonc/mdi279.
[10]Lacouture ME,Anadkat MJ,Bensadoun RJ,et al.Clinical practice guidelines for the prevention and treatment of EGFR inhibitor⁃associated dermatologic toxicities[J].Support Care Cancer,2011,19(8):1079⁃1095.doi:10.1007/s00520⁃011⁃1197⁃6.
[11]Abdullah SE,Haigentz M,Piperdi B.Dermatologic toxicities from monoclonal antibodies and tyrosine kinase inhibitors against EGFR:pathophysiology and management[J].Chemother Res Pract,2012,2012:351210.doi:10.1155/2012/351210.
[12]Štulhofer BD,Martinac I,Ledic DD,et al.Adverse reaction to cetuximab,an epidermal growth factor receptor inhibitor[J].Acta Dermatovenerol Croat,2016,24(1):70⁃72.

