血栓弹力图指导氯吡格雷用于经皮冠状动脉介入术后抗血小板治疗的临床预后观察
申文彬,杨 霞,焦云娟,牛 倩,程庆强,周思远,王 禹
1解放军371医院 心内科,河南新乡 453000;2解放军总医院 心内科,北京 100853;3新乡医学院基础医学院病理教研室,河南新乡 453000;4新乡医学院 药学院,河南新乡 453000
双联抗血小板(阿司匹林+氯吡格雷)已成为经皮冠状动脉介入术(percutaneous coronary intervention,PCI)后预防主要不良心血管事件(major adverse cardiovascular events,MACE)的经典方法。人群对于阿司匹林药物反应差异性较小(药物反应较好)。然而,由于人群氯吡格雷药物代谢基因型(细胞色素P450基因超家族,CYP)不同、合并糖尿病或钙化、急性冠状动脉综合征等因素,导致氯吡格雷药物抵抗(血小板高反应性)的发生率约为1/3,进而显著增加了MACE的发生率[1]。文献报道,双倍负荷剂量(600 mg)或双倍维持剂量(150 mg,1次/d)的氯吡格雷可降低血小板高反应(high platelet reactivity,HPR)的发生率,进而降低MACE发生率[2-3]。文献提示新一代环戊三唑嘧啶药物-可逆性血小板受体抑制剂替格瑞洛可显著降低HPR发生率,且不存在更高的出血风险[3-4]。本研究旨在探讨个体化指导维持剂量的氯吡格雷与替格瑞洛的抗血小板效果是否存在差异及其对临床预后的影响。
对象和方法
1 研究对象 选取2015年8月- 2016年8月于解放军总医院心血管内科行冠状动脉PCI介入治疗患者263例。入选标准:年龄>18岁;行冠脉PCI介入治疗。排除标准:对阿司匹林或硫酸氢氯吡格雷过敏;不能持续口服双联抗血小板药物达到12个月;同时服用华法林等抗凝药物;eGFR<30 ml/(min·1.73 m2);预期寿命<1年。按随机数字表法分为氯吡格雷组(123例)和替格瑞洛组(140例),两组基线资料差异无统计学意义(P>0.05)。见表1。

表1 氯吡格雷组和替格瑞洛组基线资料比较Tab. 1 Clinical characteristics of patients in the two groups
2 两组用药方法 1)氯吡格雷组:术前给予300 mg负荷剂量。之后采用血栓弹力图检测抗血小板效果(TEG 5000凝血分析仪,唯美血液技术医疗器械国际贸易有限公司)。ADP诱导的HPR定义为血小板聚集率≥50%[5]。HPR患者(氯吡格雷组有27例HPR患者)使用150 mg、1次/d剂量维持3个月后改用75 mg、1次/d至12个月,非HPR患者采用75 mg、1次/d共12个月;2)替格瑞洛组:以负荷剂量180 mg口服,之后改用90 mg、2次/d维持12个月。所有患者均同时服用阿司匹林(100 mg,1次/d),维持12个月。检测血栓弹力图的要求:两组患者均应用标准双联抗血小板治疗,阿司匹林100 mg/d,>5 d;硫酸氢氯吡格雷75 mg/d,>5 d,或者300 mg顿服12 h以上以及替罗非班停用24 h以上。检测患者的花生四烯酸(arachidonic acid,AA)及ADP诱导的血小板聚集率。
3 冠状动脉造影及PCI 选择经桡动脉或股动脉入路,使用6F或7F动脉鞘,桡动脉入路时常规动脉鞘内给予盐酸维拉帕米注射液1 mg,冠状动脉造影后对狭窄血管进行介入干预,包括球囊扩张(切割球囊、顺应性球囊、非顺应性球囊)、支架置入、血栓抽吸等。术中采用比伐芦定或肝素抗凝。根据美国心脏病协会的标准,支架置入成功定义为残余管腔狭窄<25%,无内膜撕裂或夹层,PCI术后血流TIMI 3级[6]。
4 随访及相关定义 所有患者在PCI术后满12个月进行电话随访。MACE:支架内血栓、脑卒中、靶血管再次血运重建、心源性死亡、胸痛症状再发作(包括心电图ST段改变)、因胸痛再次入院治疗。支架内血栓:明确的支架内血栓,即由造影确认的支架内血栓。心源性死亡:由任何心脏原因导致的死亡,也包括未知原因的死亡、与PCI手术并发症相关的死亡。脑卒中:任何原因引起的缺血性或出血性事件所导致的脑局部神经功能障碍,至少持续24 h。靶血管再次血运重建:靶血管的任何再次介入或者冠脉旁路移植治疗,其中靶血管包括处理病变血管的上游、下游和分支血管。胸痛症状再次发作:胸痛症状较术后明显加重,包括活动后、静息时以及胸痛时心电图改变。因胸痛再次入院治疗:术后因为胸痛再次入院治疗,不包括正常复查[6]。
5 统计学方法 采用SPSS17.0统计软件进行统计分析,计量资料以-x±s表示,符合正态分布和方差齐性时,采用独立样本的t检验;不符合正态分布或方差不齐时,采用独立样本的秩和检验。计数资料采用例数(构成比)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
结 果
1 两组术中PCI资料比较 两组单支病变、双支病变、3支病变、左主干病变、左前降支病变、左回旋支病变、右冠状动脉病变、置入支架数量、支架总长度、支架直径、球囊预扩张比例、球囊预扩张压力、支架释放压力、球囊后扩张比例、球囊后扩张压力以及球囊数量差异无统计学意义(P均>0.05)。见表2。
2 两组MACE发生率比较 氯吡格雷组27例(22.0%)为HPR,氯吡格雷维持剂量更改为150 mg、1次/d,3个月后将剂量调整为75 mg、1次/d,共12个月。两组中,支架内血栓、靶血管再次血运重建、心绞痛再发作、心源性死亡差异无统计学意义(P>0.05)。氯吡格雷组因胸痛再入院发生率(4.9% vs 0.7%,P=0.042)、MACE发生率显著高于替格瑞洛组(13.0% vs 5.0%,P=0.022)。见表3。
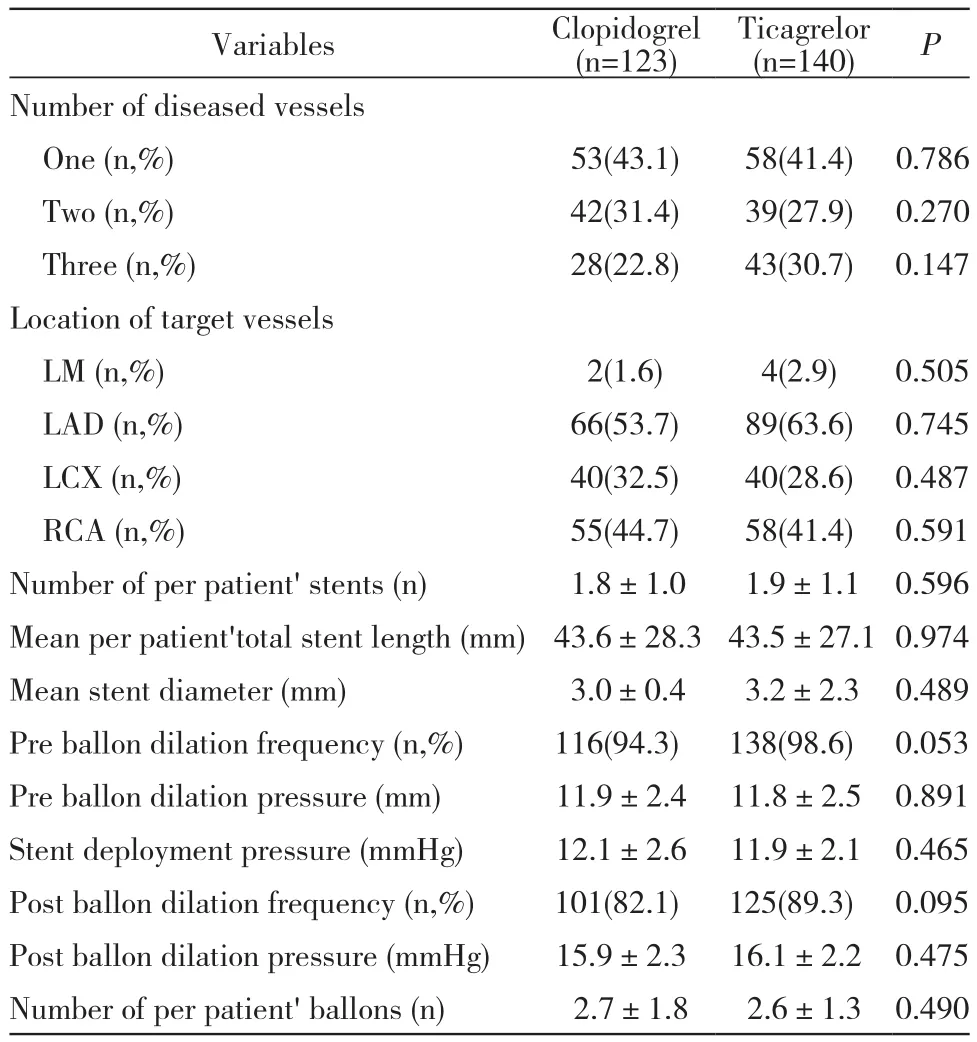
表2 两组PCI术中资料比较Tab. 2 Clinical characteristics of patients during PCI

表3 两组MACE发生率比较Tab. 3 Incidence of MACE in patients between the two groups (n, %)
讨 论
双联抗血小板已成为PCI术后预防MACE发生的经典方法。然而,人群中不同程度地存在氯吡格雷药物抵抗现象[2,7]。本研究提示,在123例使用氯吡格雷药物的患者中有27例存在氯吡格雷药物抵抗现象,发生率为22.0%,与既往研究结果相似(21%)[8]。文献报道,降低氯吡格雷药物抵抗的方法有多种,如双倍负荷剂量氯吡格雷、高剂量氯吡格雷维持剂量(150 mg甚至更高剂量)、更换氯吡格雷为新一代ADP诱导的血小板抑制剂(第三代噻吩并吡啶药物普拉格雷或环戊基三咗嘧啶类药物替格瑞洛)[9-10]。本研究针对HPR患者将氯吡格雷维持剂量调整为150 mg、1次/d,并维持3个月,之后改为75 mg、1次/d;另外一组未行血栓弹力图检测,直接使用替格瑞洛。随访12个月结果提示,氯吡格雷组MACE发生率仍显著高于替格瑞洛组。
与氯吡格雷等噻吩并吡啶药物不同,替格瑞洛是一种新型可逆的、直接起效的ADP途径抗血小板药物,拥有更强的血小板抑制效果,且起效更迅速。口服替格瑞洛负荷剂量(180 mg)后30 min可以达到口服氯吡格雷600 mg后8 h的同等效果,且停用该药物后2 ~ 3 d其抗血小板效果即可消失,针对不同类型的急性冠状动脉综合征患者可更灵活的使用。而噻吩并吡啶作为一种不可逆的ADP途径抗血小板药物,需要停用3 ~ 5 d后抗血小板药效才能完全消失[4]。另外,替格瑞洛的抗血小板效果更强,药物反应差异较小,HPR发生率更低。研究提示,替格瑞洛较氯吡格雷PCI术后的MACE发生率更低,且没有增加主要出血风险[11]。
既往研究提示,双倍剂量(150 mg)的氯吡格雷维持剂量较75 mg的维持剂量,抗血小板效果更优,发生HPR的概率更低,且PCI术后伴随着更低的MACE发生概率[3,5,10,12]。也有文献报道,双倍剂量的氯吡格雷较替格瑞洛抗血小板效果差[13]。既往研究也提示,糖尿病患者往往伴随着更高的HPR发生率,针对糖尿病患者使用双倍剂量的氯吡格雷,虽然可以降低HPR的发生率[1,14-15],但60%的患者存在较差的药物反应[7]。氯吡格雷需要通过肝两步代谢才能成为有活性的前体药物。CYP2C19是关于代谢中非常重要的基因,其野生型主要为CYP2C19*1型[16-18]。当基因突变为CYP2C19*2或者CYP2C19*3[2,9,19],人群中发生HPR的概率明显升高。突变可以发生在一个等位基因或者两个等位基因位点上[1]。针对HPR患者,当患者只有一个位点突变时,使用双倍剂量的氯吡格雷,其降低HPR的效果与未发生基因突变的患者相似[2]。但是对于两个基因位点均发生变异者,即使将氯吡格雷的维持剂量增加到300 mg,其降低HPR的效果仍然较差[2]。正是由于糖尿病、基因突变等综合因素,导致了对于HPR患者即使使用双倍剂量的氯吡格雷,药物抵抗概率仍较高,且伴随着更高的MACE发生率[4,7]。而替格瑞洛由于其本身即为活性前体药物,具有不需通过CYP2C19代谢等特殊优势、更好的抗血小板效果和临床预后[20-21]。本研究不足之处是样本量较少,观察时间较短,其有效性和安全性还有待大样本多中心临床研究进一步评价。
1 Ford NF, Taubert D. Clopidogrel, CYP2C19, and a Black Box[J].J Clin Pharmacol, 2013, 53(3): 241-248.
2 Zhang L, Yang J, Zhu X, et al. Effect of high-dose clopidogrel according to CYP2C19*2 genotype in patients undergoing percutaneous coronary intervention- a systematic review and metaanalysis[J]. Thromb Res, 2015, 135(3): 449-458.
3 Chen S, Zhang Y, Wang L, et al. Effects of Dual-Dose Clopidogrel,Clopidogrel Combined with Tongxinluo Capsule, and Ticagrelor on Patients with Coronary Heart Disease and CYP2C19*2 Gene Mutation After Percutaneous Coronary Interventions (PCI)[J]. Med Sci Monit, 2017, 23 : 3824-3830.
4 Steg PG, James S, Harrington RA, et al. Ticagrelor versus clopidogrel in patients with ST-elevation acute coronary syndromes intended for reperfusion with primary percutaneous coronary intervention: A Platelet Inhibition and Patient Outcomes (PLATO) trial subgroup analysis[J]. Circulation, 2010, 122(21): 2131-2141.
5 Chirumamilla AP, Maehara A, Mintz GS, et al. High platelet reactivity on clopidogrel therapy correlates with increased coronary atherosclerosis and calcification: a volumetric intravascular ultrasound study[J]. JACC Cardiovasc Imaging, 2012, 5(5):540-549.
6 Cutlip DE, Windecker S, Mehran R, et al. Clinical end points in coronary stent trials: a case for standardized definitions[J].Circulation, 2007, 115(17): 2344-2351.
7 Angiolillo DJ, Shoemaker SB, Desai B, et al. Randomized comparison of a high clopidogrel maintenance dose in patients with diabetes mellitus and coronary artery disease: results of the Optimizing Antiplatelet Therapy in Diabetes Mellitus (OPTIMUS)study[J]. Circulation, 2007, 115(6): 708-716.
8 Lundström A, Laska AC, Von Arbin M, et al. Glucose intolerance and insulin resistance as predictors of low platelet response to clopidogrel in patients with minor ischemic stroke or TIA[J].Platelets, 2014, 25(2): 102-110.
9 Geisler T, Anders N, Paterok M, et al. Platelet response to clopidogrel is attenuated in diabetic patients undergoing coronary stent implantation[J]. Diabetes Care, 2007, 30(2): 372-374.
10 Stone GW, Witzenbichler B, Weisz G, et al. Platelet reactivity and clinical outcomes after coronary artery implantation of drug-eluting stents (ADAPT-DES): a prospective multicentre registry study[J].Lancet, 2013, 382(9892): 614-623.
11 Wallentin L, Becker RC, Budaj A, et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes[J]. N Engl J Med, 2009, 361(11): 1045-1057.
12 Diodati JG, Saucedo JF, Cardillo TE, et al. Transferring from clopidogrel loading dose to prasugrel loading dose in acute coronary syndrome patients. High on-treatment platelet reactivity analysis of the TRIPLET trial[J]. Thromb Haemost, 2014, 112(2): 311-322.
13 Gu X, Fu X, Wang Y, et al. Comparison of ticagrelor and highdose clopidogrel on the platelet functions in patients with inadequate response to clopidogrel[J]. Am J Cardiovasc Dis, 2017, 7(1): 1-8.
14 Borissoff JI, Joosen IA, Versteylen MO, et al. Accelerated in vivo thrombin formation independently predicts the presence and severity of CT angiographic coronary atherosclerosis[J]. JACC Cardiovasc Imaging, 2012, 5(12): 1201-1210.
15 Ferreira IA, Eybrechts KL, Mocking AI, et al. IRS-1 mediates inhibition of Ca2+ mobilization by insulin via the inhibitory G-protein Gi[J]. J Biol Chem, 2004, 279(5): 3254-3264.
16 Guirgis M, Thompson P, Jansen S. Review of aspirin and clopidogrel resistance in peripheral arterial disease[J]. J Vasc Surg, 2017, 66(5): 1576-1586.
17 Vyas A, El Accaoui R, Blevins A, et al. Outcome comparison of 600 mg versus 300 mg loading dose of clopidogrel for patients with ST-elevation myocardial infarction : a meta-analysis[J]. Postgrad Med, 2014, 126(5): 176-186.
18 Yun KH, Mintz GS, Witzenbichler B, et al. Relationship Between Platelet Reactivity and Culprit Lesion Morphology: An Assessment From the ADAPT-DES Intravascular Ultrasound Substudy[J].JACC Cardiovasc Imaging, 2016, 9(7): 849-854.
19 Muller O, Hamilos M, Bartunek J, et al. Relation of endothelial function to residual platelet reactivity after clopidogrel in patients with stable angina pectoris undergoing percutaneous coronary intervention[J]. Am J Cardiol, 2010, 105(3): 333-338.
20 柳杨, 李运田, 王小冬, 等. 替格瑞洛在老年冠脉病变介入治疗中的疗效及安全性分析[J]. 解放军医学院学报, 2017, 38(5):423-425.
21 李彦平, 刘宏斌, 贾倩, 等. 冠心病合并糖尿病患者药物洗脱支架置入术后远期疗效观察[J]. 解放军医学院学报, 2013, 34(5): 428-430.

