Cobase602全自动免疫分析仪检测胃泌素释放肽前体的性能分析
林丽珍,王建伟,郑钦钦
(1、厦门大学附属福州市第二医院检验科,福建 福州 350007;2、福建省立医院南院福建省立金山医院检验科,福建 福州350008)
小细胞肺癌(SCLC)生长迅速,易复发及早期转移,而对放疗和化疗敏感,因此,对其早期诊断和合理治疗尤为重要[1-4]。神经元特异性烯醇化酶(NSE)是公认的SCLC肿瘤标志物,已应用于临床多年。血清胃泌素释放肽前体(ProGRP)是目前应用较活跃的新的SCLC肿瘤标志物,正逐步用于临床[4,5]。 酶联免疫吸附试验(ELISA)是 ProGRP 相对经典的检测方法,随着技术的不断革新,电化学发光检测ProGRP正被广泛应用。采用电化学发光法,可以及时检测,自动化程度更高,减少人工误差,同时可大大缩短检测时间[6]。根据ISO15189医学实验室认可标准[7,8],必须对其检测系统进行性能评价,本文通过分析其精密度、线性、回收率、参考范围等,从而评价该法对ProGRP检测的性能。
1 材料与方法
1.1 标本来源 来自2016年5月13日至5月17日福建省立金山医院免疫实验室接收的23份我院国内体检健康人血清标本。
1.2 仪器与试剂
1.2.1 试剂 胃泌素释放肽前体检测试剂盒(批号:190275)、胃泌素释放肽前体定标液(18819)、胃泌素释放肽前体质控液(低水平批号:186304,高水平批号:186305),试剂均来自上海罗氏诊断产品有限公司。
1.2.2 仪器 Roche Cobase602全自动免疫分析仪(上海罗氏诊断产品有限公司)。
1.3 检测方法
1.3.1 精密度评价 按照CLSI EP15-A2标准:2个浓度水平,5d实验,每天一批,每批每个水平重复测定3次。
1.3.2 线性评价 选择低浓度(L)和高浓度(H)患者标本各1份,浓度覆盖仪器说明书给出的线性范围,H和L按等比关系配制形成系列浓度血清( 如 :1L,0.8L+0.2H,0.6L+0.4H,0.4L+0.6H,0.2L+0.8H,1H)。每个实验样品在检测系统上重复测定2次,记录结果。将实测值与预期值作比较。采取平均斜率来确定系列样品应含有的待测物的预期值(X),所有样品重复测定的均值为实测值(Y),将所有结果点在X-Y坐标图上,计算回归方程:Y=bX+a。1.3.3 回收率 选择一患者标本 (浓度为 28.6pg/ml)为基础样本,取 900μl基础样本和 100μl蒸馏水作为对照样本,分别取900μl基础样本、10μl浓度为224Pg/ml和90μl蒸馏水作为回收样品1;取900μl基础样本、60μl浓度为 224Pg/ml和 40μl蒸馏水作为回收样品2;取900μl基础样本、90μl浓度为224Pg/ml和10μl蒸馏水作为回收样品3。每份样品在检测系统上测定2次,取平均值。根据以下公式计算回收率:回收率=回收浓度/加入浓度×100%;回收浓度=最终测定浓度-基础样本浓度;加入浓度=标准品浓度×标准品体积/(标准品体积+基础样本体积)[9]。
1.3.4 参考区间 参考 NCCLSC28-A2, 通过测定23份我院国内体检健康人血清标本,对<69.2Pg/ml的生物参考区间进行验证;若20份标本的检测结果均在参考区间内或仅有2个标本超出,则验证通过。否则,进行参考区间确立实验。
1.4 统计学方法 所有统计学处理均在SPSS 20.0统计软件包以及EXCEL表格上进行。线性评价中,计算出回归方程:Y=bX+a。若相关系数r≥0.975,b 在 0.95~1.05 范围内,a 接近于 0 (小于高值标本浓度的1%),则可判断线性范围;若a不接近于 0,则做 a 与 0 差异的 t检验,若 t<t(0.05,v),v=n-2,说明截距是由统计引入的,实际的标准曲线能通过原点,该测定方法在实验涉及的浓度范围内呈线性。
2 结果
2.1 精密度验证 低、高水平样本检测的批内精密度均<1/4TEa,批间精密度均<1/3TEa。该检测方法的批内及批间精密度均符合厂家要求小于10%(见表 1)。

表1 精密度验证结果
2.2 线性范围验证 ProGRP 在 10.59~1565.5pg/ml范围内具有良好线性关系 (厂家线性范围3~5000Pg/ml),R2=0.9975,b=0.985 在 0.95~1.05 范围内;a=5.086,经t检验显示 a与 0无显著性差异(P>0.05)(见表 2,如图 1)。
2.3 回收实验 根据相关公式计算的检测平均回收率为 100.8%(见表 3)。
2.4 参考区间 参考区间为<69.2Pg/ml。其中23份标本全部在该参考范围内,所检测的结果100%在参考范围之内,大于允许值90%,因此我室目前的参考范围经验证可用。(见表4)
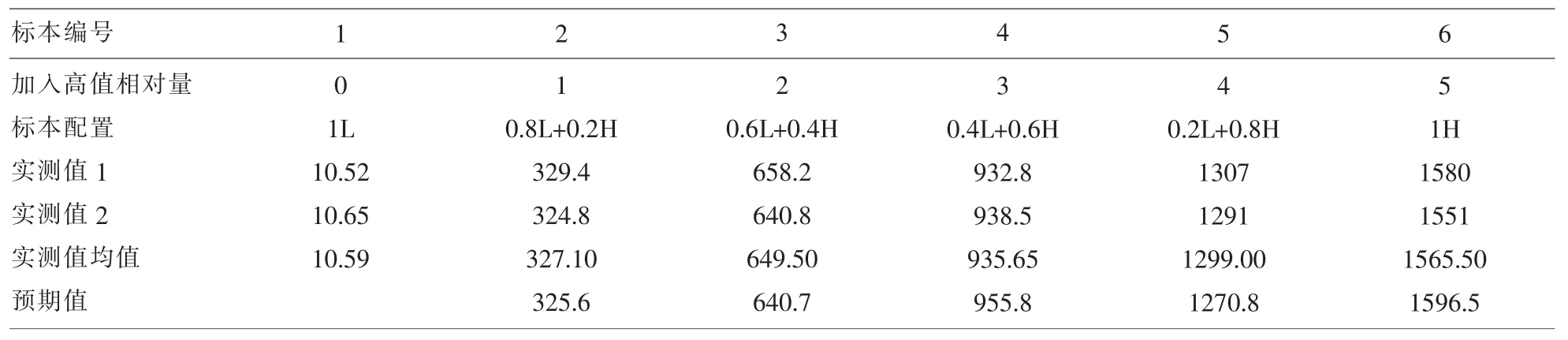
表2 线性范围验证结果
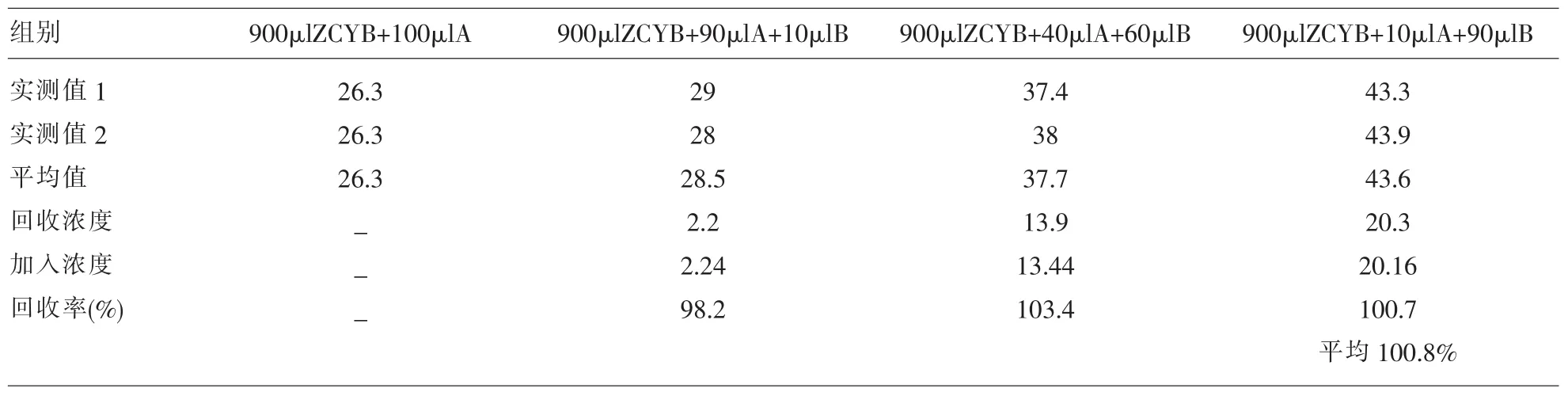
表3 回收实验结果
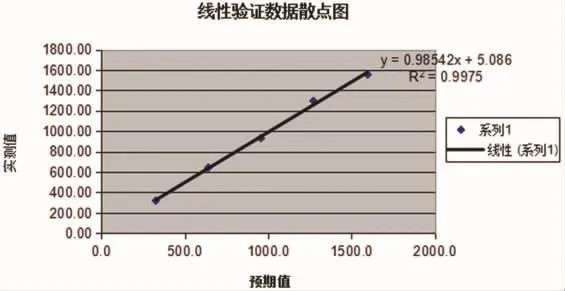
图1 线性验证数据散点图
3 讨论
肺癌是一种常见的恶性肿瘤,具有恶性度高、发病快等特点。小细胞肺癌占肺癌的20%~25%,是一种未分化、恶性程度高、病因复杂的恶性肿瘤,其生长迅速,易早期转移,且对放疗和化疗高度敏感,SCLC的早期诊断是提高疗效的关键。然而早期SCLC缺乏特异性症状和体征,影像学检查在SCLC早期诊断中具有很大的局限性。SCLC相关血清肿瘤标志物检测具有较高的灵敏度,血液标本易获取和无创等特点,在SCLC的诊断及治疗过程中日益受到重视[10,11]。神经元特异性烯醇化酶(NSE)作为SCLC标记物,其应用于临床诊断已多年,但在局限性SCLC诊断中,常出现阳性率过低,标本易受溶血、脂血影响[12,13]。胃泌素释放肽前体(ProGRP)是目前应用较活跃的一种新的小细胞肺癌肿瘤标志物,其敏感性、特异性和可靠性均优于NSE,作为诊断小细胞肺癌最明确的指标正逐步用于临床。
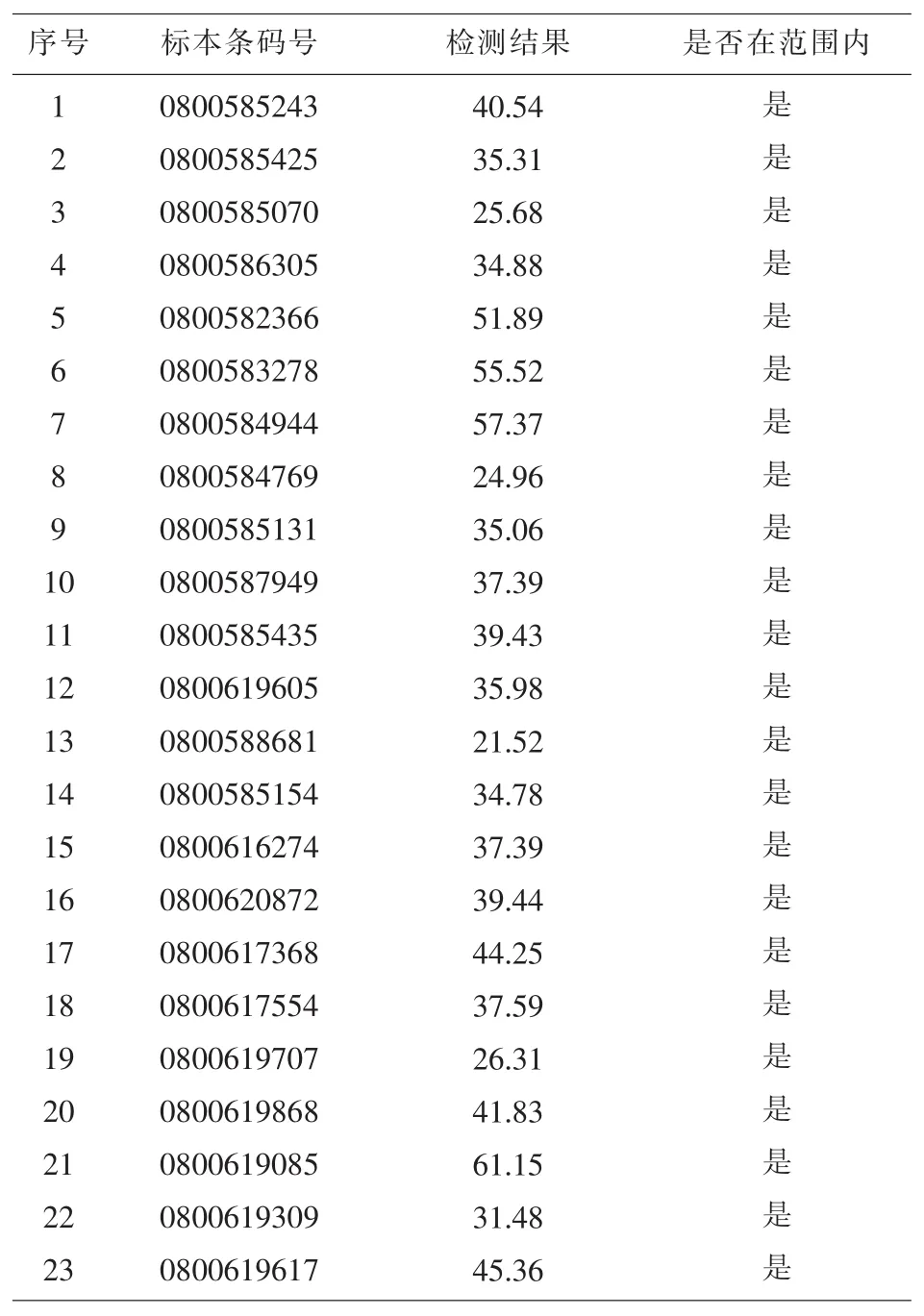
表4 参考区间验证结果
ProGRP是胃泌素释放肽(GRP)的前体结构。而GRP和ProGRP在肿瘤的发生、发展及其治疗中起着重要的作用。ProGRP显示GRP水平和GRP基因表达,是SCLC的一种新的肿瘤标志物,在国内外已经得到广泛应用。由于SCLC具有神经内分泌肿瘤的性质,因此ProGRP和NSE在SCLC的诊断中具有良好的诊断价值[14,15]。酶联免疫吸附试验(ELISA)检测ProGRP相对经典的检测方法,然而由于手工方法加样、洗涤,温育、制作标准曲线等操作步骤多,则重复性较差,人为误差较大,这就迫切需要革新技术,全自动电化学发光应运而生。在Cobase602全自动化免疫分析仪上用电化学发光法检测检测胃泌素释放肽前体(ProGRP)重复性好,人为误差小。
对检测系统或检测方法进行性能评价是临床检验质量管理的重要内容。精密度是反映检测系统整体性能的首要指标,也是进行其他方法学验证实验的前体[16]。本研究精密度评价实验按照EP15-A2文件进行,实验数据显示在Cobase602全自动化免疫分析仪上用电化学发光法检测检测胃泌素释放肽前体(ProGRP),其低、高水平批内精密度均<1/4TEa,批间精密度均<1/3TEa,均小于厂家声明的最小CV。线性评价实验根据CLSI EP6-A文件,采用简便的平均斜率法,结果显示在Cobase602全自动化免疫分析仪上用电化学发光法检测检测胃泌素释放肽前体 (ProGRP),在3-5000Pg/ml范围内具良好线性关系 (Y=0.9854X+5.0860,R2=0.9975),达到厂家的检测声明。 在定量分析验证时,准确度通常可用回收率表示,回收率越接近100%表明分析方法准确度越高。本研究回收实验结果显示,基于磁珠法的HBVDNA检测回收率为100.8%,接近100%,准确度高[17]。根据NCCLSC28-A2, 参考区间为<69.2pg/ml验证试验通过。总之,在Cobase602全自动化免疫分析仪上用电化学发光法检测检测胃泌素释放肽前体(Pro-GRP),实现了快速缩短检测时间、重复性好、人为误差小,具有良好检测性能,适合临床实验室推广使用。
[1]Genereux P,Palmerini T,Caixeta A,et al.Quantification and impact of untreated coronary artery disease after percutaneous coronary intervention:the residual SYNTAX (Synergy Between PCI with Taxus and Cardiac Surgery)score[J].J Am Coll Cardiol,2012,59(24):2165-2174.
[2]张淑艳,胡晓芳.NSE和ProGRP联合检测在小细胞肺癌中的应用价值[J].中国热带医学,2015,15(4):466-467.
[3]吴培生,徐爱晖.胃泌素释放肽前体在小细胞肺癌中的表达水平及其意义[J].中国全科医学,2014,17(32):3885-3886.
[4]刘青,黄幼芳等.胃泌素释放肽前体和神经元特异性烯醇化酶联合检测在小细胞肺癌诊断中的价值[J].临床军医杂志,2014,42(6):641-642.
[5]Oremek GM,Sapoutzis N.Progastrin releasing peptide(ProGRP),tumor marker for small cell lung cancer[J].Antica Res,2003,23(2A):895-898.
[6]张海茂,周爱凤,张蓉.胃泌素释放肽前体检测对小细胞肺癌诊治的表意义[J].中国医药指南,2014,12(27):228-229.
[7]王建伟,孙嘉锋,黄毅.基于NP968自动核酸提取仪(磁珠法)的实时荧光定量PCR系统检测HBVDNA的性能评价 [J].实验与检验医学,2015,33(5):563-564.
[8]魏旱,丛玉隆.医学实验室质量管理与认可指南[M].北京:中国计量出版社,2004:59-75.
[9]申子瑜,李萍.临床实验室管理学[M].人民卫生出版社,2003:145.
[10]陈岩松,陈燕.血清 ProGRP、CYFRA21-1、CA125 三项肿瘤标志物联合检测在肺癌诊断中的应用[J].现代诊断与治疗,2014,25(16):3608-3609.
[11]Iheas P,Casent JM.PET-CT in the staging and treatment of nonsmall-cell lung cancer[J].Clin Transl Oncol,2011,13:368-377.
[12]Frangopoulos F,Perros I,Simou G,et al.Clc053poster pro-gastrin-releasing peptide as a tumour marker of small-cell lung cancer:the first comparative evaluation with neuron-specific enolase in Greek population[J].Lung Cancer,2007,55:13-13.
[13]黄梅香,梁艺华等.胃泌素释放肽前体在小细胞肺癌诊断及治疗中应用[J].现代仪器与医疗,2015,21(3):82-84.
[14]Isenstein EM,Williams CB.The Treg/Th17cell balance:a new paradigm for auto immunity[J].PediatricRes,2009,65(24):26-31.
[15]程真珍,冶薇,封敏.胃泌素释放肽前体对小细胞肺癌诊断和预后的临床意义[J].检验医学和临床,2015,12(11):1499-1502.
[16]朱安友,王凤超等.ARCHITECT i2000SR化学发光分析仪检测胃泌素释放肽前体的性能评价[J].国际检验医学杂志,2013,34(15):2019-2020.
[17]王建伟,孙嘉锋,黄毅.基于NP968自动核酸提取仪(磁珠法)的实时荧光定量PCR系统检测HBVDNA的性能评价 [J].实验与检验医学,2015,33(5):566-567.

