NRS 2002在骨肉瘤化疗患者营养管理中的应用
蒋艳华,曾定芬,王晓芹,张 芹
四川省肿瘤医院(成都 610041)
恶性肿瘤患者营养不良是常见并发症,具有增加患者并发症、造成器官功能障碍和生活质量下降等危害,并影响患者肿瘤治疗顺利进行和生存时间。营养支持治疗的关键在于早期准确判断患者的营养状况和营养不良风险,并及时给予营养干预[1]。骨肉瘤是常见的原发恶性骨肿瘤,恶性程度极高,随着新辅助化疗的开展,越来越多的骨肉瘤患者可进行保肢治疗,生存时间延长,其5年生存率为60%~70%[2]。目前,新辅助化疗(化疗-手术-化疗)已成为骨肉瘤化疗的标准方案,基本药物包括阿霉素(ADM)、顺铂(DDP)、甲氨蝶呤(MTX)和异环磷酰胺(IFO),AP方案(ADM+DDP)为骨肉瘤主要化疗方案之一,消化道不良反应为化疗主要毒性反应之一[3]。骨肉瘤患者在接受化疗过程中,会出现不同程度的胃肠道反应,如恶心呕吐、腹胀腹泻、食欲减退等,导致患者营养摄入不足,引起并发症增加、生活质量下降,影响肿瘤的治疗和患者生存时间。NRS 2002在食管癌、肝癌、胰腺癌、胃癌、结直肠癌等恶性肿瘤患者营养筛查中的应用均取得较好的效果[4-5],而用于骨肉瘤营养筛查鲜有报告。四川省肿瘤医院自2015年4月至2016年3月对收治的采用AP方案化疗的44例骨肉瘤患者采用NRS 2002进行营养风险筛查和评估,对存在营养风险的患者给予营养治疗,取得了良好的效果,现报道如下。
1 资料与方法
1.1 临床资料
选择2014年4月至2016年3月四川省肿瘤医院收治的采用AP方案化疗的骨肉瘤患者82例为研究对象。纳入标准:1)经过病理确诊为骨肉瘤需行化疗的患者;2)化疗方案为AP方案;3)患者已签署化疗知情同意书。排除标准:1)患者因病情进展调整化疗方案;2)因经费社会支持等营养不良之外因素终止化疗者;3)转诊到基层医院继续化疗者。
其中2014年4月至2015年3月的38例患者为对照组,2015年4月至2016年3月的44例患者为观察组。其中对照组男23例,女15例,年龄8~45岁;观察组男26例、女18例,年龄9~44岁。两组患者计划化疗6周期,化疗期间指导进食营养丰富的食物。两组患者的性别、年龄、疾病分期和化疗前营养状况比较差异无统计学意义(P>0.05)(表1)。
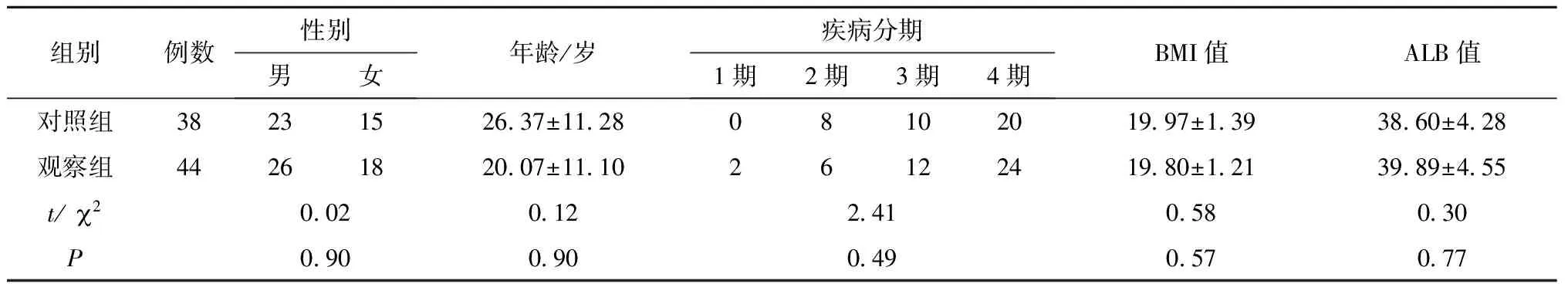
表1 两组患者一般情况比较
1.2 方法
1.2.1 对照组营养评估 采用生活质量(QOL)评分中的食欲条目评分进行营养评估。食欲条目评分标准如下(括号内为得分):几乎不能进食(1);食量<正常1/2(2);食量为正常的1/2(3);食量略少(4);食量正常(5)。评估1次/周,当QOL食欲评分≤3分时给予营养干预。对照组38例患者共采用QOL食欲条目进行营养评估648次。
1.2.2 观察组营养评估 采用NRS 2002进行动态营养评估。NRS 2002主要包括3方面内容:1)营养状况,根据营养受损情况评分0~3 分; 2)疾病情况,根据患者疾病的严重程度评分0~3 分;3)年龄,患者年龄<70岁者不加分、≥70 岁者加1 分,总分计算方法为3项评分相加,总分为 0~7 分。当评分总分值≥3分时,表明患者处于营养风险,开始制定和实施营养治疗计划;当评分总分值<3分,患者虽没有营养风险,但应在其住院期间每周进行1 次营养筛查[6]。评估1次/周,当NRS 2002评分≥3分时给予营养干预。观察组44例患者共采用NRS 2002进行营养评估667次。
1.2.3 营养干预方案 两组营养风险筛查阳性患者均采用一致的干预方案,包括营养教育、口服补充、肠内营养和肠外营养,通过每周评估体质量指数(BMI)和每3周复查血清白蛋白(ALB)进行效果评价。
1.3 观察指标
观察两组患者首次化疗前和化疗期间营养风险筛查结果阳性率(QOL食欲评分≤3分或NRS2002评分≥3分例次占总评估例次的百分比)、BMI<18.5或ALB<35 g/L的发生率和因营养不良终止化疗的发生率。观察终点为患者化疗6周期结束后或化疗终止后1月。
1.4 统计学方法
所有数据采用 SPSS 17.0 软件进行分析处理,计数资料采用2检验,计量资料采用两独立样本的非参数检验,检验水准α除特别说明外均设定为0.05。
2 结果
两组患者营养风险的阳性结果率、营养不良发生率和因营养不良致化疗终止的发生率比较,差异有统计学意义(P<0.05)(表2~4)。
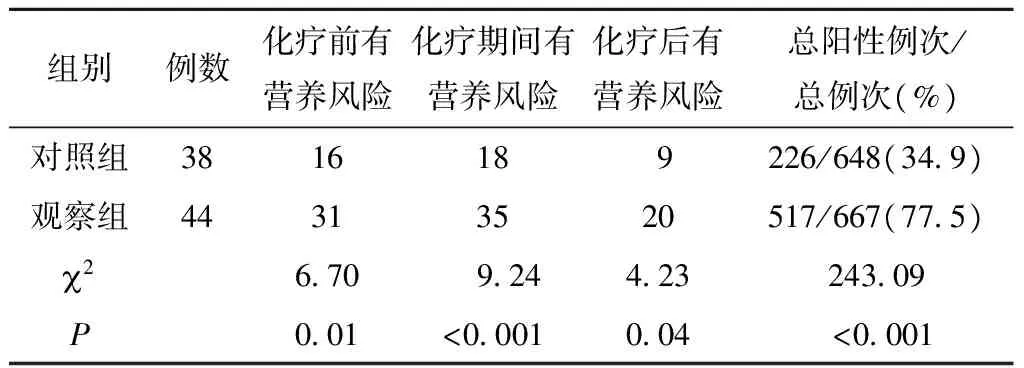
表2 两组患者营养风险筛查情况比较
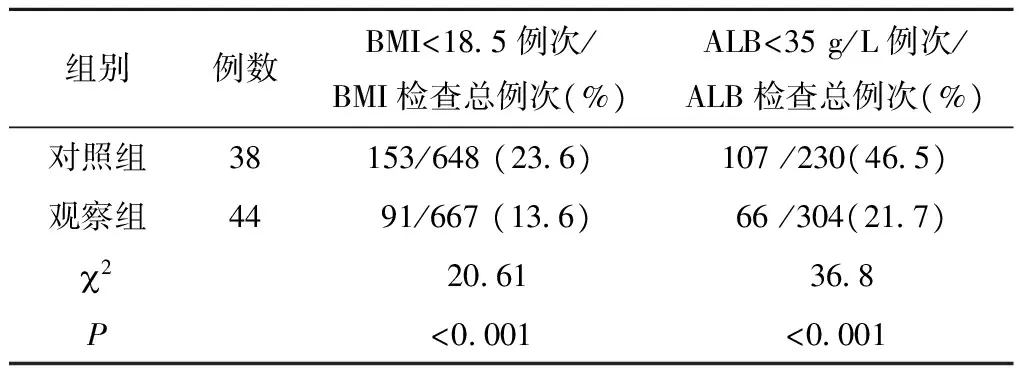
表3 两组患者化疗期间营养不良情况比较
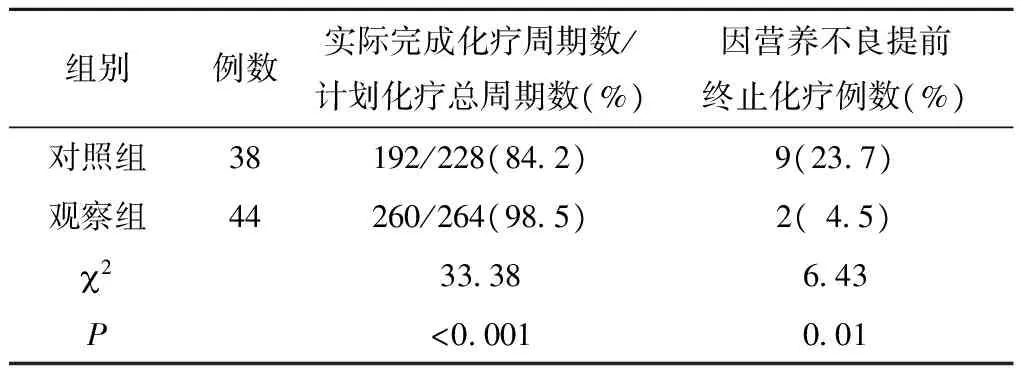
表4 两组患者化疗计划完成情况比较
3 讨论
营养风险并非发生营养不足的风险,而是指患者现有或潜在与营养有关的因素会对患者的结局发生负面影响[7]。为减少患者不良临床结局的发生,可通过对患者进行营养风险筛查,对存在营养风险的患者进行营养治疗。有研究[8-9]表明:1)患者临床不良结局与营养风险具有高度的相关性;2)营养治疗可使有营养风险的患者抗肿瘤治疗的效果和生存质量得到提高。因此,寻求敏感的合理营养风险测评工具至关重要。骨肉瘤患者营养不良风险高,应合理评估营养状况并进行营养治疗。肿瘤营养不良特指营养不足,40%~80%的患者存在营养不良,约20%的患者直接死于营养不良[10]。多种因素可导致恶性肿瘤患者发生营养不良,包括大量原料和能量被快速增长的肿瘤细胞消耗,使正常组织的生长代谢受到竞争性抑制[3];多种物质代谢异常如葡萄糖代谢加快、肌肉蛋白合成下降等[11];肿瘤自身分泌多种厌食因子,肿瘤患者精神因素抑制食欲[12]。新辅助化疗(化疗-手术-化疗)已成为骨肉瘤治疗的标准方案。恶心、呕吐是化疗最常见的不良反应,其中DDP是最强的致吐化疗药物,铂类还可使患者味觉感受敏感性降低从而发生厌食[13]。近年来,对恶性肿瘤患者的营养治疗重视程度越来越高,营养治疗在恶性肿瘤综合治疗中占有重要地位,而对患者的个体营养状况进行正确的评定,确认有适应证的患者是合理营养治疗的前提。在治疗过程中对营养治疗的疗效需要不断进行再评价,根据结果调整治疗方案[6]。
本研究结果显示,应用NRS 2002进行营养风险筛查效果优于QOL。近年来,国内外学者对QOL进行了深入广泛的临床研究,在卫生决策、患者康复和指导临床治疗方面均有应用,可作为一种独立预后因素与终结评估方法[14-15]。本研究对照组采用的QOL量表中的食欲条目进行营养筛查,此方法单一不全面,且受患者主观因素影响及制约,主观性较强。肿瘤为高代谢疾病,患者食欲未降低但并不代表没有营养不良风险。NRS 2002由丹麦肠外肠内营养协会于2003年发表,为ESPEN 推荐,适用于住院患者营养风险筛查。在欧洲,已有多项研究证明了NRS 2002的可信度和效度,NRS 2002营养风险筛查适用于94%~99%的住院患者,不仅可筛查出存在营养不良状况的患者,还可对是否存在营养不良的风险进行预测,且确认是否需要营养支持[16]。本研究观察组采用NRS 2002进行营养筛查,共进行667例次筛查,其中517例次≥3分,阳性率77.5%,而对照组中共应用QOL的食欲条目进行648例次营养筛查,其中226例次QOL评分≤3分,阳性率34.9%,两组患者阳性率差异具有统计学意义(P<0.05)。NRS 2002具有简单、有效、易行、无创及快速等优点[17],在临床工作中得到越来越广泛的应用。
NRS 2002用于骨肉瘤化疗患者营养风险筛查具有较高的可行性。住院患者并发症的发生率、住院时间和费用、病死率等均与营养不良相关。在恶性骨肿瘤中骨肉瘤的发病率约占35%,是最常见的恶性骨肿瘤[18]。新辅助化疗配合手术治疗和康复训练的综合治疗是目前骨肉瘤主要的治疗方法[19]。消化道反应、黏膜溃疡、骨髓抑制、感染等是化疗患者常见的并发症,导致患者不可避免地发生营养不良,主要表现为体质量下降,前白蛋白、白蛋白、总胆红素、丙氨酸氨基转移酶、血尿素氮等营养代谢指标改变;发生消化道反应、黏膜溃疡、Ⅳ级骨髓抑制、感染、化疗计划不能顺利完成等不良临床结局,从而影响患者进一步治疗的效果及预后[20]。由于恶性肿瘤特殊的生物学特质和对机体代谢功能的影响,恶性肿瘤患者营养不良发生率较高,对患者的治疗效果和预后造成直接影响,且严重影响患者的生存质量[21]。应用NRS 2002进行骨肉瘤化疗患者营养筛查,具有较高的敏感性,对于经NRS 2002筛查发现的存在营养风险的患者予以营养干预,其营养不良发生率明显降低,化疗耐受性提高。观察组采用NRS 2002营养筛查阳性检出率达77.5%,与对照组比较,营养干预后BMI、ALB,以及顺利完成化疗周期数差异有统计学意义(P<0.05)。对照组有9例、观察组仅有2例患者因为营养不良未能继续进行化疗方案。因此, NRS 2002营养风险筛查对骨肉瘤化疗患者具有较高的敏感性,营养干预效果明显,可改善骨肉瘤患者的临床结局。这一研究与高嵩涛等[20]研究一致。
综上所述,NRS 2002在骨肉瘤化疗患者营养管理中的应用具有较高的敏感性,能够及时筛查出具有营养不良风险的患者,从而降低患者营养不良的发生率,提高患者对化疗的耐受性和化疗计划完成率。
[1]徐仁应. 恶性肿瘤患者营养评估与营养支持[J]. 上海护理, 2011, 11(4): 93-96.
[2]梁伟民, 燕太强, 郭卫, 等. 骨肉瘤肺转移综合治疗研究进展[J]. 中华外科杂志, 2011, 49(1): 90-93.
[3]徐万鹏, 李佛保. 骨与软组织肿瘤学[M]. 第1版.北京:人民卫生出版社,2008:366.
[4]刘萍, 宋春华. NRS2002及MNA在原发性肝癌患者中应用的适用性比较[J]. 中国实用护理杂志, 2014, 30(11): 44-46.
[5]陈亚文. NRS2002在胰腺癌患者术前营养风险筛查中的应用效果观察[J]. 齐鲁护理杂志, 2012, 18(14): 16-17.
[6]CSCO肿瘤营养治疗专家委员会. 恶性肿瘤患者的营养治疗专家共识[J]. 临床肿瘤学杂志, 2012, 17(1): 59-73.
[7]do Egito E T, Medeiros Ade Q, Moraes M M,etal. Nutritional status of pediatric patients submitted to ostomy procedures[J]. Rev Paul Pediatr, 2013, 31(1): 58-64.
[8]Sorensen J, Holm L, Frost M B,etal. Food for patients at nutritional risk: a model of food sensory quality to promote intake[J]. Clin Nutr, 2012, 31(5): 637-646.
[9]Rasmussen H H, Holst M, Kondrup J. Measuring nutritional risk in hospitals[J]. Clin Epidemiol, 2010, 2: 209-216.
[10] 石汉平.中国肿瘤营养治疗指南[M].第1版.北京:人民卫生出版社,2015:21.
[11] 杨炯, 毕建威. 消化道肿瘤患者围手术期营养支持[J]. 肠外与肠内营养, 2006, 13(3): 184-187.
[12] Grossberg A J, Scarlett J M, Marks D L. Hypothalamic mechanisms in cachexia[J]. Physiol Behav, 2010, 100(5): 478-489.
[13] 石汉平, 凌文华, 李薇. 肿瘤营养学[M]. 第1版.北京:人民卫生出版社,2012:933-934.
[14] 张翠敏, 朱贵东, 阎子海, 等. 老年肺癌患者生存质量评价及影响因素分析[J]. 中国老年学杂志, 2011, 31(1): 21-23.
[15] 潘雁, 叶颖, 朱珺, 等. 应用SF-36量表分析高血压患者生命质量(QOL)的影响因素[J]. 复旦学报(医学版), 2014, 41(2): 205-209,273.
[16] 张岚. 营养风险筛查2002临床应用研究进展[J]. 天津护理, 2011, 19(1): 7-9.
[17] 陈丽飞, 朱云霞, 谢淑萍. NRS 2002在食管癌放疗患者营养风险筛查应用中的问题分析与探讨[J]. 护士进修杂志, 2016, 31(10): 900-902.
[18] Amankwah E K, Conley A P, Reed D R. Epidemiology and therapies for metastatic sarcoma[J]. Clin Epidemiol, 2013, 5: 147-162.
[19] Nathan S S, Healey J H. Demographic determinants of survival in osteosarcoma[J]. Ann Acad Med Singap, 2012, 41(9): 390-399.
[20] 高嵩涛, 郑琰, 蔡启卿, 等. 联合营养支持对有营养风险的骨肉瘤化疗患者临床结局的影响[J]. 中华临床医师杂志(电子版), 2014, 8(13): 2469-2473.
[21] 潘玲, 毛德强. NRS-2002评估473例首诊恶性肿瘤患者营养状况[J]. 重庆医学, 2013, 42(10): 1117-1118,1121.