Peutz-Jeghers综合征研究进展
林彦锋, 杨 霞
中国人民解放军第八五医院消化内科,上海 200052
Peutz-Jeghers综合征(Peutz-Jeghers syndrome,PJS)又名黑斑息肉综合征,是一种以皮肤黏膜色素沉着、胃肠道多发息肉、家族遗传性为主要特征的临床综合征。该病于1921年由Peutz首次报道,1949年JEGHERS等[1]又进行了系统描述,故命名为Peutz-Jeghers综合征。PJS被认为是一种常染色体显性遗传病,然而约45%的患者没有明确的家族史。目前认为,丝氨酸-苏氨酸激酶11/肝激酶B1(STK11/LKB1)基因突变与该病的发生密切相关。PJS严重影响了患者的生活质量并增加了患者罹患肿瘤的风险。
1 病因
目前的研究[2]认为,PJS的发生与染色体19p13.3的易感基因STK11/LKB1基因突变有关。STK11/LKB1被认为是一种肿瘤抑制基因,总长度为23 kb,具有9个编码外显子及1个非编码外显子,基因突变影响了激酶的活性,不同的基因突变可能导致患者的临床症状与病情的严重程度不同。有报道[3]对4例儿童PJS患者进行研究,发现无义突变的患者胃肠道息肉计数要明显高于错义突变的患者,因此对于STK11基因无义突变的患者需要密切监测息肉的形成与变化情况。目前的观点认为,LKB1基因的生殖系突变是家族性PJS发病的主要原因。CHEN等[4]对14例家族性PJS与5例散发性PJS研究发现,LKB1基因突变的发生率在家族性PJS中为85.7%,在所有PJS患者中为63.2%,且LKB1基因启动序列的甲基化可能与胃肠道息肉癌变的发生有关。WANG等[5]研究发现,LKB1是一种DNA损伤应答蛋白,缺乏LKB1的肿瘤细胞将对基于DNA损伤的放疗及阻碍DNA修复的化疗(如PARP抑制剂)更为敏感,这可能为PJS的治疗提供了新方向。KIM等[6]认为,STK11的突变与在不同部位出现的幽门腺黏液上皮异常增殖有着密切关联。总之,基于上述发现,认为STK11/LKB1的突变与大部分遗传性PJS的发生有关,但除此以外是否有其他基因参与PJS的发生,目前仍有待研究。
2 临床表现
PJS患者的临床表现主要包括皮肤黏膜色素沉着、消化道多发性息肉及肿瘤易感性。
约95%的PJS患者出现皮肤黏膜色素沉着,出生时少见,而多于幼年期出现,典型的色素沉着直径1~5 mm,颜色为深褐色,多分布于眼、耳、口周、肛周、颊黏膜及四肢末端,部分色素沉着可随患者年龄增长而褪色。目前尚无研究证实PJS患者的皮肤黏膜色素沉着具有恶变倾向[7]。
PJS患者消化道息肉可出现在自食管至直肠的各个部位,以小肠息肉最为多见(按息肉密度高低依次为空肠、回肠、十二指肠),其次为结肠、直肠及胃。另外,也有病例报道息肉出现在消化道以外的部位,如:胆囊[8]、膀胱、输尿管、肾盂、支气管及鼻腔[9]等。PJS患者胃肠道息肉的病理类型主要为错构瘤性息肉。胃肠道息肉可导致反复发作的肠梗阻与肠套叠,使得患者需要经历多次开腹手术与肠段切除[10]。另外,胃肠道息肉也可引起消化道出血,长此以往导致缺铁性贫血[11]。其他少见的并发症有直肠息肉脱垂[12]、发育不良[13]、胆道梗阻[14]等。研究[15]表明,PJS患者首次出现消化道症状的中位数年龄为10岁,首次接受息肉摘除术年龄为13岁。
目前认为,PJS患者发生某些肿瘤的危险性较常人更高,常见的为大肠癌、胃癌、乳腺癌、宫颈癌等,其他罕见的有甲状腺癌、肺癌及胰腺癌等[16](见表1)。PJS患者可伴发某些性腺肿瘤,含有环状小管的性索间质细胞瘤(sex cord tumors with annular tubules,SCTATs)是一种卵巢良性肿瘤,见于女性患者,大细胞钙化型睾丸支持细胞瘤(large cell calcifying sertoli cell tumors,LCST)则见于男性患者。STK11/LKB1突变的胃型宫颈癌(gastric-type endocervical adenocarcinoma,GAS)被认为预后不良[17]。
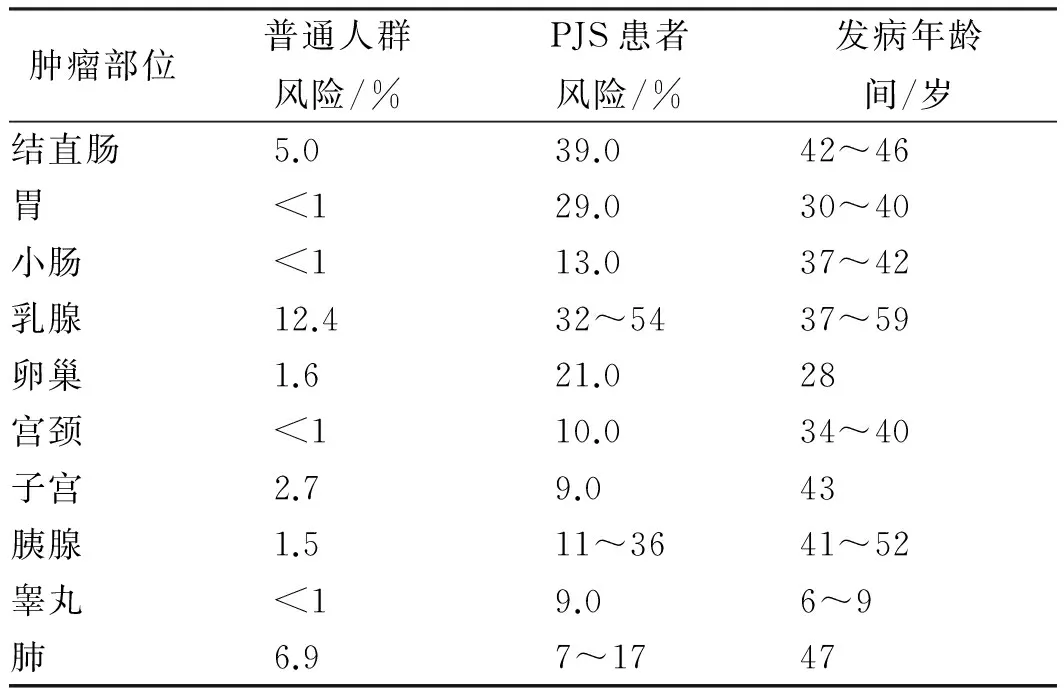
表1 PJS肿瘤累计风险[7]
3 诊断
PJS的诊断主要依据患者病史、皮肤黏膜色素沉着等临床表现及内镜下或影像学发现胃肠道息肉等证据。对于胃与大肠的息肉可通过胃十二指肠镜及结肠镜进行诊断,并可在内镜下取活检行病理检查。对于小肠息肉的诊断目前主要有胶囊内镜(CE)、CT小肠造影(CTE)、磁共振小肠造影(MRE)等手段。冯瑞等[18]利用CT小肠造影对29例PJS患者进行胃肠道息肉的检查,CT检出率为96.6%(28/29),证实了CT小肠造影对PJS病灶的定位、定性、鉴别诊断及随访具有较高的应用价值及可行性。URQUHART等[19]比较了CE与MRE对PJS胃肠道息肉的诊断效果,结果MRE相比CE对于胃肠道息肉的检出具有更高的阳性预测值。目前公认的诊断标准主要为2007年马略卡会议提出的欧洲共识[20],符合以下任意一条标准即可诊断为PJS:(1)两处以上组织学确定的PJS型错构瘤性息肉;(2)任何数量的PJS型息肉+至少一个直系亲属有PJS史;(3)典型皮肤黏膜色素沉着+至少一个直系亲属有PJS史;(4)任何数量的PJS型息肉+典型皮肤黏膜色素沉着。另外,利用分子生物学技术检测STK11基因的突变情况也是PJS诊断的重要依据之一,同时可以用于PJS家族遗传性的研究。
4 治疗
PJS患者的皮肤黏膜色素沉着由于不引起临床症状及无恶变可能,一般可以不予处理。童晓荣等[21]报道了利用Q开关紫翠宝石激光治疗PJS患者的皮肤黏膜色素沉着,取得了一定疗效。目前PJS治疗的关键在于胃肠道息肉的处理。对于胃及大肠内的息肉可通过胃十二指肠镜及结肠镜对息肉进行切除。对于小肠息肉的治疗目前依然有很大挑战。气囊辅助内镜(balloon assisted enteroscopy,BAE)技术由于可以在诊断的同时予以息肉摘除等处置,避免了患者行外科手术治疗,目前已经成为PJS小肠息肉的主要检查与治疗手段[22]。俎站飞等[23]报道了181例接受BAE治疗的PJS患者,术后出血发生率为1.9%,穿孔发生率为1.4%,证明了经BAE镜下治疗PJS患者小肠息肉是一种安全、有效的诊疗手段。对于经内镜及影像学确诊的PJS,建议对>1 cm息肉进行干预治疗,治疗的目的在于降低消化道出血、贫血、肠梗阻、肠套叠等并发症出现的可能,并降低胃肠道息肉恶变的风险。规律的内镜监测与内镜下息肉摘除可有效降低患者因急性肠梗阻而进行急诊手术的风险。外科手术治疗创伤较大、术后并发症较多,目前不建议作为胃肠道息肉的首选治疗方式,但其对于内镜下无法治疗的息肉及某些PJS患者急腹症的处理方面依然具有不可替代的作用[24]。术中结合内镜检查可以提高胃肠道息肉的检出率。手术方式主要包括肠段切开息肉摘除术,对于息肉数量较多的肠段可行部分肠段切除术,但需注意保留足够长度的小肠,以防术后短肠综合征的发生。王石林等[25]报道了局部治疗(内镜)+解救治疗(手术)+预防治疗(药物干预)的综合治疗模式用于PJS胃肠道息肉的临床治疗,结果证明这一综合治疗模式是积极、有效的。
对于PJS合并肠套叠及恶性肿瘤应以相应的标准方式治疗,而性腺肿瘤则建议行保守治疗。ZHONG等[26]报道了1例PJS合并直肠肿瘤的患者,予以腹腔镜下直肠结肠切除-回肠肛门吻合术,取得了良好的效果。对于PJS患者若怀疑有宫颈腺癌危险应建议行宫颈细胞学检查,对于检查出有宫颈非典型增生患者,建议行手术切除[17]。
5 随访
PJS患者随访的关键在于对胃肠道息肉的干预治疗及发现潜在的恶变可能。费翔等[27]报道了11例PJS息肉恶变的患者,确诊时的中位年龄为31.36岁,且最小者年仅16岁就发生多灶性息肉恶变,这提示临床诊疗PJS患者时需高度警惕息肉恶变可能。对于有家族史的患者,建议及早进行基因诊断以明确STK11基因突变类型及评估预后。ZHENG等[28]报道了利用多重连接依赖性探针扩增试验(multiplex ligation-dependent probe amplification assay,MLPA)检测STK11基因突变的技术,这对于PJS的早期诊断提供了一种有效的基因检测技术。对于无家族病史的患者,主要依据患者的临床表现进行诊断,建议其一级亲属无论是否符合PJS诊断标准,均需进行规律随访。SYNGAL等[29]提出了对于PJS患者建议的随访计划如表2所示。
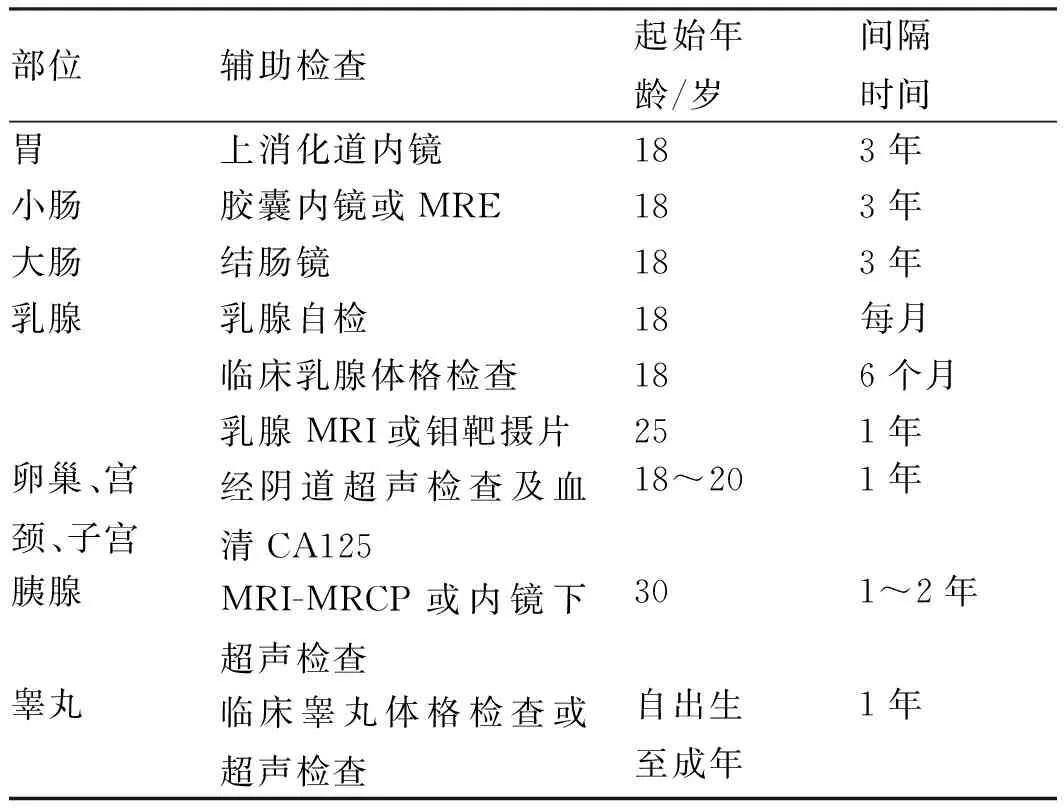
表2 PJS随访监测计划
6 展望
PJS目前尚无有效的根治方法,早诊断、早治疗及规律的随访被认为可以降低PJS的发病率与死亡率。目前针对细胞信号通路及其关键酶的分子靶向药物是PJS药物治疗研究的热点。选择性COX-2抑制剂如塞来昔布等已被证实可以预防家族性腺瘤性息肉病结直肠息肉的发生,但目前尚无循证医学证据证实选择性COX-2抑制剂可以减少PJS患者息肉的发生,且由此带来的心脑血管不良反应也限制了其在PJS治疗中的应用[30]。也有研究[31]发现,mTOR抑制剂如雷帕霉素等可能对PJS的治疗有效,已在动物实验中取得成功,但目前尚无人类试验证实雷帕霉素可以有效抑制息肉的生长。另外,以“济生乌梅丸”为代表的中药也为PJS息肉的预防性治疗提供了另一个选择[32]。PJS的药物治疗将是未来重要的研究方向。
[1] JEGHERS H, MCKUSICK V A, KATZ K H. Generalized intestinal polyposis and melanin spots of the oral mucosa, lips and digits; a syndrome of diagnostic significance [J]. N Engl J Med, 1949, 241(26): 1031-1036. DOI: 10.1056/NEJM/949122924601.
[2] ARETZ S, STIENEN D, UHLHAAS S, et al. High proportion of large genomic STK11 deletions in Peutz-Jeghers syndrome [J]. Hum Mutat, 2005, 26(6): 513-519.DOI: 10.1002/humu.20253.
[3] FU J, WEN Z, WANG F, et al. Genetic and clinical analyses of southern Chinese children with Peutz-Jeghers syndrome [J]. Genet Test Mol Biomarkers, 2015, 19(9): 528-531.DOI: 10.1089/gtmb.2015.0109.
[4] CHEN C, ZHANG X, WANG D, et al. Genetic screening and analysis of LKB1 gene in Chinese patients with Peutz-Jeghers syndrome [J]. Med Sci Monit, 2016, 22: 3628-3640.
[5] WANG Y S, CHEN J, CUI F, et al. LKB1 is a DNA damage response protein that regulates cellular sensitivity to PARP inhibitors [J]. Oncotarget, 2016, 7(45): 73389-73401.DOI: 10.18632/oncotarget.12334.
[6] KIM E N, KIM G H, KIM J, et al. A pyloric gland-phenotype ovarian mucinous tumor resembling lobular endocervical glandular hyperplasia in a patient with Peutz-Jeghers syndrome [J]. J Pathol Transl Med, 2017, 51(2): 159-164.DOI: 10.4132/jptm.2016.07.01.
[7] MCGARRITY T J, AMOS C I, BAKER M J, et al. Peutz-Jeghers syndrome [J/OL]. 2016. https://www.ncbi.nlm.nih.gov/books/NBK1266.
[8] 秦全红, 潘彦珞, 章明放, 等. 伴有胆囊息肉的Peutz-Jeghers综合征一例[J]. 中华外科杂志, 2006, 44(5): 360.DOI: 10.3760/j:issn:0529-5815.2006.05.023.
[9] 马晶影, 周兵, 黄谦, 等. Peutz-Jeghers综合征表现为鼻息肉一例[J]. 中华耳鼻咽喉头颈外科杂志, 2016, 51(2): 135-136.DOI: 10.3760/cma.j.issn.1673-0860.2016.02.016.
MA J Y, ZHOU B, HUANG Q, et al. Nasal polyposis in Peutz-Jeghers syndrome: a case report [J]. Chin J Otorhinolaryngol Head Neck Surg, 2016, 51(2): 135-136.DOI: 10.3760/cma.j.issn.1673-0860.2016.02.016.
[10] 唐琪, 周平, 陈晓, 等. Peutz-Jeghers综合征肠套叠的累积危险度与临床特征[J]. 中华消化杂志, 2014, 34(2): 118-120.DOI: 10.3760/cma.j.issn.0254-1432.2014.02.011.
TANG Q, ZHOU P, CHEN X, et al. High cumulative risk and clinical feature of intussusception in patients with Peutz-Jeghers syndrome [J]. Chin J Dig, 2014, 34(2): 118-120.DOI: 10.3760/cma.j.issn.0254-1432.2014.02.011.
[11] 郭良耀, 赵小亭, 李威. Peutz-Jeghers综合征并难治性缺铁性贫血一例[J]. 中华内科杂志, 2001, 40(6): 425.DOI: 10.3760/j.issn:0578-1426.2001.06.025.
[12] CANO-CONTRERAS A D, MEIXUEIRO-DAZA A, GRUBE-PAGOLA P, et al. Giant rectal polyp prolapse in an adult patient with the Peutz-Jeghers syndrome [J]. BMJ Case Rep, 2016, 2016, pii: bcr2016215629.DOI: 10.1136/bcr-2016-215629.
[13] RATHI C D, SOLANKE D B, KABRA N L, et al. A rare case of solitary Peutz Jeghers type hamartomatous duodenal polyp with dysplasia [J]. J Clin Diagn Res, 2016, 10(7): OD03-OD04.DOI: 10.7860/JCDR/2016/20236.8094.
[14] DE SILVA W S, PATHIRANA A A, GAMAGE B D, et al. Extra-ampullary Peutz-Jeghers polyp causing duodenal intussusception leading to biliary obstruction: a case report [J]. J Med Case Rep, 2016, 10: 196.DOI: 10.1186/s13256-016-0990-8.
[15] AMOS C I, KEITHERI-CHETERI M B, SABRIPOUR M, et al. Genotype-phenotype correlations in Peutz-Jeghers syndrome [J]. J Med Genet, 2004, 41(5): 327-333.
[16] VAN LIER M G, WAGNER A, MATHUS-VLIEGEN E M, et al. High cancer risk in Peutz-Jeghers syndrome: a systematic review and surveillance recommendations [J]. Am J Gastroenterol, 2010, 105(6): 1258-1265.DOI: 10.1038/ajh.2009.725.
[17] MESERVE E E, NUCCI M R. Peutz-Jeghers syndrome: pathobiology, pathologic manifestations, and suggestions for recommending genetic testing in pathology reports [J]. Surg Pathol Clin, 2016, 9(2): 243-268.DOI: 10.1016/j.path.2016.01.006.
[18] 冯瑞, 宋云龙, 王萍, 等. 多层螺旋CT在黑斑息肉综合征诊断中的应用价值[J]. 中国医学装备, 2016, 13(4): 67-71.DOI: 10.3969/J.ISSN.1672-8270.2016.04.021.
FENG R, SONG Y L, WANG P, et al. The application values of MSCT in diagnosis of Peutz-Jeghers syndrome [J]. China Medical Equipment, 2016, 13(4): 67-71.DOI: 10.3969/J.ISSN.1672-8270.2016.04.021.
[19] URQUHART P, GRIMPEN F, LIM G J, et al. Capsule endoscopy versus magnetic resonance enterography for the detection of small bowel polyps in Peutz-Jeghers syndrome [J]. Fam Cancer, 2014, 13(2): 249-255.DOI: 10.1007/s10689-014-9700-0.
[20] BEGGS A D, LATCHFORD A R, VASEN H F, et al. Peutz-Jeghers syndrome: a systematic review and recommendations for management [J]. Gut, 2010, 59(7): 975-986.DOI: 10.1136/gut.2009.198499.
[21] 童晓荣, 李延, 刘凌, 等. 调Q开关紫翠宝石激光治疗40例色素沉着-肠息肉综合征唇部皮疹的疗效观察[J]. 中国美容医学杂志, 2012, 21(1): 87-88.DOI: 10.3969/j.issn.1008-645.2012.01.035.
TONG X R, LI Y, LIU L, et al. Q-Switched Alexandrite laser treatment of facial lentigines in 40 chinese subjects with Peutz-Jeghers syndrome [J]. Chinese Journal of Aesthetic Medicine, 2012, 21(1): 87-88.DOI: 10.3969/j.issn.1008-645.2012.01.035.
[22] 赵晓军, 李娜, 王昕, 等. 气囊辅助小肠镜治疗Peutz-Jeghers综合征的临床价值[J]. 胃肠病学和肝病学杂志, 2015, 24(5): 525-526.DOI: 10.3969/j.issn.1006-5709.2015.05.010.
ZHAO X J, LI N, WANG X, et al. Clinical value of balloon assisted enteroscopy for patients with Peutz-Jeghers syndrome [J]. Chin J Gastroenterol Hepatol, 2015, 24(5): 525-526.DOI: 10.3969/j.issn.1006-5709.2015.05.010.
[23] 俎站飞, 毛高平, 张亚飞, 等. 气囊辅助小肠镜对Peutz-Jeghers综合征患者小肠息肉治疗的安全性评价[J]. 世界华人消化杂志, 2014, 22(33): 5174-5178.DOI: http://dx.dol.org/10.11569/wcjd.v22.133.5174.
ZU Z F, MAO G P, ZHANG Y F, et al. Safety of balloon assisted enteroscopy for treatment of small bowel polyps in patients with Peutz-Jeghers syndrome [J]. World Chinese Journal of Digestology, 2014, 22(33): 5174-5178.DOI: http://dx.dol.org/10.11569/wcjd.v22.133.5174.
[24] 戴益琛, 宋于刚, 肖冰, 等. 黑斑息肉综合征52例内镜与外科治疗[J]. 临床内科杂志, 2005, 22(7): 455-457.DOI: 10.3969/j.issn.1001-9057.2005.07.009.
DAI Y C, SONG Y G, XIAO B, et al. The endoscopic and surgical treatment of 52 patients with Peutz-Jegher syndrome [J]. J Clin Intern Med, 2005, 22(7): 455-457.DOI: 10.3969/j.issn.1001-9057.2005.07.009.
[25] 王石林, 顾国利, 魏学明, 等. Peutz-Jeghers综合征临床综合治疗模式初探(附71例报道)[J]. 中国普外基础与临床杂志, 2012, 19(5): 502-506.
WANG S L, GU G L, WEI X M, et al. Clinical comprehensive therapy of Peutz-Jeghers syndrome (report of 71 cases ) [J]. Chin J Bases Clin General Surg, 2012, 19(5): 502-506.
[26] ZHONG M E, NIU B Z, JI W Y, et al. Laparoscopic restorative proctocolectomy with ileal pouch-anal anastomosis for Peutz-Jeghers syndrome with synchronous rectal cancer [J]. World J Gastroenterol, 2016, 22(22): 5293-5296.DOI: 10.3748/wig.v22.i22.5293.
[27] 费翔, 于鹏飞, 杨海瑞, 等. Peutz-Jeghers综合征肠道息肉恶变的临床分析[J]. 中国普外基础与临床杂志, 2016, 23(5): 598-600.DOI: 10.7507/1007-9424.20160160.
[28] ZHENG B, WANG C, JIA Z, et al. A clinical and molecular genetic study in 11 Chinese children with Peutz-Jeghers syndrome [J]. J Pediatr Gastroenterol Nutr, 2017, 64(4): 559-564.DOI: 10.1097/MPG.0000000000001316.
[29] SYNGAL S, BRAND R E, CHURCH J M, et al. ACG clinical guideline: Genetic testing and management of hereditary gastrointestinal cancer syndromes [J]. Am J Gastroenterol, 2015, 110(2): 223-263.DOI: 10.1038/ajg.2014.435.
[30] UDD L, KATAJISTO P, ROSSI D J, et al. Suppression of Peutz-Jeghers polyposis by inhibition of cyclooxygenase-2 [J]. Gastroenterology, 2004, 127(4): 1030-1037.
[31] ROBINSON J, LAI C, MARTIN A, et al. Oral rapamycin reduces tumour burden and vascularization in Lkb1(+/-) mice [J]. J Pathol, 2009, 219(1): 35-40.DOI: 10.1002/path.2562.
[32] 顾国利, 魏学明, 徐丽梅, 等. Peutz-Jeghers综合征预防性治疗的研究[J]. 胃肠病学和肝病学杂志, 2012, 21(4): 380-383.DOI: 10.3969/j.issn.1006-5709.2012.04.028.
GU G L, WEI X M, XU L M, et al. Preventative treatment of Peutz-Jeghers syndrome [J]. Chin J Gastroenterol Hepatol, 2012, 21(4): 380-383.DOI: 10.3969/j.issn.1006-5709.2012.04.028.

