缺血性卒中后应激性高血糖与早期血管性认知功能障碍的相关性
周邑东,袁怀武,计仁杰,罗本燕
1浙江大学医学院 附属第一医院神经内科,杭州 310003 2宁波市第一医院神经内科,浙江宁波 315000
·论著·
缺血性卒中后应激性高血糖与早期血管性认知功能障碍的相关性
周邑东1,2,袁怀武1,计仁杰1,罗本燕1
1浙江大学医学院 附属第一医院神经内科,杭州 3100032宁波市第一医院神经内科,浙江宁波 315000
目的探究应激性高血糖对缺血性卒中患者早期血管性认知功能障碍(VCI)发生的影响及预测价值。方法将422例非糖尿病急性缺血性卒中患者依据空腹血糖水平分为未出现应激性高血糖组(<6.1 mmol/L)、应激性血糖轻度升高组(6.1~7.0 mmol/L)和应激性血糖显著升高组(≥7.0 mmol/L),以简易精神状态量表、阿尔茨海默病评定量表认知分量表、临床痴呆量表评定早期认知功能,根据认知诊断标准将患者分为认知功能正常组、血管性轻度认知功能障碍组和血管性痴呆组,对应激性血糖升高程度与认知功能障碍程度进行相关性分析。结果共62例患者出现应激性高血糖,发生率14.7%,教育程度高[(8.39±3.85)年比(6.62±4.39)年,P=0.037)]、既往有心血管病史(45.2%比18.3%,P=0.001)的非糖尿病脑梗死患者早期发生应激性高血糖的风险增加。共筛查出VCI患者270例,发生率64.0%。年龄、性别、吸烟、美国国立卫生研究院卒中量表评分、汉密尔顿抑郁量表评分、应激性高血糖、心血管病史与非糖尿病缺血性卒中后早期发生VCI相关(P<0.05)。多因素非条件Logistic回归分析显示,应激性高血糖(OR=3.086,95%CI=1.065~8.929)是非糖尿病缺血性卒中患者早期发生VCI的独立危险因素。应激性血糖轻度升高组与显著升高组出现认知功能障碍的风险均高于血糖正常组,其中显著升高组又高于轻度升高组(61.11%比75.00%比90.91%),应激性高血糖水平与缺血性卒中后早期血管性认知功能障碍严重程度呈正相关(rs=0.185,P=0.007)。结论应激性高血糖与缺血性卒中早期血管性认知障碍存在显著相关性。
缺血性卒中;应激性高血糖;血管性认知障碍
据世界卫生组织统计,目前卒中已成为全球第三大成人致残主因及首要死因之一。血管性认知功能障碍是脑卒中后常见的并发症之一,流行病学调查显示卒中后约有30%患者出现不同程度的认知障碍,部分具有隐匿性,可严重损害康复效果及预后生活质量[1],因此早期筛查对改善患者预后尤为重要。应激反应是机体在严重疾病或创伤时发生的一种保护性反应,但在不同情况下也可能表现为应激损伤加剧病情恶化。急性脑卒中初期常有应激反应参与,应激性高血糖是其中重要表现之一。有统计显示,几乎40%的卒中患者早期伴有不同程度的应激性高血糖[2]。以往的临床研究多倾向于证实糖尿病患者高血糖水平与急性脑卒中神经功能缺损程度存在相关性[3],本研究通过分析大样本临床资料,探究非糖尿病患者脑梗死急性期应激性高血糖与认知功能损害的相关性,分析预测血管性认知障碍发生风险。
对象和方法
对象选取2013年11月至2015年11月浙江大学医学院附属第一医院、嘉兴市第二医院及宁波市第一医院收治的非糖尿病脑梗死患者422例。纳入标准:(1)年龄≥18岁;(2)临床诊断为缺血性脑卒中,根据世界卫生组织定义的卒中定义[4],即突发的局灶性或全面性神经功能缺损的临床征象,并且神经功能缺损的临床征象持续时间超过24 h,排除其他非血管性原因(如原发性脑肿瘤、脑转移瘤、硬膜下血肿、癫痫发作后麻痹、脑外伤等)造成的脑功能障碍;(3)起病时间≤14 d。排除标准:(1)因各种症状(包括语言障碍)无法完成检查者;(2)既往有认知障碍病史;(3)拒绝签署知情同意书;(4)既往有糖尿病史,入院后经糖化血红蛋白及糖耐量试验确认糖尿病或糖耐量异常的患者;(5)有严重心肺、肝脏、肾脏疾病患者及有与高血糖有关的疾病(如甲状腺、肾上腺和垂体疾病);(6)有严重焦虑、抑郁及精神障碍疾病者。其中男性290例、女性132例,年龄25~84岁,平均(60.91±12.40)岁。既往有高血压病史274例(64.9%)、高脂血症史22例(5.2%),既往卒中史44例(10.4%)、心血管病史94例(22.3%)、吸烟史198例(46.9%)、饮酒史186例(44.1%)。
分组
按血糖水平分组:所有入选患者于入院次日清晨抽取空腹静脉血检测血糖,以急性期空腹血糖≥6.1 mmol/L为应激性高血糖标准,分为未出现应激性高血糖组(<6.1 mmol/L)360例、应激性血糖轻度升高组(6.1~7.0 mmol/L)40例、应激性血糖显著升高组(≥7.0 mmol/L)22例。
按认知功能分组:依据以下认知功能诊断标准,患者被分为3组:认知功能正常组(n=152)、血管性轻度认知功能障碍组(n=196)和血管性痴呆组(n=74)。(1)美国心脏协会/美国卒中协会血管性轻度认知功能障碍诊断标准,临床结果分为“很可能、可能、不稳定、否”,本研究将诊断为“很可能”的患者列入血管性轻度认知功能障碍组(根据轻度认知功能障碍的分型情况,血管性轻度认知功能障碍分为4个亚型,分别为:遗忘型、遗忘合并其他认知领域型、非遗忘性单个认知领域型、非遗忘性多个认知领域型。分型必须基于认知功能测试,至少4个认知功能领域必须被测试:执行、注意、记忆、语言、视空间功能。分型必须基于这样一个前提:认知功能必须较之前基线水平下降,至少累计1个认知功能领域。日常生活能力正常或轻度损害,独立于现存的运动或感觉异常症状。很可能血管性轻度认知功能障碍:①有认知功能损害及脑血管病影像学证据,并且在临床卒中和认知功能缺陷发生之间存在明确的短暂性联系,或者在认知功能障碍严重程度和模式与弥漫皮质下脑血管病病理之间存在明确的联系;②在卒中之前或之后,未提示非血管性神经退行性疾病导致的逐步进展的认知功能缺陷的病史。可能血管性轻度认知功能障碍:有认知功能损害及脑血管病影像学证据,但是,①在脑血管病和认知功能缺陷的发生不存在明确的关系;②血管性轻度认知功能障碍的诊断依据不足;③严重失语妨碍认知评估,然而,那些临床事件导致失语但之前书面记录表明认知功能正常的患者可以被归类为很可能血管性轻度认知功能障碍;④有证据提示可能存在影响认知功能的脑血管疾病之外的变性疾病,如神经变性疾病病史、生物标记物或基因检测提示阿尔茨海默病、癌症或精神疾病或代谢性疾病等可能影响认知功能的疾病病史。不稳定性血管性轻度认知功能障碍:那些之前被诊断为很可能血管性轻度认知功能障碍或可能血管性轻度认知功能障碍,但之后症状恢复到正常水平的患者)。(2)美国国立神经疾病与卒中研究所和瑞士神经科学研究国际协会血管性痴呆诊断标准,临床诊断结果分为“很可能、可能、肯定、否”,本研究将诊断为“很可能”的患者列入血管性痴呆组(很可能血管性痴呆:痴呆:认知功能较以往减退,记忆力损害及二项或二项以上认知领域内的功能损害,这些功能缺陷足以影响患者日常生活,而不单纯由卒中所致的躯体障碍引起。脑血管病:神经病学检查有局灶性体征,脑影像学检查有脑血管疾病证据。以上两个诊断具相关性至少有下列1个或1个以上的表现:痴呆表现发生在卒中后3个月内;有突发的认知功能恶化,或波动性、阶段性进展的认知功能缺损。可能血管性痴呆:存在痴呆并有局灶性神经体征,但无脑影像学检查的脑血管损害;痴呆和卒中之间缺乏明显的短暂的联系;虽有脑血管病存在,但缓慢起病,病程特征不符。肯定血管性痴呆:临床上符合很可能血管性痴呆;组织病理学检查证实血管性痴呆;未超过年龄限定数目的神经纤维缠结和老年斑;无其他引起痴呆的临床和病理疾病)。(3)单因素及多因素分析时,血管性轻度认知功能障碍组与血管性痴呆组统一并入血管性认知功能障碍组。
基线资料入院时记录以下资料:(1)人口学特征:包括性别、年龄、受教育程度、身高及体质量(体质量指数);(2)血管危险因素:高血压、高脂血症、心血管病史、脑血管病史、吸烟史、饮酒史;(3)临床数据收集:头颅核磁共振扫描、美国国立卫生院卒中量表(National Institutes of Health Stroke Scale,NIHSS)评估卒中后急性期神经功能缺损情况、汉密尔顿抑郁量表(Hamilton Depression Rating Scale,HAMD)评估卒中后抑郁状态。
认知量表评估入院10 d后由经专业训练的神经心理评估师应用以下3种认知量表评估所有患者认知功能:简易精神状态量表、阿尔茨海默病评定量表认知分量表、临床痴呆量表。
统计学处理采用SPSS 21.0软件进行统计学分析,分类变量采用2检验进行单因素分析,连续变量以均数±标准差表示,非正态变量以中位数及四分位间距表示,两组患者基线特征比较采用独立样本t检验进行单因素分析。缺血性脑卒中后早期发生血管性认知功能障碍危险因素先采用单因素分析,进一步采用多因素非条件Logistic回归分析,等级资料相关性采用Spearman相关分析,P<0.05为差异有统计学意义。
结 果
基线水平应激性高血糖组受教育程度、既往心血管病史较未出现应激性高血糖组高(P=0.037,P=0.001),其他指标两组比较差异无统计学意义(表1);不同梗死部位与应激性高血糖发生风险均无相关性(36例缺失影像学资料)(P>0.05)(表2)。
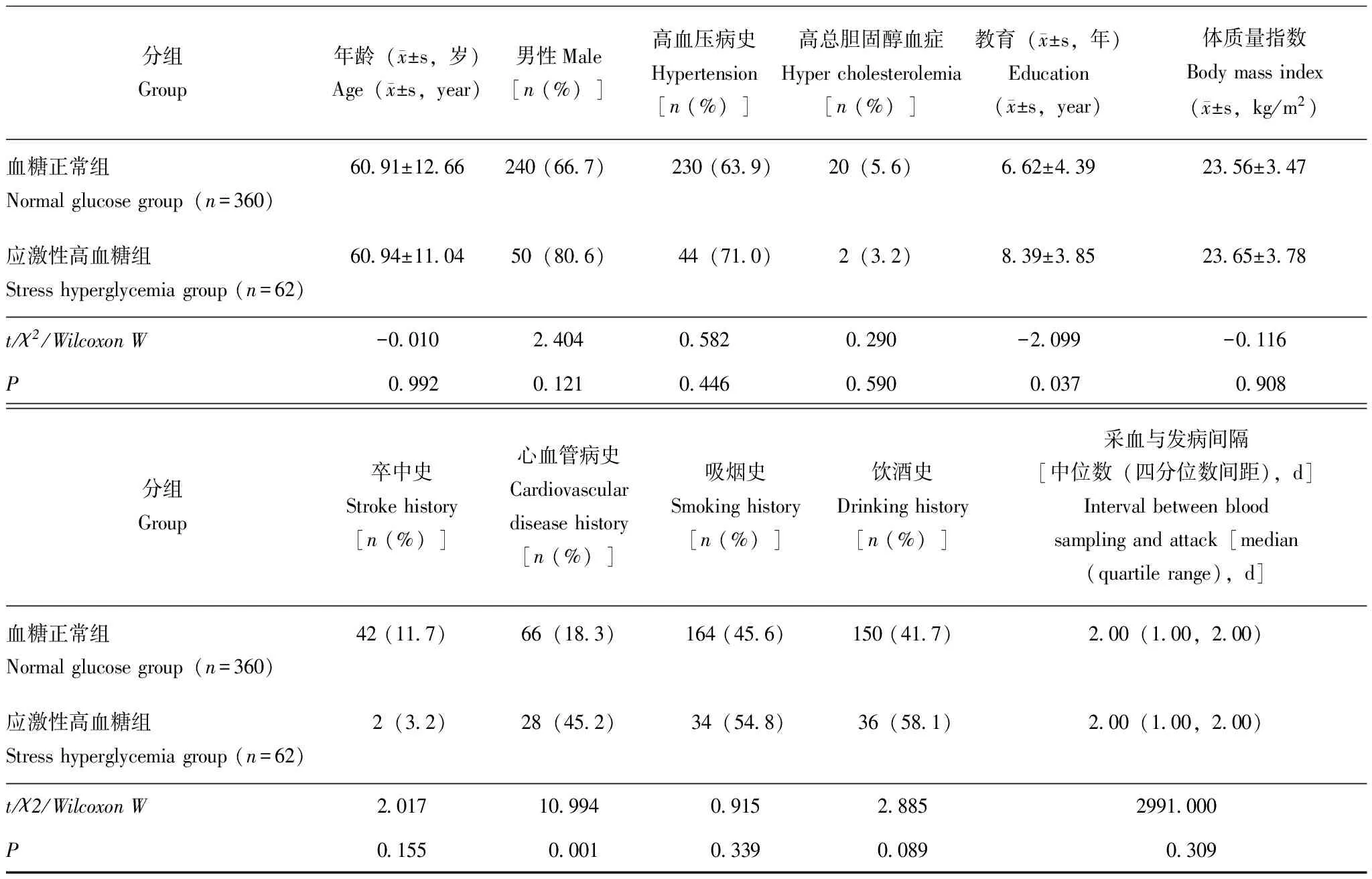
表 1 血糖正常组与应激性高血糖组基线比较Table 1 Comparison of baseline data between normal glucose group and stress hyperglycemia group
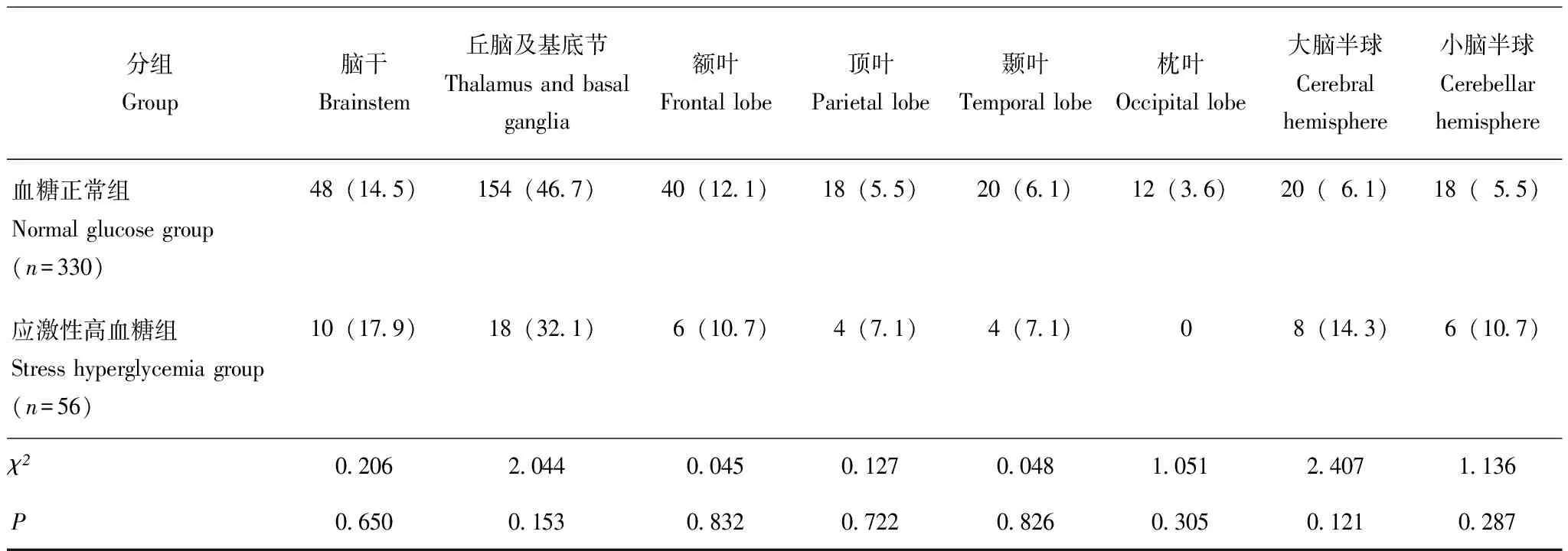
表 2 不同梗死部位与应激性高血糖发生风险分析[n(%)]Table 2 Risks of stress hyperglycemia in patients with different regions of infarction[n(%)]
缺血性脑卒中后早期发生血管性认知功能障碍的单因素分析血管性认知功能障碍(vascular cognitive impairment,VCI)组和正常组的年龄、性别、心血管病史、吸烟史、NIHSS评分、HAMD评分、应激性高血糖比较,差异均有统计学意义(P<0.05),与缺血性卒中后早期VCI的发生相关(表3)。
缺血性脑卒中后早期发生VCI的多因素分析将自变量因素分别赋值,年龄:≤40岁=0,41~50岁=1,51~60岁=2,61~70岁=3、>70岁=4;性别:女性=0,男性=1;高血压病:否=0,是=1;卒中史:否=0,是=1;心血管病史:否=0,是=1;吸烟史:否=0,是=1;饮酒史:否=0,是=1;NIHSS评分:≤8分=0,>8分=1;HAMD评分:<8分=0,≥8分=1;应激性高血糖:否=0,是=1;以VCI的发生作为因变量,带入 Logistic回归模型进行多因素分析,结果显示:应激性高血糖(OR=3.086,95%CI=1.065~8.929,P=0.038)是缺血性卒中后早期发生VCI的独立危险因素。
应激性高血糖与血管性认知障碍程度的等级相关性经Spearman等级相关分析显示,应激性高血糖水平与非糖尿病脑梗死早期血管性认知功能障碍严重程度呈正相关(rs=0.185,P=0.007)(表4)。
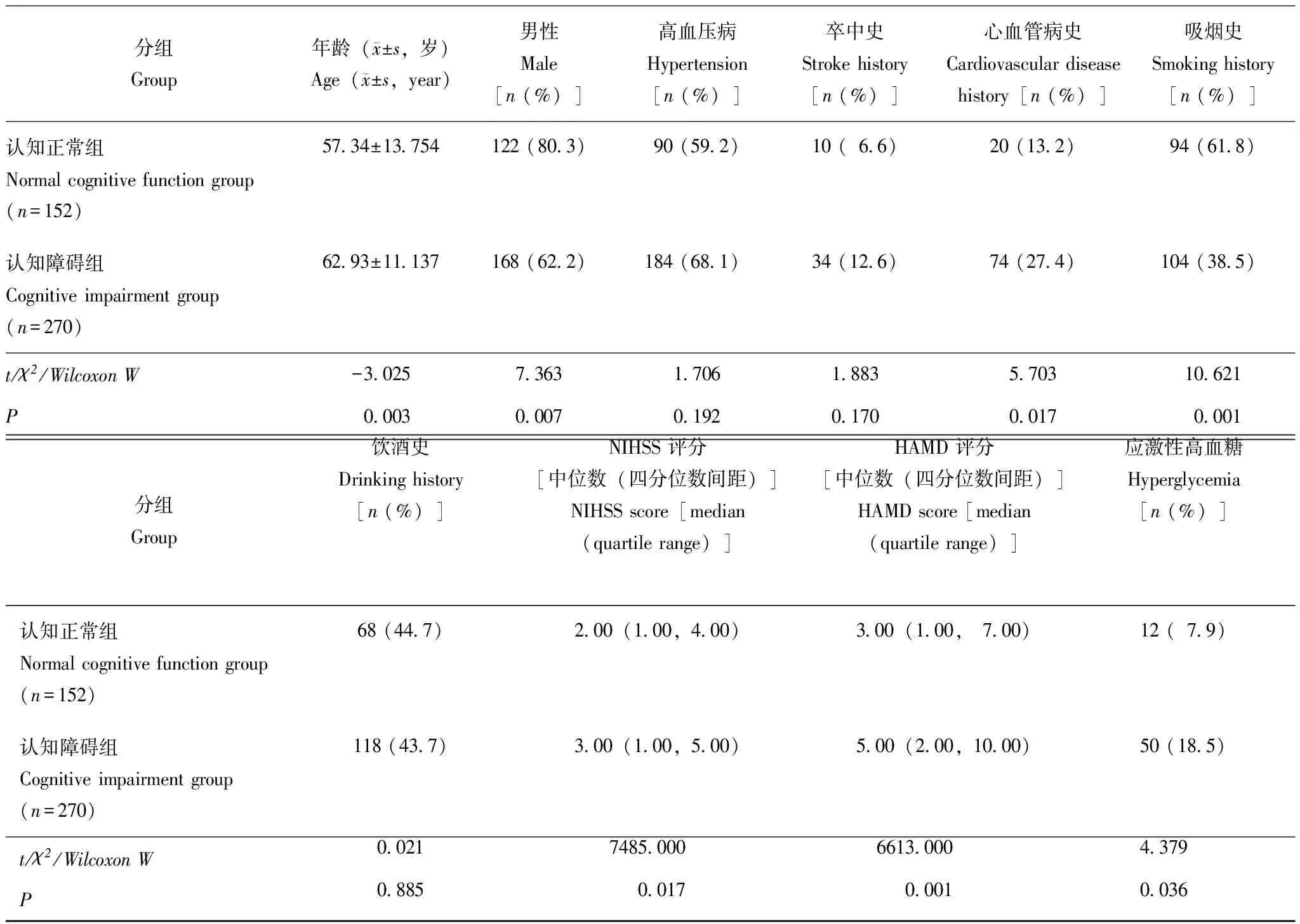
表 3 缺血性脑卒中后早期发生血管性认知功能障碍的单因素分析Table 3 Univariate analysis of vascular cognitive impairment with early occurrence in post-ischemic stroke time
NIHSS:美国国立卫生研究院卒中量表;HAMD:汉密尔顿抑郁量表
NIHSS:National Institute of Health Stroke Scale;HAMD:Hamilton Depression Rating Scale
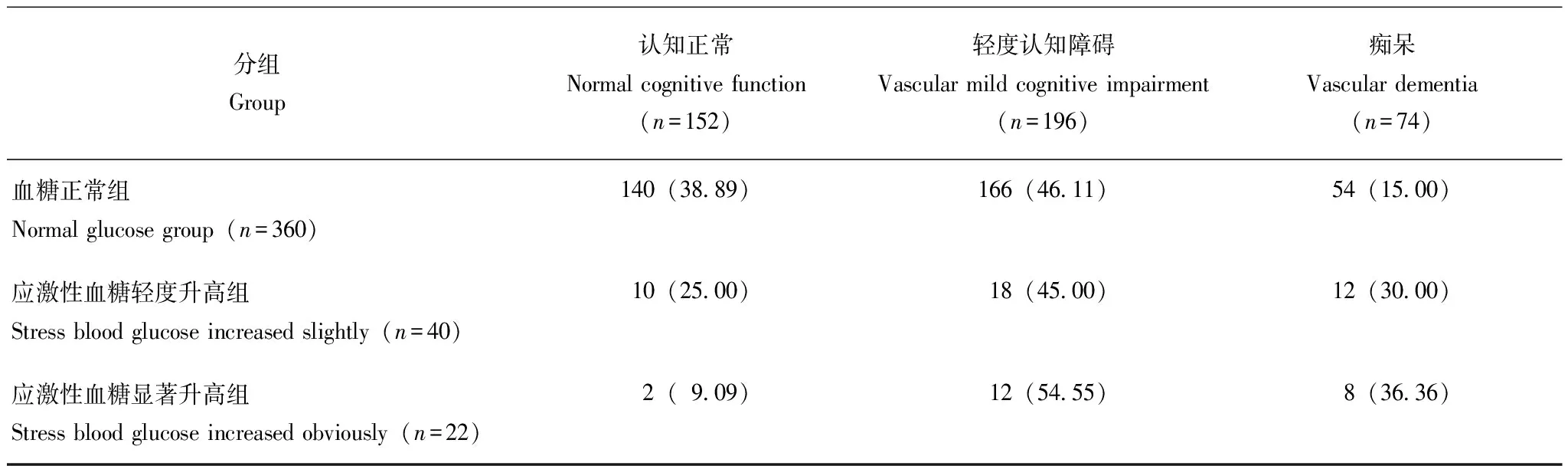
表 4 不同应激性高血糖水平患者血管性认知障碍程度[n (%)]Table 4 Different degrees of stress hyperglycemia in patients with different levels of vascular cognitive impairment [n (%)]
讨 论
血管性认知功能障碍由脑血管病变引发,发病率高,起病隐匿,预后差,严重损害患者的人际交流及生活自理能力,有报道卒中后3个月内血管性认知障碍发生率为6%~55%[5],本研究在422例患者中筛查出270例存在不同程度的认知障碍,发生率为64.0%,其中血管性轻度认知功能障碍196例、血管性痴呆74例,表明国内血管性认知障碍同样存在着高发病率。各项临床资料对比显示,年龄、性别、吸烟史、NIHSS评分、HAMD评分、应激性高血糖、心血管病史与缺血性卒中早期认知障碍存在相关性,随后多因素分析进一步显示,应激性高血糖是非糖尿病脑梗死患者预后早期发生血管性认知功能损害的独立危险因素。但有吸烟史的患者认知障碍发生的比例相对低,有研究显示,尼古丁能在一定程度上预防神经系统退行性疾病[6],但在血管性痴呆中的作用机制尚不清楚。
本研究显示62例患者出现应激性高血糖,发生率14.7%,其中血糖轻度升高40例、血糖显著升高22例,教育程度较高、既往有心血管病史的患者发生卒中后应激性高血糖的风险相对较高。
将空腹血糖水平与认知功能障碍程度作分组相关性分析,结果显示应激性血糖轻度升高组与显著升高组出现认知功能障碍的比例均高于血糖正常组,而显著升高组认知受损比例又高于轻度升高组。进一步分析显示,血糖升高水平与早期血管性认知障碍严重程度呈正相关。本研究证实应激性高血糖与缺血性卒中早期血管性认知功能障碍存在等级相关性。目前国内外相关领域研究较少,曾有研究显示应激性高血糖是影响认知功能的危险因素之一[7]。
应激性高血糖认知功能相对较差的机制可能是:(1)在缺血缺氧状态下,出现应激反应性血糖升高后,葡萄糖无氧酵解加速,乳酸水平明显升高,引起酸中毒,酸中毒又进一步促进缺血区生化改变,加重脑组织缺氧、水肿,导致梗死灶扩大[8];(2)高血糖使细胞外液处于高渗状态,出现细胞内脱水,破坏血管内皮细胞[9],激活内源性凝血系统,促使血小板聚集、纤溶异常,致使血管狭窄甚至阻塞,进一步加重脑组织缺血缺氧;(3)高血糖反应促进过氧化物生成增多,细胞膜钙离子通道过度开放,兴奋性氨基酸堆积,产生神经毒性作用,导致线粒体损伤,神经元细胞凋亡[10]。某种意义上非糖尿病患者出现应激性高血糖相比原有糖尿病史的患者,急性期神经功能受损更显著[11]。
针对非糖尿病患者缺血性卒中早期是否需要进行人为血糖干预,迄今为止的多项临床研究尚无一致结论。有荟萃分析显示,在入住ICU的急性重症脑卒中患者中,无论既往是否存在糖尿病史,均采取严格的胰岛素血糖控制策略,在降低死亡率方面得到明显获益[12];但另一方面,有国外回顾性研究显示,急性缺血性卒中早期应用胰岛素严格控制血糖,在促进神经功能恢复方面未发现明显效果[13]。相比之下,胰岛素控制可能会带来负面效应,约11%的患者有潜在的症状性低血糖风险,甚至因此而引起持续性神经功能障碍[14]。
综上,血管性认知功能损害早期临床上难以被察觉,具有隐匿性,并容易逐步进展为血管性痴呆,而应激性高血糖的发生预示了缺血性脑卒中患者早期出现认知功能减退、生活质量下降的风险增加,因此,监测非糖尿病患者血糖应激性升高程度成为早期筛查卒中后血管性认知障碍的重要手段。由于现阶段筛查仅限于急性期认知状态,无法代表远期认知情况,故结论可能存在客观局限性,随着本研究下阶段的随访逐步完善,可做出后续相关性报道,进一步探讨更优化的卒中后应激性高血糖的管理策略,更好地促进认知功能回归。
[1] Gorelick PB,Scuteri A,Black SE,et al. Vascular contributions to cognitive impairment and dementia:a statement for healthcare professionals from the American Heart Association/American Stroke Association[J].Stroke,2011,42(9):2672- 2713. doi:10. 1161/STR. 0b013e3182299496.
[2] Hafez S,Coucha M,Bruno A,et al. Hyperglycemia,acute ischemic stroke,and thrombolytic therapy[J].Transl Stroke Res,2014,5(4):442- 453. doi:10. 1007/s12975- 014- 0336-z.
[3] Masrur S,Cox M,Bhatt DL,et al. Association of acute and chronic hyperglycemia with acute ischemic stroke outcomes post-thrombolysis:findings from get with the guidelines-stroke[J].J Am Heart Assoc,2015,4(10):e002193. doi:10. 1161/JAHA. 115. 002193.
[4] Kunitz SC,Gross CR,Heyman A,et al. The pilot Stroke Data Bank:definition,design,and data[J].Stroke,1984,15(4):740- 746. doi:10. 1161/01. STR. 15. 4. 740.
[5] Bella R,Ferri R,Lanza G,et al. TMS follow-up study in patients with vascular cognitive impairment-no dementia[J].Neurosci Lett,2013,8(534):155- 159. doi:10. 1016/j. neulet. 2012. 12. 017.
[6] Gao J,Adam BL,Terry AV. Evaluation of nicotine and cotinine analogs as potential neuroprotective agents for Alzheimer’s disease[J].Bioorg Med Chem Lett,2014,24(6):1472- 1478. doi:10. 1016/j. bmcl. 2014. 02. 008.
[7] Zhou A,Jia J. A screen for cognitive assessments for patients with vascular cognitive impairment no dementia[J].Int J Geriatr Psychiatry,2009,24(12):1352- 1357. doi:10. 1002/gps.2265.
[8] Pandey A,Saxena K,Verma M,et al. Correlative study between neuron-specific enolase and blood sugar level in ischemic stroke patients [J].J Neurosci Rural Pract,2011,2(1):50- 54. doi:10. 4103/0976- 3147. 80099.
[9] Elgebaly MM,Ogbi S,Li W,et al. Neurovascular injury in acute hyperglycemia and diabetes:a comparative analysis in experimental stroke[J].Transl Stroke Res,2011,2(3):391- 398. doi:10. 1007/s12975- 011- 0083- 3.
[10] Rehni AK,Nautiyal N,Perez-Pinzon MA,et al. Hyperglycemia/hypoglycemia-induced mitochondrial dysfunction and cerebral ischemic damage in diabetics [J].Metab Brain Dis,2015,30(2):437- 447. doi:10. 1007/s11011- 014- 9538-z.
[11] Lindsberg PJ,Tuomi T,Kaste M. Oral glucose tolerance test should be performed after stroke and transient ischemic attack[J].Int J Stroke,2011,6(4):317- 320. doi:10. 1111/j. 1747- 4949. 2011. 00619. x.
[12] Dungan KM,Braithwaite SS,Preiser JC. Stress hyperglycaemia[J].Lancet,2009,373(9677):1798- 1807. doi:10. 1016/S0140- 6736(09)60553- 5.
[13] Bellolio MF,Gilmore RM,Ganti L. Insulin for glycaemic control in acute ischaemic stroke [J].Cochrane Database Syst Rev,2014,(1):CD005346. doi:10. 1002/14651858. CD005346.pub4.
[14] Wan Sulaiman WA,Hashim HZ,Che Abdullah ST,et al. Managing post stroke hyperglycaemia:moderate glycaemic control is better?An update [J].EXCLI J,2014,8(13):825- 833.
CorrelationofStressHyperglycemiaafterIschemicStrokewithEarlyVascularCognitiveImpairment
ZHOU Yidong1,2,YUAN Huaiwu1,JI Renjie1,LUO Benyan1
1Department of Neurology,the First Affiliated Hospital,College of Medicine,Zhejiang University,Hangzhou 310003,China2Department of Neurology,Ningbo First Hospital,Ningbo,Zhejiang 315000,China
LUO Benyan Tel:0571- 87235101,E-mail:luobenyan@zju.edu.cn
ObjectiveTo investigate the influence and forecast value of stress hyperglycemia on the early vascular cognitive impairment (VCI) in stroke patients.MethodsTotally 422 patients with acute non-diabetic stroke were divided into three groups according to the fasting plasma glucose level:the euglycemia group (<6.1 mmol/L),the mild stress hyperglycemia group (6.1- 7.0 mmol/L),and the severe stress hyperglycemia group (≥7.0 mmol/L).Mini-mental state examination,Alzheimer’s disease rating scale cognitive subscale,and clinical dementia rating scale were used to evaluate early cognition in post-stroke patients,and patients were divided into three groups accordingly:normal cognitive function group,mild VCI group,and vascular dementia group.Correlation analysis was carried out on the level of stress hyperglycemia and the degree of VCI.ResultsOf these 422 patients,stress hyperglycemia was identified in 62 cases (14.7%).The risk of stress hyperglycemia was higher in patients with a high degree of education [(8.39±3.85)yearsvs.(6.62±4.39)years,P=0.037)] or a history of cardiovascular disease (45.2%vs.18.3%,P=0.001).VCI was detected in 270 patients (64.0%).Age,sex,smoking,National Institute of Health Stroke Scale score,Hamilton Depression Rating Scale score,stress hyperglycemia,and history of cardiovascular disease were related with early VCI after non-diabetic ischemic stroke (P<0.05).Multivariate Logistic regression analysis showed that stress hyperglycemia was an independent risk factor for VCI in patients with non-diabetic ischemic stroke (OR=3.086,95%CI=1.065- 8.929).The risks of cognitive impairment in the mild stress hyperglycemia group and the severe stress hyperglycemia group were higher than that of the euglycemia group,while it was also higher in the severe stress hyperglycemia group than in the mild stress hyperglycemia group (61.11%vs.75.00%vs.90.91%).Stress hyperglycemia was positively correlated with the high risk of early cognitive impairment in stroke patients (rs=0.185,P=0.007).ConclusionThere is a significant correlation between stress hyperglycemia and early VCI after ischemic stroke.
ischemic stroke;stress hyperglycemia;vascular cognitive impairment
ActaAcadMedSin,2017,39(6):749-755
“十二五”国家科技支撑计划(2011BAI08B02) Supported by the “12thFive-Year” National Science and Technology Supporting Program (2011BAI08B02)
罗本燕 电话:0571- 87235101,电子邮件:luobenyan@zju.edu.cn
R741
A
1000- 503X(2017)06- 0749- 07
10.3881/j.issn.1000- 503X.2017.06.003
2016- 11- 24)

