GS方案一线化疗后替吉奥维持治疗晚期胰腺癌的疗效和安全性
王彩玲 王俊生 周静
GS方案一线化疗后替吉奥维持治疗晚期胰腺癌的疗效和安全性
王彩玲 王俊生 周静
作者单位:455000 安阳 河南安阳市肿瘤医院内六科
目的观察晚期胰腺癌GS方案(吉西他滨+替吉奥)一线化疗疾病控制后替吉奥单药维持治疗的疗效和安全性。方法41例晚期胰腺癌患者经GS方案化疗达疾病控制后随机分为替吉奥组20例和对照组21例,替吉奥组继续替吉奥原剂量维持治疗直至疾病进展,对照组仅定期复查,每2个周期评价疗效。观察两组疗效及不良反应。结果替吉奥组中位无进展生存期为6.8个月,中位总生存期为8.9个月;对照组中位无进展生存期为4.1个月,中位总生存期为5.7个月,两组比较差异均有统计学意义(P<0.05)。两组患者常见不良反应主要为骨髓抑制和消化道反应,以Ⅰ~Ⅱ度为主,其中替吉奥组白细胞降低、延迟性腹泻、恶心呕吐及手足综合征发生率与对照组比较差异有统计学意义(P<0.05)。结论GS方案一线化疗后替吉奥维持治疗晚期胰腺癌具有良好的疗效与耐受性,值得临床推广应用。
胰腺肿瘤;晚期;吉西他滨;维持治疗;临床疗效
胰腺癌是消化道常见的恶性肿瘤之一,起病隐匿,早期症状不典型,85%的患者确诊时已发生淋巴结转移或远处转移[1],失去手术根治切除的机会。化疗在晚期胰腺癌治疗中备受重视,化疗后有效率及生存率均得以提高。本研究观察GS方案(吉西他滨+替吉奥)一线化疗疾病控制后替吉奥单药维持治疗晚期胰腺癌的疗效和不良反应,现将结果报道如下。
1 资料与方法
1.1 一般资料
收集2010年4月至2015年8月河南安阳市肿瘤医院收治的晚期胰腺癌患者,所有患者均采用GS方案化疗4个周期后获疾病控制,影像学检查至少有1个可测量病灶,ECOG评分<2分,血常规、肝肾功能及心电图等检查均正常,无化疗禁忌证,预计生存期>3个月。共41例患者符合标准纳入研究,化疗4个周期后,将41例患者随机分为2组,其中替吉奥组20例,对照组21例。替吉奥组男性12例,女性8例,年龄43~70岁,中位年龄54岁;ECOG评分 0分9例,1分11例;手术 17例,未手术3例;肝转移18例,腹腔转移7例。对照组男性15例,女性6例,年龄45~71岁,中位年龄57岁;ECOG评分 0分12例,1分9例;手术15例,未手术6例;肝转移13例,腹腔转移10例,两组患者性别、年龄、ECOG评分及转移部位等差异无统计学意义(P>0.05),具有可比性。本研究均征得患者知情同意。
1.2 治疗方法
所有患者均采用GS方案一线化疗:吉西他滨1 000 mg/m2,d1、d8;替吉奥(S-1)d1~14,2 次/d,早晚口服给药,按体表面积<1.25 m2予40 mg/次;体表面积≥1.25 m2但<1.5 m2予50 mg/次;体表面积≥1.5 m2予60 mg/次;21 d为1个周期,共4个周期。对照组40 d后来院复查,必要时给予止痛等对症处理;替吉奥组继续原剂量口服替吉奥维持化疗,口服托烷司琼胶囊止吐,严重胃肠道反应者给予甲强龙和托烷司琼注射液治疗。化疗期间白细胞发生Ⅲ~Ⅳ度骨髓抑制,给予造血细胞集落刺激因子;血小板发生Ⅲ~Ⅳ度骨髓抑制,予重组人血小板生成素;每连续用药2个周期后评价疗效,直至疾病进展。
1.3 评价标准
近期客观疗效按WHO实体瘤疗效评定标准进行评估,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和疾病进展(PD)。疾病有效率(RR)=(CR+PR)/总例数×100%,疾病控制率(DCR)=(CR+PR+SD)/总例数×100%。无进展生存期为患者首次用药至疾病进展的时间,总生存时间为首次用药至死亡的时间。毒副反应按照美国国立癌症研究院通用毒性标准(NCICTC)3.0版进行评价。
1.4 统计学处理
采用SPSS 17.0软件进行数据分析。计数资料比较采用χ2检验;生存分析采用Kaplan-Meier法,组间比较行log-rank检验。以P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效
替吉奥组获CR 0例、PR 4例、SD 14例、PD 2例,疾病有效率为20%,疾病控制率为90%;对照组获CR 0例,PR 0例,SD 7例,PD 14例,疾病有效率为 0,疾病控制率为33.3%,两组疾病有效率及疾病控制率比较差异均有统计学意义(P<0.05)。
2.2 不良反应
两组患者常见不良反应主要为骨髓抑制、消化道反应,其中替吉奥组白细胞降低、延迟性腹泻、恶心呕吐及手足综合征发生率与对照组比较差异有统计学意义(P<0.05),但多以Ⅰ~Ⅱ级为主,患者均可耐受。替吉奥组发生Ⅲ度血小板下降2例,经升血小板治疗后恢复。两组均无治疗相关死亡患者。见表1。
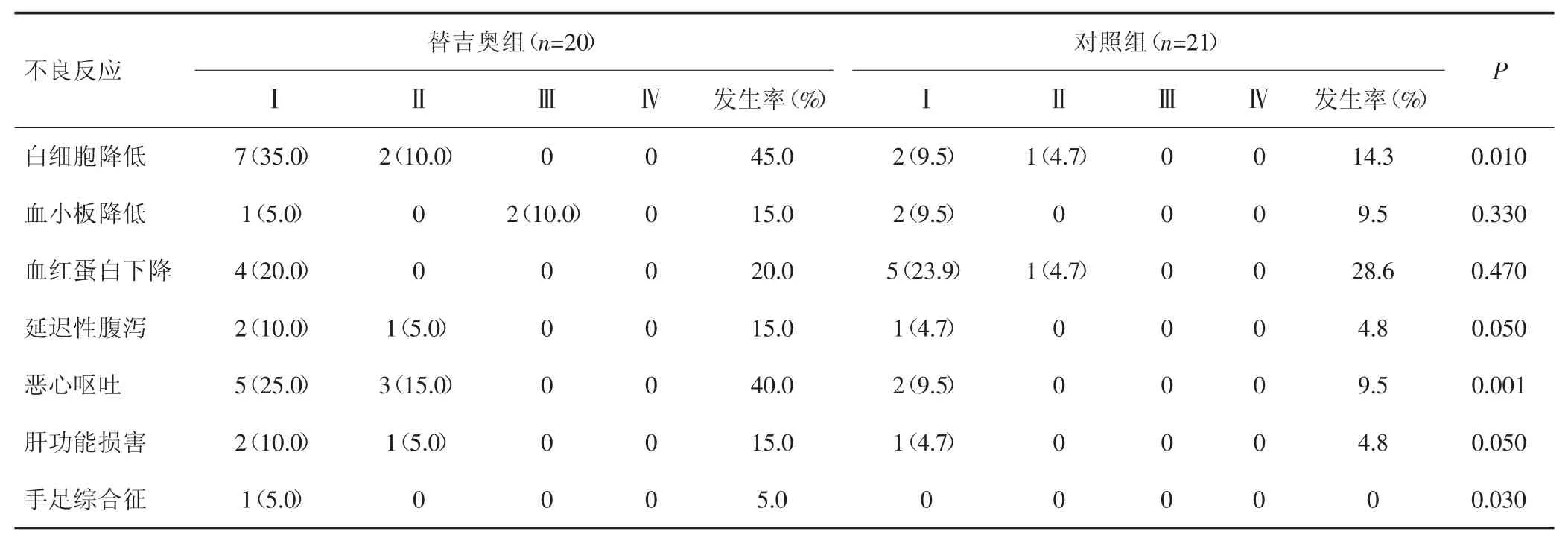
表1 两组不良反应比较[n(%)]
2.3 生存情况
替吉奥组共化疗113个周期,中位无进展生存期为 6.8 个月(95%CI:6.43~7.18),中位总生存期为 8.9个月(95%CI:8.14~9.46)。对照组中位无进展生存期为 4.1 个月(95%CI:3.95~4.23),中位总生存期为5.7 个月(95%CI:5.15~6.25),两组无进展生存和总生存曲线比较差异均有统计学意义(P<0.05)。见图1、图2。
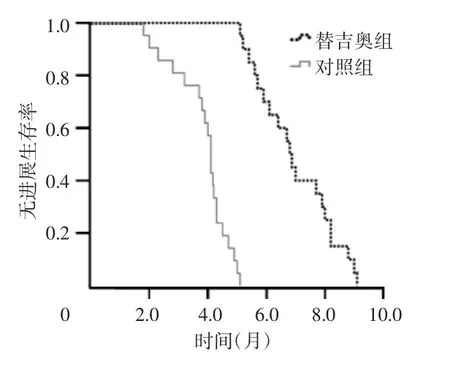
图1 两组无进展生存曲线比较
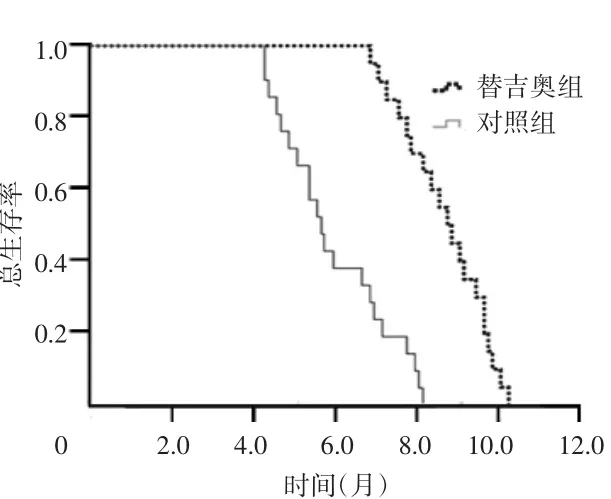
图2 两组总生存曲线比较
3 讨论
胰腺癌发病率和死亡率在我国呈持续上升趋势[2],发病率居第6位,可能与环境、生活习惯、遗传易感性等因素有关[3]。大约80%的患者确诊时已属中晚期,仅20%的患者有手术治疗机会[4],然而即使手术,多数患者仍面临复发。对于晚期及术后复发的胰腺癌患者,化疗成为主要的治疗手段,选择疗效可靠、耐受良好的治疗方案,对提高患者生活质量、延长生存期具有重要意义。
吉西他滨是一种人工合成的嘧啶核苷类似物,研究发现其对多种肿瘤有效,临床多用于非小细胞肺癌、乳腺癌、食管癌、膀胱癌及胰腺癌等肿瘤治疗[5-6]。单药吉西他滨治疗晚期胰腺癌客观缓解率为5.4%~19.0%,疾病控制率为23%~40%[7-8]。吉西他滨单药曾被推荐为一线治疗胰腺癌的首选用药[9]。替吉奥是第三代氟尿嘧啶衍生物口服抗癌剂。研究表明,替吉奥单药治疗晚期胰腺癌的疗效不低于吉西他滨[10],而吉西他滨和替吉奥具有协同抗肿瘤活性[11],且不存在交叉性毒性。有研究显示替吉奥能改善吉西他滨难治性胰腺癌患者的预后[12]。推测GS方案或可提高晚期胰腺癌疗效及安全性。
目前晚期胰腺癌有效的化疗方案较少,化疗后缓解期较短,疾病进展较快。国外研究显示,吉西他滨联合替吉奥方案治疗晚期胰腺癌的无疾病进展期为5.7个月,中位生存期为9.4~10.1个月[13-14]。而国内研究表明GS方案治疗晚期胰腺癌有效率达44.0%~46.2%,无疾病进展期为4.6个月,中位生存期为6.1个月[15]。本研究对照组中位无进展生存期为4.1个月,中位总生存期为5.7个月,与国内研究结果相近,但与国外仍有一定差距,考虑与患者体质、用药剂量或纳入研究的病例数较少有关。目前有关晚期胰腺癌患者一线化疗疾病得到控制后应用维持化疗的临床随机对照研究较少,本研究采用GS方案一线化疗获疾病缓解后替吉奥单药维持治疗,中位无进展生存期为6.8个月,中位总生存期为8.9个月,与对照组相比,中位无进展生存期和中位总生存期明显提高。
两组不良反应主要为胃肠道反应及骨髓抑制,替吉奥维持治疗不良反应发生率较高,其中白细胞降低、消化道反应及手足综合征发生率两组比较差异有统计学意义,但多为Ⅰ~Ⅱ级,患者均可耐受,未影响后续治疗,均无治疗相关死亡患者。说明GS方案化疗后替吉奥维持治疗晚期胰腺癌可取得良好疗效,安全、可行。但本研究样本量较少,有关结论尚需进一步研究。
[1]李娜,李薇,何倩,等.替吉奥联合吉西他滨一线治疗晚期胰腺癌疗效观察[J].安徽医药,2014,18(10):1957-1959.
[2]马 臣,姜永晓,刘曙正,等.中国胰腺癌发病趋势分析和预测[J].中华流行病学杂志,2013,34(2):160-163.
[3]Chen W,Liang D,Zhang S,et al.Pancreatic Cancer Incidence and Mortality Patterns in China,2009[J].Asian Pac J Cancer Prev,2013,14(12):7321-7324.
[4]Paulson AS,Tran Cao HS,Tempero MA,et al.Therapeutic advances in pancreatic cancer[J].Gastroenterology,2013,144(6):1316-1326.
[5]Laskin JJ,Nicholas G,Lee C,et al.Phase I/Ⅱ trial of custirsen(OGX-011),an inhibitor of clusterin,in combination with a gem-citabine and platinum regimen in patients with previously untreated advanced non small cell lung cancer[J].Thorac Oncol,2012,7(3):579-586.
[6]Li L,Schaid DJ,Fridley BL,et al.Gemcitabine metabolic pathway genetic polymorphisms and response in patients with non-smallcell lung cancer[J].Pharmacogenet Genomics,2012,22(2):105-116.
[7]潘伟明.吉西他滨联合奥沙利铂治疗晚期胰腺癌35例[J].药物与临床,2011,8(4):74-75.
[8]马守成,赵达,侯小明,等.吉西他滨联合康莱特治疗晚期胰腺癌的临床疗效研究[J].现代肿瘤医学,2012,20(7):1415-1417.
[9]Hu J,Zhao G,Wang HX,et al.A meta-analysis of gemcitabine containing chemotherapy for locally advanced and metastatic pancreatic adenocarcinoma[J].J Hematol Oncol,2011,4:11-12.
[10]Fukutomi A,Okusaka T,Sugimori K,et al.Updated results of the GEST study:randomized phaseⅢ study of gemcitabine plus S-1(GS)versus S-1 versus gemcitabine(GEM)in unresectable advanced pancreatic cancer in Japan and Taiwan[J].J Clinical Oncology,2012,30:130.
[11]Morimoto Y,Takeuchi O,Takitawa A,et al.Effect of a combination of S-1 and gemcitabine on cell cycle regulation in pancreatic cancer cell lines[J].Anti-cancer Drugs,2012,23(5):505-514.
[12]Nakai Y,Isayama H,Sasaki T,et al.Impact of S-1 in patients with gemcitabine-refractory pancreatic cancer in Japan[J].Japanese Journal of Clinical Oncology,2010,40(8):774-780.
[13]Song H,Han B,Park CK,et al.Phase II trial of gemcitabine and S-1 for patients with advanced pancreatic cancer[J].Cancer Chemother Pharmacol,2013,72(4):845-852.
[14]Conroy T,Desseigne F,Ychou M,et al.FOLFIRINOX versus gemcitabine for metastatic pancreatic cancer[J].N Engl J Med,2011,364(19):1817-1825.
[15]王新林,宋锦文,等.替吉奥胶囊联合吉西他滨治疗晚期胰腺癌的疗效分析[J].现代肿瘤医学,2014,22(3):588-590.
Efficacy and safety of maintenance chemotherapy with S-1 following treatment with gemcitabine and S-1 for advanced pancreatic cancer
Wang Cailing,Wang Junsheng,Zhou Jing(Department of Medical,Anyang Tumor Hospital,Anyang 455000,P.R.China)
ObjectiveTo observe efficacy and side effects of S-1 maintenance chemotherapy for patients with advanced pancreatic cancer initially treated with gemcitabine and S-1.MethodsA total of 41 patients with advanced pancreatic cancer
gemcitabine and S-1 as first-line therapy,and then they were randomly divided into a group that received maintenance therapy with S-1 alone until progression of disease(n=20),and a control group that was merely observed(n=21).Every two cycles,efficacy and adverse reactions were compared between the two groups.ResultsMedian progression-free survival was 6.8 months in the S-1 group and 4.1 months in the control group.Median overall survival was 8.9 months in the S-1 group and 5.7 months in the control group.The differences between the two groups were significant(Plt;0.05).The main adverse reactions included bone marrow aplasia and gastrointestinal reactions,most of which were grade Ⅰ-Ⅱ.Patients in the S-1 group showed significantly higher rates of low leucocyte neutrophil,nausea/vomiting and hand-foot syndrome(P<0.05).Conclusions Maintenance chemotherapy with S-1 alone following initial therapy with gemcitabine and S-1 is safe and effective in patients with advanced pancreatic cancer.
Pancreatic neoplasms;Advanced stage;Gemcitabine;Maintenance chemotherapy;Clinical effects
R735.9
A
1674-5671(2017)05-04
10.3969/j.issn.1674-5671.2017.05.11
[2017-05-23收稿][2017-07-24修回][编辑 罗惠予]

