硫辛酸联合依帕司他和硫辛酸治疗糖尿病周围神经病变临床疗效比较的Meta分析
王晓彤,林海雄,徐 帅,卢颖琨
1广州中医药大学附属深圳市宝安中医院(集团),广东深圳 518133 2广州中医药大学第一临床医学院,广州 510405 3广州中医药大学中药学院,广州 510006
·论著·
硫辛酸联合依帕司他和硫辛酸治疗糖尿病周围神经病变临床疗效比较的Meta分析
王晓彤1,林海雄2,徐 帅3,卢颖琨2
1广州中医药大学附属深圳市宝安中医院(集团),广东深圳 5181332广州中医药大学第一临床医学院,广州 5104053广州中医药大学中药学院,广州 510006
目的比较硫辛酸联合依帕司他与硫辛酸治疗糖尿病周围神经病变(DPN)患者的临床疗效。方法收集2016年2月以前CNKI、CBM、维普、万方、PubMed等数据库中硫辛酸联合依帕司他对比硫辛酸治疗DPN的临床试验资料,采用Cochrane系统及Jadad评分对文章进行质量评估,RevMan5.3软件对多项研究结果的总体效应进行Meta分析。结果共纳入9项研究。Meta分析结果显示:硫辛酸显效率明显低于硫辛酸联合依帕司他[RR=0.58,95%CI(0.47,0.71),P<0.00001],正中运动神经传导速度[WMD=-4.94,95%CI(-7.41,-2.46),P<0.0001]、腓总运动神经传导速度[WMD=-5.08,95%CI(-7.68,-2.49),P=0.0001]、正中感觉神经传导速度[WMD=-4.24,95%CI(-6.20,-2.29),P<0.0001]和腓总感觉神经传导速度[WMD=-3.66,95%CI(-5.02,-2.31),P<0.00001]也明显低于联合用药。敏感性分析显示结果稳健。但纳入研究存在设计报道简单、主观指标少、随访时间短等问题。结论硫辛酸联合依帕司他可提高显效率,增加正中或腓总神经的运动神经传导速度和感觉神经传导速度。由于目前纳入文献质量普遍不高,需谨慎考虑此结论,希望有更多高质量的随机对照试验支持。
硫辛酸联合依帕司他;硫辛酸;糖尿病周围神经病变;Meta分析
糖尿病周围神经病变(diabetic peripheral neuropathy,DPN)是糖尿病最常见的慢性并发症。据统计,预计到2030年,全球糖尿病患者将达到4.72亿人,其中DPN将使近2.36亿人承担巨额经济负担[1],因此,防治DPN具有重要意义。DPN发病机制较为复杂,包括高血糖毒性所致多元醇旁路的激活、非酶促糖基化产物的沉积、局部血流微循环障碍、免疫失调、脂代谢紊乱、氧自由基损伤及神经营养因子缺乏等。目前认为,改善代谢失衡是治疗DPN的主要措施[2]。抗氧化应激药物硫辛酸、醛糖还原抑制剂依帕司他均具有改善神经元缺氧及微血管功能的作用[3]。Meta分析发现,依帕司他改善DPN症状及神经传导速度与甲钴胺相似[4];静脉滴注硫辛酸相对安慰剂可明显缓解周围神经病变症状(SMD:-2.8,95%Cl:-4.2~-1.5)[5]。近年来,二者联合运用防治DPN亦日益彰显出优势[6- 15],但现有的研究规模小,参考意义有限,缺乏系统评价。本研究采用循证医学的方法,比较了硫辛酸联合依帕司他与硫辛酸治疗DPN患者的显效率、运动神经传导速度和感觉神经传导速度,以期为今后的临床应用提供参考。
资料和方法
文献纳入标准和排除标准研究对象:诊断为DPN的患者,患者来源、数量、病情类型不限;排除动物实验。干预措施:试验组为硫辛酸联合依帕司他治疗,对照组为硫辛酸治疗。试验组和对照组的基础对症治疗完全一致。设计方案:纳入随机对照试验(randomized controlled trials,RCTs)或临床对照试验。排除横断面研究、病例对照研究、队列研究等。结局指标:纳入报道了显效率、正中运动神经传导速度、腓总运动神经传导速度、正中感觉神经传导速度、腓总感觉神经传导速度的文献;排除没有这些指标的研究。其中显效:自觉症状明显好转或消失,膝反射明显好转或基本恢复正常,肌电图神经传导速度增大>5 m/s或恢复正常。
文献检索策略以“依帕司他”并且“硫辛酸”并且“周围神经病变”为主题词,检索CNKI。以“依帕司他”与“硫辛酸”与“周围神经病变”为主题词,检索万方数据库。以“依帕司他”AND“硫辛酸”AND“周围神经病变”为主题词,检索CBM文献。以“依帕司他”与“硫辛酸”与“周围神经病变”为主题词,检索中文期刊数据库(维普)。检索PubMed:以((“diabetic”[All Fields] AND “pripheral neuropathy”[All Fields]) AND(“thioctic acid”[MeSH Terms] OR(“thioctic”[All Fields] AND “acid”[All Fields]) OR “thioctic acid”[All Fields]) OR(“lipoic”[All Fields] AND “acid”[All Fields]) OR “α-lipoic acid”[All Fields]) AND(“epalrestat”[Supplementary Concept] OR “epalrestat”[All Fields]))检索,时间截止至2016年2月,检索不受发表类型限制。
资料提取质量评价由两名研究者分别独立检索文献,进行提取,通过阅读文献检出符合纳入标准文献,如有分歧通过讨论解决,意见不一致时通过请教专家、讨论解决。纳入研究的方法学质量评价采用Cochrane协作网推荐的评价方法进行风险评估及纳入质量的评判,其中包括:选择偏倚、实施偏倚、测量偏倚、失访偏倚、报告偏倚,其他偏倚[16]。同时对纳入研究进行Jadad评分:1~3分为低质量,3~5分为高质量[17]。
统计分析以临床显效率、运动神经传导速度、感觉神经传导速度作为评价指标,分别将全部试验数据合并,采用RevMan 5.3软件进行效应模型的Meta分析。二分变量采用相对危险度(risk ratio,RR)表示合并效应量,连续变量采用加权均数差(weighted mean difference,WMD),并给出95%Cl。运用stata对发表偏倚进行Begg’s检验和Egger’s检验。
异质性评价及敏感性分析对全部研究结果均进行异质性评价,如存在异质性则进行探索型Meta分析,以找出其原因。纳入研究结果间的异质性采用χ2检验;若各文献存在同质性(I2≤50%或P>0.05),采用固定效应模型。若文献间存在异质性时(I2>50%或P≤0.05),则考虑开展亚组分析、敏感性分析或采用随机效应模型。
结 果
文献检索结果经CNKI、CBM、维普、万方、PubMed检索,共检索出168篇,通过题目及摘要初筛剩余22篇,经ENDNOTE查重后剩余10篇。根据结局指标纳入,乔彦等[15]的研究因无报道纳入的结局指标之一予排除。最终9篇进入系统评价[6- 14](表1)。
质量评价根据Cochrane协助网的风险评估方法,纳入研究具有可比性,但存在不同程度的偏倚,其中1篇[7]未提及随机分配,1篇[13]为低偏倚风险,其余均存在中偏倚风险(图1~2)。Jadad评分普遍不高,3分以上仅1篇[13](表1)。

表 1 纳入文献的一般资料Table 1 Characteristics of included studies
A:硫辛酸300 mg,iv,qd;B:硫辛酸 600 mg,iv,qd;C:硫辛酸 450 mg,iv,qd;D:硫辛酸胶囊200 mg,tid,po;E:依帕司他片50 mg,tid,po;NCV:神经传导速度;MNCV:运动神经传导速度;SNCV:感觉神经传导速度;EMG:肌电图;FPG:空腹血糖
A:lipoic acid 300 mg,iv,qd;B:lipoic acid 600 mg,iv,qd;C:lipoic acid 450 mg,iv,qd;D:lipoic acid capsule 200 mg,tid,po;E:epalrestat 50 mg,tid,po;NCV:nerve conduction velocity;MNCV:motor nerve conduction velocity;SNCV:sensory nerve conduction velocity;EMG:electromyogram;FPG:fasting plasma glucose
图1 偏倚风险图:复审作者对所有纳入研究的偏倚风险百分比评判
Fig1 Risk of bias graph:review authors’ judgments about each risk of bias item presented as percentages across all included studies

图2 偏倚风险总结:复审作者对每个纳入研究的偏倚风险评判
Fig2 Risk of bias summary:review authors’ judgments about each risk of bias item for each included study
显效率共纳入6个研究,具有同质性(χ2=5.82,I2=14%,P=0.32),用固定效应模型;合并效应量RR=0.58;95%CI(0.47,0.71),差异有统计学意义(P<0.00001)(图3)。
运动神经传导速度(正中神经) 共纳入9个研究,异质性高(χ2=198.67,I2=96%,P<0.00001),用随机效应模型;合并效应量为加权均值WMD=-4.94,95%CI(-7.41,-2.46),差异有统计学意义(P<0.0001)(图4)。
运动神经传导速度(腓总神经) 共纳入9个研究,异质性高(χ2=322.89,I2=98%,P<0.00001),用随机效应模型;合并效应量为WMD=-5.08,95%CI(-7.68,-2.49),差异有统计学意义(P=0.0001)(图5)。
感觉神经传导速度(正中神经) 共纳入9个研究,异质性高(χ2=189.07,I2=96%,P<0.00001),用随机效应模型;合并效应量为WMD=-4.24,95%CI(-6.20,-2.29),差异有统计学意义(P<0.0001)(图6)。
感觉神经传导速度(腓总神经) 共纳入9个研究,异质性高(χ2=64.66,I2=88%,P<0.00001),用随机效应模型;合并效应量为WMD=-3.66,95%CI(-5.02,-2.31),差异有统计学意义(P<0.00001)(图7)。
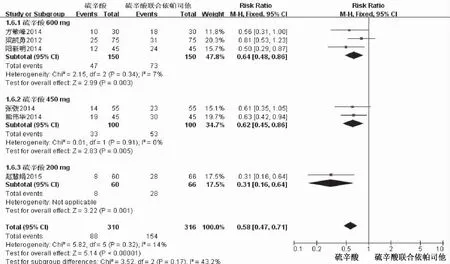
DPN:糖尿病周围神经病变
DPN:diabetic peripheral neuropathy
图3 硫辛酸联合依帕司他与硫辛酸治疗DPN显效率结局森林图
Fig3 Forest plot of lipoic acid combined with epalrestat versus lipoic acid in the treatment of DPN:markedly effective rate

MNCV:运动神经传导速度
MNCV:motor nerve conduction velocity
图4 硫辛酸联合依帕司他与硫辛酸治疗DPN正中运动神经传导速度结局森林图
Fig4 Forest plot of lipoic acid combined with epalrestat versus lipoic acid in the treatment of DPN:median MNCV

图5 硫辛酸联合依帕司他与硫辛酸治疗DPN腓总运动神经传导速度结局森林图
Fig5 Forest plot of lipoic acid combined with epalrestat versus lipoic acid in the treatment of DPN:peroneal MNCV

SNCV:感觉神经传导速度
SNCV:sensory nerve conduction velocity
图6 硫辛酸联合依帕司他与硫辛酸治疗DPN正中感觉神经传导速度结局森林图
Fig6 Forest plot of lipoic acid combined with epalrestat versus lipoic acid in the treatment of DPN:median SNCV
敏感性分析腓总感觉神经传导速度排除文献前后得出的结论一致,提示本研究结果稳健;其余敏感性分析亦未见明显异常。同时发现,去除高凌等[9]的研究后,静滴硫酸锌600 mg的异质性低(I2=0,P=0.60),合并效应量为WMD=-4.96<-3.96,95%CI(-5.80,-4.12),差异有统计学意义(P<0.00001),其结果参考价值更高(表2)。
亚组分析进一步对硫酸锌 600 mg按照疗程进行亚组分析,结果显示,高凌等[9]研究所在的亚组异质性均较高。此外,除正中运动神经传导速度外,疗程21 d的亚组异质性普遍较低,参考价值更高(表3)。
发表偏倚对9篇腓总感觉神经传导速度文献进行漏斗图分析,见漏斗图基本对称,经Begg’s检验结果为Z=-0.10,P=1.000;Egger’s检验结果为t=-1.32,P=0.228(图8)。

图7 硫辛酸联合依帕司他与硫辛酸治疗DPN腓总感觉神经传导速度结局森林图
Fig7 Forest plot of lipoic acid combined with epalrestat versus lipoic acid in the treatment of DPN:peroneal SNCV

表 2 敏感性分析Table 2 Sensitivity analysis of the included studies

表 3 亚组分析Table 3 Subgroup analysis of the included studies

图8 腓总感觉神经传导速度漏斗图
Fig8 Funnel plot of peroneal SNCV
讨 论
据报道,糖尿病患者中DPN的患病率约30%~90%,四肢远端感觉、运动障碍是其主要临床特点,具体表现为肢体麻木、挛急疼痛,肌肉无力或萎缩、腱反射减弱或消失等[18]。一方面,糖尿病患者高血糖状态可引起细胞内外氧化应激水平过度升高,产生自由基,导致神经元、血管内皮细胞损伤[19]。因此,改善氧化应激状态是防治DPN的有效措施之一。硫辛酸作为一种强氧化剂,具有消除氧自由基、超氧基的活性,能够抗氧化,增加神经营养血管的血流量,增强神经Na+-K+-ATP酶活性,保护血管内皮功能,抑制神经内氧化应激状态,增加神经传导的速度[20]。另一方面,糖尿病患者山梨醇果糖代谢障碍,导致周围神经神经膜细胞坏变,髓鞘脱失和轴突变性。依帕司他是非竞争性、可逆性的醛糖还原酶抑制剂,能抑制多元醇代谢中的醛糖还原酶活性,使葡萄糖不能代谢成山梨醇,并减轻其在神经元内蓄积,从而改善DPN的症状,加快神经传导速度[21- 22]。本研究挖掘联合用药对比单纯硫辛酸治疗DPN,结果发现单纯硫辛酸防治DPN的显效率比硫辛酸联合依帕司他低,同时,运动神经传导速度、感觉神经传导速度均低于联合用药方案。
存在问题及展望:偏倚风险方面,纳入文献大部分无详细记载随机分组的具体方法,各组性别比例不详,或仅描述各组基线特征一样,无法排除性别差异等问题,不排除选择性偏倚;隐藏分配方面,医生、受试者、评估者的双盲缺乏描述,少数文献甚至无作者联系方式,不利于对原研究的详细了解;对于失访的记载,许多研究无明确规范描述;这些都直接导致了文献的Jadad评分普遍不高。敏感性分析发现,本研究结果稳健;同时,高凌等[9]的研究是导致硫辛酸600 mg改善腓总感觉神经传导速度异质性高的原因;疗程亚组分析发现,高凌等[9]所在亚组异质性均较高,该研究不能排除实施偏倚、测量偏倚、失访偏倚,同时,药物厂家、指标检测方法及灵敏度差异也是重要因素。随访方面,许多文章随访时间较短,只能提供短期疗效,无法提供长期预后评估。结局指标方面,可进一步报道多伦多评分系统等主观指标[23]。不良反应事件记载无明确的定义及定量指标分析。希望临床研究进一步规范设计,详细阐述科学设计,提供多中心、大样本、随机、双盲并长期随访的RCT并进一步分析,才能得到更加可靠、有意义的结论,为临床提供借鉴。
综上,硫辛酸联合依帕司他与硫辛酸相比,可提高显效率,增加正中或腓总神经的运动神经传导速度和感觉神经传导速度。但由于目前纳入文献质量普遍不高,需谨慎考虑此结论,希望有更多高质量的大样本双盲随机对照试验支持。
[1] Tesfaye S,Selvarajah D. Advances in the epidemiology,pathogenesis and management of diabetic peripheral neuropathy[J].Diabetes Metab Res Rev,2012,28(Suppl 1):8- 14. doi:10.1002/dmrr.2239.
[2] Hosseini A,Abdollahi M. Diabetic neuropathy and oxidative stress:therapeutic perspectives[J].Oxid Med Cell Longev,2013,2013:15. doi:10.1155/2013/168039.
[3] Tesfaye S. Recent advances in the management of diabetic distal symmetrical polyneuropathy[J].J Diabetes Investig,2011,2(1):33- 42. doi:10.1111/j.2040- 1124.2010.00083.x.
[4] 贾佳,余江毅. 依帕司他治疗糖尿病周围神经病变的Meta分析[J].中国糖尿病杂志,2013,21(9):782- 788. doi:10.3969/j.issn.1006- 6187.2013.09.005.
[5] Bartkoski S,Day M. Alpha-lipoic acid for treatment of diabetic peripheral neuropathy[J].Am Fam Physician,2016,93(9):786.
[6] 何宇梅,李先花,尹昭. 依帕司他联合硫辛酸治疗老年糖尿病周围神经病变疗效及安全性的临床观察[J].中国老年保健医学,2013,11(3):51- 52. doi:10.3969/j.issn.1672- 4860.2013.03.023.
[7] 方敏峰. 硫辛酸联合依帕司他治疗糖尿病周围神经病变疗效观察[J].现代医药卫生,2014,30(4):483- 484. doi:10.3969/j.issn.1009- 5519.2014.04.002.
[8] 颜斌. α-硫辛酸联合依帕司他治疗2型糖尿病周围神经病变临床疗效评价[J].中南医学科学杂志,2015,43(2):169- 171. doi:10.15972/j.cnki.43- 1509/r.2015.02.012.
[9] 高凌,杨颖,田源. 依帕司他联合α硫辛酸治疗糖尿病周围神经病变的疗效[J].实用药物与临床,2013,16(8):684- 685. doi:10.3969/j.issn.1673- 0070.2013.08.009.
[10] 梁凯勇,欧小娟,卢燕琼,等. 硫辛酸联合依帕司他治疗DPN疗效观察[J].实用糖尿病杂志,2012,8(3):46- 47.
[11] 熊伟华. 依帕司他联合α-硫辛酸治疗糖尿病周围神经病变[J].中国实用医药,2014,9(36):109- 110.
[12] 阳新明. 依帕司他联合α硫辛酸治疗糖尿病周围神经病变临床观察[J].中国社区医师:医学专业,2014,30(32):12- 13. doi:10.3969/j.issn.1007- 614x.2014.32.6.
[13] 赵慧娟,孟姝含,张秀娟. 硫辛酸治疗66例糖尿病周围神经病变的疗效观察[J].上海医药,2015,36(23):30- 32.
[14] 张弢,王晓梅,李湘,等. 依帕司他联合硫辛酸治疗糖尿病周围神经病变临床疗效[J].中国现代药物应用,2014,8(3):138- 139.
[15] 乔彦,赵景宏,何明海,等. α-硫辛酸联合依帕司他治疗周围神经病变的临床研究[J].实用糖尿病杂志,2015,11(2):21- 23.
[16] Higgins JPT,Altman DG,Sterne JAC. Chapter 8:Assessing risk of bias in included studies[M]//Higgins JPT,Green S. Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0(updated March 2011):The Cochrane Collaboration. 2011.http://www.cochrane-handbook.org.
[17] Jadad AR,Moore RA,Carroll D,et al. Assessing the quality of reports of randomized clinical trials:is blinding necessary[J].Control Clin Trials,1996,17(1):1- 12. doi:10.1016/0197- 2456(95)00134- 4.
[18] 庞国明,闫镛,朱璞,等. 糖尿病周围神经病变中医诊疗规范初稿[J].中华中医药杂志,2010,25(2):260- 264.
[19] 屈玲,梁晓春. 糖尿病周围神经病变与氧化应激关系的研究现状[J].中国中西医结合杂志,2007,27(8):764- 767.
[20] Kawai T,Takei I,Tokui M,et al.Effects of epalrestat,an aldose reductase inhibitor,on diabetic peripheral neuropathy in patients with type 2 diabetes,in relation to suppression of N-epsilon-carboxymethyl lysine[J].J Diabetes Complications,2010,24(6):424- 432. doi:10.1016/j.jdiacomp.2008.10.005.
[21] Ohmura C,Watada H,Azuma K,et al.Aldose reductase inhibitor,epalrestat,reduces lipid hydroperoxides in type 2 diabetes[J].Endocr J,2009,56(1):149- 156.doi:10.1507/endocrj.K08E- 237.
[22] Li QR,Wang Z,Zhou W,et al. Epalrestat protects against diabetic peripheral neuropathy by alleviating oxidative stress and inhibiting polyol pathway[J].Neural Regen Res,2016,11(2):345- 351. doi:10.4103/1673- 5374.177745.
[23] Zhang W,Zhong W,Yang M,et al.Evaluation of the clinical efficacy of multiple lower-extremity nerve decompression in diabetic peripheral neuropathy[J].Br J Neurosurg,2013,27(6):795- 799. doi:10.3109/02688697.2013.798854.
LipoicAcidCombinedwithEpalrestatversusLipoicAcidinTreatingDiabeticPeripheralNeuropathyAMeta-analysis
WANG Xiaotong1,LIN Haixiong2,XU Shuai3,LU Yingkun2
1Shenzhen Bao’an District TCM Hospital Group,the Affiliated Hospital of Guangzhou University of Chinese Medicine,Shenzhen,Guangdong 518133,China2The First School of Clinic Medicine,Guangzhou University of Chinese Medicine,Guangzhou 510405,China3School of Chinese Materia Medica of Guangzhou University of Chinese Medicine,Guangzhou 510006,China
LIN Haixiong Tel:020- 36598701,E-mail:lhxiong@foxmail.com
ObjectiveTo compare the clinical effectiveness of lipoic acid combined with epalrestat versus lipoic acid in treating diabetic peripheral neuropathy(DPN).MethodsRandomized controlled trials(RCTs) and clinical controlled trials on lipoic acid versus epalrestat for DPN before February 2016 were searched through five databases:CNKI,CBM,VIP,Wanfang,and PubMed. The quality of the included trials were assessed using Cochrane software and Jadad scores. Data were analyzed with Review Manager 5.3 software.ResultsNine studies were included in the analysis. Meta analysis showed that the lipoic aid monotherapy was significantly inferior to lipoic acid-epalerestat combination therapy [RR=0.58,95%Cl(0.47,0.71),P<0.00001]. Inferiority of the lipoic acid monotherapy was also shown in nerve conduction velocity with WMDs of-4.94 [95%Cl(-7.41,-2.46),P<0.0001] for median motor nerve conduction velocity(MNCV),-5.08 [95%Cl(-7.68,-2.49),P=0.0001] for peroneal MNCV,-4.24 [95%Cl(-6.20,-2.29),P<0.0001] for median sensory nerve conduction velocity(SNCV),and-3.66 [95%Cl(-5.02,-2.31),P<0.00001] for peroneal SNCV. Sensitivity analysis showed that the results were robust. However,the included trials were limited by simple design,few subjective indicators,and short follow-up time.ConclusionsLipoic acid combined with epalrestat is better than lipoic acid alone in the treatment of DPN,as well as the MNCV and SNCV of median or peroneal nerve. Due to the low quality of the included studies,high-quality RCTs are warranted to validate the results.
lipoic acid combined with epalrestat;lipoic acid;diabetic peripheral neuropathy;Meta-analysis
广州中医药大学大学生创新训练计划项目(201710572271)Supported by the College Students’ Innovative Entrepreneurial Training Program of Guangzhou University of Chinese Medicine(201710572271)
林海雄 电话:020- 36598701,电子邮件:lhxiong@foxmail.com
R977.6
A
1000- 503X(2017)05- 0656- 09
10.3881/j.issn.1000- 503X.2017.05.010
ActaAcadMedSin,2017,39(5):656-664
2016- 07- 13)

