全二维气相色谱-飞行时间质谱测定地下水中低环多环芳烃及其衍生物
张红庆,饶 竹*,王晓春,许丹丹,谷子欣,秦 恺,郭 峰,战 楠
(1.国家地质实验测试中心 生态地球化学重点实验室,北京 100037;2.鞍山师范学院 化学与生命科学学院,辽宁 鞍山 114016;3.中国矿业大学 地球科学与测绘工程学院,北京 100083;4.中国地质大学 材料与化学学院,湖北 武汉 430074)
全二维气相色谱-飞行时间质谱测定地下水中低环多环芳烃及其衍生物
张红庆1,饶 竹1*,王晓春2,许丹丹3,谷子欣4,秦 恺3,郭 峰1,战 楠1
(1.国家地质实验测试中心 生态地球化学重点实验室,北京 100037;2.鞍山师范学院 化学与生命科学学院,辽宁 鞍山 114016;3.中国矿业大学 地球科学与测绘工程学院,北京 100083;4.中国地质大学 材料与化学学院,湖北 武汉 430074)
建立了地下水中低环多环芳烃及其衍生物的全二维气相色谱-飞行时间质谱(GC×GC-TOF MS)检测方法。对比研究了液液萃取(LLE)和固相萃取(SPE)对地下水中低环多环芳烃及其衍生物的提取效率,优选液液萃取为前处理方法。在优化条件下,除1,2,3,4-四氢萘(r=0.987 2)和联苯(r=0.989 9)外,其它目标物在0.1~1 000 μg/L范围内具有良好的线性关系,相关系数(r)均大于0.99。地下水的平均加标回收率为63.3%~111%,除喹啉的相对标准偏差(RSD,n=6)为24.9%外,其余目标物的RSD均小于9.5%,方法检出限在1.63~14.7 ng/L之间。该方法用于河北地区6个地下水样中低环多环芳烃及其衍生物的检测,4个样品有检出,最高浓度达353 ng/L。
低环多环芳烃;衍生物;全二维气相色谱-飞行时间质谱;地下水
多环芳烃衍生物是多环芳烃的氢被卤素、氧原子等所取代、加成反应生成的一类化合物[1-2],部分多环芳烃衍生物比多环芳烃具有更强的“致癌、致畸和致基因突变作用”[3-4],近年来日益受到关注。其中低环多环芳烃衍生物的挥发性较强,易挥发到大气环境中,对人体健康造成威胁。多环芳烃衍生物主要来自于化石燃料和生物燃料等的不完全燃烧,在地表水、土壤、沉积物、大气及食品中均有检出[5-9]。特别是部分毒性较大、挥发性和迁移性较强的多环芳烃衍生物极易通过大气沉降、降雨等方式进入地下水,从而对地下水安全构成威胁,然而此方面的研究鲜有报道。
水中多环芳烃及其衍生物的前处理方法主要有固相萃取法(SPE)[10-12]和液液萃取法(LLE)[13-16]。由于地下水样品中多环芳烃及其衍生物含量较低,所以对样品前处理方法和仪器分析要求较高。SPE有机溶剂用量少,绿色环保,但选择性强,回收不稳定;而LLE为经典样品前处理方法,广谱、经济、准确度高,更适合地下水中多种痕量有机污染物的同时提取。全二维气相色谱-飞行时间质谱联用仪(GC×GC-TOF MS)是近年来出现的新技术,它克服了传统一维色谱峰容量低的局限性,通过一维色谱柱(1DGC)、二维色谱柱(2DGC)连续分离,达到了GC×GC分离能力,再结合飞行时间质谱快速、高灵敏度的检测能力,使之成为当前复杂混合物的最强分离分析技术之一[17-19]。本文利用这种新技术建立了地下水中低环多环芳烃及其衍生物快速、同时分析的方法,为进一步开展地下水中新型多环芳烃衍生物的研究和调查提供技术支撑。
1 实验部分
1.1 仪器与试剂
全二维气相色谱-飞行时间质谱(GC×GC-TOF MS),美国LECO公司:GC×GC系统由Agilent 7890B气相色谱仪和双喷口热调制器组成,MPS进样器(德国Gerstel公司),飞行时间质谱仪为美国LECO公司的PEGASUS 4D,数据处理系统为Chroma TOF软件;LABOROTA-4003型旋转蒸发仪(德国Heidolph公司);Milli-Q超纯水系统(美国Millipore公司);Rxi-5Sil MS气相色谱毛细管柱(30 m×0.25 mm×0.25 μm,美国Restek公司);Rxi-17Sil MS气相色谱柱(1.2 m×0.15 mm×0.15 μm,美国Restek公司)。HLB小柱(3 mL/60 mg,美国Waters公司);1 L棕色细颈螺旋口预清洗样品瓶(美国Thermo公司)。
目标化合物的保留时间和特征离子见表1,内标:苊-D10;替代物:萘-D8,均购自美国AccuStandard公司。
正己烷(HPLC级,美国Fisher Scientific公司),二氯甲烷(HPLC/ACS级,北京J&K百灵威科技公司),丙酮(农残级,美国Fisher Scientific公司);恒大冰泉矿泉水。
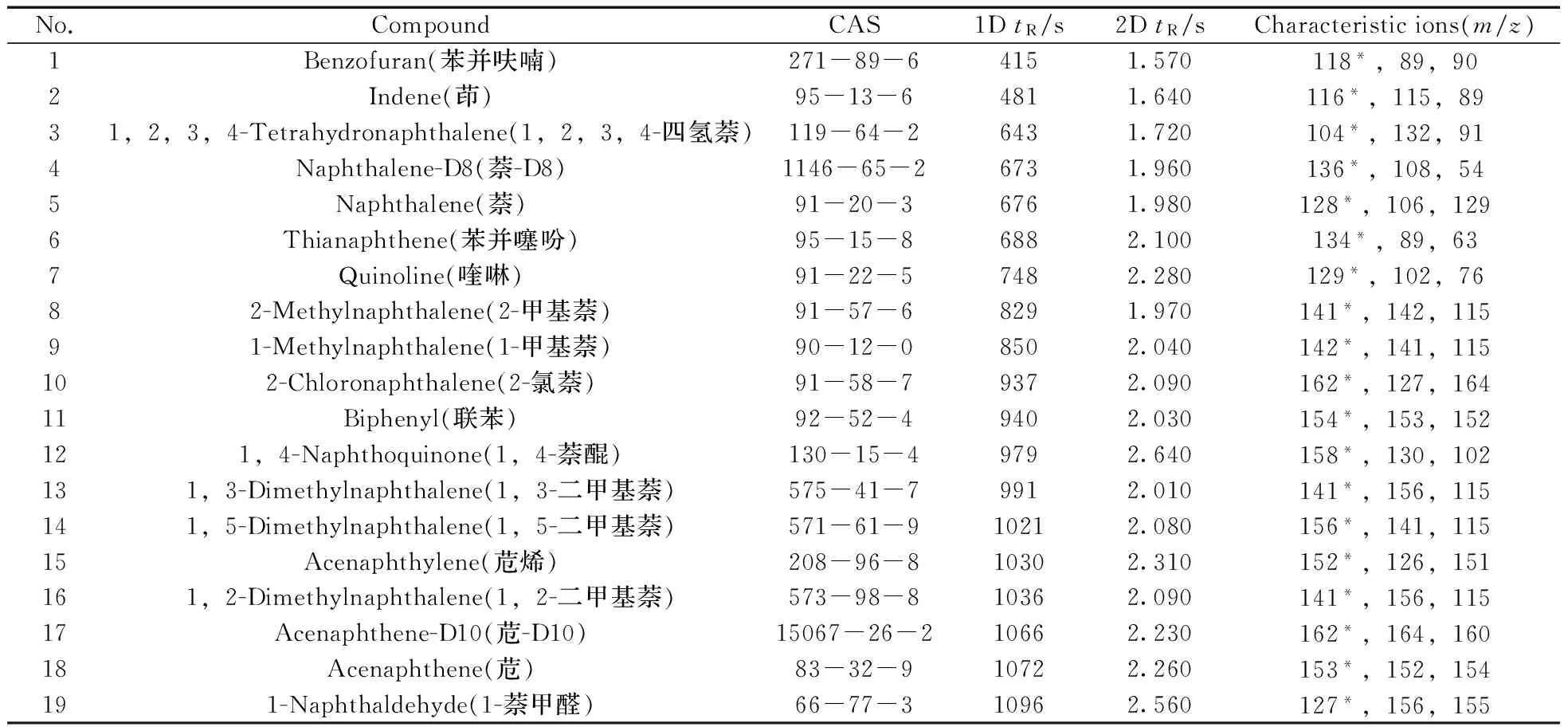
表1 多环芳烃及其衍生物的保留时间和特征离子Table 1 Retention times and characteristic ions of PAHs and their derivatives
*quantitative ion;1DtR:1stdimension retention time;2DtR:2nddimension retention time
1.2 样品前处理
量取1 L地下水样于1 L分液漏斗中,分别加入30.0 g NaCl、20 μL替代物标准溶液(10.0 μg/mL)和50 mL二氯甲烷-正己烷(1∶1)混合萃取溶剂,摇匀排气,于振荡器上振摇萃取10 min,静置分层后,将有机相转移至250 mL平底烧瓶中;后两次分别加入30 mL正己烷,重复上述操作,合并3次有机相,加适量无水硫酸钠除水,旋蒸浓缩至2~3 mL;然后转移至KD浓缩瓶中,氮吹至1.0 mL以下,加入20 μL 10.0 μg/mL混合内标标准溶液,正己烷定容至1.0 mL,待测。
1.3 气相色谱条件
色谱柱:一维柱:Rxi-5Sil MS气相色谱柱(30 m×0.25 mm×0.25 μm,美国Restek公司);二维柱:Rxi-17Sil MS气相色谱柱(1.2 m×0.15 mm×0.15 μm,美国Restek公司)。进样口温度:275 ℃,传输线温度:280 ℃;载气:氦气(纯度≥99.999%);进样量:2 μL;不分流进样;载气流速:1.5 mL/min;一维柱程序升温:初始温度60 ℃,保留0.5 min;以6 ℃/min升至200 ℃;最后以25 ℃/min升至300 ℃。二维炉温补偿温度:5 ℃,调制解调器补偿温度:15 ℃。调制周期:3 s,热吹时间0.6 s。以目标物的色谱保留时间、质谱图定性,内标法定量。
1.4 质谱条件
电子轰击源(EI源),电离电压70 eV,采集速率:100(谱图/s),检测电压:-1 750 V,离子源温度:240 ℃;扫描方式:全扫描模式;特征离子定量分析。
2 结果与讨论
2.1 固相萃取条件的优化
本实验对固相萃取(SPE)的洗脱溶剂进行了考察,使用HLB(Waters)固相萃取柱,依次用10 mL二氯甲烷、5 mL丙酮、10 mL甲醇和10 mL超纯水活化小柱,上样,干燥,10 mL洗脱溶剂淋洗,氮吹定容至0.5 mL,样品富集体积500 mL,富集倍数1 000倍。分别选择二氯甲烷、二氯甲烷-正己烷(1∶1)、二氯甲烷-正己烷(1∶4)、二氯甲烷-正己烷(4∶1)和丙酮-二氯甲烷(1∶4) 5种溶剂作为SPE的洗脱溶剂,得到的基质加标回收率为17.7%~136%。这表明固相萃取小柱不能稳定、完全选择性吸附挥发性较强的多环芳烃及其衍生物,且小柱在干燥除水过程中耗时较长,易使目标物挥发损失。
2.2 液液萃取与固相萃取的对比研究
对比研究了固相萃取(SPE)和液液萃取(LLE)两种前处理方法对目标物的提取回收率,液液萃取方法操作见“1.2”所述。对比结果显示,液液萃取的回收率(63.7%~101%)整体高于固相萃取,故选择回收率高且稳定的液液萃取作为样品前处理方法。
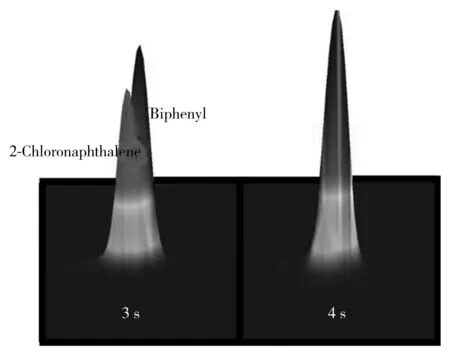
图1 联苯和2-氯萘在调制周期分别为3 s和4 s时的色谱图Fig.1 The comprehensive two-dimensional gas chromatography(GC×GC)surface plot of 2-chloronaphthalene and biphenyl in modulation period for 3 s and 4 s
2.3 调制周期的选择
全二维气相色谱的调制器主要起浓缩、聚焦、再进样的作用,合适的调制周期有利于化合物更好的分离,降低目标物的检出限[20]。如果调制周期过短,会使第一维流出的组分未能在同一周期内完成调制就进入下一周期,影响目标物的定性和定量;如果调制周期过长,减少了一维峰的切割次数,易出现共流出现象,从而导致一维色谱分辨率下降[21]。所以在满足分离度的条件下,应选择尽可能短的调制周期,有利于定性分析。本实验考察了调制周期分别为2、3、4 s时的效果,发现2 s的调制周期太短,个别目标物未能在同一周期内完成调制;4 s的调制周期过长,联苯和2-氯萘有共流出现象(见图1);而3 s时,全部目标物在同一周期流出且分离良好;所以选择调制周期为3 s。
2.4 方法的性能指标
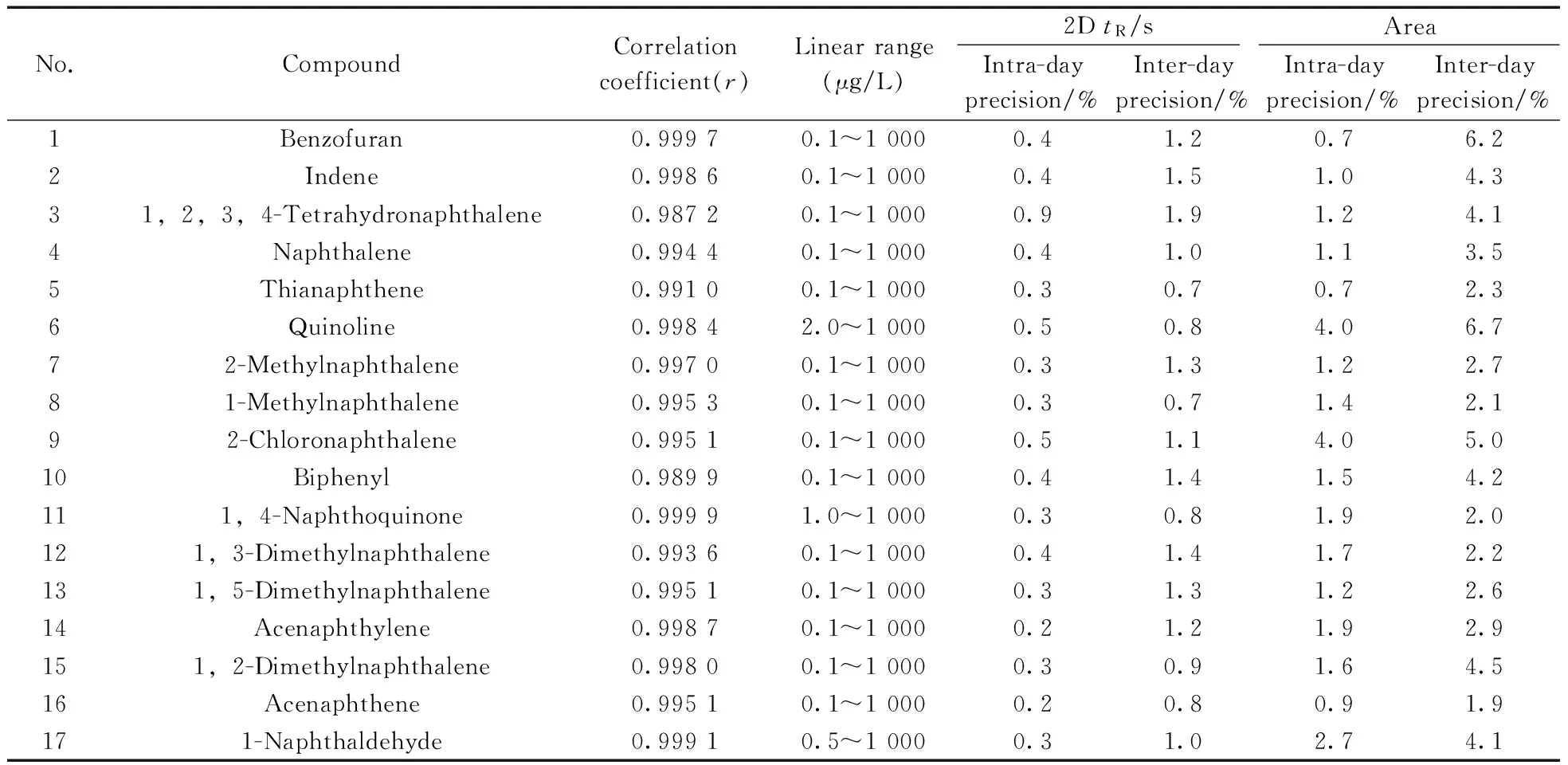
分别配制0.1、0.2、0.5、1.0、2.0、5.0、10.0、20.0、50.0、100、200、500、800、1 000 μg/L的多环芳烃衍生物混合标准溶液,其中内标和替代物浓度均为200 μg/L。在优化条件下上机测定,内标法定量,得到的相关系数见表2。除了1,2,3,4-四氢萘(r=0.987 2)和联苯(r=0.989 9)外,各目标组分在0.1~1 000 μg/L质量浓度范围内具有良好的线性,相关系数(r)均大于0.99。同一天内连续7次测定100 μg/L混合多环芳烃衍生物标准溶液,得到各目标物保留时间和峰面积的日内(Intra-day)精密度分别小于1.0%和4.0%;连续3 d测定100 μg/L多环芳烃衍生物混合标准溶液,保留时间和峰面积的日间(Inter-day)精密度分别小于2.0%和6.7%,表明仪器分析方法稳定性良好,结果见表2。实验配制了0.01~20.0 μg/L的多环芳烃衍生物混合标准溶液,分别按3倍信噪比和10倍信噪比作为仪器检出限(LOD)和仪器定量下限(LOQ),各目标物的LOD和LOQ分别为0.1~2.0 μg/L和0.3~7.5 μg/L,结果见表3。优化条件下200 μg/L低环多环芳烃衍生物的二维色谱图见图2。
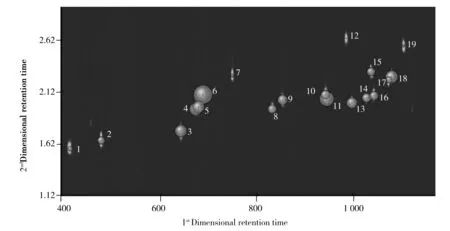
图2 低环多环芳烃衍生物的二维色谱图Fig.2 The comprehensive two-dimensional gas chromatography(GC×GC) contour plot of low-ring PAHs derivativesthe serial number of peaks correspond to the compound in Table 1
No.CompoundCorrelationcoefficient(r)Linearrange(μg/L)2DtR/sAreaIntra-dayprecision/%Inter-dayprecision/%Intra-dayprecision/%Inter-dayprecision/%1Benzofuran0.99970.1~10000.41.20.76.22Indene0.99860.1~10000.41.51.04.331,2,3,4-Tetrahydronaphthalene0.98720.1~10000.91.91.24.14Naphthalene0.99440.1~10000.41.01.13.55Thianaphthene0.99100.1~10000.30.70.72.36Quinoline0.99842.0~10000.50.84.06.772-Methylnaphthalene0.99700.1~10000.31.31.22.781-Methylnaphthalene0.99530.1~10000.30.71.42.192-Chloronaphthalene0.99510.1~10000.51.14.05.010Biphenyl0.98990.1~10000.41.41.54.2111,4-Naphthoquinone0.99991.0~10000.30.81.92.0121,3-Dimethylnaphthalene0.99360.1~10000.41.41.72.2131,5-Dimethylnaphthalene0.99510.1~10000.31.31.22.614Acenaphthylene0.99870.1~10000.21.21.92.9151,2-Dimethylnaphthalene0.99800.1~10000.30.91.64.516Acenaphthene0.99510.1~10000.20.80.91.9171-Naphthaldehyde0.99910.5~10000.31.02.74.1
分别配制6个20 ng/L,7个100 ng/L和6个500 ng/L的地下水基质加标样品,按照优化分析条件测定,得到各目标物的平均回收率和相对标准偏差(RSD),见表3。目标物的回收率为63.3%~111%;除了喹啉的RSD为24.9%外,其余均小于9.5%。根据MDL=t(n-1,0.99)×s计算方法检出限(LOD),通过平行分析6个接近LOD浓度(20 ng/L)的地下水基质加标样品,得到方法LOD为1.63~14.7 ng/L,满足地下水中低环多环芳烃衍生物的分析要求。
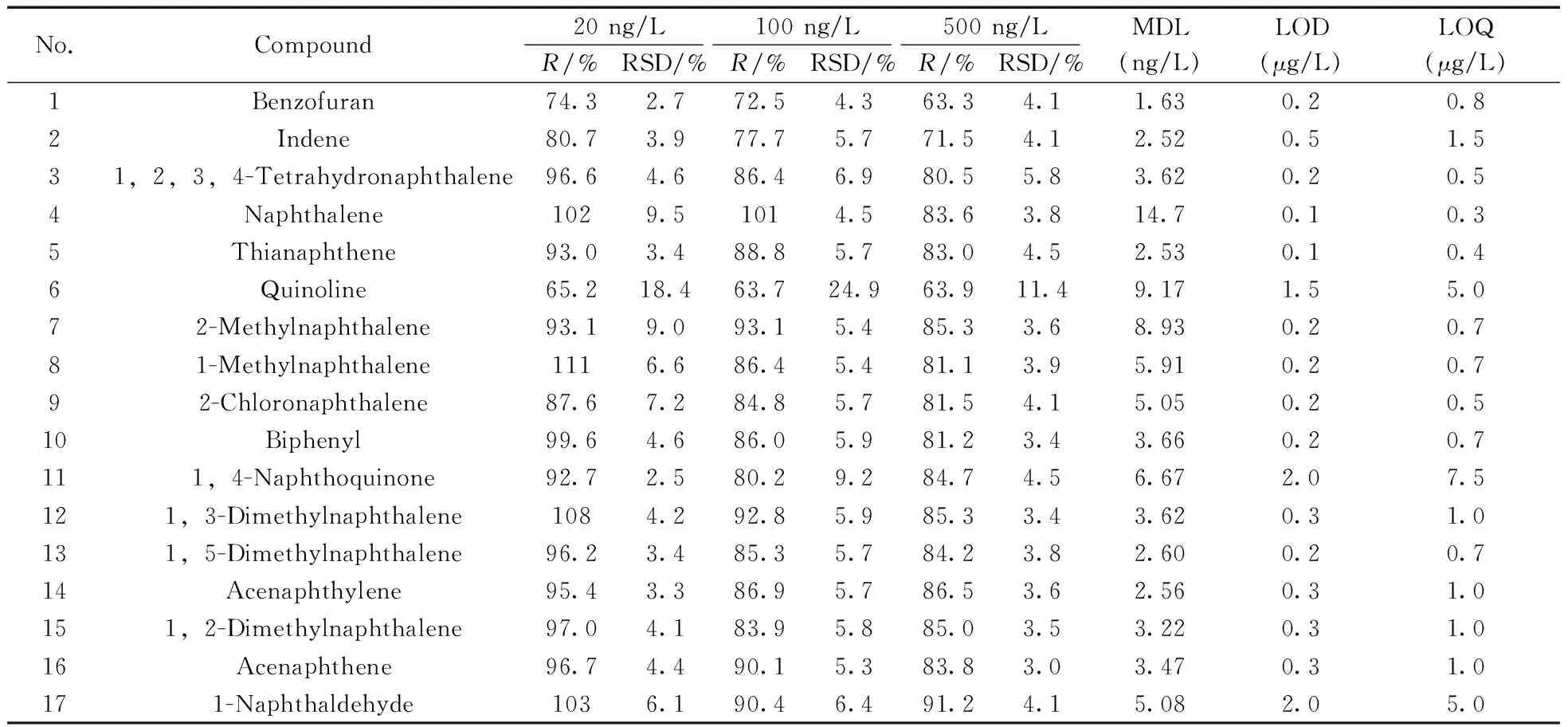
表3 方法的回收率、检出限、仪器检出限及定量下限Table 3 Recovery,detection limits,instrument detection limits and quantitative limits of the method
2.5 实际样品测定
采用新建立的GC×GC-TOF MS分析方法对河北部分地区6个地下水样品进行了分析测定。共检出10种目标物,检出率为59%,检出浓度在3.43~353 ng/L之间,其中浓度最大的为1,3-二甲基萘(表4)。6个样品中有4个检出,阳性检出率为67%,说明河北地区地下水中确实存在一定程度的多环芳烃污染。
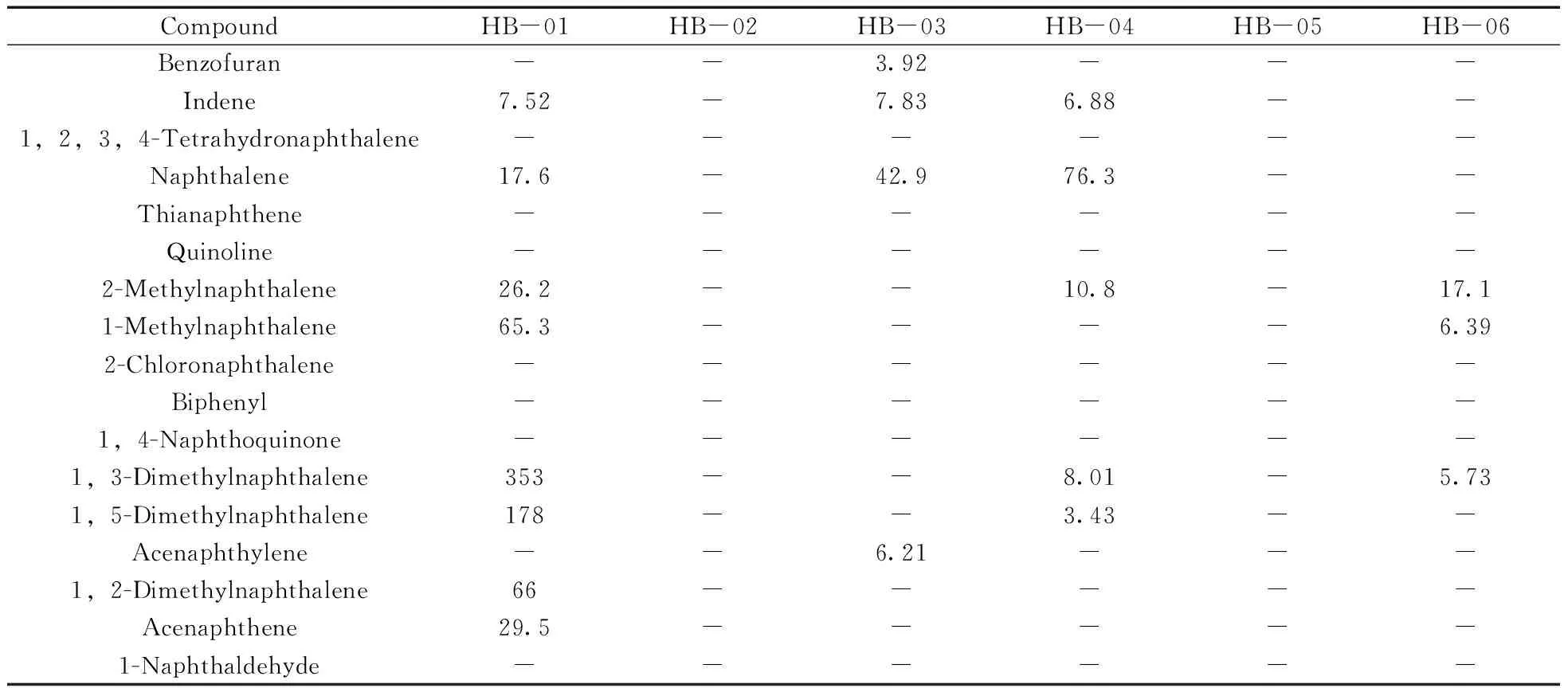
表4 河北地区地下水的检测结果Table 4 Analytical results of groundwater of Hebei province ρ/(ng·L-1)
-:not detected
3 结 论
本文建立了液液萃取/全二维气相色谱-飞行时间质谱测定地下水中低环多环芳烃及其衍生物的分析方法。通过对比研究,液液萃取的回收率(63.7%~101%)显著优于固相萃取回收率(17.7%~136%),液液萃取更适于地下水中痕量多环芳烃衍生物的富集。所建立分析方法在0.1~1 000 μg/L范围内呈良好线性关系,方法检出限为1.63~14.7 ng/L;各目标物的回收率为63.3%~111%,满足地下水检测质量控制要求。该方法已用于河北部分地下水中低环多环芳烃及其衍生物的测定,检测结果表明地下水中确实存在一定程度的多环芳烃污染,值得关注。
[1] Arey J,Zielinska B,Atkinson R,Winer A M,Ramdahl T,Jr Pitts J N.Atmos.Environ.,1986,20(12):2339-2345.
[2] Weber R,Iino F,Takashi I,Takeuchi M,Takesh S,Masaki S.Chemosphere,2001,44(6):1429-1438.
[3] Sun J L,Jing X,Chang W J,Chen Z X,Zeng H.EcotoxicolEnvironmentalSafety,2015,113:31-37.
[4] Lundstedt S,White P A,Lemieux C L,Lynes K D,Lambert I B,Oberg L,Haglund P,Tysklind M.Ambio-AJournaloftheHumanEnvironment,2007,36(6):475-485.
[5] Ahmadvand M,Sereshti H,Parastar H.J.Chromatogr.A,2015,1413:117-126.
[6] Yuta K,Fumikazu I,Takeshi O.Int.J.Environ.Anal.Chem.,2015,95(12):1157-1168.
[7] Shamsipur M,Hassan J.J.Chromatogr.A,2010,1217(30):4877-4882.
[8] Obrist D,Zielinska B,Perlinger J A.Chemosphere,2015,134:98-105.
[9] Zhao X,Liu X,Zhao Z,Huang C,Zhang M,Wang H,Wang X.J.Sep.Sci.,2009,32(12):2051-2057.
[10] Ma J,Xiao R,Li J,Yu J,Zhang Y,Chen L.J.Chromatogr.A,2010,1217(34):5462-5469.
[11] Zhang S,Zhang Q,Darisaw S,Ehie O,Wang G.Chemosphere,2007,66(6):1057-1069.
[12] Qiao M,Qi W,Liu H,Qu J.J.Chromatogr.A,2013,1291:129-136.
[13] Gao R,Rao Z,Guo X C,Huang Y,Li X J.J.Instrum.Anal.(高冉,饶竹,郭晓辰,黄毅,李晓洁.分析测试学报),2014,33(5):539-544.
[14] Li Z,Romanoff L C,Trinidad D A,Hussain N,Jones R S,Porter E N,Jr Patterson D G,Sjödin A.Anal.Chem.,2006,78(16):5744-5751.
[15] Li S,Rao Z.RockMin.Anal.(李松,饶竹.岩矿测试),2009,28(2):157-160.
[16] Li N,Zhang H Q,Rao Z,Xu D D,Gu Z X.J.Instrum.Anal.(黎宁,张红庆,饶竹,许丹丹,谷子欣.分析测试学报),2017,36(2):252-256.
[17] Wilson R B,Hoggard J C,Synovec R E.Anal.Chem.,2012,84(9):4167-4173.
[18] Gallacher C,Thomas R,Taylor C,Lord R,Kalin R M.Chemosphere,2017,178:34-41.
[19] Omais B,Courtiade M,Charon N,Thiebaut D,Quignard A,Hennion M C.J.Chromatogr.A,2011,1218(21):3233-3240.
[20] Zheng M H,Wu J J.Chin.J.Chromatogr.(郑明辉,吴嘉嘉.色谱),2011,29(4):281-282.
[21] Guo Y W,Li H Y,Ma Y Q,Song X J.Adm.Technol.Environ.Monit.(郭亚伟,李海燕,马玉琴,宋晓娟.环境监测管理与技术),2013,25(2):43-46.
Determination of Low-ring PAHs and Their Derivatives in Groundwater by GC×GC-TOF MS
ZHANG Hong-qing1,RAO Zhu1*,WANG Xiao-chun2,XU Dan-dan3,GU Zi-xin4,QIN Kai3,GUO Feng1,ZHAN Nan1
(1.Key Laboratory of Eco-geochemistry,National Research Center for Geoanalysis,Beijing 100037,China;2.College of Chemistry and Life Sciences,Anshan Normal University,Anshan 114016,China;3.College of Geoscience and Surveying Engineering,China University of Mining and Technology,Beijing 100083,China;4.Faculty of Materials Science and Chemistry,China University of Geosciences,Wuhan 430074,China)
A method was developed for the determination of low-ring polycyclic aromatic hydrocarbons(PAHs)and their derivatives in groundwater by liquid-liquid extraction(LLE)followed by comprehensive two-dimensional gas chromatography coupled to time-of-flight mass spectrometry(GC×GC-TOF MS).Compared with solid phase extraction(SPE),liquid-liquid extraction(LLE) shows higher extraction recoveries for samples,thus LLE was selected as the sample pretreatment method.The optimized results showed that the method has a good linear range of 0.1-1 000 μg/L with the correlation coefficients(r) higher than 0.99 for most of the targets,except for 1,2,3,4-tetrahydronaphthalene(r=0.987 2) and biphenyl(r=0.989 9).The spiked recoveries of the targets ranged from 63.3%to 111%with relative standard deviations less than 9.5%(RSD,n=6),except for quinoline(RSD,24.9%),and the detection limits ranged from 1.63 ng/L to 14.7 ng/L.The method was applied in the determination of low-ring PAHs and their derivatives in real groundwater samples from Hebei province,and the pollutants in two-thirds of samples were detected with the maximum concentration of 353 ng/L.
low-ring PAHs;derivatives;GC×GC-TOF MS;groundwater
10.3969/j.issn.1004-4957.2017.10.005
O657.3
A
1004-4957(2017)10-1197-06
2017-04-27;
2017-06-20
中国地质调查项目(DD20160312,DD20160323,1212011120283,1212010816028)
*
饶 竹,硕士,研究员,研究方向:环境有机污染分析,Tel:010-68999554,E-mail:raozhu@126.com

