利用废旧轮胎橡胶颗粒吸附VOCs的研究
谈莉,王洪波,盛祥锐,曾嘉,王雪涵,王宁,2
(1.山东建筑大学 市政与环境工程学院,山东 济南 250101;2.上海市大气颗粒物污染防治重点实验室,上海 200433)
随着工业的迅速发展,我国每年废旧轮胎数量在逐步增加[1]。大量废旧轮胎长期堆放将占用土地资源、破坏植被[2-3],并可能引发火灾。目前对废旧轮胎的再利用方式包括制备胶粉、再生胶及热裂解等[4-6]。有研究使用废旧轮胎颗粒吸附环境污染物,包括重金属镉[7]、有害有机物[8]、水环境中的砷[9]以及石油泄漏的溢油等污染物等[10]。
挥发性有机物(VOCs)除了影响人类健康[11],还是大气臭氧(O3)和二次有机气溶胶等的重要前体物,是环境空气研究领域关注的重点内容之一[12]。本研究使用废旧轮胎橡胶制成的颗粒为吸附剂,通过实验室模拟,探究废旧轮胎颗粒作为气态VOCs吸附剂的吸附性能。
1 实验部分
1.1 材料与仪器
橡胶颗粒(一号橡胶颗粒为干净的橡胶颗粒,粒径小,无杂质,颗粒密度为0.566 g/m3;二号橡胶颗粒粒径偏大,有部分线头等杂质,颗粒密度为0.473 g/m3;锯末(粒径1~2 mm);正己烷,色谱纯;苯,分析纯。
MX6复合气体检测仪;QC-1S大气采样仪;PVC反应柱(h=0.5 m,r=25 mm),自制。
1.2 静态吸附
实验前,校准VOCs检测器,并检测锥形瓶瓶内气体背景浓度。按图1连接实验装置,将锥形瓶内充满正己烷/苯气体。记录VOCs初始浓度,迅速倒入10 g橡胶颗粒,摇晃后静置10 min,然后每间隔10 min检测记录数据1次,直至测得第12个数据。设置3组平行。整个实验过程中,尽量用封口膜封闭瓶口。
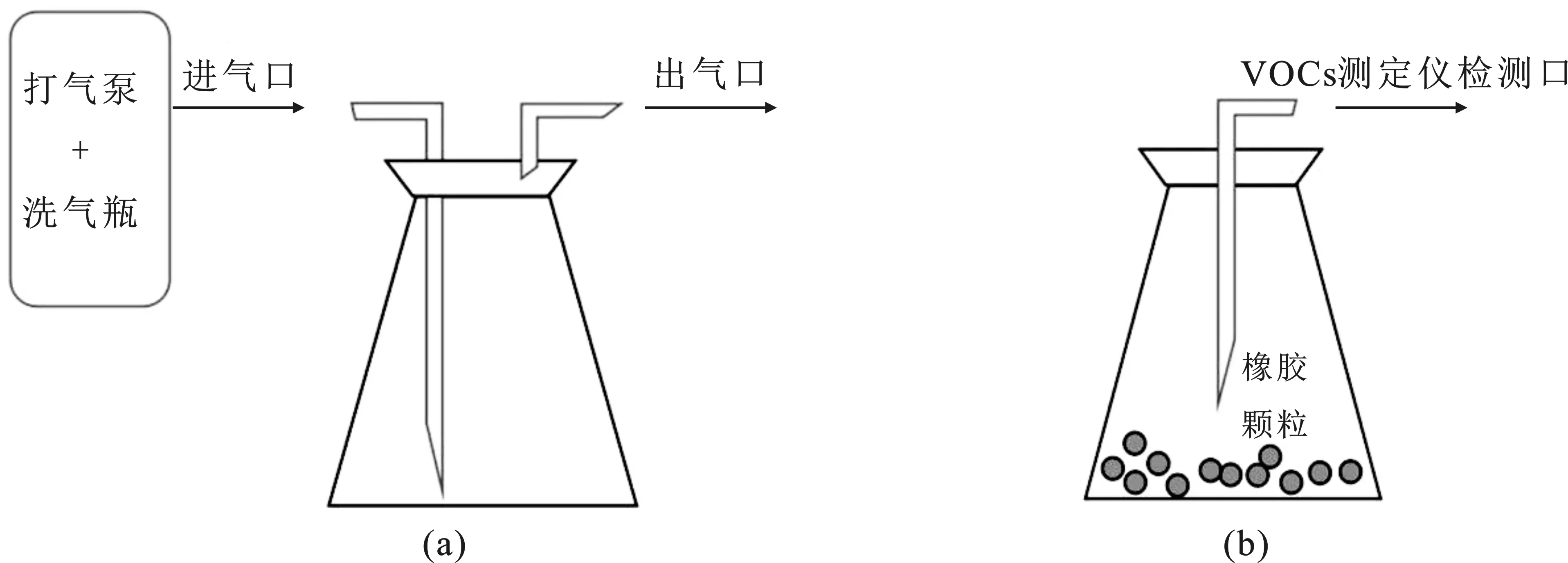
图1 静态吸附实验装置示意图
1.3 动态吸附
实验前,用VOCs检测器检测锥形瓶瓶内气体浓度,仪器显示数据需低于5 ppm方可使用。按照图2连接实验装置。进行正己烷吸附实验时,将流量计调至0.1 L/min;进行苯气体吸附实验时,将流量计调至0.02 L/min。而后在反应柱中填充10 g橡胶颗粒,打开采样仪,开始将正己烷/苯气体鼓入反应柱中。实验进行40 min,将检测器连接电脑,导出数据并保存。空柱、10,20,30 g橡胶颗粒吸附苯/正己烷实验均重复上述步骤。设置3组平行。
采用MX6复合气体检测仪测得的数据显示为异丁烯浓度数据,在实验结束处理数据时,需转换为相应的正己烷/苯的数据。转换关系如下:
异丁烯单位ppm转换为mg/m3:
正己烷吸附量=4.06×异丁烯吸附量
苯吸附量=0.55×异丁烯吸附量
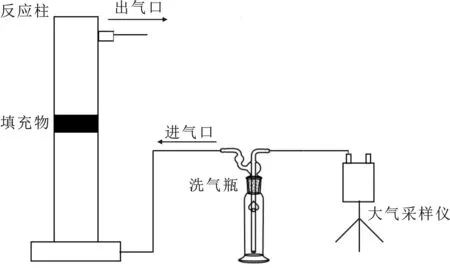
图2 动态吸附实验装置示意图
2 结果与讨论
2.1 静态吸附实验
分别选用30 g的一号、二号橡胶颗粒以及与橡胶颗粒结构类似的锯末作为对比,质量相同的3种样品对正己烷和苯的吸附结果见图3。

图3 不同样品对正己烷/苯的吸附量
由图3(a)可知,前30 min,吸附正己烷的能力由强到弱排序依次为二号橡胶颗粒>一号橡胶颗粒>锯末,可能的原因是二号橡胶颗粒密度较小,橡胶颗粒可以与正己烷气体充分接触,短时间内吸附量较大。30 min后,对正己烷的吸附能力由强到弱排序依次为一号橡胶颗粒>二号橡胶颗粒>锯末。反应进行一段时间后,一号、二号橡胶颗粒吸附正己烷都接近饱和,一号橡胶颗粒更为纯净,含橡胶颗粒成分更高,吸附正己烷气体的量略大于二号橡胶颗粒。锯末吸附正己烷的量最少,表明锯末对正己烷几乎无吸附能力,橡胶颗粒对正己烷有着较好的吸附效果。随着静置时间增加,单位质量的橡胶颗粒对于正己烷的吸附量可达0.18 mg/g, 锯末对于正己烷吸附量保持在0.05 mg/g范围。废旧轮胎研磨颗粒二号橡胶颗粒对于正己烷的吸附能力与一号纯橡胶颗粒相近,且橡胶颗粒粒径越小、与正己烷气体接触面积越广,对正己烷的吸附越好。
由图3(b)可知,橡胶颗粒吸附苯的反应主要发生在在前40 min内,40 min后,橡胶颗粒对苯气体的吸附量趋于饱和。橡胶颗粒吸附苯的量维持在0.072 mg/g左右,锯末吸附苯的量一直维持在0.008 mg/g左右。与橡胶颗粒吸附正己烷的实验相比较,吸附苯的量较少,原因在于实验容器内正己烷的初始浓度12 433.8 mg/m3,远高于苯的初始浓度 1 742.6 mg/m3。 橡胶颗粒对于苯气体有着更好的吸附效果。
橡胶颗粒质量对正己烷/苯的吸附效率见图4。
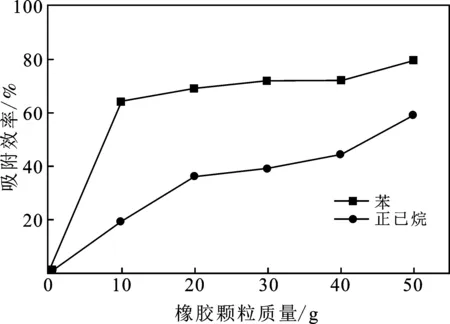
图4 不同质量橡胶颗粒对正己烷、苯的吸附效率
由图4可知,在容器内正己烷总浓度保持3 055.99 mg/m3的条件下,相同质量的橡胶颗粒吸附有机物效率,苯>正己烷。虽然橡胶颗粒吸附正己烷和苯的吸附效率都呈上升趋势,但对苯的吸附效率总是大于正己烷吸附效率。当加入橡胶颗粒50 g时,对苯的吸附效率高达79.48%,吸附正己烷效率为59.37%。
2.2 动态吸附实验
2.2.1 正己烷 由图5可知,在正己烷充气速度恒定的情况下,30 min内,空柱内正己烷的含量可高达11 450.331 mg/m3, 对比空柱,10,20,30 g橡胶颗粒对于正己烷气体都有着较好的吸附,当反应柱中加入10 g 橡胶颗粒时,对正己烷的最大去除量为2 991 mg/m3, 占反应柱中正己烷总浓度的26.1%;当反应柱中加入20 g橡胶颗粒时,对正己烷的最大去除量为7 526 mg/m3, 占反应柱中正己烷总浓度的65.7%;当反应柱中加入30 g橡胶颗粒时,对正己烷的最大去除量为9 240.41 mg/m3,占反应柱中正己烷总浓度的80.7%,单位质量的橡胶颗粒对于正己烷的吸附量最大,高达0.591 mg/g。对比静态吸附,橡胶颗粒对正己烷在静态吸附中的的吸附量为0.18 mg/g,显然,动态吸附过程中橡胶颗粒对正己烷的吸附效果更好。在动态吸附中,橡胶颗粒与正己烷充分接触反应,反应柱中的橡胶颗粒吸附正己烷直至吸附饱和,故单位质量的橡胶颗粒在动态吸附过程中对正己烷的吸附量高于在静态吸附过程中的量。

图5 动态实验橡胶颗粒吸附正己烷(mg/m3)
2.2.2 苯 由图6可知,在苯气体充气速度恒定的情况下,25 min内,空柱内苯的含量可高达628.4 mg/m3。 在加入橡胶颗粒的反应柱中,实验进行20 min后,橡胶颗粒对苯的吸附量均达饱和。当反应柱中加入10 g橡胶颗粒时,对苯的最大去除量为292.07 mg/m3,占反应柱中正己烷总浓度的46.5%;当反应柱中加入20 g橡胶颗粒时,对苯的最大去除量为408.76 mg/m3,占反应柱中正己烷总浓度的65.0%;当反应柱中加入30 g橡胶颗粒时,对苯的最大去除量为509.06 mg/m3,占反应柱中正己烷总浓度的81.0%。在加入30 g橡胶颗粒时,单位质量的橡胶颗粒对于苯气体的吸附量最大,为0.059 mg/g。对比橡胶颗粒动态吸附正己烷的效果,橡胶颗粒吸附苯的效果与吸附正己烷的接近,可能的原因是苯和正己烷为含有相同碳数的芳烃和直链,且分子量接近。对比橡胶颗粒静态吸附苯的效果,静态吸附实验中,橡胶颗粒对苯的吸附量为0.072 mg/g,比动态吸附效果较好。在静态吸附与动态吸附实验中,两种反应容器中苯的最高总浓度接近,同质量的橡胶颗粒对苯的吸附效果也应相同。但实验结果中,橡胶颗粒在动态吸附过程中对正己烷的吸附量略低于在静态吸附中的量,是由于苯在实验中较易液化,导致仪器测得容器中苯的浓度过低,使得实际吸附正己烷的量低于仪器测得的数据,故导致同质量的橡胶颗粒对苯的吸附效果静态吸附比动态吸附好。
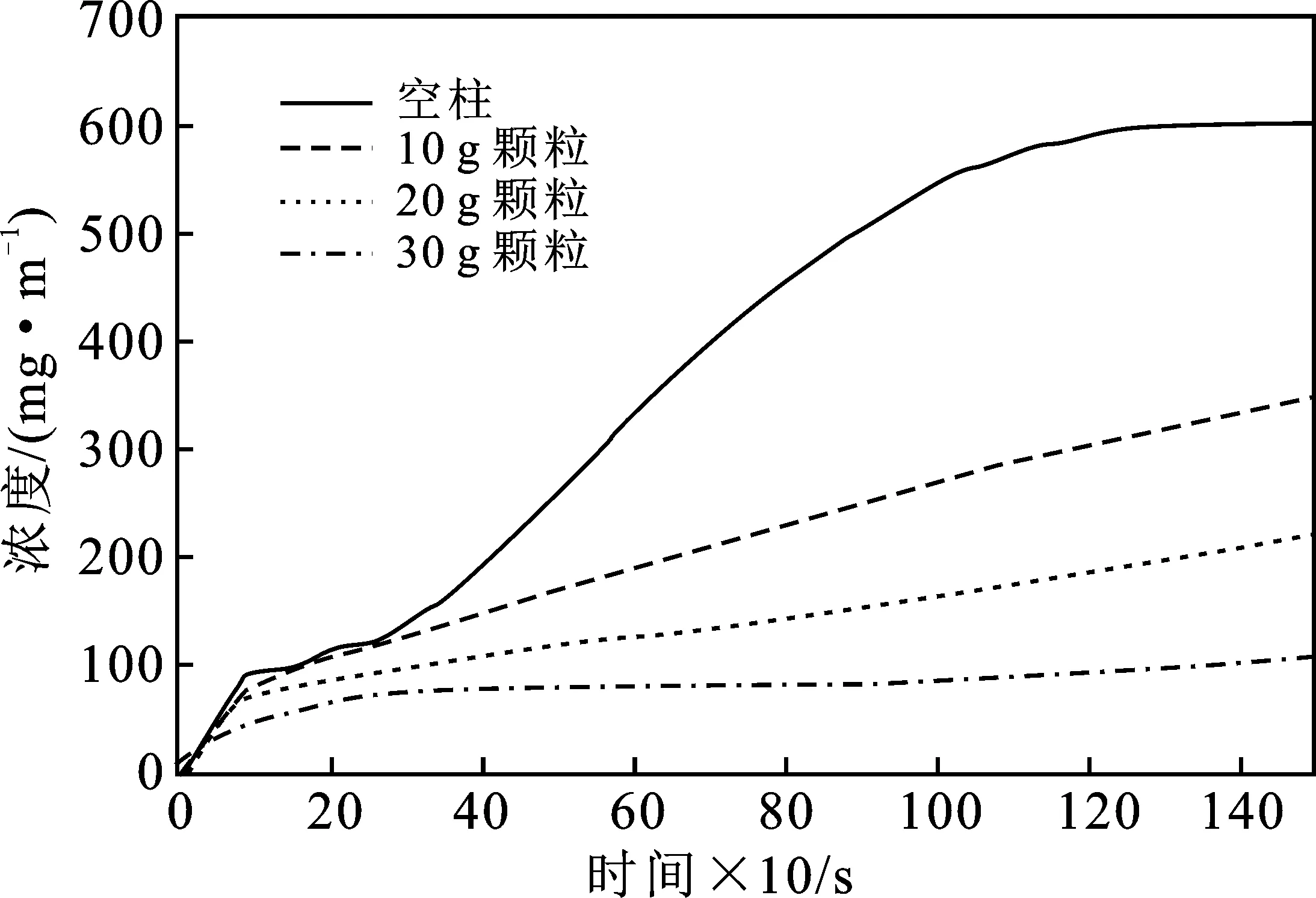
图6 动态实验橡胶颗粒吸附苯(mg/m3)
2.3 吸附等温线
实验中,橡胶颗粒吸附正己烷/苯达到平衡时,分别用 Langmuir 方程和 Freundlich 方程对正己烷、苯的吸附等温线进行拟合[13-15]。
2.3.1 Langmuir吸附等温线经取倒数[13]:
(1)
式中Qe——吸附剂的平衡吸附量,mg/g;
Qm——吸附剂的饱和吸附量,mg/g;
KL——Langmuir平衡常数。
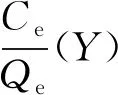
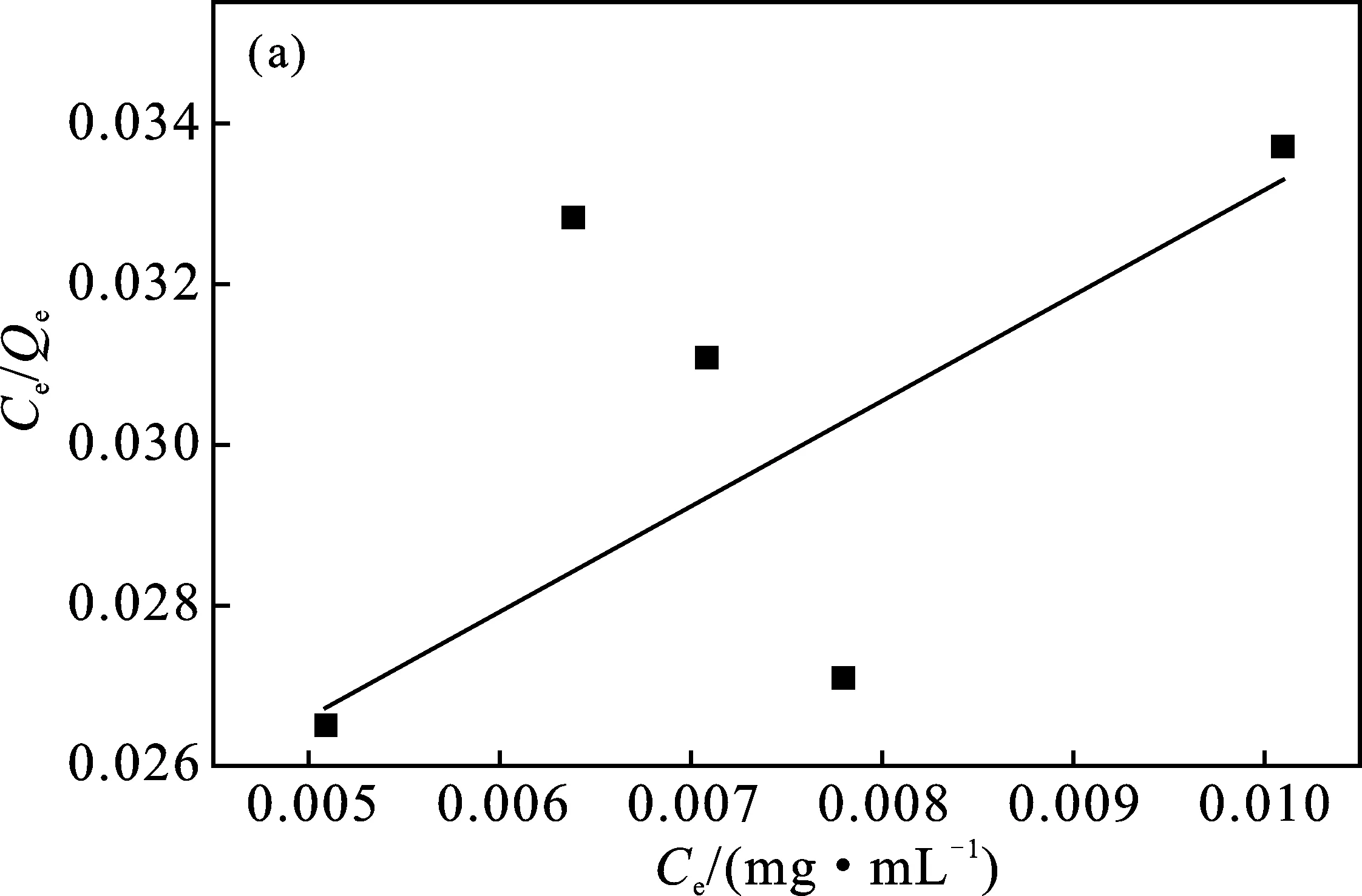
图7 Langmuir方程拟合等温线
由图7可知,橡胶颗粒吸附正己烷吸附等温方程式相关系数R2=0.333,橡胶颗粒吸附苯相关系数R2=0.016 4,可见橡胶颗粒吸附正己烷/苯不符合Langmuir吸附等温方程式,表明橡胶颗粒吸附正己烷/苯并不是单分子层吸附。
2.3.2 Freundlich吸附等温线 在10 ℃下,对橡胶颗粒的吸附过程采用Freundlich方程进行拟合。其表达式线性形式:
(2)
式中KF——Freundlich平衡常数;
n——无量纲常数,表示吸附强度。
橡胶颗粒吸附正己烷、吸附苯的结果见图8。

图8 Freundlich方程拟合等温线
由图8(a)得到线性回归方程,其斜率为1/n=0.750 3, 截距为lgKF,可以求出KF=0.282 0。 因此,橡胶颗粒吸附正己烷的Freundlich吸附等温线可表示为:
Qe=0.282×Ce0.750 3
见图8(b),得到线性回归方程,其斜率为1/n=1.044 6,截距为lgKF,可以求出KF=0.016 1。因此,一号橡胶颗粒吸附正己烷的Freundlich吸附等温线见表1。
Qe-1=0.016 1×Ce1.044 6
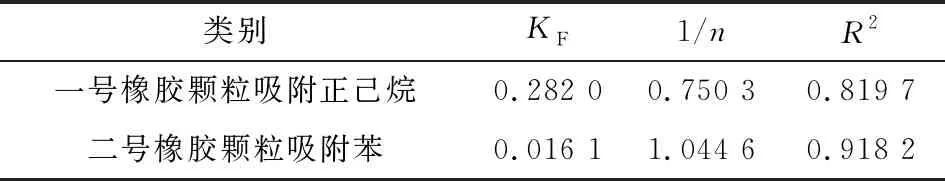
表1 Freundlich吸附等温线相关参数的拟合结果
表1列出了橡胶颗粒吸附正己烷/苯的Freundlich吸附等温线相关参数的拟合结果。
一般认为,Freundlich常数1/n>2,表示吸附较难;n=1,为线性吸附;0.1<1/n<1,表示吸附容易进行。由表1可知,橡胶颗粒对于正己烷和苯都较易吸附。
2.4 吸附动力学
一号橡胶颗粒对正己烷的吸附动力学实验结果见图9。
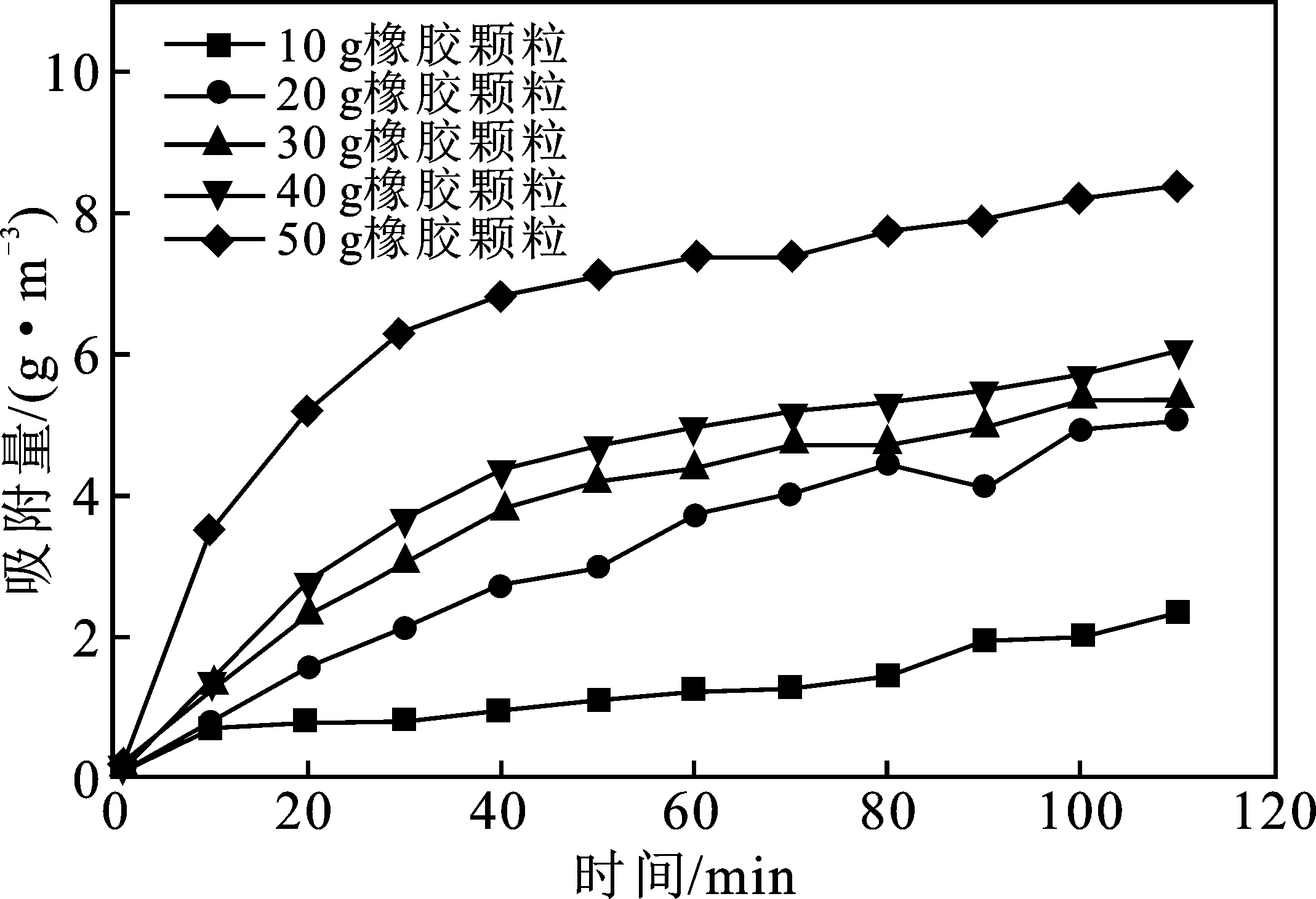
图9 不同质量一号橡胶颗粒对正己烷的吸附量
由图9可知,在刚加入50 g橡胶颗粒时,就呈现出了良好的吸附效果。20 min后,20,30,40 g橡胶颗粒对正己烷的吸附量的趋势呈现一致。相同时间段内,随着加入橡胶颗粒质量的增多,橡胶颗粒对瓶内正己烷的吸附量增加,可认为橡胶颗粒质量与对正己烷的吸附量呈正比关系。
分别用拟一级、拟二级动力学模型、颗粒内扩散模型拟合实验结果[16-19]。
拟一级动力学模型:
ln(Qe-Qt)=lnQe-K1t
(3)
式中Qt——吸附时间为t时刻的吸附量,mg/g;
K1——一级吸附速率常数,min-1。
拟二级动力学模型:
(4)
式中K2——二级吸附模型的平衡速率常数,g/(mg·min)。
颗粒内扩散模型:
(5)
式中Kp——颗粒内扩散模型的速率常数;
C——涉及厚度和边界层的常数。
拟一级、拟二级动力学模型拟合结果见表2。

表2 拟一级动力学模型和拟二级动力学模型的比较
由表2可知,橡胶颗粒吸附正己烷不符合拟二级动力学模型。橡胶颗粒吸附VOCs拟一级动力学模型见图10。
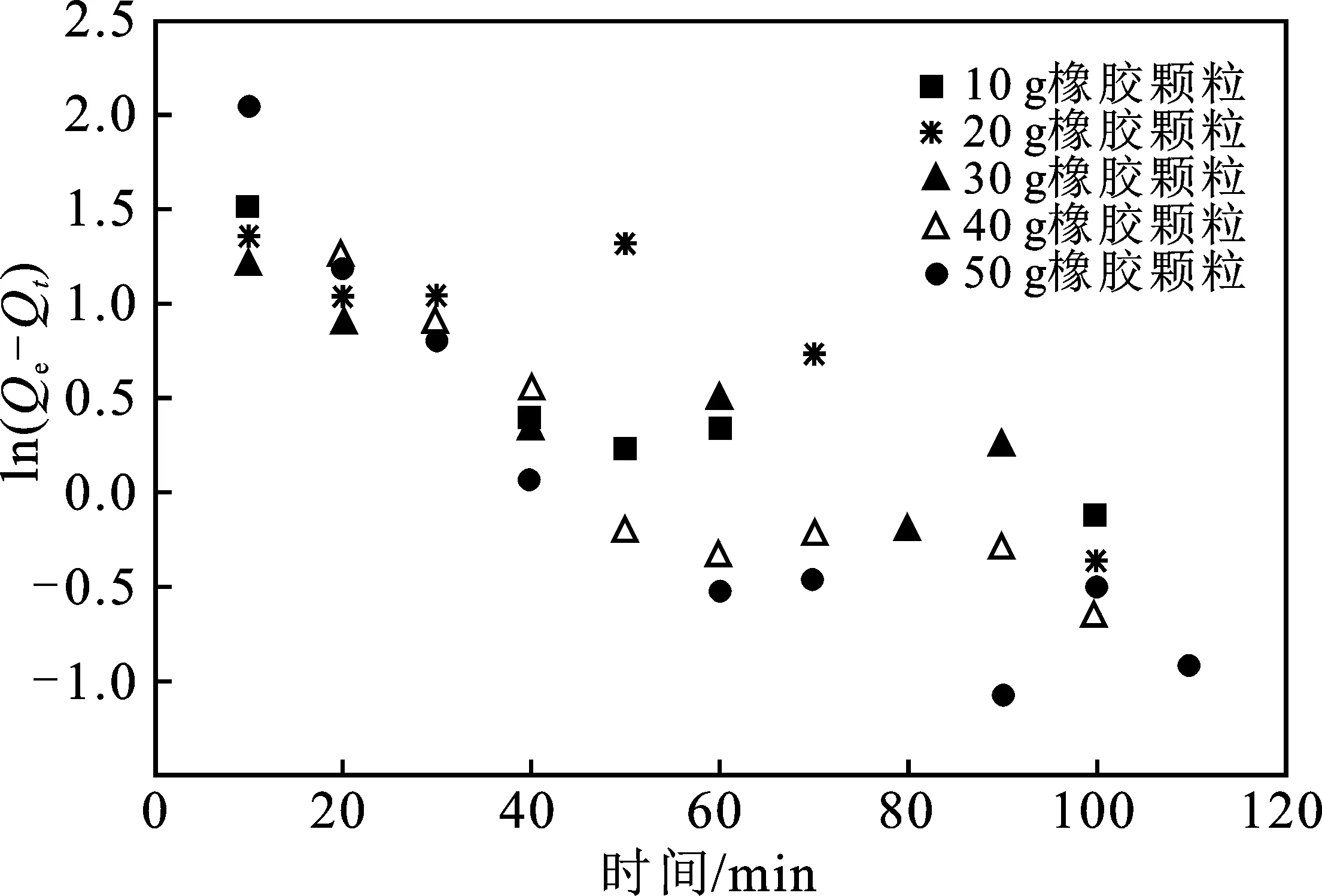
图10 不同质量橡胶颗粒吸附正己烷拟一级动力学模型计算
以放入橡胶颗粒30 g实验结果为例,作出ln(Qe-Qt)关于t的关系曲线,得到线性方程y=-0.494 6x-1.584 5,斜率为-K1,则K1=0.494 6,截距为lnQe=-1.584 5,得Qe=0.205 mg/g。则速率方程为:v=0.494 6Qt。
颗粒内扩散模型见图11。
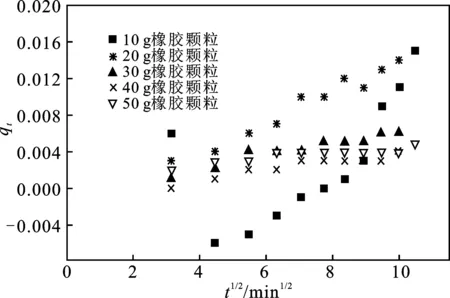
图11 橡胶颗粒吸附正己烷的颗粒内扩散模型
由图11可知,Qt关于t1/2的关系为直线,但是都不经过原点,这表明颗粒内扩散不是控制吸附过程的唯一步骤,吸附过程受其他吸附阶段的共同控制。
3 结论
(1)采用废弃轮胎橡胶颗粒、锯末吸附苯和正己烷,静态实验表明,橡胶颗粒较锯末吸附效果更好,且粒径更小的一号橡胶颗粒对苯和正己烷的吸附效果更佳。
(2)苯在实验过程中较易液化,故导致在充满苯气体的容积为1 290 mL的实验容器内橡胶颗粒吸附苯的阶段仅发生在短短10 min内,吸附效率达80%。之后的吸附结果不准确,误差较大。正己烷较稳定,用50 g橡胶颗粒吸附正己烷时,吸附效率可达60%。
(3)动态吸附实验室温8~10 ℃,正己烷在反应柱中较稳定,实验进行30 min,对比空柱、锯末,橡胶颗粒对于正己烷有很明显的吸附效果;由于苯较易液化,控制反应柱内苯的气体浓度较低,实验进行25 min,在实验第7 min,橡胶颗粒对于苯气体就表现出了良好的吸附效果,对比空柱实验数据,橡胶颗粒吸附苯的量明显大。
(4)橡胶颗粒吸附苯和正己烷满足 Freundlich 吸附等温方程,且Freundlich常数1/n<2,表示橡胶颗粒对于苯和正己烷都较易吸附,符合拟一级动力学模型,并且颗粒内扩散不是控制吸附过程的唯一步骤。

