基于抑郁模型大鼠miR-665表达及靶基因功能分析探讨开心解郁方抗抑郁疗效机制*
王联生,黄世敬,潘菊华,王彦云,张 颖,陈宇霞
(中国中医科学院广安门医院 北京 100053)
基于抑郁模型大鼠miR-665表达及靶基因功能分析探讨开心解郁方抗抑郁疗效机制*
王联生,黄世敬**,潘菊华,王彦云,张 颖,陈宇霞
(中国中医科学院广安门医院 北京 100053)
目的:通过考察中药开心解郁方干预抑郁症模型大鼠海马miR-665表达变化并对miR-665的靶基因进行生物信息分析,探讨miR-665在抑郁症的发病及开心解郁方抗抑郁机制中的作用。方法:建立慢性应激抑郁症大鼠模型并用开心解郁方干预42天,取海马组织提取总RNA,采用RT-qPCR检测各组大鼠海马miR-665相对表达量,并采用TargetScan和microRNAorg数据库对miR-665进行靶基因预测,采用DAVID数据库对预测得到的靶基因进行GO功能富集分类及KEGG信号通路分析。结果:与正常组比较,模型组大鼠海马miR-665表达水平显著增高,差异具有统计学意义(P<0.01);与模型组比较,中药组及西药组大鼠海马miR-665表达水平显著降低,差异具有统计学意义(P<0.05)。miR-665靶基因的生物学功能主要富集于有机物质反应等;信号通路主要富集于N-糖链的合成等。结论:miR-665可能参与了抑郁症病理机制过程调控,通过改善其表达异常可能为开心解郁方的抗抑郁机制之一,通过对其靶基因的功能预测分析对于后期继续研究开心解郁方干预miR-665的具体作用机制提供了方向和理论基础。
抑郁症 miR-665 生物信息分析 开心解郁方
抑郁症是一种以显著而持久的抑郁状态为特征的常见的情感障碍性疾病,该病具有高治病率、高致残率及高复发率等特点,对患者的身心健康带来严重危害。据世界卫生组织(WHO)2012年统计目前全世界抑郁症患者约有3.5亿,每年因该病自杀者近百万人[1]。抑郁症为多因素共同致病,其形成的神经生物学机制至今了解有限。一般认为与神经递质改变、神经内分泌免疫功能失调、神经元可塑性及神经再生障碍有关。中医药在抑郁症的防治过程中发挥了重要的作用,开心解郁方为临床上治疗抑郁症的有效方剂。本实验室前期研究发现开心解郁方具有明显抗抑郁临床疗效,其作用机制与改善神经元损伤、保护血脑屏障、调节情感调节因子5-羟色胺(5-HT)及其受体亚型的表达等有关[2-4]。
miRNA是近年来发现的与疾病密切相关的小分子RNA[5],可通过调控神经元的生成、神经可塑性及信号传导通路关键性元件的基因表达等参与抑郁症的病理过程[6,7]。miR-665是新近发现的一个与中枢神经系统功能密切相关的miRNA分子,在海马神经元的凋亡及神经保护过程中具有调控作用[8]。本研究旨在探讨中药开心解郁方对慢性应激抑郁模型大鼠海马miR-665表达影响,并应用生物信息学方法对miR-665的靶基因进行功能分析,为抑郁症的防治以及中医药治疗抑郁症提供新的理论依据。
1 实验材料
1.1 实验动物
选择成年健康雄性SD大鼠,体重220±20 g,(由北京维通利华实验动物中心提供),动物合格证号:SCXK(京)2012-0001,。
1.2 实验药物
开心解郁丸由人参、柴胡、赤芍、茯苓、远志等组成(中国中医科学院广安门医院大兴制剂室,批号:20140418)。
1.3 主要试剂
水合氯醛(国药集团化学试剂有限公司,批号:20150508);miScript II RT Kit试剂盒(p/n 218160),由德国QIAGEN公司提供;miScript SYBR Green PCR Kit试剂盒(德国QIAGEN公司,p/n 218073;盐酸氟西汀(美国礼来公司,批号:4139A)。
1.4 主要仪器
定量 PCR仪(p/n 7900HT),由美国 Applied Biosystems公司提供;PCR仪(p/n 9700),由美国ABI公司提供;离心机(p/n 5418),由德国eppendorf公司提供;振荡器-1(p/n GL-88B),由中国其林贝尔公司提供。
2 实验方法
2.1 动物模型复制
慢性不可预见性温和应激(CUMS)抑郁症大鼠模型建立:参照Willner等[9]方法改进将大鼠予以禁水、禁食、夹尾、潮湿垫料、水平振荡、电击足底、冰水游泳、明暗颠倒等刺激。这些刺激每天随机采取一种,使动物不能预料刺激发生。孤养,CUMS的同时单笼隔离饲养。
2.2 实验动物分组与给药
实验前大鼠每组5只正常饲养,适应环境后进行行为学评分,选行为学得分相近者随机分为:正常组(常规饲养);模型组(CUMS+孤养42天);中药组(模型基础上给予开心解郁方,灌胃给药剂量为0.90 g·kg-1·d-1,治疗42天);西药组(模型基础上给予盐酸氟西汀,灌胃给药剂量为2.0 mg·kg-1·d-1,治疗42天)。
2.3 行为学观察
于造模42天后所有大鼠单笼饲养,配制1%蔗糖溶液,第1天每笼放置2瓶糖水;第2天每笼左右分别放置1瓶糖水,1瓶纯水;第3天禁水24 h;第4天给每笼左右分别放置1%蔗糖水和纯水各1瓶并称重,120 min后,取2瓶水再次称重。记录每只大鼠的糖水消耗量、纯水消耗量,以及糖水消耗百分率。
2.4 海马组织提取
所有大鼠用水合氯醛深度麻醉,腹腔取血后用4℃生理盐水灌流(心尖进针插入右心室,剪开左心耳),灌流结束后,断头取脑,剥离海马组织,标号,入液氮速冻,转入-80℃冰箱储层待测。
2.5 miR-665表达测定
选取正常组、模型组、中药组及西药组大鼠整个海马组织标本各10例,通过分离、沉淀、洗涤及溶解来提取海马组织中总RNA。然后通过设计miR-665特异性颈环反转录引物进行逆转录反应,反应体系于PCR仪中,37℃下逆转录反应1 h,反应完全后95℃下5 min终止反应。实时荧光定量PCR反应条件为94℃下15 s,55℃下30 s,70℃下30 s,40个循环。表达结果采用2-△△Ct法分析miR-665相对表达量。
2.6 miR-665靶基因预测及功能分析
使用GeneSpring1 3.1软件,分别通过TargetScan(http://www.targetscan.org/)和 microRNAorg(http://www.microrna.org/microrna/home.do/)数据库对 miR-665 进行靶基因预测。为增加预测结果的准确性,对两个数据库预测到的靶基因取交集。再采用DAVID数据库对预测得到的靶基因进行功能富集分析,应用Gene Ontology(GO)进行功能富集分类,应用KEGG进行信号通路分析。通过Fisher Exact Test计算基因功能的显著性水平。
2.7 数据分析
所测数据均以均值±标准差(x±s)表示,釆用SPSS16.0统计软件进行分析。服从正态分布且方差齐者采用单因素方差分析(One-Way ANOVA),两两比较用LSD或T检验;不服从正态分布者,釆用Kruskal-Wallis秩和检验,P<0.05表示差异有统计学意义。
3 实验结果
3.1 行为学结果
各组大鼠于造模前糖水消耗百分率组间无明显差异,基线良好。42天后糖水消耗百分率模型组低于正常组,差异具有统计学意义(P<0.05);开心解郁方中药组糖水消耗百分率高于模型组,差异具有统计学意义(P<0.05);盐酸氟西汀西药组糖水消耗百分率高于模型组,差异具有统计学意义(P<0.01)。说明造模后模型大鼠的糖水消耗百分率明显降低,开心解郁方及盐酸氟西汀可明显增加模型大鼠的糖水消耗百分率。
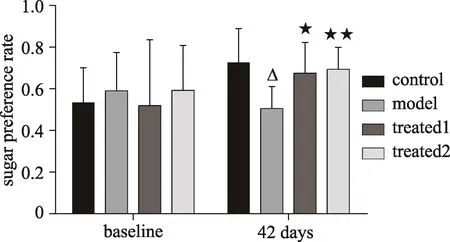
图1 糖水偏嗜实验结果
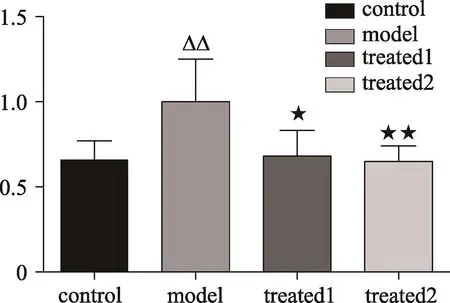
图2 miR-665 RT-qPCR检测结果
3.2 各组大鼠海马miR-665相对表达量结果
RT-qPCR检测各组大鼠海马miR-665相对表达量结果显示,与正常组比较,模型组大鼠海马miR-665表达水平显著增高,差异具有统计学意义(P<0.01);与模型组比较,中药组大鼠海马miR-665表达水平显著降低,差异具有统计学意义(P<0.05),西药组大鼠海马miR-665表达水平显著降低,差异具有统计学意义(P<0.01)。
3.3 miR-665靶基因的功能富集分析结果
采用TargetScan和microRNAorg两个数据库分别预测miR-665的靶基因,结果取二者交集共得到327个靶基因。将预测得到的靶基因进行GO分析和KEGG信号通路分析。结果显示miR-665靶基因的生物学功能主要富集于有机物质反应、内源性刺激反应、激素刺激反应、细胞因子介导信号通路、无机物的反应、神经冲动传递、细胞增殖调控和程序性细胞死亡的调节;信号通路主要富集于N-糖链的合成、急性髓系白血病、碱基切除修复、白细胞跨内皮迁移、趋化因子信号转导通路和癌症通路。见表1,2。
4 讨论
抑郁症属于中医的“郁证”、“癫证”、“脏躁”、“百合病”等范畴。理气开郁为郁病基本治则。开心解郁方是在长期的临床实践中总结用于治疗抑郁症的有效方剂,由古方开心散与四逆散合方加减而成,方中人参大补元气,开郁化滞,柴胡疏肝解郁,二药合用培元开郁,共为君药;巴戟天补肾助阳,茯苓健脾安神,二药助人参培元固本;枳实行气通滞,赤芍养血活血,二药助柴胡开郁行滞,共为臣药;远志化痰解毒,甘草调和诸药,共为佐使药。全方合用,共凑益气开郁之功效。前期研究发现开心解郁方治疗抑郁症临床疗效显著,增加额叶及顶叶脑血流值,改善脑组织形态结构,调节单胺类神经递质水平,促进BDNF及其受体表达,有效保护海马神经元及神经血管单元稳态[2-4]。
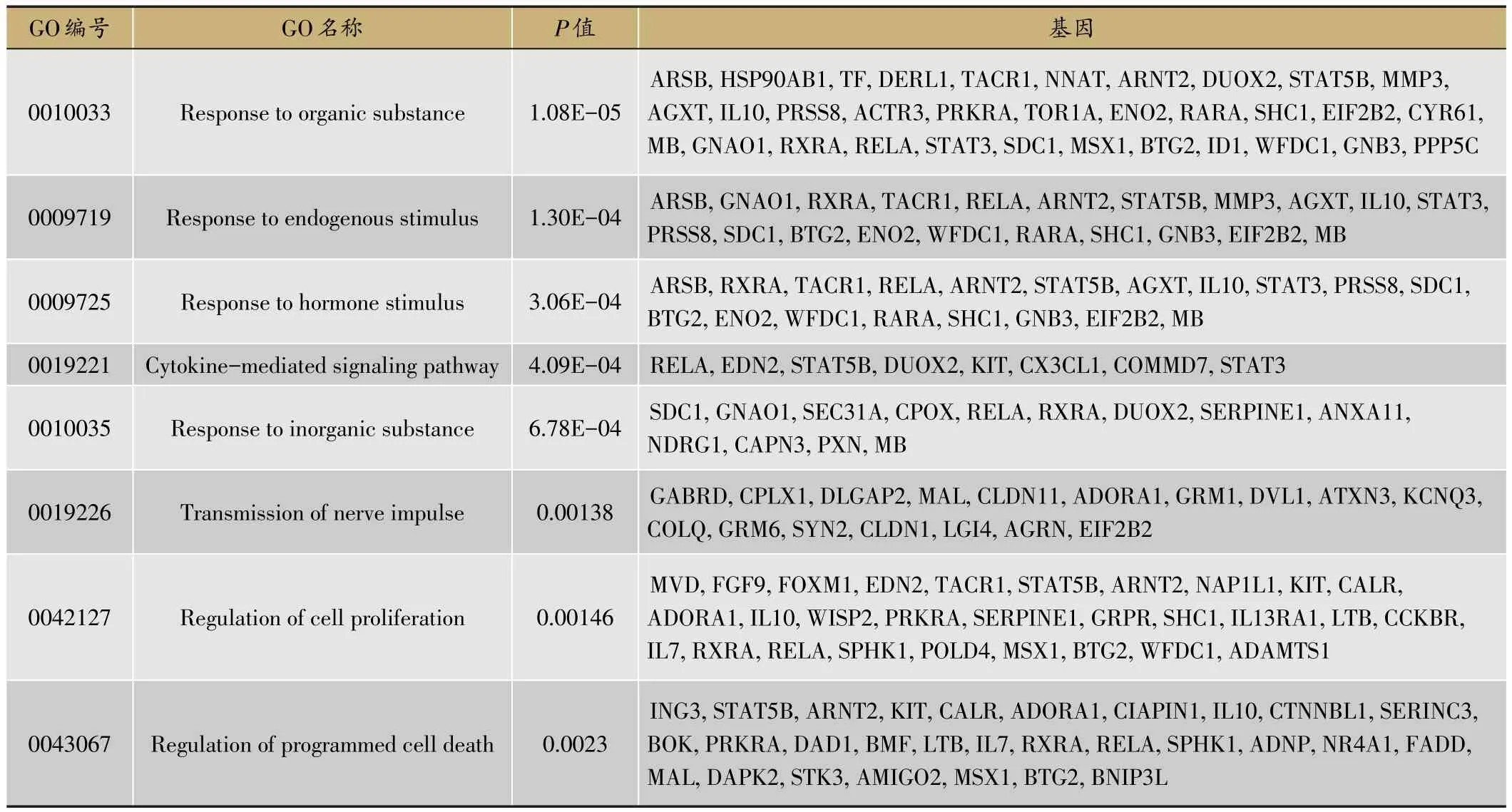
表1 miR-665靶基因的GO富集分析结果
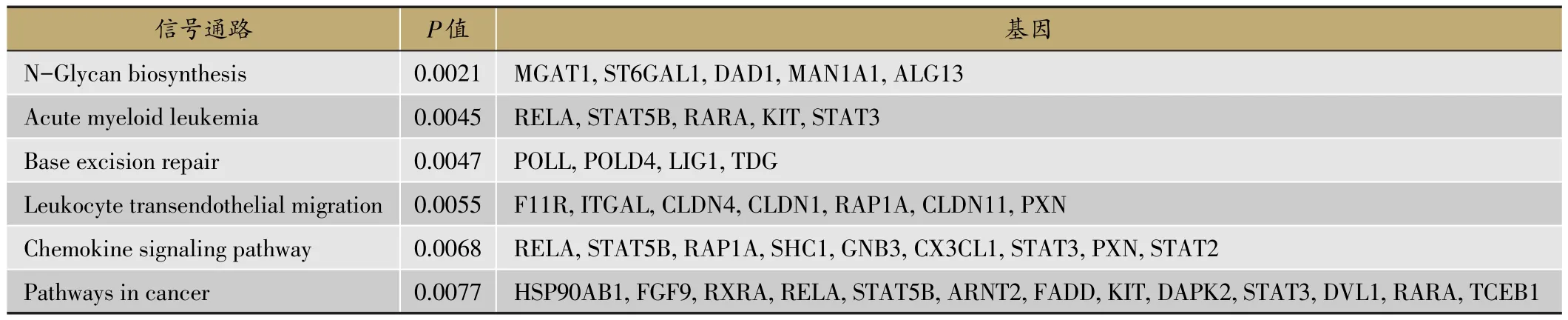
表2 miR-665靶基因信号通路富集分析结果
miRNA是一种内源性高度保守的非编码单链RNA,由大约22个核糖核苷酸组成,主要通过与其靶基因结合调控其表达和下游蛋白翻译过程,在细胞增殖与凋亡以及疾病发生发展过程中发挥着重要的作用[9]。通过对抑郁症自杀人群的脑组织miRNA表达谱分析结果发现,抑郁症患者前额皮质中存在miRNA表达显著性异常[10]。Belzeaux等[11]通过检测16名重度抑郁症患者外周单核细胞中miRNA的表达变化,结果发现14个miRNA(miR-148a,miR-381,miR-1243,hasmiR-107,miR-200c,miR-494,miR-579,miR-133a,miR-517b,miR-589,miR-636,miR-652,miR-941,miR-425-3p)表达出现显著异常,且这些异常变化的miRNA随抗抑郁药物治疗后临床症状的改善而发生相应的变化。可见miRNA参与了抑郁症的病理以及抗抑郁药物的作用机制过程。文献报道miRNA主要参与了抑郁症海马神经元的生成、突触可塑性以及BDNF的表达等方面病理生理机制的调控。如miR-124a可通过调控Notch信号通路决定神经干细胞的分化参与调节海马神经元生成[12]。miR-134和BDNF间存在一个复杂的调控网络,过表达miR-134可通过抑制cAMP应答元件结合蛋白(CREB)损伤突触的可塑性,抑制BDNF的表达[13]。最新的研究发现,miR-665参与了中枢神经系统功能的调控,Sun等[14,15]发现miR-665可通过靶向抑制Bcl-2样蛋白1(BCL2L1)的表达参与调控海马星形胶质细胞的凋亡、再生。Lu等[16]通过体内外实验研究探讨miR-665在七氟醚麻醉诱导的认知功能障碍中的作用,发现miR-665表达水平对于学习记忆功能具有明显的影响,其机制可能与调控海马神经元的凋亡相关,胰岛素样生长因子2(Insulinlike Growth Factor 2,IGF 2)可能为其下游靶标。
本研究在前期临床研究和动物实验的基础上,进一步观察在中药开心解郁方干预慢性应激抑郁症模型大鼠的过程中海马miR-665表达水平的变化。对miR-665可能参与抑郁症发生发展的机制及开心解郁方的作用靶点进行初步研究。研究表明慢性应激抑郁模型大鼠海马miR-665表达水平显著增高,开心解郁方及盐酸氟西汀可显著降低其表达水平,提示miR-665可能参与了抑郁症病理机制过程调控,通过改善其表达异常可能为开心解郁方的抗抑郁机制之一,其具体作用机制有待于进一步研究。
另外对miR-665的靶基因进行生物信息学分析,首先采用TargetScan、microRNAorg两个数据库对其靶基因进行预测,进一步采用GO分析和KEGG通路分析探讨其可能参与的生物学功能。结果提示:miR-665靶基因主要与有机物质反应、内源性刺激反应、激素刺激反应等生物学过程相关,主要参与了N-糖链的合成、急性髓系白血病及碱基切除修复等信号通路。通过对其靶基因的功能预测分析将为我们后期继续研究开心解郁方干预miR-665的具体作用机制提供一定的方向和理论基础。
1 朱宏,孙静.应激与抑郁症关系的研究进展.精神医学杂志,2013,26(5):388-390.
2 Ying Z,Huang S,Wang Y,et al.Mechanism underlying the protective effect of Kaixin Jieyu Fang on vascular depression following cerebral white matter damage.Neural Regeneration Research,2014,9(1):61-68.
3 Pan J,Lei X,Wang J,et al.Effects of Kaixinjieyu,a Chinese herbal medicine preparation,on neurovascular unit dysfunction in rats with vascular depression.Bmc Complementaryamp;Alternative Medicine,2014,15(1):1-14.
4 黄世敬,张先慧,王彦云,等.Effects of Kaixin Jieyu Decoction(开心解郁汤)on Behavior,Monoamine Neurotransmitter Levels,and Serotonin ReceptorSubtype Expression in the Brain of A Rat Depression Mode.中国结合医学杂志(英文版),2014,20(4):280-285.
5 Schirle N T,Sheu-Gruttadauria J,Macrae I J.Gene regulation.Structural basis for microRNA targeting.Science,2014,346(6209):608.
6 Wakabayashi T,Hidaka R,Fujimaki S,et al.MicroRNAs and Epigenetics in Adult Neurogenesis.Adv Genet,2014,86:27-44.。
7 Kim H H,Kim P,Phay M,et al.Identification of precursor microRNAs within distal axons of sensory neuron.J Neurochem,2015,134(2):193-199.
8 Lu X,Lv S,Mi Y,et al.Neuroprotective effect of miR-665 against sevoflurane anesthesia-induced cognitive dysfunction in rats through PI3K/Akt signaling pathway by targeting insulin-like growth factor 2.Am J Transl Res,2017,9(3):1344.
9 Stappert L,Roese-Koerner B,Brüstle O.The role of microRNAs in human neuralstem cells,neuronal differentiation and subtype specification.Cell Tissue Res.,2015,359(1):47-64.
10 Bocchio-Chiavetto L,Maffioletti E,Bettinsoli P,et al.Blood microRNA changes in depressed patients during antidepressanttreatment.Neuropsychopharmacology,2013,23(7):602-611.
11 Belzeaux R,Bergon A,Jeanjean V,et al.Responder and nonresponder patients exhibit different peripheral transcriptional signatures during major depressive episode.Transl Psychiatry,2012,2:e185.
12 Xian Shuang L,Michael C,Rui Lan Z,et al.MicroRNA Profiling in Subventricular Zone after Stroke:MiR-124a Regulates Proliferation of Neural Progenitor Cells through Notch Signaling Pathway.PLoS One,2011,6(8):e23461.
13 Gao J,Wang W Y,Mao Y Wet al.A novel pathway regulates memory and plasticity via SIRT1 and miR-134.Nature,2010,466(7310):1105-1109.
14 Sun W C,Liang Z D,Pei L.Propofol-induced rno-miR-665 targets BCL2L1,and influences apoptosis in rodent developing hippocampal astrocytes.Neurotoxicology,2015,51:87-95.
15 Sun W C,Pei L.rno-miR-665 targets BCL2L1(Bcl-xl)and increases vulnerability to propofol in developing astrocytes.J Neurochem.,2016,138(2):233-242.
16 Lu X,Lv S,Mi Y,et al.Neuroprotective effect of miR-665 against sevoflurane anesthesia-induced cognitive dysfunction in rats through PI3K/Akt signaling pathway by targeting insulin-like growth factor 2.Am J Transl Res,2017,9(3):1344.
Expression of miR-665 and BioinformaticAnalysis on Its Target Genes of Kai-Xin Jie-Yu Decoction Based on Depression Model Rats
Wang Liansheng,Huang Shijing,Pan Juhua,Wang Yanyun,Zhang Yin,Chen Yuxia
(Guang’anmen Hospital,China Academy of Chinese Medical Sciences,Beijing 100053,China)
This study was aimed to detect the expression of miR-665 in the hippocampal of depression rat model treated withKai-Xin Jie-Yu(KXJY)decoction and bioinformatic analysis of target genes of miR-665,in order to investigate the role of miR-665 in the pathogenesis of depression and the antidepressant mechanism of KXJY decoction.The rat model of chronic stress depression was established and then treated with KXJY decoction for 42 days.The total RNA from hippocampus tissues was extracted.And the relative expression of miR-665 in hippocampus of rats in each group was detected by RT-qPCR.TargetScan and microRNAorg databases were used to predict target genes for miR-665.DAVID database was used to classify GO function and to analyze KEGG signaling pathway of target genes.The results showed that compared with the normal group,the expression level of miR-665 in hippocampus of the model group was significantly higher with significant difference(P<0.01).Compared with the model group,the expression level of miR-665 in hippocampus of Chinese medicine group and western medicine group decreased significantly with significant difference(P<0.01).The biological functions of miR-665 target genes were mainly concentrated in the response to organic substance.The signal pathway was mainly concentrated in N-Glycan biosynthesis.It was concluded that miR-665 may be involved in the pathological process of depression,by correcting the abnormal expression of miR-665,which may be one of the antidepressant mechanisms of KXJY decoction.Through the analysis and prediction of the target genes,it provided a certain direction and theoretical basis for further study on the specific mechanism of KXJY decoction intervention on miR-665.
Depression,miR-665,biological information analysis,Kai-Xin Jie-Yudecoction
10.11842/wst.2017.08.014
R965
A
2017-06-13
修回日期:2017-07-12
* 国家自然科学基金(81573790):基于lncRNA-miRNA网络对神经血管单元稳态调控探讨益气开郁中药抗抑郁机制,负责人:黄世敬;北京市科技计划(No.Z161100001816013):开心解郁丸治疗血管性抑郁的医疗机构制剂研究,负责人:黄世敬
** 黄世敬,博士生导师,研究员,主任医师。主要从事中医脑病、抑郁症及中药研发。
(责任编辑:陈 宁,责任译审:王 晶)

