粗盐水中掺兑卤水的试验研究
,,
(连云港碱业有限公司,江苏 连云港 222042)
粗盐水中掺兑卤水的试验研究
谢佃村,穆素莲,周军梅
(连云港碱业有限公司,江苏 连云港 222042)
通过把卤水和粗盐水按不同比例搀兑,测出了饱和卤水掺入粗盐水中后各主要成分含量变化的规律,并模拟盐水除钙除镁工艺,对盐水精制的效果进行了试验研究。
粗盐水;搀兑卤水;除钙;除镁;试验
为了研究淮安卤水使用对我公司纯碱生产的影响,把卤水和粗盐水按不同比例搀兑,观察其主要成分含量变化以及对盐水精制工序带来的影响,为利用卤水制备纯碱提供科学依据。
1 对原盐(工业用盐)主要组分的测定
1.1 氯离子含量的测定
称取24.5377 g(精确至0.0001 g)在100~105 ℃下烘干恒重的原盐,溶解定容于500 mL容量瓶中,此为原盐溶液(A)。
取上述溶液25.00 mL于250 mL容量瓶中,加蒸馏水至刻度,摇匀。然后用移液管取25.00 mL于250 mL锥形瓶中,加入约25 mL蒸馏水,加10%K2CrO4溶液3~4滴,在充分摇动下,用c(AgNO3)=0.05006 mol/L的标准滴定溶液滴定至悬浊液由淡黄色变为微砖红色,经充分摇动不消失即为终点。平行测定2次。
消耗AgNO3标液:37.10 mL。
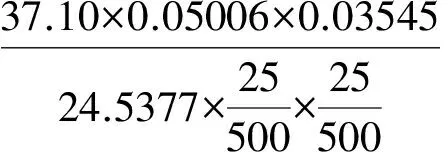
=53.68
平均Cl-%=53.68
1.2 钙离子含量的测定
取原盐溶液(A)25.00 mL于250 mL三角瓶中,加入2 mol/L的NaOH约2.5 mL,调节pH=12,加1%钙指示剂2~3滴,立即用c(EDTA)=0.025 mol/L的标准滴定溶液滴定至溶液由酒红色变为纯蓝色为终点。
消耗EDTA标液:1.70 mL。
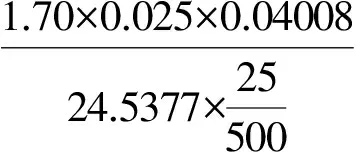
平均Ca2+%=0.14
1.3 镁离子含量的测定
取原盐溶液(A)25.00 mL于250 mL三角瓶中,加5 mL氨性缓冲溶液,加0.5%的铬黑T指示剂2~3滴,摇匀后,立即以c(EDTA)=0.025 mol/L的标准滴定溶液滴定至溶液由酒红色变为纯蓝色为终点。记录EDTA标液用量,减去测定钙所消耗的EDTA标液用量,即得滴定镁离子所消耗的EDTA标液用量。
消耗EDTA标液:10.10 mL。
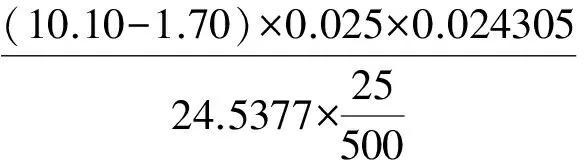
×100=0.42
平均Mg2+%=0.42
1.4 硫酸根含量的测定(EDTA络合法)
取原盐溶液(A)50.00 mL于250 mL三角瓶中,加1+1 HCl溶液10滴(约0.5 mL),加热近沸,加20.00 mL 0.025 mol/L的BaCl2-MgCl2混合液煮沸5 min,冷却后,加入5 mL氨性缓冲溶液,2~3滴0.5%的铬黑T指示剂,摇匀后,用c(EDTA)=0.025 mol/L的标准滴定溶液滴定至溶液由酒红色变为纯蓝色为终点。
滴定所消耗的EDTA标液体积:34.99 mL。
空白:滴定20.00 mL 0.025 mol/L的BaCl2-MgCl2混合液消耗EDTA标液23.82 mL;
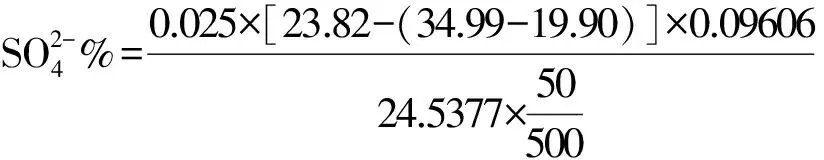
×100=0.85

表1 测得原盐成分
2 粗盐水与饱和卤水掺合试验
2.1 饱和卤水的制备
取江苏油田淮安输送的卤水1桶(约25 L)(17 ℃密度为1.2175),加入原盐500 g,经充分摇匀后,静置48 h,取上清液备用。
2.2 粗盐水提取
取盐水车间化盐槽的粗盐水25 L,经过滤后备用。
2.3 掺合比例及用量
按照“粗盐水:饱和卤水的比例”分不同的比例配比样品,如表2所示。
2.4 掺合液中主要成分的测定
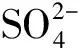
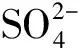
取10.00 mL掺合液于250 mL烧杯中,加1 mL 1+1 HCl,用表面皿盖好,加热至沸,取下烧杯,在不断搅拌下,逐滴加入10%BaCl2溶液25 mL,然后在80~90 ℃水浴上保温2 h,使BaSO4结晶长大。用无灰滤纸过滤,用冷水分数次洗涤烧杯和沉淀,直至滤液加AgNO3试液不混浊为止。将沉淀同滤纸一起移入已恒重的磁坩埚中,放进烘箱中,放进烘箱于100~105 ℃下烘干,再转入高温炉中,将滤纸徐徐灰化(勿使滤纸着火),待滤纸全部灰化后,升温至800 ℃灼烧1 h,取出冷却3~5 min后放入干燥器内,冷却至室温后称重。重复灼烧30 min,至恒重(±0.2 mg为止)。以上每个项目平行测定两次,取平均值。
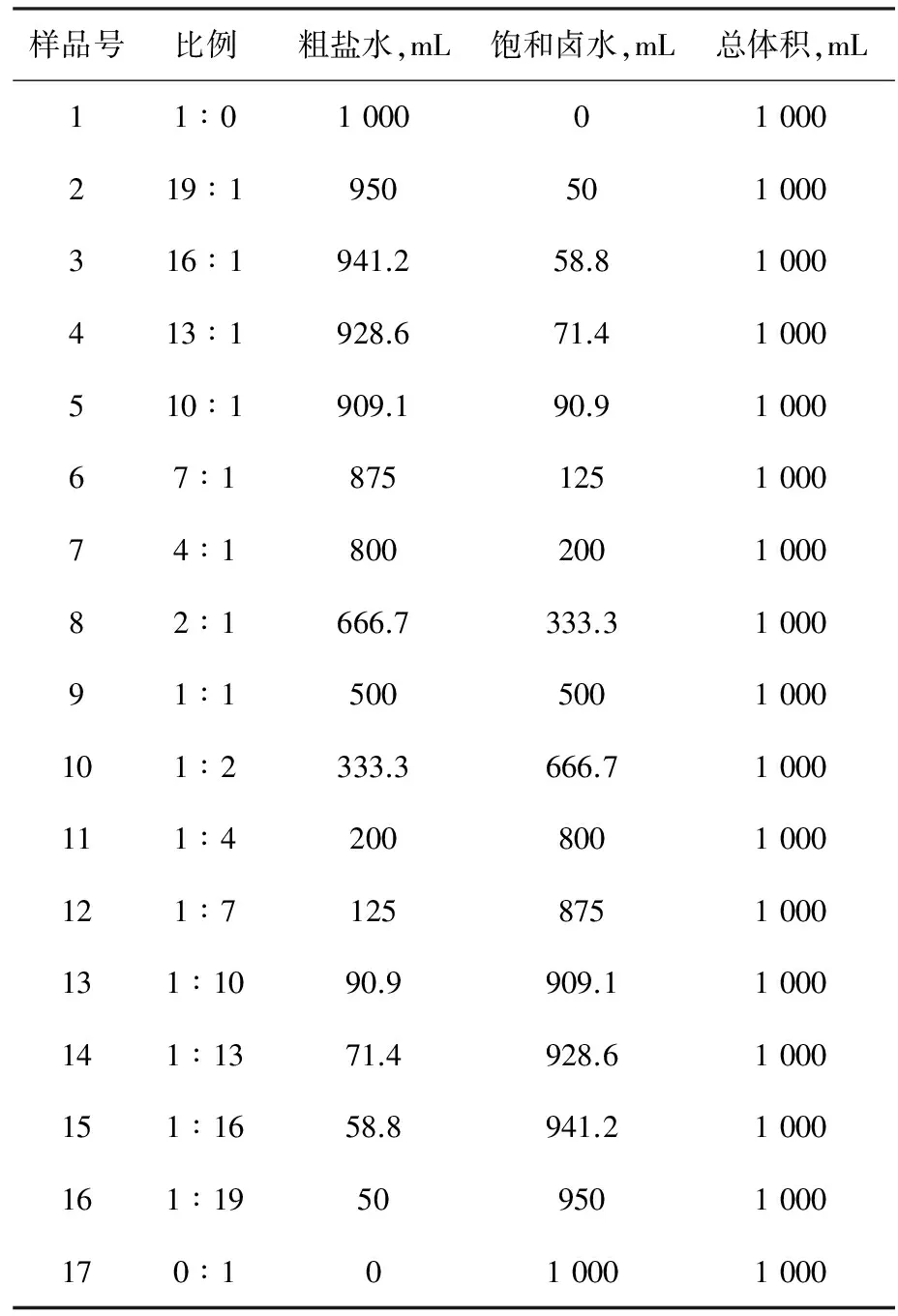
表2 粗盐水与饱合卤水掺兑量
结果计算:
1)重量法:
式中:A——空坩埚重,g;B——坩埚+硫酸钡沉淀重,g; 0.4116——将硫酸钡换算为硫酸根的系数。
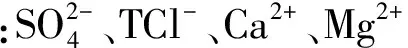
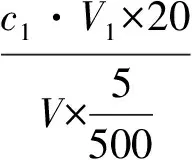
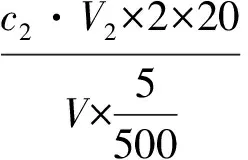
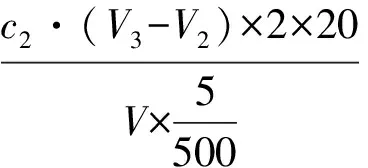
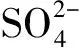
注:*—50.00 mL为稀释后的取样量,随着硫酸根含量的增加,取样量应随之减小。
不同比例掺合液的测定数据表3所示。
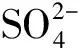
2.5 掺合液除镁后主要成分的测定
2.5.1 按下式计算需加入的灰乳量
c(Mg2+)×V1=c[Ca(OH)2]×V2
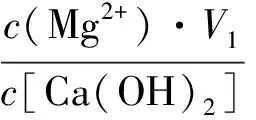
式中:V2——灰乳的加入量, mL;V1——取掺合液的体积,500 mL;c(Mg2+)——测得Mg2+的浓度,tt;c[Ca(OH)2]——加入灰乳的浓度,151.45 tt。
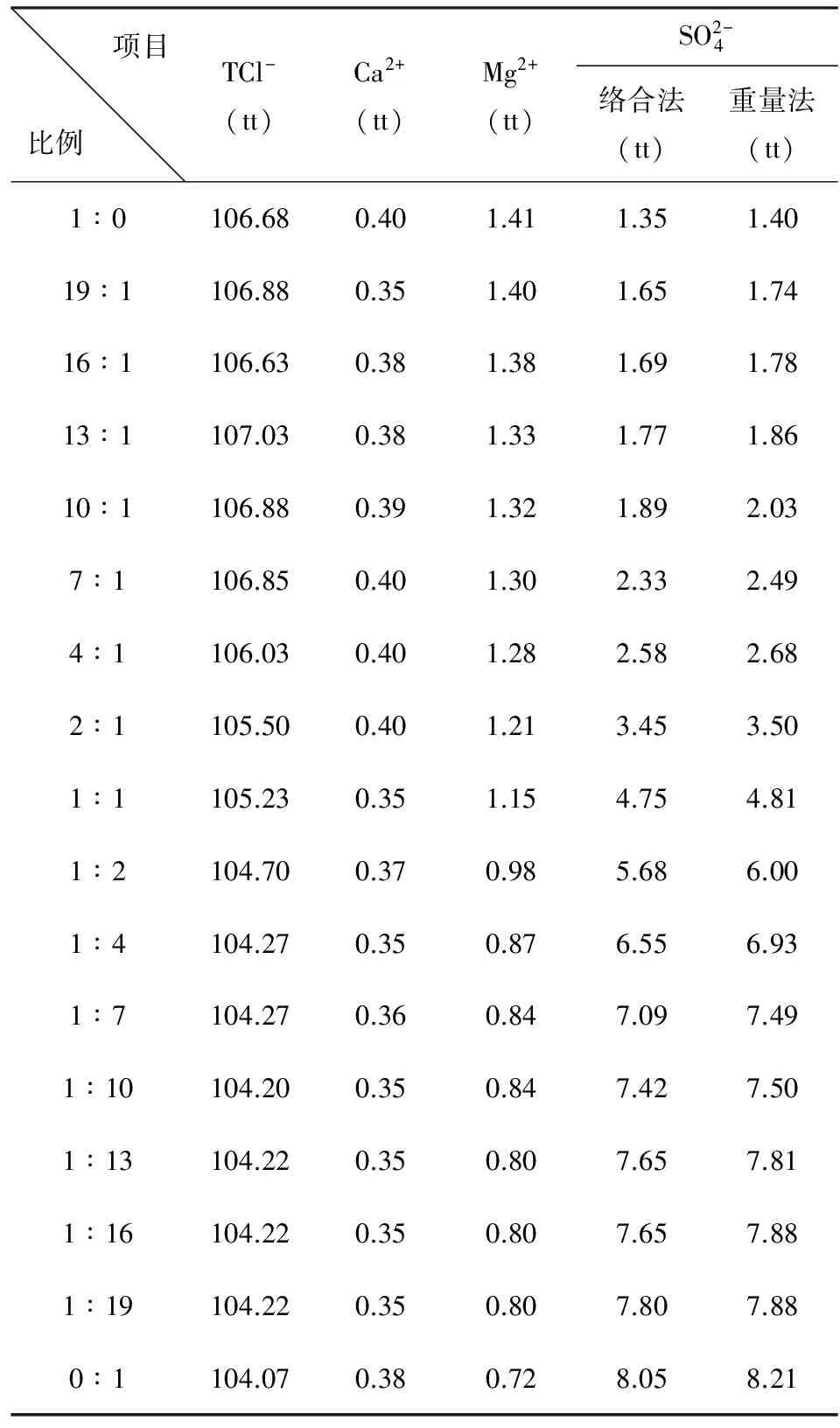
表3 掺合液中主要成分
2.5.2 各样品灰乳的加入量
对19∶1,16∶1,13∶1和1∶19四个样按计算量加入灰乳;而对1∶1,1∶2,1∶4,1∶7四个样按计算量减少10%的量加入灰乳;其余九个样按计算过量10%加入灰乳。充分搅匀后,放置2 h。
2.5.3 除镁后主要成分的测定
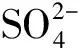
2.6 掺合液除钙后主要成分的测定
按下式计算的量加入纯碱液,并且过量约10%:
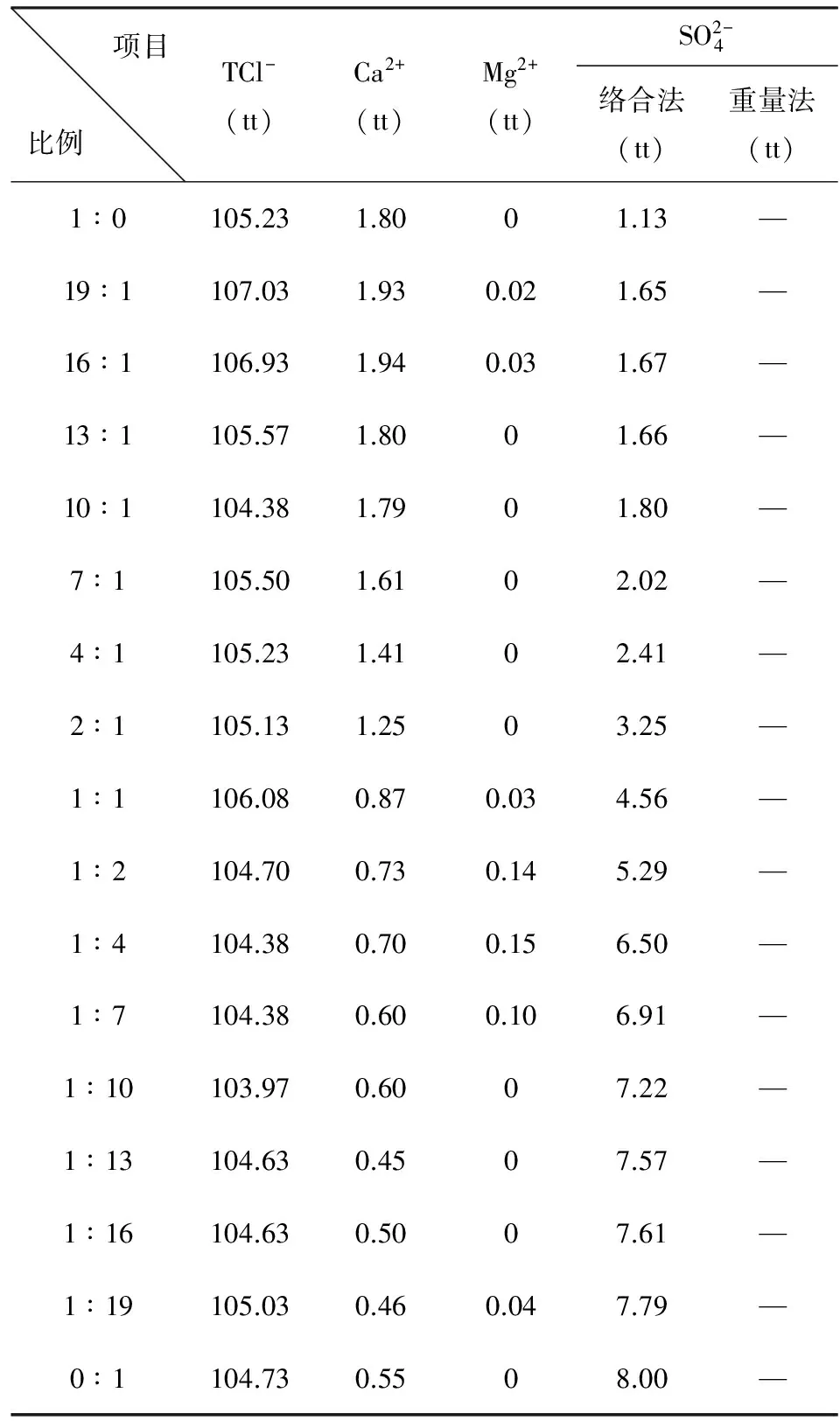
表4 掺合液除镁后主要成分
c(Ca2+)·V1=c(Na2CO3)·V2
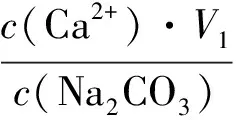
式中:V2——纯碱液的加入量, mL;V1——取掺合液的体积,450 mL;c(Ca2+)——除镁液中钙的浓度,tt;c(Na2CO3)——加入的纯碱液的浓度,54.60 tt。
从表5中可以看出,只要Mg2+能基本除净,加入过量的纯碱液后,Ca2+都能除干净,而Mg2+没有除净的,就会残留一点Ca2+,这可能是两者相互影响的结果。
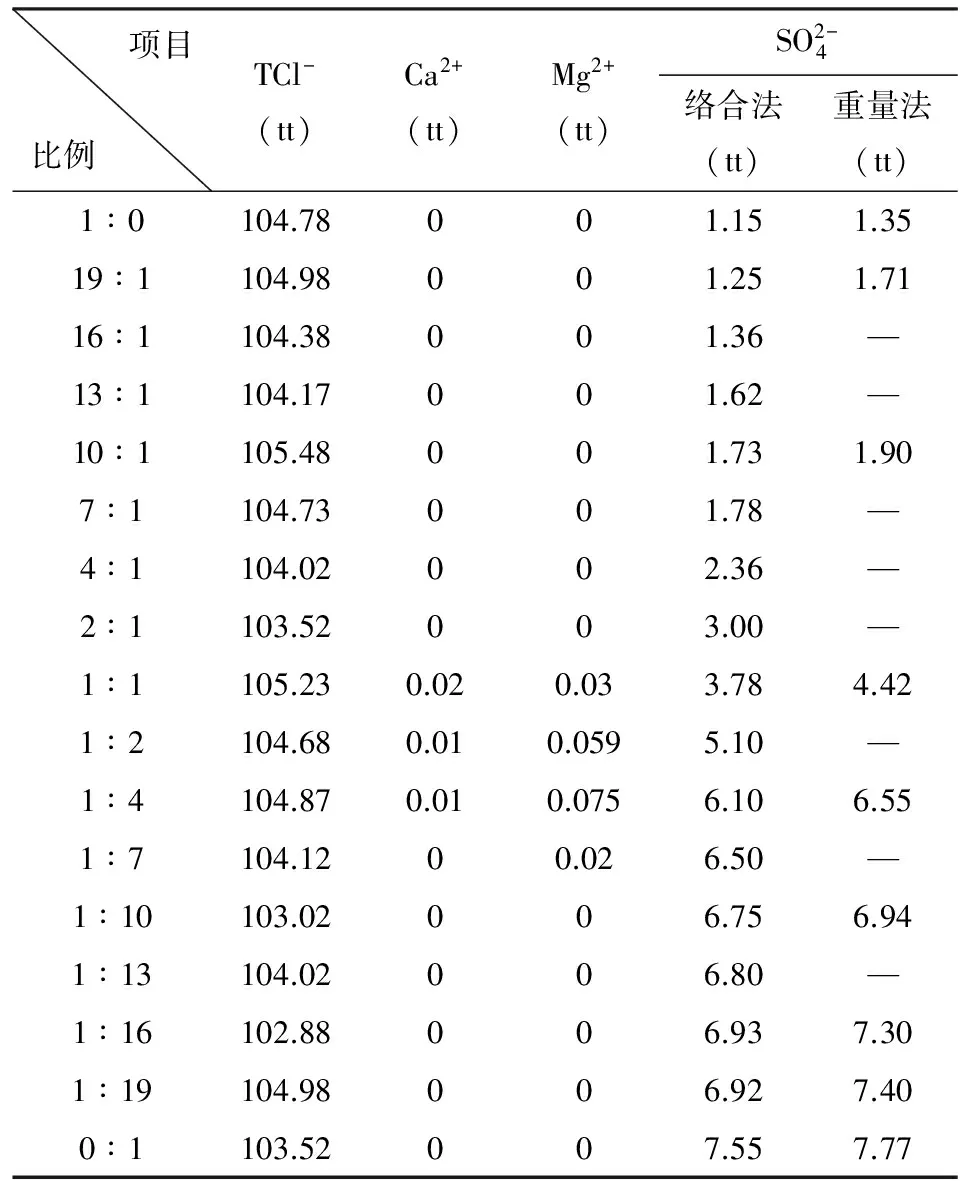
表5 掺合液除钙后主要成分
3 试验结论
从总体上看,本试验测出了饱和卤水按不同比例掺入粗盐水中后各主要成分含量的变化规律,即随着卤水搀兑比例的不断增加,镁的浓度逐渐降低,而硫酸根的浓度则逐步升高。
本试验的另一个主要目的是研究盐水精制过程中,各主要成分的变化情况,特别是硫酸根的变化趋势。从测出的数据表中可见,只要控制好灰乳和纯碱液的用量,钙、镁离子是可以除尽的。本试验对纯碱生产中卤水的使用具有重要的指导意义。
[1] 李国瑞,陈歆文.纯碱生产分析[M].沈阳:辽宁科学技术出版社,1989
[2] 刘珍.化验员读本[M].北京:化学工业出版社,1983
[3] 武汉大学.分析化学(第二版)[M].北京:高等教育出版社,2003
TQ114.161
A
1005-8370(2017)05-14-04
2017-06-22
谢佃村(1966—),大学,现为连云港碱业有限公司质检中心主任。

