西地那非联合辛伐他汀治疗慢性阻塞性肺疾病合并肺动脉高压患者的效果分析
姜妤 郭小青 陈曦 杨敏 许巧玲
·论著·
西地那非联合辛伐他汀治疗慢性阻塞性肺疾病合并肺动脉高压患者的效果分析
姜妤 郭小青 陈曦 杨敏 许巧玲
目的探讨西地那非联合辛伐他汀治疗慢性阻塞性肺疾病合并肺动脉高压患者的临床效果分析。方法将2016年1月至2017年1月治疗的92例慢性阻塞性肺疾病合并肺动脉高压患者随机分为2组,2组均给予低流量吸氧,平喘、化痰、解除痉挛以及强心、利尿、改善心功能等常规对症治疗,在此基础上,对照组给予西地那非治疗,观察组给予西地那非联合辛伐他汀治疗,比较2组患者的临床疗效、肺功能、血氧分压、血氧饱和度、肺动脉压力及右心功能、各项实验室指标。结果观察组治疗有效率为95.65%,较对照组的76.09%显著提高,2组有明显差异(P<0.05);2组治疗前FEV1、FEV1/FVC、FVC、SpO2、PaCO2、PaO2无明显差异(P>0.05);观察组治疗后FEV1、FEV1/FVC、FVC、SpO2、PaCO2、PaO2明显优于对照组,2组差异有统计学意义(P<0.05);两组治疗前PASP、mPAP、PVR、RVESD、RVEF、6MWD无显著差异(P>0.05);观察组治疗后PASP、PVR、RVESD、RVEF、6 MWD明显较对照组提高,2组差异有统计学意义(P<0.05);2组患者治疗前血浆NO、eNOS、hs-CRP、TNF-α、IL-1、IL-6、ET-1无明显差异(P>0.05);观察组治疗后血浆NO、eNOS、hs-CRP、TNF-α、IL-1、IL-6、ET-1较对照组明显改善,两组有统计学差异(P<0.05)。结论西地那非联合辛伐他汀治疗慢性阻塞性肺疾病合并肺动脉高压有确切疗效,能够改善肺功能及右心功能,有效扩张血管,降低肺动脉高压,减少全身炎症反应,具有积极的临床意义。
慢性阻塞性肺疾病合并肺动脉高压;西地那非;辛伐他汀;临床效果
慢性阻塞性肺疾病(COPD)是临床常见的呼吸系统疾病,其以不完全可逆的气流受限为显著特征,病情呈进行性发展,病理表现为慢性肺泡性低氧,主要与与肺部对有害气体或有害颗粒的异常炎症反应有关。若气流严重受限,COPD可并发肺动脉高压(pulmonary hypertension,PH),使得病情加重,易发展为肺源性心脏病,甚至导致有心衰竭和死亡[1]。由于COPD合并PH的病情复杂,发病机制尚未完全明确,目前临床无特效治疗方法,多通过对症治疗、增加活动耐量、防止病情进展等进行处理,常规的治疗手段包括强心、利尿、抗血小板聚集等,但疗效有限[2]。临床治疗PH的药物较多,他汀类药物、5-磷酸二酯酶抑制剂、前列环素等均有不同程度治疗效果[3]。辛伐他汀具有抗氧化、恢复内皮功能及抗炎等作用,阻止动脉管壁重构,西地那非可扩张肺血管、降低肺动脉压[4]。本研究分析西地那非联合辛伐他汀治疗慢性阻塞性肺疾病合并肺动脉高压患者的临床效果,旨在提高临床对本病的治疗效果,汇报如下。
1 资料与方法
1.1 一般资料 将2016年1月至2017年1月在保定市第一中心医院呼吸内科治疗的92例慢性阻塞性肺疾病合并肺动脉高压患者随机分为2组。观察组46例,男30例,女16例;年龄41~78岁,平均年龄(63.4±4.5)岁;COPD病程6个月~7年,平均病程(3.4±1.6)年;对照组46例,男28例,女18例;年龄44~81岁,平均年龄(64.1±5.3)岁;COPD病程8个月~11年,平均病程(5.1±2.2)年;本研究经我院伦理委员会审批批准,所有患者均知情同意自愿加入;2组患者的性别比、年龄、肺功能、肺动脉压力等明显差异无统计学意义(P>0.05),具有可比性。
1.2 诊断标准 所有患者符合符合中华医学会呼吸病学分会2007年《慢性阻塞性肺疾病诊治指南》《肺动脉高压筛查诊断与治疗专家共识》中的相关诊断标准[5],肺动脉收缩压(SPAP)>30 mm Hg,FEV1占预计值百分比≤65%,FEV1占用力肺活量(FVC)≤70%;心功能分级根据纽约心脏病学会心功能分级标准,NYHA在Ⅰ~Ⅱ级[6]。
1.3 排除标准 排除近3个月内服用过他汀类及内皮素受体拮抗剂者、严重肺部感染者、严重肝肾功能异常者、过敏性鼻炎、支气管哮喘、肺动脉栓塞、合并心脏疾病者[7]。
1.4 治疗方法 所有患者入院后对原发疾病进行治疗,给予吸氧或机械通气,平喘、化痰、解除气道痉挛,强心、抗炎、利尿等对症处理;通过吸入糖皮质激素抗炎、扩张支气管,使用头孢类的抗菌药提高抗感染能力[8]。在此基础上,对照组服用西地那非(辉瑞制药有限公司生产,国药准字H20020258)50 mg/次,2次/d。观察组在对照组基础上服用辛伐他汀(杭州默沙东制药有限公司生产,国药准字H19990366)40 mg/次,2次/d[9]。4周为1个疗程,连续服用3个疗程后评价疗效。治疗期间禁止服用硝酸酯类扩血管药物[10]。
1.5 疗效判定标准 显效:症状及体征明显好转,缺氧症状明显减轻,呼吸等级下降2个等级,肺动脉高压较治疗前降低15%以上,氧分压有所上升;有效:症状及体征有所改善,缺氧症状有所缓解,呼吸等级下降1个等级,肺动脉高压降低5%~14%,氧分压上升不明显;无效:症状及体征无明显改善,仍有明显缺氧症状,呼吸等级无变化,肺动脉高压下降低于5%,氧分压下降[11]。
1.6 观察指标 治疗前后分别检查肺功能及血气分析各指标,包括一秒用力呼吸容积(FEV1)、用力呼气量占用力肺活量比值(FEV1/FVC)、用力肺活量(FVC),抽取前臂肺动脉血测定血氧饱和度(SpO2)、动脉血二氧化碳分压(PaCO2)、肺泡氧分压(PaO2);治疗前后分别检查肺动脉压及右心功能各指标,采用彩色多普勒诊断仪测定收缩期肺动脉压(PASP)、平均肺动脉压(mPAP)、肺血管阻力(PVR)、右心室收缩末径
(RVESD)、右心室射血分数(RVEF)、 6 min步行距离(6MWD);治疗后复查各项血生化指标,包括一氧化氮(NO)、一氧化氮合酶(eNOS)、超敏C-反应蛋白(hs-CRP)、肿瘤坏死因子-α(TNF-α)、血浆细胞因子白介素-1(IL-1)、白介素-6(IL-6)、血浆内皮素-1(ET-1)。
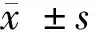
2 结果
2.1 2组患者临床疗效比较 观察组治疗有效率为95.65%,较对照组的76.09%显著提高,2组差异有统计学意义(P<0.05)。见表1。

表1 2组患者临床疗效比较 n=46,例
注:与对照组比较,*P<0.05
2.2 2组患者治疗前后肺功能及血气分析各指标比较 2组治疗前FEV1、FEV1/FVC、FVC、SpO2、PaCO2、PaO2无明显差异(P>0.05);观察组治疗后FEV1、FEV1/FVC、FVC、SpO2、PaCO2、PaO2明显优于对照组,2组有显著差异(P<0.05)。见表2。
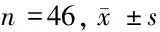

项目观察组治疗前治疗后t值P值对照组治疗前治疗后t值P值FEV1(L)1.05±0.141.31±0.18∗3.707<0.050.98±0.121.13±0.13∗#3.023<0.05FEV1/FVC(%)48.45±4.0672.57±4.32∗5.651<0.0548.98±3.9666.75±4.14∗#4.679<0.05FVC(L)1.42±0.332.08±0.24∗4.303<0.051.45±0.291.72±0.19∗#3.654<0.05SpO2(%)82.92±4.2694.15±5.01∗4.675<0.0583.08±4.1190.14±4.73∗#4.032<0.05PaCO2(mmHg)67.69±4.0548.32±4.59∗5.238<0.0566.98±3.9758.07±4.04∗#3.978<0.05PaO2(mmHg)53.79±4.4282.64±4.91∗6.083<0.0552.87±3.9678.84±4.21∗#5.215<0.05
注:与治疗前比较,*P<0.05;与观察组比较,#P<0.05
2.3 2组患者治疗前后肺动脉压和右心功能比较 2组治疗前PASP、mPAP、PVR、RVESD、RVEF、6MWD无显著差异(P>0.05);观察组治疗后PASP、PVR、RVESD、RVEF、6MWD明显较对照组提高,两组差异有统计学意义(P<0.05)。见表3。
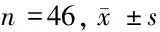

项目观察组治疗前治疗后t值P值对照组治疗前治疗后t值P值PASP(mmHg)63.42±10.0144.95±9.16∗5.453<0.0563.29±9.8750.12±9.56∗#4.657<0.05mPAP(mmHg)54.65±16.4136.31±14.70∗5.078<0.0555.03±16.8243.11±15.15∗#4.243<0.05PVR(dyn·s-1·cm-1)1267±621 798±414∗5.657<0.051256±657 947±483∗#4.451<0.05RVESD(mm)33.41±8.94 27.35±7.42∗4.546<0.0533.70±9.3829.19±8.06∗#3.963<0.05RVEF(%)47.50±5.08 57.35±4.53∗5.219<0.0548.13±4.7954.95±4.84∗#4.347<0.056MWD(m)251.94±34.62 383.25±31.46∗6.023<0.05254.16±37.58305.61±30.75∗#4.873<0.05
注:与治疗前比较,*P<0.05;与观察组比较,#P<0.05
2.4 2组患者治疗前后各项生化指标比较 2组患者治疗前血浆NO、eNOS、hs-CRP、TNF-α、IL-1、IL-6、ET-1无明显差异(P>0.05);观察组治疗后血浆NO、eNOS、hs-CRP、TNF-α、IL-1、IL-6、ET-1较对照组明显改善,2组差异有统计学意义(P<0.05)。见表4。
3 讨论
PH是COPD患者常见的严重并发症之一,主要是由于COPD患者的气道、肺血管及肺实质发生的慢性非特异性炎症引起的气道壁损伤、修复、结构重塑,进而导致气道狭窄,使得通气/血流比失调,遂产生低氧血症、肺血管痉挛、肺血管内反应性红细胞增多,进而引起肺血管压力和阻力增加[12]。超微结构显示,COPD后期肺泡壁逐步纤维化,毛细血管床减少,继而出现肺动脉高压,右心射血受阻,肺动脉干、右心代偿性增大,逐步出现右心功能衰竭[13]。
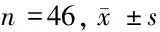

项目观察组治疗前治疗后t值P值对照组治疗前治疗后t值P值NO(ng/ml)13.56±8.7325.47±13.71∗6.751<0.0512.92±8.5818.69±10.24#5.018<0.05eNOS(U/ml)13.95±9.2728.88±14.36∗6.543<0.0514.35±9.7721.26±12.42∗#5.472<0.05hs⁃CRP(ng/L)21.62±3.437.02±1.05∗7.845<0.0521.79±3.7613.13±2.74∗#4.872<0.05TNF⁃α(mg/L)35.75±6.3921.87±4.63∗5.349<0.0535.44±5.9330.16±6.30∗#3.783<0.05IL⁃1(ng/L)63.21±5.5456.52±6.18∗5.342<0.0563.25±4.7961.66±4.63∗#3.905<0.05IL⁃6(ng/L)27.08±3.7924.31±4.41∗4.896<0.0527.57±3.7526.89±4.72∗#3.578<0.05ET⁃1(ng/L)6.36±2.313.02±1.22∗4.651<0.056.39±2.284.51±3.42∗#3.987<0.05
注:与治疗前比较,*P<0.05;与观察组比较,#P<0.05
目前临床对COPD合并PH尚缺乏满意的治疗策略,治疗目标是延长患者的生存期,一般是在COPD基础疾病治疗的基础上,针对引发PH的三个主要途径进行干预,如内皮素途径、一氧化氮途径、前列环素途径[14]。
西地那非为5型磷酸二酯酶(PED-5)抑制剂。NO可激活cGMP,阻断Ca2+内流,舒张血管平滑肌,降低血压[15];PED-5是肺动脉血管中主要的磷酸二酯酶,PED-5选择性的与cGMP结合,使得cGMP水解增加,而PED-5抑制剂能够减少cGMP的水解,提高血中cGMP水平,从而促进肺动脉血管舒张,减轻肺循环阻力,降低肺动脉压,纠正通气/血流比值失调[16]。同时,PDE-5抑制剂有抗增殖作用,通过逆转血管重构,进一步降低肺血管阻力[17]。临床研究证实,他汀类药物对减轻肺部炎性反应以及肺功能改善方面具有非常好的疗效[18]。辛伐他汀为他汀类的代表药物,不仅能够降低血脂,还能抑制肺血管重构、降低肺动脉高压出现几率,有效减轻肺动脉内膜增生,改善血管内皮功能,促进血管再生,降低肺动脉高压的临床症状,从而达到治疗效果[19,20]。临床通过对辛伐他汀的深入研究显示,对比IL-1、IL-6、hs-CRP等炎性因子发现[21],本药能显著改善全身炎症状况,对COPD合并PH具有较好的疗效。
本研究结果显示,观察组治疗有效率为95.65%,较对照组的76.09%显著提高,2组有明显差异(P<0.05);观察组治疗后FEV1、FEV1/FVC、FVC、SpO2、PaCO2、PaO2明显优于对照组,2组有显著差异(P<0.05);观察组治疗后PASP、PVR、RVESD、RVEF、6MWD明显较对照组提高,2组差异有统计学意义(P<0.05);观察组治疗后血浆NO、eNOS、hs-CRP、TNF-α、IL-1、IL-6、ET-1较对照组明显改善,2组有统计学差异(P<0.05)。充分证明西地那非联合辛伐他汀能有效缓解COPD合并PH病情,降低肺动脉压,改善右心功能,增强血管内皮的修复和再生,减轻全身炎症状态,具有确切的临床效果。乔树斌[22]研究认为,西地那非联合阿托伐他汀治疗COPD合并PH能够显著改善FEV1、FEV1/FVC、PaO2、SpO2、mPAP、 RVESD、RVEF、TNF-α、hs-CRP等指标,且联合用药不增加药物不良反应,与本研究结果一致。
综上所述,西地那非联合辛伐他汀治疗COPD合并PH疗效明显,能有效抑制肺血管重建,逆转肺血管的病理变化,降低肺动脉高压,延缓病情进展,促进心肺功能恢复,提高生存质量,具有积极的临床意义。
1 孙小军.辛伐他汀联合西地那非治疗慢性阻塞性肺疾病合并肺动脉高压的临床研究.中国当代医药,2013,20:70-71.
2 李丽,曹学彬,王晶璞,等.大珠红景天注射液联合辛伐他汀治疗慢性阻塞性肺疾病合并肺动脉高压的临床研究.现代药物与临床,2016,31:1403-1406.
3 李曰富.辛伐他汀对COPD患者肺动脉高压的治疗效果.中华临床医师杂志(电子版),2016,10:149-150.
4 庞伯健.辛伐他汀联合西地那非对慢性阻塞性肺疾病肺动脉高压患者心肺功能的影响.中国药业,2015,25:6-7.
5 马肖龙.阿奇霉素联合辛伐他汀治疗慢性阻塞性肺疾病合并肺动脉高压的临床疗效.中国临床药理学杂志,2015,31:250-252.
6 蒋衣果,周梅芳,朱建军.辛伐他汀联合法舒地尔治疗COPD合并肺动脉高压患者临床效果观察.西部医学,2016,28:709-712.
7 马峰,朱卫华.小剂量大环内酯类药物联合辛伐他汀治疗慢性阻塞性肺疾病合并肺动脉高压疗效评价.医学综述,2016,22:170-172.
8 鲁惠敏,梁新亮,张传军,等.西地那非联合贝前列素或阿托伐他汀治疗肺动脉高压的临床观察.中国现代应用药学,2012,29:1134-1136.
9 真娟,华树成.西地那非治疗COPD合并肺动脉高压30例临床分析.吉林医学,2011,32:75-77.
10 Vitulo P,Stanziola A,Confalonieri M,et al. Sildenafil in severe pulmonary hypertension associated with chronic obstructive pulmonary disease:A randomized controlled multicenter clinical trial. J Heart Lung Transplant,2016,13:276-282.
11 朱协坤.阿奇霉素联合辛伐他汀治疗慢性阻塞性肺疾病合并肺动脉高压的临床疗效.海峡药学,2015,27:134-135.
12 赵献明,许春平,曾波,等.阿托伐他汀联合西地那非在慢性阻塞性肺疾病相关肺动脉高压患者的临床观察.医学信息,2010,5:2673-2675.
13 曹艳红,朱蓉.辛伐他汀治疗COPD合并肺动脉高压的临床研究.临床肺科杂志,2012,17:247-249.
14 张睿花,林泉,王笑英.辛伐他汀治疗老年慢性阻塞性肺疾病合并肺动脉高压患者对细胞因子水平及肺功能的影响.中国老年学杂志,2015,35:7105-7106.
15 唐晨.辛伐他汀治疗对慢性阻塞性肺疾病合并肺动脉高压患者心肺功能及炎性细胞因子的影响.现代中西医结合杂志,2017,26:851-853.
16 周海平.西地那非联合瑞舒伐他汀治疗COPD合并肺动脉高压的临床应用.河北医学,2014,20:1888-1890.
17 杨朝,葛利军,赵霞,等.西地那非治疗慢性阻塞性肺疾病相关肺动脉高压的疗效.中国老年学杂志,2015,35:1156-1157.
18 王海燕,张继友,金宁.前列地尔联合西地那非治疗肺动脉高压的疗效观察.广州医药,2011,42:17-19.
19 Bae HK,Lee H,Kim KC,et al. The effect of sildenafil on right ventricular remodeling in a rat model of monocrotaline-induced right ventricular failure.Korean J Pediatr,2016,59:262-270.
20 何飞,彭雪梅.探讨拘椽酸西地那非片对慢性阻塞性肺疾病(COPD)合并肺动脉高压(PH)患者的临床疗效.中国医药指南,2012,11:186-187.
21 张双,刘霞,张佩,等.阿魏酸钠联合阿托伐他汀治疗肺动脉高压疗效观察.临床肺科杂志,2013,18:932-933.
22 乔树斌.西地那非联合阿托伐他汀治疗COPD并肺动脉高压效果观察.山东医药,2015,55:70-72.
10.3969/j.issn.1002-7386.2017.20.027
R 563
A
1002-7386(2017)20-3136-04
2017-06-02)
071000 河北省保定市第二医院(姜妤、郭小青);河北省保定市第一中心医院(陈曦、杨敏、许巧玲)

