荧光法测定橙汁中维生素C的含量
何春晓
(陇东学院 化学化工学院,甘肃 庆阳 745000)
荧光法测定橙汁中维生素C的含量
何春晓
(陇东学院化学化工学院,甘肃庆阳745000)
维生素C经Cu2+氧化后,在一定条件下和邻苯二胺反应产生具有强荧光的喹喔啉,据此建立一种灵敏而又快速的测定维生素C的荧光分析法。实验中对缓冲溶液的浓度及pH值、氧化剂Cu2+的用量、邻苯二胺的浓度、氧化时间及反应时间进行了优化。结果表明,在最佳条件下,维生素C浓度在0.8~80μg·mL-1范围内与ΔF呈良好的线性关系,线性回归方程为△F=37.875c-8.4993,R2=0.9991。采用本法测得橙汁中维生素C的含量为135.5μg·mL-1。
维生素C;荧光法;橙汁
维生素C,又称抗坏血酸,是人体中所必需的营养物质之一。大多数新鲜水果和绿色蔬菜中都含有维生素C,如白菜、菜花、子姜、青椒、柚子、草莓、枣等果蔬中都富含大量的维生素C,其中青椒、沙田柚、新鲜枣中维生素C含量相对较高[1-2],平均含量在100~250mg/100g之间。因此,人们应该多吃富含维生素C的果蔬以维持人体的健康。基于维生素C的重要性,建立一种灵敏而又快速的检测维生素C的方法势在必行。目前测量维生素C的方法主要有流动注射化学发光法[3]、荧光法[4-6]、高效液相色谱法[7]、2,4-二硝基苯肼法[8]、碘量法[9-10]、2,6-二氯酚靛酚法[11]、紫外分光光度法[12-13]等。荧光法因具有灵敏度高、选择性好、操作简单等优点而被人们广泛使用。本文采用荧光法对橙汁中维生素C的含量进行了测定,为样品中维生素C含量的测定提供了一种思路。
1 实验部分
1.1 仪器与试剂
仪器:HITACHIF-7000荧光光谱仪(日本日立公司),电子天平(北京赛多利斯天平有限公司),PHS-3C精密pH计(上海精密科学仪器有限公司)。
试剂:抗坏血酸(分析纯,天津市大茂化学试剂厂),邻苯二胺(化学纯,天津市百世化工有限公司),其余试剂均为分析纯,实验用水均为二次蒸馏水。
材料:美汁源酷儿橙汁饮料。
1.2 实验原理
维生素C本身没有荧光,与氧化剂Cu2+作用后,和邻苯二胺反应生成强荧光的喹喔啉,其荧光强度与维生素C的浓度在一定范围内呈线性关系,据此测定维生素C的含量。
1.3 实验方法
在10mL比色管中加入20μg·mL-1维生素C溶液,0.2mol·L-1HAc-NaAc缓冲溶液(pH值=5),0.04mg·mL-1CuSO4溶液,加上塞子摇匀氧化15min后再加入0.08mg·mL-1的邻苯二胺溶液,用水定容至刻度,反应25min后在激发波长369nm,发射波长430nm的条件下测定维生素C工作液的荧光强度F,同时测定试剂空白溶液的荧光强度F0,两者的差值△F=F-F0即为相对荧光强度。
2 结果与讨论
2.1 荧光光谱
图1中曲线1、2分别为试剂空白溶液和维生素C工作液的荧光光谱图。从图中可以看出,试剂空白溶液的荧光值F0基本为零,而维生素C工作液的荧光强度则明显增强。这主要是由于氧化型维生素C与邻苯二胺作用产生具有强荧光的喹喔啉。
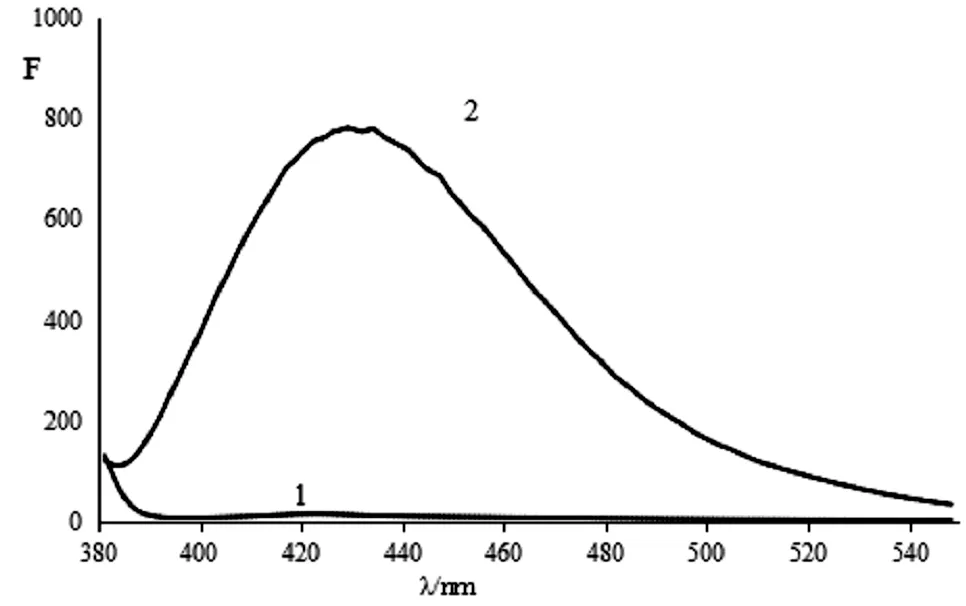
图1 荧光光谱图
2.2 缓冲溶液浓度的选择
实验中,我们分别测试了HAc-NaAc、NaOH-KH2PO4、NaOH-KHC8H4O4三种缓冲体系对荧光强度的影响,结果发现以HAc-NaAc作为缓冲剂,体系的荧光强度稳定,效果最佳。
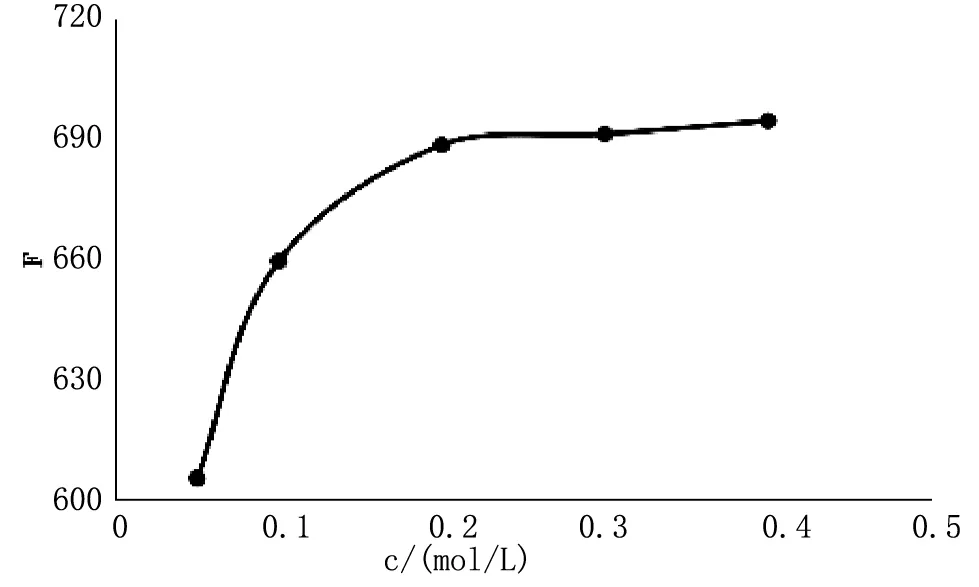
图2 缓冲溶液浓度对荧光强度的影响
本文探究了HAc-NaAc缓冲溶液的浓度在0.05~0.4mol·L-1范围内变化时对体系荧光强度的影响。从图中我们可以看出,起始随着缓冲溶液浓度的增大,荧光强度逐渐增大,当浓度增大至0.2mol·L-1后,体系的荧光强度基本趋于稳定。因此,实验中以0.2mol·L-1作为缓冲溶液的最佳浓度。
2.3 缓冲溶液pH的选择
实验中对缓冲溶液的pH做了优化,结果如图3所示。从图中可以看出,当pH值=5时体系的荧光强度最大,因此实验中以pH值=5作为缓冲溶液的最佳pH值。
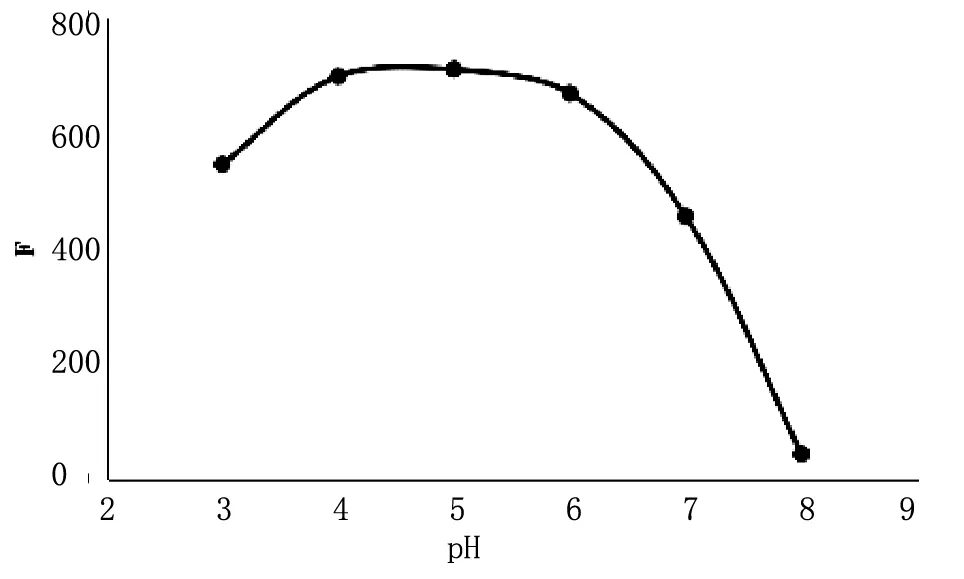
图3 缓冲溶液pH值对荧光强度的影响
2.4 氧化剂Cu2+用量的选择
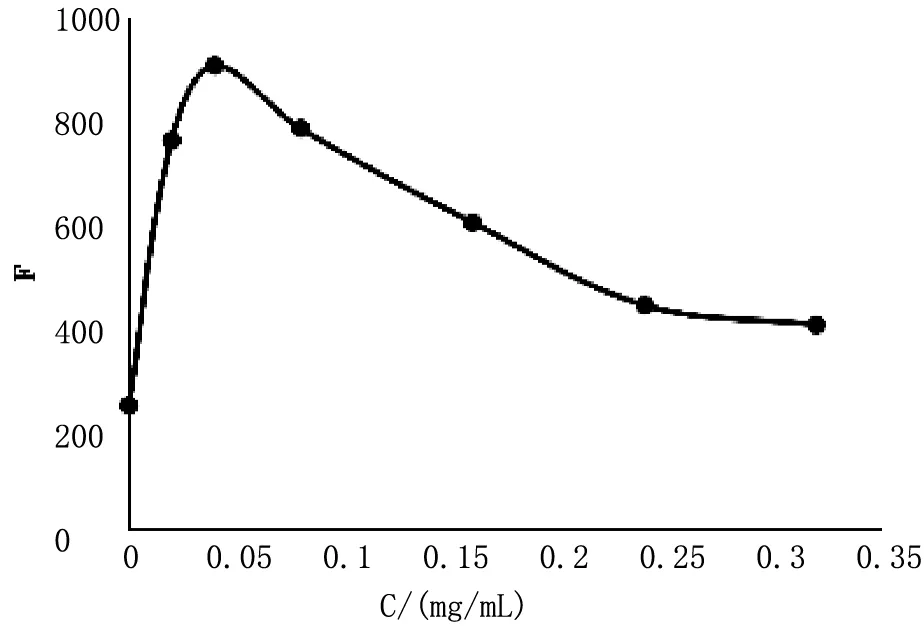
图4 Cu2+浓度对荧光强度的影响
Cu2+的用量对荧光强度的影响很大。维生素C极易被氧化,实验中探究了Cu2+浓度在0.00~0.32mg·mL-1范围内变化时对体系荧光强度的影响,结果如图4所示。由图可知,当c(Cu2+)<0.04mg·mL-1时,曲线呈上升趋势,说明氧化不完全,当c(Cu2+)=0.04mg·mL-1时,荧光强度达到最大,因此选择0.04mg·mL-1为Cu2+的最佳浓度。
2.5 邻苯二胺浓度的选择
邻苯二胺的浓度是实验中至关重要的一个条件,因此文中对邻苯二胺的浓度做了相应的优化,结果如图5所示。当邻苯二胺浓度≥0.06mg·mL-1时,体系的荧光强度趋于稳定,为了使反应完全,文中选择0.08mg·mL-1为最佳实验浓度。
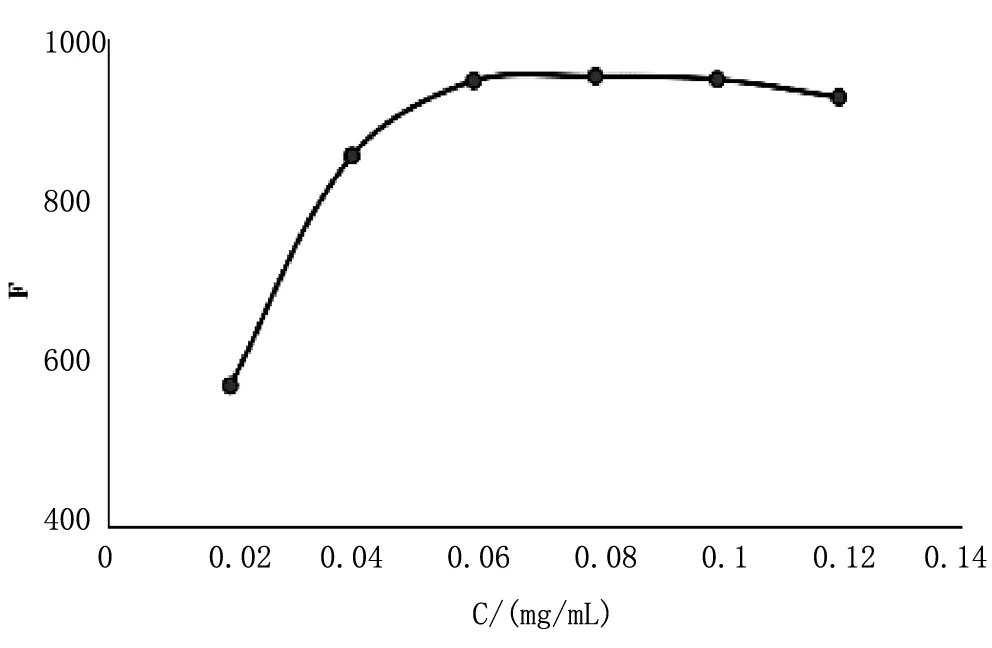
图5 邻苯二胺浓度对荧光强度的影响
2.6 氧化时间和反应时间的选择
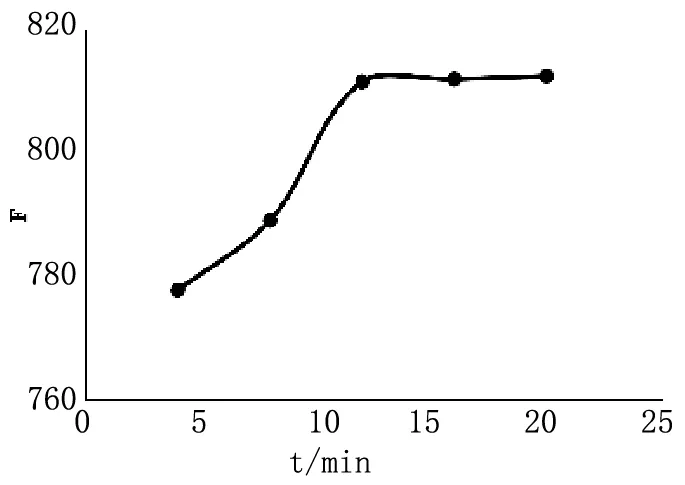
图6 氧化时间对荧光强度的影响
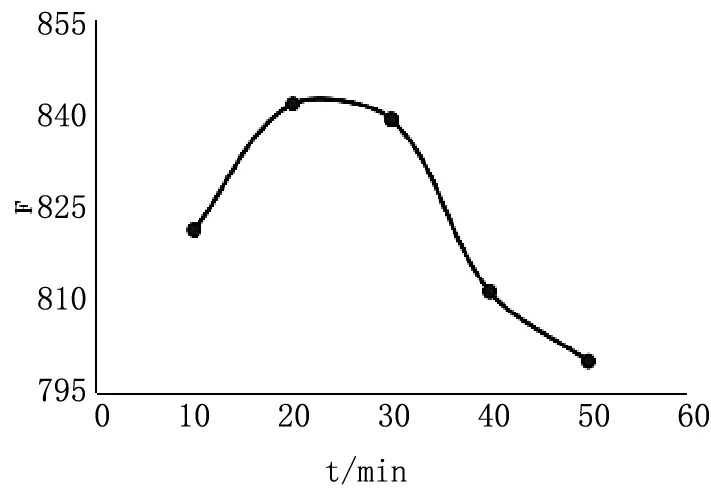
图7 反应时间对荧光强度的影响
室温下一般的氧化反应大多数都是慢反应。实验中分别测定了不同氧化时间下的荧光强度值。实验结果如下所示,从图中可以看出,当t≥10min时,氧化基本完成且趋于稳定,为了使氧化反应能够进行彻底,实验中选用15min作为最佳氧化时间。维生素C被Cu2+氧化后和邻苯二胺作用产生喹喔啉,实验中对反应不同时长后的荧光值进行了测定,结果如图7所示。随着反应时间的增长,荧光强度逐渐增大,在反应20~30min之间,曲线基本趋于平稳,30min以后荧光强度又逐渐减小。因此,本文选择25min作为最佳反应时间。
2.7 工作曲线的制备
图8为维生素C的浓度与相对荧光强度之间的关系曲线图。从图中可以看出,维生素C浓度在0.8~80μg·mL-1范围内与体系的相对荧光强度△F呈良好的线性关系,线性回归方程为△F=37.875c-8.4993,R2=0.9991。
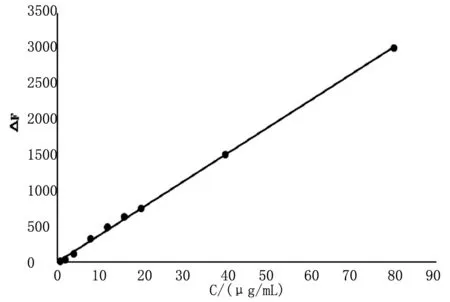
图8 工作曲线
2.8 样品的处理及测定
取30mL橙汁,加水稀释至50mL,加入2.5g活性炭粒,搅拌脱色,静置片刻后过滤,取滤液于50mL容量瓶中,加水定容至刻度线,即得样品工作液。将样品工作液放入冰箱内保存备用。
取10mL比色管,加入3.5mL上述样品工作液,按照实验方法平行测定11次样品溶液的荧光强度F和试剂空白溶液的荧光强度F0,取其平均值,测得相对荧光强度△F=661.7。
利用标准曲线法测得稀释后的样品溶液中维生素C的含量为17.0μg·mL-1,则原橙汁样品中维生素C的含量为135.5μg·mL-1。
3 结论
本文采用荧光法测定维生素C的含量,通过实验确定了反应所需的最佳条件,并测得橙汁中维生素C的含量为135.5μg·mL-1,该法有望于对各种果蔬中维生素C的含量进行测定。
[1] 傅 维,杨彩霞.荧光分光光度法测定几种天津市售水果中维生素C的含量[J].安徽农业科学,2011,39(23):14392-14393.
[2] 姚建华,黄亚励,席晓岚,等.荧光法测定部分果蔬中维生素C含量[J].贵阳医学院学报,1997,22(4):18-19.
[3] 王建国,汪敬武,易绣光.流动注射化学发光法测定饮料中维生素C的含量[J].江西农业学报,2009,21(5):99-101.
[4] 龚时琼,赵丽华,陈芳,等.荧光法快速检测水果和蔬菜中的抗坏血酸[J].实验室研究与探索,2012,31(10):19-21.
[5] 张 娜,康玉胜.荧光法测定片剂中抗坏血酸的含量[J].兰州文理学院学报(自然科学版),2014,28(1):5-7.
[6] 李 杨,冯 镇.呼伦贝尔地区不同乳粉中维生素C含量的分析[J].内蒙古科技与经济,2015,8(1):94-95.
[7] 刘国如,刘永锁,陈振玲,等.高效液相色谱法测定维生素C注射液含量[J].中国医药导报,2011,8(27):50-51.
[8] 徐美玲.2,4-二硝基苯肼法对三种蔬菜维生素C含量的测定[J].菏泽学院学报,2015,37(2):52-55.
[9] 杨玉萍.直接碘量法测定果蔬中维生素C含量实验教学[J].新乡学院学报(自然科学版),2012,29(5):471-472.
[10] 严 苹,罗月生,陈碧琼.碘量法测定橙子维生素C的含量[J].广州化工,2016,44(14):121-122.
[11] 李国树,文美琼,魏朔.云南五种野生蔬菜维生素C含量的测定及比较[J].楚雄师范学院学报,2009,24(3):57-63.
[12] 开启余.紫外分光光度法测定VC银翘片中维生素C含量[J].福建分析测试,2015,24(3):35-37.
[13] 陈玉锋,庄志萍.紫外分光光度法测定橙汁中维生素C的含量[J].安徽农业科学,2011,39(1):236-237.
(本文文献格式:何春晓.荧光法测定橙汁中维生素C的含量[J].山东化工,2017,46(16):82-84.)
Determination of Vitamin C in Orange Juice by Fluorescence Spectrophotometry
He Chunxiao
(College of Chemistry and Chemical Engineering, Longdong University, Qingyang 745000, Gansu)
A sensitive and rapid method was established based on Vitamin C was oxidized by Cu2+which can react with o-diaminobenzene to produce a fluorescent quinoxaline. In the essay, the concentration of buffer solution and pH, the amount of oxidant(Cu2+) and o-diaminobenzene, the oxidation time and reaction time were optimized. The results showed that under the optimal conditions, the vitamin C concentration in the range of 0.8~80μg·mL-1had a good linear relationship with △F, the linear regression equation was △F=37.875c-8.4993,R2=0.9991. Using this method, we measured the content of vitamin C in orange juice was 135.5μg·mL-1.
vitamin C; fluorescence spectrophotometry;orange juice
O657.34
:A
:1008-021X(2017)16-0082-03
2017-05-30
何春晓(1987—),女,甘肃庆阳人,讲师,硕士,主要从事分析化学的教学与研究。

