蔗糖水解速率常数测定实验教学内容的改进
周崇松,郭 纤,曾凡花,邓 斌
(湘南学院 化学生物与环境工程学院,湖南 郴州 423000)
蔗糖水解速率常数测定实验教学内容的改进
周崇松,郭 纤,曾凡花,邓 斌*
(湘南学院 化学生物与环境工程学院,湖南 郴州 423000)
旋光度法测定蔗糖水解速率常数是大学物理化学实验中最常见的实验项目之一。本文对该实验项目的教学内容进行了深入讨论,充分利用实验数据,获得了该反应的正、逆反应速率常数及反应平衡常数的计算,拓展了化学反应动力学相关的微观认识。
反应速率常数;平衡常数;蔗糖水解;可逆反应
旋光度法测定蔗糖水解速率常数的实验在大学物理化学实验中非常普遍,主要是因为该实验条件相对简单,实验可重复性较好,属于化学反应动力学方面的典型实验项目。开设该实验可强化学生有关反应级数确定、简单反应级数的速率方程、反应速率常数、反应半衰期等方面的知识。
分析多个高校开设该实验项目的情况可知,实验的数据处理都是直接采用ln(αt-α∞)~t作图,拟合成一直线,其斜率的负值被认为是该反应的速率常数。实际上,该反应使用了酸作为催化剂,并且有水参与了水解反应过程,属于二级反应[1],应当需要扣除水和催化剂的浓度项。此外,该反应还是一个非常典型的可逆反应。因而,还需要考虑该反应的正、逆反应的速率常数及平衡常数。在该实验教学过程中,可拓展更多微观反应动力学知识。
论文以常规的旋光度测定方法,按照可逆反应进行数据处理,分别得出正逆反应速率常数和反应平衡常数。
1 蔗糖水解速率常数测定实验方法
1.1 蔗糖水解过程中αt的测定
旋光仪预热,零点的校正,记录α水,并记录室温T0。
准确称取蔗糖10.0 g,溶于蒸馏水中,用50.0 mL容量瓶配制成溶液。取50.0 mL 4.0 mol·L-1HCl 溶液加到蔗糖溶液的锥形瓶中混合,并在HCI溶液加入一半时开始计时作为反应的起始时间。不断振荡摇动,迅速取少量混合液清洗旋光管二次,然后将此混合液注满旋光管,盖好玻璃片,旋紧套盖(检查是否漏液和有气泡)。擦净旋光管两端玻璃片,立刻置于旋光仪中。测量时间t时溶液的旋光度 t。测定时要迅速准确。先调节好旋光仪,并记下时间,再读取旋光度数值。测定第2、4、6、8、10、15、20、25、30、35、40、45min的旋光度。
1.2 α∞的测定
将步骤1.2中剩余的混合液密闭置于55℃水浴中温热45min,加速水解反应,然后冷却至室温,按上述操作测其旋光度,并间隔10min后再次测其旋光度,直到旋光度不再改变为止,记为 α∞。实验结束,并记录室温T∞。
2 数据处理原理
蔗糖水解反应的计量方程式为:(浓度单位为mol·L-1)
C12H22O11+ H2O ↔ C6H12O6(果糖) + C6H12O6(葡萄糖)
设:t=0时, cA,055.56 0 0
t=t 时, cA55.56 cA,0-cAcA,0-cA
t=t∞时, cA,e55.56 cA,0-cA,ecA,0-cA,e
蔗糖水解速率极慢,在酸性介质中反应速率大大加快,故H3O+为催化剂,其浓度反应前后不变。反应中,H2O是大量的,反应前后与溶质浓度相比,看成它的浓度不变,故蔗糖水解反应可看做一级反应。在不考虑蔗糖水解副反应情况下,采用旋光度法测定蔗糖水解速率常数的方程式[1-2]如下:

(1)
从该反应速率方程形式来看,具有1-1型的对峙反应特征,教学中采用ln(αt-α∞)~t作图也证实该反应符合1-1型对峙反应。因此本文按照1-1型对峙反应进行后续的数据处理,t=0、t、t∞时物质浓度关系如前文所示,设正逆反应速率常数分别为k1和k-1。

(2)
当t=t∞时,
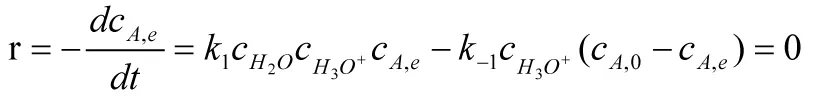
将(3)带入(2)整理得:

(4)
对(4)定积分得:

(5)
对比(5)和(1)式可知,通过(1)式作图拟合斜率求解的k应为:

(6)
此外,由(3)式子同时可知:

(7)
其中Kc是蔗糖水解反应的经验平衡常数,当旋光仪没有恒温热套时,该实验温度就是室温(取T0和T∞的平均温度),通常不是25℃,很难查到相关的数据。本文可采用推算法求解平衡时蔗糖的浓度cA,e,然后通过(7)式子计算出Kc,方法如下:
设在该实验温度条件下,旋光度与物质的比旋光度成正比,比例系数为K',利用旋光度具有加和性,则有:

当t=0时,cA=cA,0;再利用前面ln(αt-α∞)~t作图,用外推法求出t=0的旋光度α0,代入(8)式计算出比例系数K'。
当t=t∞时,cA=cA,e,利用α∞计算出cA,e,从而代入(7)式获得Kc。
最后联立(6)和(7)式求解出k1和k-1。

3 实例数据分析结果
3.1 实验结果

表1 蔗糖水解反应过程中旋光度及其数据处理结果
室温:24℃;α水=(+0.20+0.15+0.20+0.05+0.15)/5=+0.15;α∞,1=α∞,2=-4.00;使用盐酸浓度cH3O+=4.0 mol·L-1。校正后α∞=-4.15,cA,0=0.2924 mol·L-1,混合溶液盐酸实际浓度cH3O+=2.0 mol·L-1。其它αt结果见表1。
3.2 数据处理
将原始数据按照流程处理,得到的数据如表1所示,以ln(α-α∞)对t作图见图1。

图1 蔗糖水解反应ln(α-α∞)对t的函数图
根据拟合直线方程为ln(αt-α∞) = -0.03374 t + 2.93262,相关系数R2=0.9955,表明直线拟合很好。利用直线斜率求出:

又根据截距求α0,

将cA,0和α0的值代入(8)式,求出t=0时, K'=0.7513 L·mol-1。然后,将K'、cA,0和 α∞值代入(8)式,求出t= t∞时,cA,e=0.05724 mol·L-1,所以:
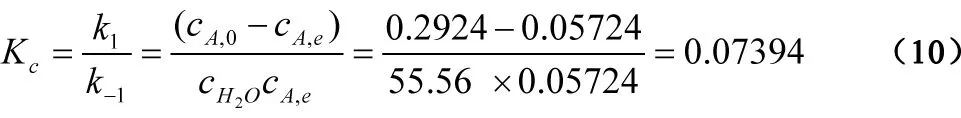
联立方程(9)和(10)式,解出k1=0.0002442 min-1,k-1=0.003303min-1。
4 结论
论文从常规的旋光度法测定蔗糖水解速率常数实验出发,充分利用数据处理的功能,对该反应的正逆反应速率常数及平衡常数进行了推算,拓宽了实验教学的内容,加强了典型复杂反应相关知识,并提高了对正逆反应速率常数与化学平衡的微观认识。
[1] 复旦大学.物理化学实验[M].3版.庄继华等修订.北京: 高等教育出版社,2012:98.
[2] 李强国,刘文奇,肖圣雄,等.基础化学实验[M].南京:南京大学出版社,2012:315.
(本文文献格式:周崇松,郭 纤,曾凡花,等.蔗糖水解速率常数测定实验教学内容的改进[J].山东化工,2017,46(15):148-149.)
The Improvement on Experimental Content About the Determination of Rate Constant of Sucrose Hydrolysis
ZhouChongsong,GuoXian,ZengFanhua,DengBin*
(College of Chemistry&Biology and Environmental Engineering,Xiangnan University, Chenzhou 423000,China)
To determine the rate constant of sucrose hydrolysis using rotation spectrophotometry is one of the most common experimental projects in university physical chemistry experiments.The experiment content has been developed through in-depth discussions about the experimental result. The positive and reverse reaction rate constant and the reactive equilibrium constant can be obtained by making full use of the experimental data. Some microscopic understanding relating chemical reaction kinetics has been excavated.
reaction rate constant;equilibrium constant;sucrose hydrolysis;reversible reaction
2017-05-18
湘南学院校级科研项目(编号2014XJ51)
周崇松(1978—),男,湖南郴州人,博士,主要从事理论与计算化学研究;通讯作者:邓 斌(1972—),男,教授,主要从事纳米材料科学研究。
G642.423
B
1008-021X(2017)15-0148-02

