芩黄清肺散的质量标准研究
刘俊丹,曾诗梅,雷金梅,陈文杰,李紫元,梁伟燊,唐陆平,何永明
(佛山科学技术学院兽医系,广东佛山 528000)
芩黄清肺散的质量标准研究
刘俊丹△,曾诗梅△,雷金梅,陈文杰,李紫元,梁伟燊,唐陆平*,何永明*
(佛山科学技术学院兽医系,广东佛山 528000)
为建立芩黄清肺散的质量标准,采用显微鉴定和薄层色谱法(TLC)对方剂中黄芩、大黄、枇杷叶和甘草进行定性鉴别。采用高效液相色谱法(HPLC)对黄芩苷进行含量测定,色谱柱为依利特C18柱(250 mm×4.6 mm,5 μm);流动相为甲醇-水-磷酸(47∶53∶0.2);流速1 mL/min;检测波长280 nm;柱温40℃;进样量20 μL。显微鉴定结果表明,韧皮纤维单个散在或数个成束,梭形,长60 μm~250 μm,壁厚,孔沟细(黄芩);草酸钙族晶,直径60 μm~ 140 μm(大黄);非腺毛为单细胞,常弯曲(枇杷叶);木纤维成束,周围薄壁细胞含草酸钙方晶,形成晶鞘纤维(甘草)。TLC结果表明,供试品中,在与对照品或对照药材色谱相应的位置上显示相同颜色的斑点,阴性对照无干扰。HPLC结果显示,黄芩苷在0.241 μg ~1.208 μg(r=0.999 9)具有良好的线性范围,精密度、稳定性、重复性的RSD<3.0%,加样回收率为100.49%(RSD=1.71%,n=9)。该研究所建立标准可用于芩黄清肺散的质量控制。
芩黄清肺散;显微鉴别;薄层色谱;高效液相色谱;黄芩苷;含量
芩黄清肺散是课题组自创的特色纯中药制剂,由黄芩、大黄、枇杷叶和甘草等4味中药组成,具有清肺热、止咳喘的功效[1],用于鸡传染性喉气管炎的治疗。为了控制药品质量,本试验采用显微鉴别和TLC法对方剂中的4味药材进行定性鉴别;用HPLC法对方剂中君药黄芩的主要成分黄芩苷含量进行定量检测,现将研究结果报告如下。
1 材料与方法
1.1 材料
1.1.1 仪器设备 1×71型倒置荧光显微镜,日本Olympus公司产品;DD70薄层扫描色谱仪,德国DESAGA公司;岛津LC-20 A型系列高效液相色谱仪(SPD-M20A紫外检测器,LABSOL DB CH MLCPOA色谱工作站);恒温水浴锅(H.H.S21.6),广州红云电器二厂生产;电热鼓风干燥箱(DHG-9075A),上海一恒科学仪器有限公司产品;超声波清洗机(HN1012),中国华南超声设备厂产品;点样毛细管,华西医科大学仪器厂产品;电子天平,赛多利斯科学仪器(BSA2245-CW),北京有限公司产品;100 mm×200 mm双槽玻璃层析缸(P-1),上海信谊仪器厂有限公司产品;薄层层析硅胶G和硅胶H板(201509012),青岛海洋化工有限公司产品。
1.1.2 药品与试剂 黄芩对照药材(批号:120955-201309);黄芩苷(批号:110715-201318);大黄对照药材(批号:121249-201304);大黄酸(批号:110757-200206);枇杷叶对照药材(批号:121261-201303);熊果酸(批号:110742-201421);甘草对照药材(批号:120904-201519),以上药品均购自中国食品药品检定研究院。芩黄清肺散,佛山科学技术学院兽医药理学实验室提供;各缺少上述药物之一的4种阴性对照样品,佛山科学技术学院兽医药理学实验室提供;磷酸、甲醇为色谱纯(Merk),乙醇、甲酸、冰醋酸、正己烷、甲苯、丙酮、乙酸乙酯、丁酮、硫酸、盐酸、氨水、三氯化铁、水合氯醛等均为分析纯,水为超纯水。
1.2 方法
1.2.1 显微鉴别 取过0.15 mm筛的样品适量,用水合氯醛(水合氯醛50 g,加水15 mL和甘油10 mL溶解)进行透化,根据各味中药的显微特征在显微镜下进行观察。
1.2.2 薄层色谱鉴别
1.2.2.1 黄芩的薄层色谱鉴别 参照文献[2]进行。取芩黄清肺散2 g,加甲醇50 mL,超声处理30 min,滤过,滤液浓缩至10 mL,滤过,取滤液作为供试品溶液。分别取缺黄芩的芩黄清肺散2 g和黄芩对照药材1 g,同法制成阴性对照品溶液和对照药材溶液。再取黄芩苷对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。按照薄层色谱法(通则0502)试验。分别吸取上述对照药材溶液、供试品溶液和阴性对照品溶液各3 μL以及黄芩苷对照品溶液2 μL,分别点在同一硅胶G薄层板上,以乙酸乙酯-丁酮-甲酸-水(5∶3∶1∶1)为展开剂,置展开缸中预饱和30 min,展开,取出,晾干,喷以20 g/L三氯化铁乙醇溶液。
1.2.2.2 大黄薄层色谱鉴别 取芩黄清肺散0.4 g,加20 mL甲醇,浸1 h后滤过,取10 mL蒸干,残渣加水10 mL,再加1 mL盐酸,水浴加热后加乙醚萃取2次,每次10 mL,合并乙醚液,蒸干,残渣加三氯甲烷1 mL使溶解,作为供试品溶液。分别取0.4 g缺大黄的芩黄清肺散和0.2 g大黄对照药材,同法制成阴性对照品溶液和对照药材溶液。再取大黄酸对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液[2-3]。按照薄层色谱法(通则0502)试验。吸取上述4种溶液各4 μL,分别点于同一硅胶H薄层板上,以正己烷-乙酸乙酯-甲酸(8∶3∶0.2)为展开剂,置展缸中预饱和30 min,展开,晾干,置紫外光灯(365 nm)下检视。
1.2.2.3 枇杷叶薄层色谱鉴别 参照文献[2]进行。取芩黄清肺散2 g,加甲醇20 mL,超声处理20 min,滤过,滤液蒸干,残渣加甲醇5 mL使溶解,作为供试品溶液。分别取缺枇杷叶的芩黄清肺散和枇杷叶对照药材2 g,同法制成阴性对照品溶液和对照药材溶液。再取熊果酸对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。按照薄层色谱法(通则0502)试验。吸取上述4种溶液各4 μL,分别点于同一硅胶G薄层板上,以甲苯-丙酮(5∶1)为展开剂,展开,晾干,喷以100 ml/L硫酸乙醇溶液,在105℃加热至斑点显色清晰。
1.2.2.4 甘草薄层色谱鉴别 取本品10 g,加700 mL/L乙醇50 mL,超声处理30 min,滤过,滤液加盐酸3 mL,摇匀,加热回流1 h,滤过,滤液蒸干,残渣加水20 mL分次溶解,用乙醚振摇提取3次,每次20 mL,合并乙醚提取液,再用水洗涤3次~5次,每次20 mL,弃去水液,乙醚液加氨水10 mL,萃取2次,收集氨水加盐酸10 mL后用乙醚萃取2次,每次10 mL,后水洗3次~4次,收集乙醚液,蒸干,加甲醇定容到2 mL,作为供试品溶液。同法制备甘草阴性对照溶液。取甘草对照药材粉末1 g,加700 mL/L乙醇20 mL,超声处理30 min,滤过,滤液加浓盐酸2 mL,摇匀,按供试品溶液制备方法制成对照药材溶液4 mL。按照薄层色谱法(通则0502)试验,吸取上述对照药材溶液、供试品溶液及阴性对照溶液各1 μL,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲酸(4∶1∶0.5)上层为展开剂[4],展开,取出,晾干,喷以100 mL/L硫酸乙醇溶液,在105℃加热至斑点显色清晰,分别置日光和紫外光灯(365 nm)下检视。
1.2.3 含量测定 参照文献[2,5-7]进行。
1.2.3.1 色谱条件 色谱柱:色谱柱为依利特C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水-磷(47∶53∶0.2);检测波长为280 nm;流速1 mL/min;柱温40℃;进样量20 μL;理论板数按黄芩苷峰计算应不低于2 500。
1.2.3.2 对照品溶液制备 黄芩苷对照品约3 mg,精密称定,于50 mL容量瓶中,加甲醇溶解并稀释至刻度。摇匀,超声处理至黄芩苷溶解,制成每1 mL含约60 μg左右的母液,即得。使用前用0.45 μm的滤膜过滤。
1.2.3.3 供试品溶液制备 取芩黄清肺散约0.6 g,精密称定,加700 mL/L乙醇40 mL,加热回流3 h,放冷,用滤纸过滤,滤液置100 mL容量瓶中,用少量700 mL/L乙醇分次洗涤,洗液滤入同一瓶中,加700 mL/L乙醇定容,摇匀。精密量取1 mL,置10 mL量瓶中,加甲醇至刻度,摇匀,用0.45 μm的微孔滤膜过滤到EP管中,备用。
1.2.3.4 阴性对照品溶液的制备 取自制的阴性对照品按1.2.3.3供试品的溶液制备方法制成阴性对照品溶液。
1.2.3.5 系统适应性试验 分别取上述对照品溶液、供试品溶液和阴性对照品溶液各20 μL,注入高效液相色谱仪,记录其色谱图。
1.2.3.6 线性范围考察 使用前精密吸取1.2.3.2中的母液2、4、6、8、10 mL,置于10 mL容量瓶中,用甲醇稀释至刻度,摇匀,得到黄芩苷的浓度分别为12、24、36、48、60 μg/mL。吸取20 μL,精密吸取同一份对照品溶液20 μL,在1.2.3.1条件下重复进样6次,测定峰面积,求出黄芩苷的RSD 。
1.2.3.7 精密度试验 精密吸取同一份对照品溶液20 μL,在1.2.3.1条件下重复进样6次,测定峰面积,求出黄芩苷的RSD。
1.2.3.8 稳定性试验 取同一批供试品溶液,按1.2.3.3方法制备,依上述色谱条件分别在0、4、8、12、24 h进样20 μL,记录色谱图,测定峰面积,求出RSD。
1.2.3.9 重复性试验 取同一供试品平行称取6份,每份约0.6 g,精密称取。分别按1.2.3.3的方法进行制样,按1.2.3.1方法测定,按外标法计算含量,求得黄芩苷含量的RSD值。
1.2.3.10 回收率试验 称取同一批已知含量的芩黄清肺散约0.15 g,精密称定,以当前样品含量的0.8、1.0、1.2倍,分别精密加入黄芩苷,按1.2.3.3的方法制备溶液,进样时每个提取液进样测定2次,根据公式计算回收率:回收率%=(C-A)/B,式中C为加入对照品后的测得值;A为样品中所含被测成分量;B为加入对照品量。
2 结果
2.1 显微鉴定结果
根据黄芩韧皮纤维单个散在或数个成束,梭形,长60 μm~250 μm,壁厚,孔沟细;大黄草酸钙族晶,直径60 μm~140 μm;枇杷叶单细胞非腺毛,常弯曲;甘草纤维成束,壁厚,周围薄壁细胞含草酸钙方晶,形成晶鞘纤维[8](图1)。
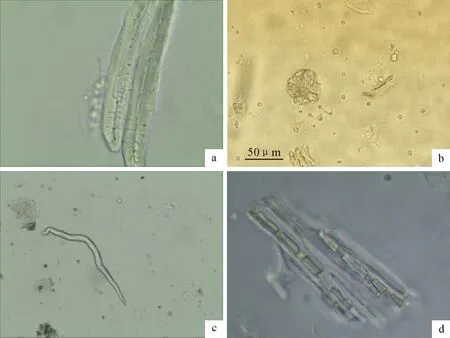
a.黄芩,韧皮纤维; b.大黄,草酸钙簇晶,直径60 μm~140 μm; c.枇杷叶,单细胞非腺毛;d.甘草,草酸钙方晶
a.RadixScutellariae,phoem fibers;b.RadixetRhizomaRhei,clusters of calcium oxalate,60 μm~140 μm in diameter;c.FoliumEriobotryae,non-gland hairs,unicellular;d.RadixetRhizomaglycyrrhizae,prisms of calcium oxalate
图1芩黄清肺散的显微鉴别结果
Fig.1 Microscopic identification results of Qinhuang qingfei powder
2.2 薄层色谱鉴别结果
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,且阴性对照无干扰(图2)。
2.3 HPLC检测结果
2.3.1 系统试验性 在1.2.3.1色谱条件下,理论塔板数黄芩苷峰为3 575(药典为不低于2 500),黄芩苷的分离度为1.8(药度典要求大于1.5),阴性对照在相应的位置无干扰峰(图3、图4和图5)。
2.3.2 线性考察 以对照品浓度作为横坐标(x),峰面积作纵坐标(y),得出线性回归方程:y=60 732x-267 829,r=0.999 9。结果表明,黄芩苷在0.241 μg ~1.208 μg范围内,具有很好的线性关系。
2.3.3 精密度、稳定性、重复性 精密度试验中黄芩苷的RSD为1.78%,稳定性试验的RSD为0.63%及重复性试验中黄芩苷含量的RSD值为0.99%,三者RSD值均小于3%,符合规定。
2.3.4 加样回收率 按1.2.3.1色谱条件测定,结果平均加样回收率为100.49%,RSD为1.71%(表1)。
3 讨论

a.黄芩;b.大黄;c.枇杷叶;1.标准品;2.对照药材;3~5.供试品;6.阴性对照;d.甘草:1 .对照药材;2~4.供试品;5.阴性对照
a.RadixScutellariae; b.RadixetRhizomaRhei; c.FoliumEriobotryae;1.Standard;2.Control herbs;3-5.Samples;6.Negative control;d.RadixetRhizomaglycyrrhizae; 1.Control herbs;2-4 Samples;5.Negative control
图2芩黄清肺散薄层色谱图
Fig.2 Thin-layer chromatography of Qinhuang Qingfei powder
对药材进行定性检查有显微鉴别和薄层色谱法,近年来高效薄层色谱发展迅速,具有低成本、高效、灵敏度和分辨率更高的特点,在甘草成分的检测上有应用[9-10]。本试验用一般薄层色谱法也能检测出方剂中的各类药材,方法简便、重复性强,可用于芩黄清肺散的质量标准控制。按照药典中各味药的显微特征进行黄芩、大黄、枇杷叶和甘草的显微鉴定,效果良好(图1)。按2015年版兽药典中黄芩和枇杷叶的薄层色谱法进行鉴别,黄芩、枇杷叶效果较好。大黄的TLC鉴别试验中,展开剂尝试了氯仿-乙酸乙酯(6∶1)[11]、石油醚-乙酸乙酯-甲酸(15∶5∶1)[12]、甲苯-乙酸乙酯-甲酸(15∶2∶1)[13]。此外,
还用二次展开方式,第1次用石油醚-乙酸乙酯-冰醋酸(9∶2∶0.5)展开,展距9 cm后再以氯仿-甲醇-冰醋酸(8∶2∶0.2)[14]为展开剂,结果都不理想,对照品仍在原点。最后以正己烷-乙酸乙酯-甲酸(8∶3∶0.2)为展开剂[15],用硅胶H板进行试验结果良好。
甘草用正丁醇-冰醋酸-水(6∶1∶2)为展开剂,GF254板进行试验[16],效果不好。改用兽药典方法,用乙酸乙酯-甲酸-冰醋酸-水(15∶1∶1∶2)展开后在日光下观察结果,斑点分离度不高,无法判断结果,而在365 nm时阴性对照有干扰。此外,按照新近发布的桑仁清肺口服液的方法进行试验,用GF254板,以乙酸乙酯-甲酸-冰醋酸-水(15∶1∶1∶2)为展开剂,展开结果与三氯甲烷-水-甲醇(13∶6∶2)、正丁醇-水-冰醋酸(8∶2∶1)类似[17-18],即阴性和供试品相应的位置有相应的斑点。
因此,根据方剂中甘草含量太低,而其他杂质有干扰,结合组方的特征和甘草的性质尝试用盐酸加热回流后先用乙醚得到低极性的物质,除去色素,再让氨水与甘草次酸和其他成分结合,后加盐酸得到甘草次酸,然后再用乙醚萃取得到更纯的甘草次酸和甘草其他成分。结果显示与对照药材相比,供试品相应的位置出现斑点,阴性对照无干扰。方法独特,分离度好。
芩黄清肺散中黄芩为君药,黄芩总黄酮具有较好的降血脂作用[19],而黄芩苷是黄芩中的一种黄酮,其为抗炎的主要药效物质,且在方中所占比例大,含量高,以其作为含量测定的指标成分,可以准确的反映本方剂的质量,因此,选择黄芩苷作为定量分析的成分[20]。但是试验没有对成品进行不同批次的检测,因此不能制定该方剂的质量标准方法。芩黄清肺散用加热回流下的方法提取,分离度好,方法简便准确,重复性好,可有效的控制本品质量。
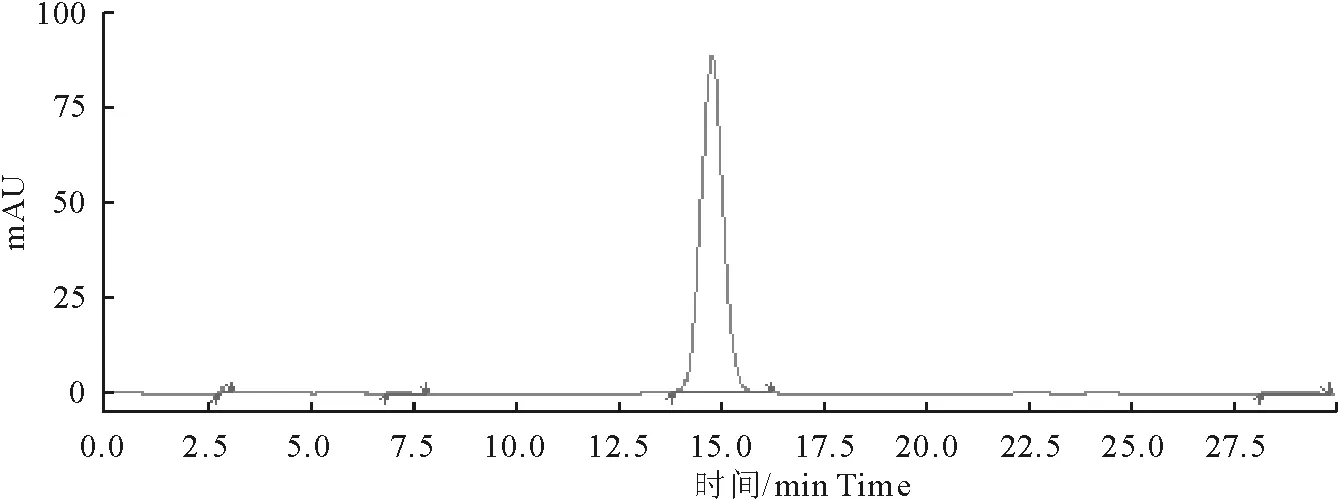
图3 黄芩苷标准品HPLC色谱图
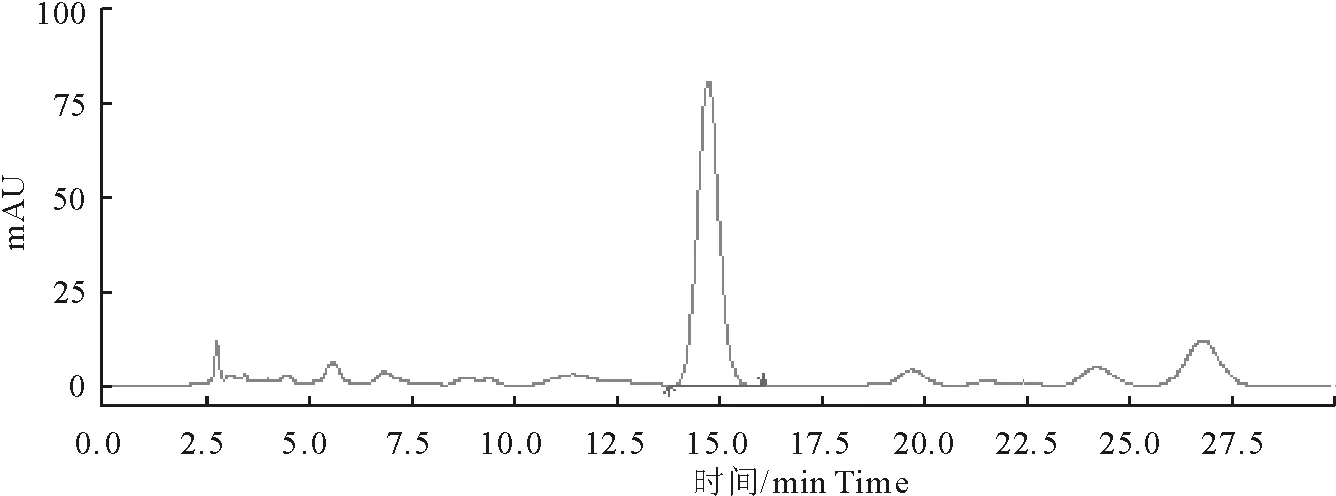
图4 芩黄清肺散HPLC色谱图
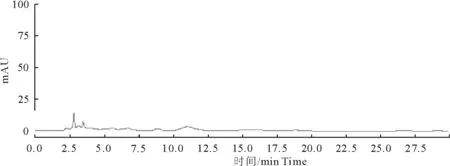
图5 黄芩的阴性对照品HPLC色谱图

表1 回收率测试结果
致谢:特别感谢广州中医药大学博士生导师张军教授在甘草薄层鉴别中给予我们的指导和支持!
[1] 何永明,张浩吉,杨 鸿,等.“黄芩、大黄”合剂对人工诱发传染性喉气管炎患鸡血液SOD、MDA水平的影响[J].中国家禽,2003,25(17):9-11.
[2] 中国兽药典委员会.中华人民共和国兽药典:二部[S].北京:中国农业出版社,2015:444-445,31,293.
[3] Tian Y G,Qin S M,Ding L.Thin layer chromatography identification for rhubarb and phellodendri amurensis cortex in shuang-bai cataplasm and study of skin irritation assay[J].J Biol Regul Homeost Agent,2015,29(2):479-484.
[4] 尚晓娜,宋平顺,杨 锡,等.HPLC梯度波长法同时测定甘肃省不同产地甘草中6种成分含量及主成分分析研究[J].中国现代中药,2012,14(9):27-31.
[5] 白凤芝,孙 录,刘玉梅,等.高效液相色谱法测定银花泌炎灵片中野黄芩苷含量[J].中国药业,2016,25(3):45-46.
[6] 李灵娟,付文力,李登云,等.清瘟解毒口服液黄芩苷的HPLC法测定[J].黑龙江畜牧兽医,2016(23):270-273.
[7] Li B Q,Chen J,Li J J,et al.High‐performance liquid chromatography with photodiode array detection and chemometrics method for the analysis of multiple components in the traditional Chinese medicine Shuanghuanglian oral liquid[J].J Separa Sci,2015,38(24):4187-4195.
[8] 中华人民共和国药典.中药材显微鉴别彩色图鉴[S].北京:人民卫生出版社,2009.
[9] Alam P,Alajmi M F,Siddiqui N A,et al.Determination of bioactive marker glycyrrhizin inGlycyrrhizaglabraroot and commercial formulation by validated HPTLC-densitometric method[J].海岸生命医学杂志:英文版,2014,2(11):882-887.
[10] Liu X,Li Q,Lv C,et al.Combination of the advantages of chromatographic methods based on active components for the quality evaluation of licorice[J].J Separa Sci,2015,38(24):4180-4186.
[11] 胡红艳,李 艳,黄秋明.复方茵陈合剂中栀子和大黄的薄层色谱鉴别[J].中国药业,2010,19(17):26.
[12] 岑艳华,蔡丽云,陈 华.活血祛瘀片中三七、大黄的薄层色谱鉴别[J].临床医学工程,2011,18(6):915-916.
[13] 陈勇军,黄云祥,王杏娥.茵黄利胆颗粒中大黄、茵陈的薄层色谱鉴别[J].中医学报,2014(11):1635-1636.
[14] 叶 强,余葱葱.大黄全成分薄层色谱条件研究[J].亚太传统医药,2013,9(3):15-16.
[15] 张 洁.全蝎散中大黄、冰片的薄层色谱鉴别研究[J].亚太传统医药,2013,9(1):30-31.
[16] 赖克道,刘 元,文志云,等.薄层色谱法定性鉴别小柴胡颗粒中的柴胡、甘草[J].广西医学,2009,31(6):886-887.
[17] 许红辉,李晓燕,张永锋,等.连花清瘟胶囊质量标准研究[J].中国药业,2013,22(18):60-62.
[18] 祁 红,刘传统.胆炎颗粒质量标准的建立[J].中国药师,2013,16(3):462-464.
[19] 雷燕妮.黄芩总黄酮对高血脂大鼠的降血脂作用研究[J].动物医学进展,2014,35(7):64-68.
[20] 王厚伟,高德民,田景振.高效液相色谱法测定复方黄芩消炎片中黄芩苷的含量[J].中国实验方剂学杂志,2007,13(4):13-15.
StudyonQualityStandardofQinhuangQingfeiPowder
LIU Jun-dan,ZENG Shi-mei,LEI Jin-mei,CHEN Wen-jie,LI Zi-yuan,LIANG Wei-shen,TANG Lu-ping,HE Yong-ming
(DepartmentofVeterinaryMedicine,FoshanUniversity,Foshan,Guangdong,528000,China)
The objective was to establish the quality standard of Qinhuang Qingfei powder.The qualitative identification ofRadixScutellariae,RadixetRhizomaRhei,FoliumEriobotryaeandRadixetRhizomaglycyrrhizaewas conducted by microscopic identification and thin layer chromatography (TLC) in the prescription.The content of baicalin in the prescription was determined by high performance liquid chromatography (HPLC):the column was elite C18 column (250 mm×4.6 mm,5 μm) with the mobile phase of methanol-water-phosphoric acid (47∶53∶0.2) at a flow rate of 1 mL/min;the detection wavelength was 280 nm;column temperature was 40℃;and the injection volume was 20 μL.The results of microscopic identification were showed below.Phoem fibers scattered singly or in bundles,fusiform,60 μm-250 μm long,thick-walled,with fine pit-canals (RadixScutellariae).Clusters of calcium oxalate,60 μm-140 μm in diameter (RadixetRhizomaRhei).Non-gland hairs,large,unicellular and curved (FoliumEriobotryae).Xylem fibers in bundles,which were surrounded by parenchymatous cells containing prisms of calcium oxalate and formed crystal sheath-fibres (RadixetRhizomaglycyrrhizae).TLC results showed that there were the same color spots on the chromatography corresponding positions between test samples and reference substance or reference drug,and no interference in negatiive control.The linear range of the carlibation was 0.241 μg-1.208 μg (r=0.999 9).The RSDs of precision,stability and reproducibility tests were lower than 3.0%.The recovery rate was 100.49%(RSD=1.71%,n=9).The established standard can be used for the quality control of Qinhuang Qingfei powder.
Qinhuang Qingfei powder;microscopic identification; TLC; HPLC; baicalin;content
2017-02-08
十二五农村领域国家科技计划项目(2011BAD34B00);农业部行业科技专项项目(201003060-09);广东省省级科技计划项目(2015A040404048);佛山市科技计划项目(佛财工〔2015〕 143 );广东省教育厅高校科研项目(2016KTSCX149);广东大学生科技创新培育专项资金立项项目;佛山科学技术学院研究生自由探索基金项目
刘俊丹(1991-),女,广西玉林人,硕士研究生,主要从事中兽药研制和开发工作。△同等贡献作者。 *
S853.75
:A
:1007-5038(2017)09-0061-06

