用氢氧化钠从银渣中浸出硒碲试验研究
熊庆丰,范兴祥,余宇楠,刘 琼,刘振楠,姚春玲
(1.贵研铂业股份有限公司,云南 昆明 650106;2.昆明冶金高等专科学校 冶金材料学院,云南 昆明 650033;3.全国再生金属行业稀散及贵金属二次资源循环利用重点实验室,云南 昆明 650033)
用氢氧化钠从银渣中浸出硒碲试验研究
熊庆丰1,范兴祥2,3,余宇楠2,3,刘 琼1,刘振楠2,3,姚春玲2,3
(1.贵研铂业股份有限公司,云南 昆明 650106;2.昆明冶金高等专科学校 冶金材料学院,云南 昆明 650033;3.全国再生金属行业稀散及贵金属二次资源循环利用重点实验室,云南 昆明 650033)
银渣主要含银、硒及少量铁、铜、铋、锑、碲、铅等,硒以亚硒酸银形式存在。研究了用氢氧化钠从银渣中选择性浸出硒、碲,考察了浸出时间、反应温度、液固体积质量比、氢氧化钠浓度对硒、碲浸出率的影响。试验结果表明:氢氧化钠浓度和液固体积质量比对硒、碲浸出率影响较大,硒和部分碲被浸出,其他元素如银、铜、铁等及部分碲留在渣中,浸出过程具有选择性;在反应温度95 ℃、液固体积质量比4∶1、氢氧化钠初始质量浓度200 g/L、搅拌速度250 r/min条件下浸出4 h,硒、碲浸出率分别为97.22%和36.75%。此外,也研究了用硝酸浸出碱浸渣中的银。浸出渣衍射分析结果表明,渣中残留的硒主要以亚硒酸钠形式存在,需要用氢氧化钠再次浸出。
银渣;碱;浸出;硒;碲
硒为稀散金属,自然界中有工业开采价值的单独矿床很少[1]。硒是一种重要的半导体材料,主要用于电子、医药领域,如半导体器件、光电及热电器件、硒太阳能电池、激光器件、激光和红外光导材料等[2]。硒资源短缺,特别是中国硒用量越来越大,供不应求。目前,硒主要从有色金属电解阳极泥、制酸厂酸泥和造纸厂污泥等物料中综合提取[3]。提硒方法主要有真空蒸馏法[4]、氧压酸浸法[5]、亚硫酸钠直接浸出法[6-7]、加钙固硒法[8]、离子交换法[9]、扩散渗析法[10]、氧化焙烧法[11]、二氧化硫还原法[12-13]等。在强化浸出方面,用双氧水作氧化剂在硫酸体系中强化微波浸出,硒浸出率达99%[14]。针对含硒碲银渣,在对比上述方法的优缺点基础上,研究了采用环境友好、操作简单、成本更低的氢氧化钠直接浸出硒和碲。
1 试验部分
1.1 试验原料
试验所用银渣取自国内某贵金属冶炼厂,粒度-74 μm占85%,化学分析结果见表1,XRD衍射分析结果见图1。
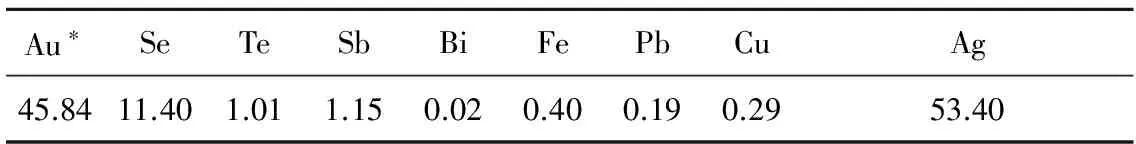
表1 银渣的主要成分 %
*.单位为g/t。

图1 银渣的XRD图谱
由图1看出:物料中的硒主要以亚硒酸银(Ag2SeO3)形式存在,该物质相当稳定,溶度积为1.0×10-15;碲主要以亚碲酸(H2TeO3)形式存在。
1.2 试验原理与方法
银渣中的硒和碲用氢氧化钠浸出时的反应为:
Ag2O↓+H2O;
(1)

(2)

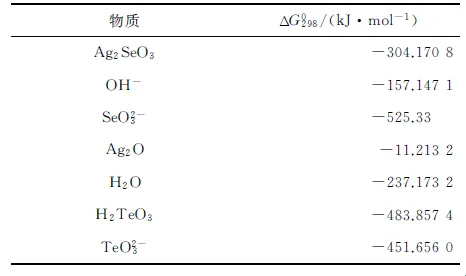
表2 相关热力学数据
试验方法:按要求加入配制好的氢氧化钠溶液于反应器中,开启搅拌,待温度升到预定值后,加入一定量银渣,在不同反应时间、温度、液固体积质量比、氢氧化钠浓度等条件下进行试验。反应结束后过滤、洗涤,得到浸出液和浸出渣,分别测定其中硒、碲含量,计算硒、碲浸出率。
2 试验结果与讨论
2.1 反应温度对硒、碲浸出率的影响
称取100 g银渣,在浸出时间4 h、液固体积质量比4∶1、氢氧化钠初始质量浓度250 g/L、搅拌速度250 r/min条件下,反应温度对硒、碲浸出率的影响试验结果如图2所示。可以看出,硒、碲浸出率随温度升高而提高:反应温度升到95 ℃时,硒、碲浸出率分别达97.22%和36.75%;反应温度超过95 ℃后,硒、碲浸出率升高幅度较小。浸出需在密闭反应釜中进行,对设备耐温耐压的要求更严格。综合考虑,确定适宜的反应温度为95 ℃。

图2 反应温度对硒、碲浸出率的影响
2.2 浸出时间对硒、碲浸出率的影响
称取100 g银渣,在反应温度95 ℃、液固体积质量比4∶1、氢氧化钠初始质量浓度250 g/L、搅拌速度250 r/min条件下,浸出时间对硒、碲浸出率的影响试验结果如图3所示。
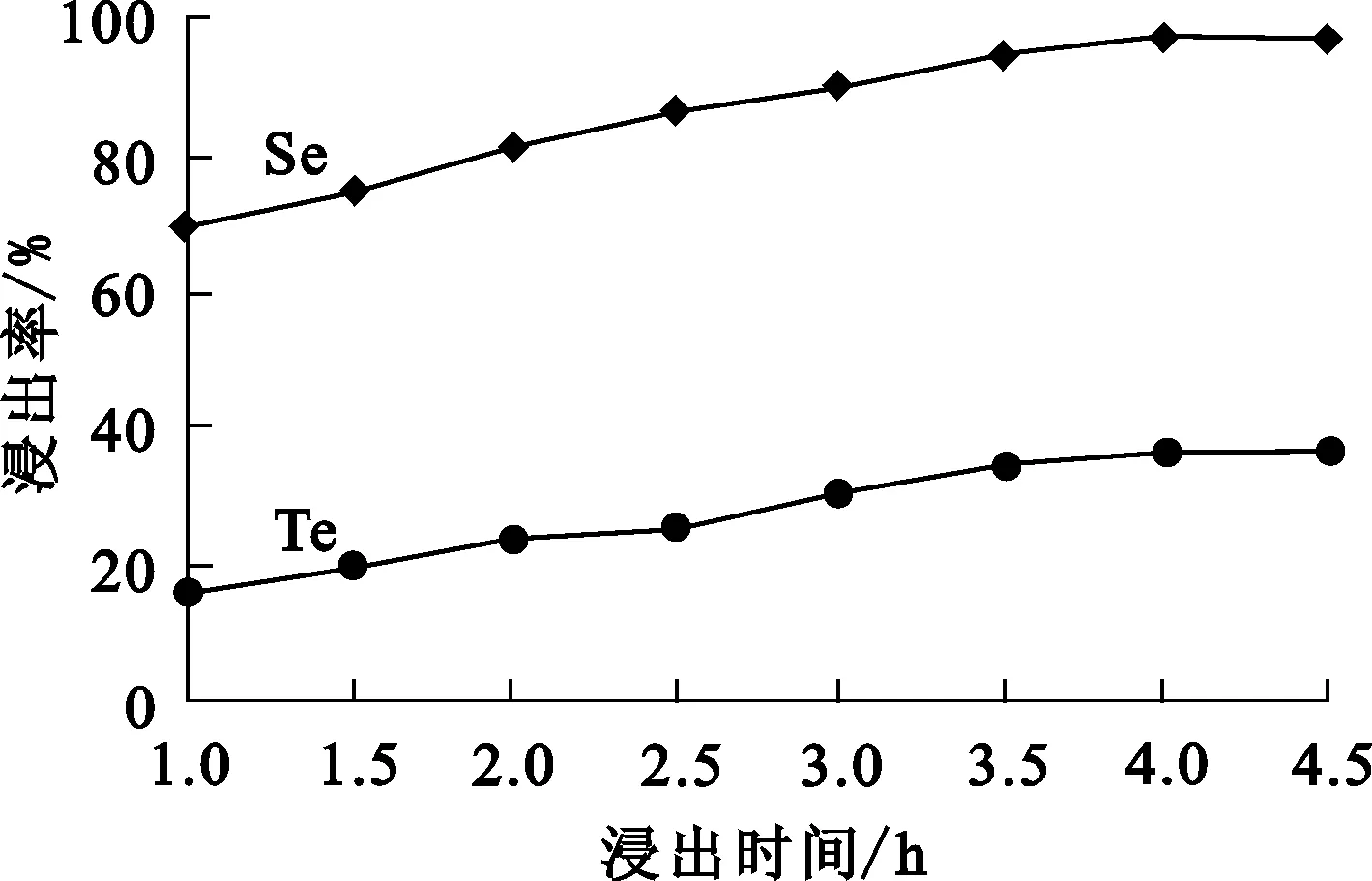
图3 浸出时间对硒、碲浸出率的影响
由图3看出:浸出时间在1~4 h范围内,硒、碲浸出率随浸出时间延长而升高;浸出时间超过4 h后,硒、碲浸出率变化不大。浸出时间过长不仅增大能耗,同时也降低生产效率,因此,确定适宜的浸出时间为4 h。
2.3 氢氧化钠初始质量浓度对硒、碲浸出率的影响
称取100 g银渣,在浸出时间4 h、反应温度95 ℃、液固体积质量比4∶1、搅拌速度250 r/min条件下,氢氧化钠初始质量浓度对硒、碲浸出率的影响试验结果如图4所示。
银渣中的硒主要以亚硒酸银形式存在,氢氧化钠主要与亚硒酸银反应,根据反应式(1)可计算出所需氢氧化钠理论量为19.78 g。由图4看出:硒、碲浸出率随氢氧化钠浓度增大而提高,且反应速度加快;当氢氧化钠质量浓度为50 g/L时,体系中氢氧化钠质量为20 g,与理论所需氢氧化钠较为接近,此时硒、碲浸出率分别为69.11%和4.26%;氢氧化钠质量浓度提高到100 g/L,体系中氢氧化钠质量为理论量的2倍,硒、碲浸出率分别为85.98%和25.19%,硒、碲浸出率提高明显;氢氧化钠质量浓度超过200 g/L后,硒、碲浸出率变化不大。综合考虑,确定适宜的氢氧化钠初始质量浓度为200 g/L,此时体系中氢氧化钠质量为理论量的4倍。

图4 氢氧化钠初始质量浓度对硒、碲浸出率的影响
2.4 液固体积质量比对硒、碲浸出率的影响
称取100 g银渣,在浸出时间4 h、反应温度95 ℃、氢氧化钠初始质量浓度200 g/L、搅拌速度250 r/min条件下,液固体积质量比对硒、碲浸出率的影响试验结果如图5所示。
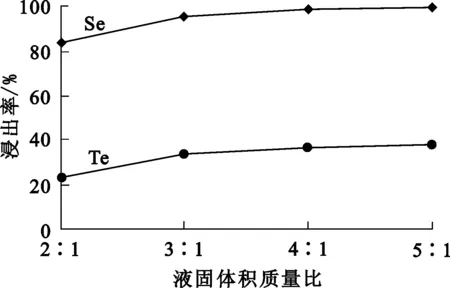
图5 液固体积质量比对硒、碲浸出率的影响
由图5看出,硒、碲浸出率随液固体积质量比增大逐渐提高:液固体积质量比较小时,浸出体系黏度较大,浸出剂扩散速度慢;随液固体积质量比增大,体系黏度逐渐降低,硒、碲浸出反应速度加快,浸出率提高明显;液固体积质量比为5∶1时,硒、碲浸出率较高,但碱耗较大、浸出液体积较大,对后续酸化提取硒、碲不利。所以,综合考虑,确定适宜的液固体积质量比为3∶1。
3 综合试验
在上述单因素试验结果基础上,进行了5 kg规模的加压浸出综合试验。反应釜体积50 L,浸出时间4 h,反应温度95 ℃,液固体积质量比4∶1,氢氧化钠初始质量浓度200 g/L,搅拌速度250 r/min,敞开体系。试验结果表明,硒、碲浸出率分别为98.01%和37.01%,与条件试验指标基本吻合;银及铜、铁等留在浸出渣中,渣产率为57.97%。浸出渣分析结果见表3,可以看出,锑、铅等有部分浸出。

表3 浸出渣分析结果 %
*.单位为g/t。
对碱浸渣用稀硝酸浸出银,控制液固体积质量比4∶1,硝酸体积分数55%,浸出时间4 h,搅拌速度250 r/min。此条件下,银浸出率为97.46%,渣率为3.81%,渣中硒、碲、银、金分别为24.52%、1.28%、62.74%和2 283.5 g/t。酸浸渣的XRD衍射分析结果(图6)表明,其中仍含有少量亚硒酸银。要提高硒、碲浸出率,还需用氢氧化钠再次浸出酸浸渣。金可在提银后用王水直接浸出。
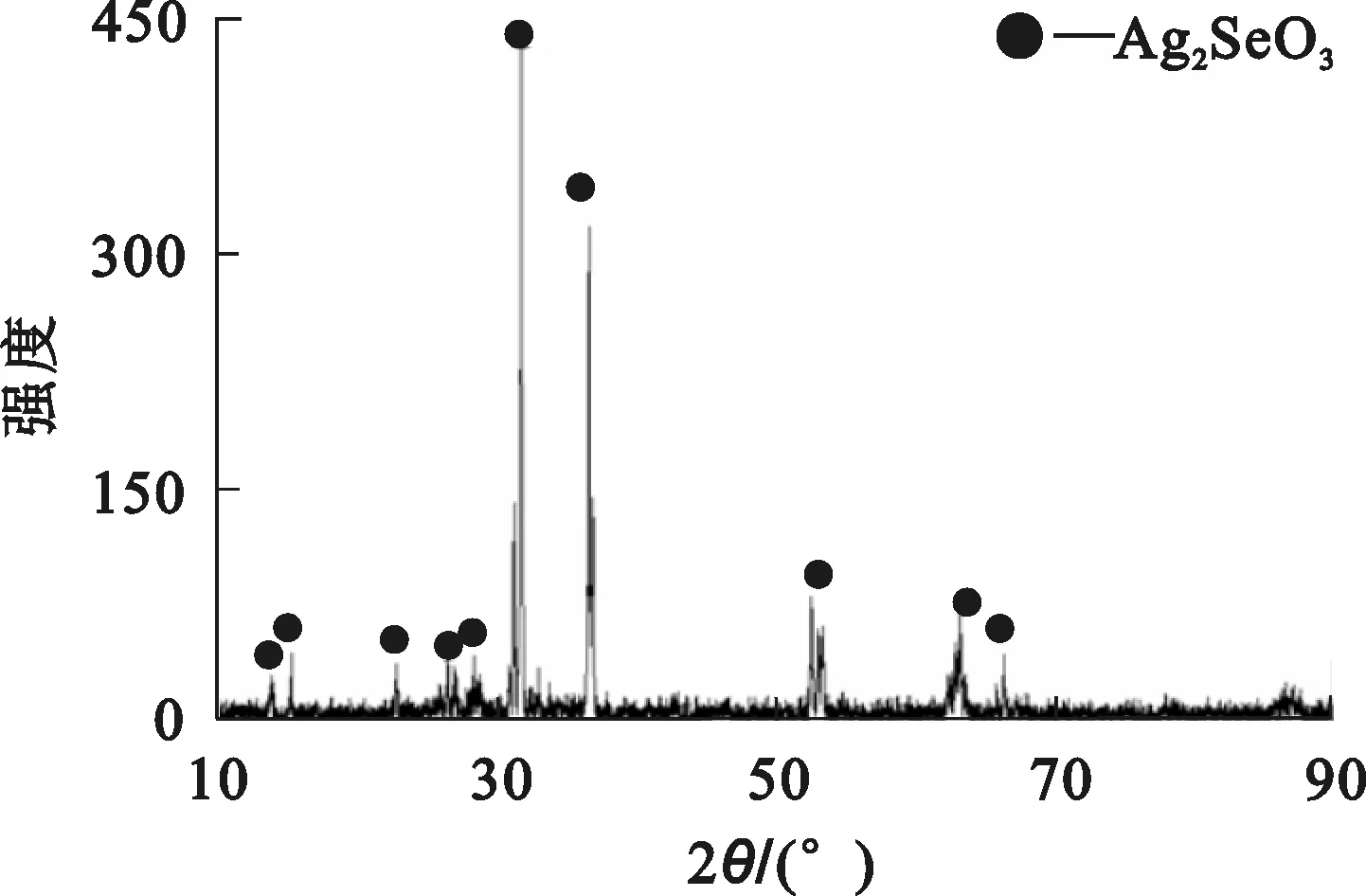
图6 酸浸渣的XRD图谱
4 结论
用氢氧化钠直接浸出银渣中的硒、碲是可行的。在浸出时间4 h、反应温度95 ℃、液固体积质量比4∶1、氢氧化钠初始质量浓度200 g/L、搅拌速度250 r/min适宜条件下,硒、碲浸出率分别为98.01%和37.01%。氢氧化钠对硒的选择性较好,银进入浸出渣中。碱浸渣中的银用硝酸浸出,银浸出率可达97%。酸浸渣中仍存在少量以亚硒酸银形式存在的硒,需用氢氧化钠再次浸出。
方法选择性好,操作简单,硒浸出率较高,且浸出液中主要含硒及少量碲,较为纯净,可进一步分离硒、碲。
[1] 李倩,张宝,申文前,等.硒酸泥制备粗硒新工艺[J].中南大学学报(自然科学版),2011,42(8):2209-2214.
[2] 高远,吴昊,王继民.高纯硒的制备方法[J].稀有金属,2009,33(2):276-278.
[3] 彭国敏,张玉明,张福元,等.高铅含硒物料湿法处理回收硒的工艺研究[J].稀有金属,2015,39(10):928-933.
[4] 赖建林.从真空炼硒炉渣中回收硒[J].稀有金属,1998,22(4):270-273.
[5] 蔡创开,庄荣传,林鸿汉.从铜阳极泥中氧压浸出有价金属试验研究[J].湿法冶金,2015,34(5):376-379.
[6] 和晓才,谢刚,李怀仁,等.高铅、高银酸泥中亚硫酸钠浸硒的工艺研究[J].稀有金属,2012,36(2):454-455.
[7] 张佳峰,张宝,郭学益,等.Na2SO3浸出法提纯粗硒工艺研究[J].稀有金属材料与工程,2011,40(1):121-125.
[8] 王晓武,范兴祥,李永祥.从含硒酸泥中提取硒的试验研究[J].湿法冶金,2013,32(5):316-318.
[9] 卫芝贤,杨文斌,王靖芳.离子交换法从铜阳极泥中提取纯硒[J].稀有金属,1989,13(4):300-303.
[10] 侯晓川,杨润德,李贺.扩散渗析法从镍钼矿冶炼烟尘提硒废液中分离酸的研究[J].稀有金属与硬质合金,2014,42(3):15-18.
[11] 孙永泉.低温焙烧硒锑矿脱硒的研究[J].稀有金属与硬质合金,1993(增刊1):271-273.
[12] 郑雅杰,陈昆昆,孙召明.SO2还原沉金后液回收硒碲及捕集铂钯[J].中国有色金属学报,2011,21(9):2258-2263.
[13] 张福元,郑雅杰,孙召明,等.采用亚硫酸钠还原法从沉金后液中回收稀贵金属[J].中国有色金属学报,2015,25(8):2293-2298.
[14] 马致远,杨洪英.响应曲面法优化铜阳极泥微波浸出硒工艺[J].中南大学学报(自然科学版),2015,46(7):2391-2395.
[15] WEAST R C.CRC Handbook of chemistry and physics[M].Florida:CRC Press INC,1989.
[16] 肖峰.铅冰铜碱性高压浸出液富集硒的工艺研究[D].长沙:中南大学,2011.
Leaching of Selenium and Tellurium From Silver Residue Using Sodium Hydroxide
XIONG Qingfeng1,FAN Xingxiang2,3,YU Yu’nan2,3,LIU Qiong1,LIU Zhennan2,3,YAO Chunling2,3
(1.Sino-platinumMetalsCo.,Ltd.,Kunming650106,China;2.Metallurgy&MaterialEngineeringFaculty,KunmingMetallurgyCollege,Kunming650033,China; 3.TheNationalRenewableMetalIndustryKeyLaboratoryofRecyclingRareandPreciousMetalsSecondaryResources,Kunming650033,China)
The silver residue contains silver,selenium,tellurium and a small amount of iron,copper,bismuth,antimony and lead.Selenium in the slag exists in the form of silver selenite.The selective leaching of selenium and tellurium from the silver residue using sodium hydroxide was researched.The effects of leaching time,temperature,liquid-to-solid ratio and sodium hydroxide concentrate on leaching of selenium and tellurium were examined.The results show that sodium hydroxide concentration and liquid-to-solid ratio have significant influence on leaching of selenium and tellurium.Other elements such as silver,copper,iron and part of tellurium are remained in the leaching slag.The leaching process can selective leach for selenium and tellurium.Under the conditions of leaching time of 4 h,leaching temperature of 95 ℃,liquid-to-solid ratio of 4∶1,concentration of sodium hydroxide of 200 g/L and stirring speed of 250 r/min,the leaching rate of selenium and tellurium are 97.22% and 36.75%,respectively.The silver in the leaching slag of sodium hydroxide is leached using nitric acid solution.A small amount of selenium in the acidic leaching residue mainly exists in the form of sodium selenite which still needs leaching again using sodium hydroxide.
silver slag;sodium hydroxide;leaching;selenium;tellurium
2017-01-12
昆明冶金高等专科学校引进人才科研经费资助项目(2015RC001)。
熊庆丰(1974-),男,湖南汨罗人,本科,高级工程师,主要研究方向为贵金属电子浆料。
范兴祥(1974-),男,云南建水人,博士,研究员,主要研究方向为有色冶金。E-mail:fanxingxiang@tom.com。
TF803.21;TF843.5
A
1009-2617(2017)04-0281-04
10.13355/j.cnki.sfyj.2017.04.007

