乳腺癌MCF⁃7细胞p21WAF1/CIP1启动子区雌激素受体α的高功能结合位点
邹丹,冯秀艳,周伟强
(沈阳医学院 1.病理生理学教研室;2.辽宁省环境污染与微生态重点实验室,沈阳 110034)
乳腺癌MCF⁃7细胞p21WAF1/CIP1启动子区雌激素受体α的高功能结合位点
邹丹1,冯秀艳2,周伟强2
(沈阳医学院 1.病理生理学教研室;2.辽宁省环境污染与微生态重点实验室,沈阳 110034)
目的研究雌激素受体(ER)α募集于p21WAF1/CIP1启动子区调控其转录活性的具体作用位点,明确辛二酰苯胺异羟肟酸(SAHA)及瘦素(leptin)在调节p21WAF1/CIP1启动子功能中的分子机制。方法将处于对数生长期的乳腺癌MCF-7细胞在无血清培养基中饥饿24 h后,分别用20 μmol/L的SAHA 0.88 μL(SAHA组)、0.625 nmol/L的leptin 10 μL(leptin组)处理24 h,对照组在完全型RPMI-1640培养基中培养细胞。应用染色质免疫共沉淀技术将各组细胞裂解液与ERα抗体孵育,收集纯化结合ERα抗体的DNA片段,应用实时PCR法检测p21WAF1/CIP1启动子区从转录起始点到其上游(+2~-4 000 bp)f1~f10片段的DNA相对表达量并用2-ΔΔCt法分析。结果对照组中,与ERα抗体结合的f1、f2、f8片段DNA相对表达量较f9片段高出2倍以上(P<0.01)。与对照组比较,SAHA及leptin组f1~f10片段与ERα抗体结合能力均降低,其中SAHA组f8片段DNA相对表达量达最低值(P<0.01),且明显低于leptin组(P<0.01)。SAHA组中以f8片段为对照,其他片段与ERα抗体结合能力均较其升高(P<0.05或0.01)。leptin组中以f8片段为对照,其他片段与ERα抗体结合能力均较其降低,除f1外均有统计学差异(P<0.01)。结论乳腺癌细胞增殖过程中细胞增殖信号招募ERα至p21WAF1/CIP1启动子区,且p21WAF1/CIP1启动子区-2 800 bp~-3 200 bp区域存在与ERα高度结合的靶功能区。
乳腺癌;MCF-7细胞;p21WAF1/CIP1;雌激素受体α;辛二酰苯胺异羟肟酸;瘦素
乳腺癌的发生发展与多种参与肿瘤细胞增殖、凋亡、侵袭、转移的蛋白有关。雌激素受体(estrogen receptor,ER)阳性的乳腺癌MCF-7细胞,其生长与增殖主要受ER信号系统驱动,此信号系统亦可被瘦素(leptin)信号系统激活[1]。leptin是肥胖基因的表达产物,主要由脂肪细胞合成和分泌,通过与瘦素受体OB-Rb结合发挥作用。p21WAF1/CIP1是细胞周期依赖性蛋白激酶抑制剂,可使细胞周期停滞、促进细胞凋亡并抑制癌细胞的转移和侵袭。本课题组的前期工作证实leptin处理后的乳腺癌细胞p21WAF1/CIP1mRNA及蛋白表达水平远远低于leptin未处理组细胞[2]。组蛋白去乙酰化酶(histone deacetylase,HDAC)抑制剂辛二酰苯胺异羟肟酸(suberoylanilide hydroxamic acid,SAHA)可抑制HDAC活性,通过上调p21WAF1/CIP1引起细胞周期阻滞于G1期而抑制细胞增殖[3]。本研究的目的是找出ERα募集于p21WAF1/CIP1启动子区调控其转录活性的具体作用位点,明确SAHA及leptin在调节p21WAF1/CIP1启动子功能过程中的分子机制。
1 材料与方法
1.1 材料
人乳腺癌细胞株MCF-7(美国ATCC细胞库),SAHA、leptin(美国Sigma),完全型RPMI-1640培养液、改良型RPMI-1640培养液、磷酸盐缓冲液1×、PierceTMAgarose ChIP试剂盒、CO2恒温细胞培养箱、超净工作台(美国Thermo),ERα抗体(美国Abcam),0.25%胰酶-EDTA(美国Gibco),Power SYBR®Green PCR Master Mix、7500 RealTime PCR仪(美国Life Technologies),p21WAF1/CIP1f1~f10引物(上海生工生物工程有限公司),Biofuge 28RS低温高速离心机(德国Heraeus),倒置显微镜(日本Olympus),SKD1807-E摇床(美国Scilogex),恒温混匀器(美国Eppendorf)。
1.2 方法
1.2.1 细胞培养:将MCF-7细胞接种在完全型RPMI-1640培养液(10%胎牛血清,100 U/mL青霉素,100 U/mL链霉素)中,37℃、5%CO2孵箱饱和湿度条件下贴壁传代培养,每2~3 d换液并传代1次。0.25%胰酶-EDTA消化。经2~3次传代,取对数生长期的细胞等量分成3组,分别接种于完全型RPMI-1640培养液中,24 h后再将细胞置于改良型RPMI-1640培养液中进行同步化处理24 h,此后将3组细胞分别定义为SAHA组(完全型RPMI-1640培养液10 mL+20 μmol/L的SAHA 0.88 μL)、leptin组(完全型RPMI-1640培养液10 mL+0.625 nmol/L的leptin 10 μL),对照组(加等量完全型RPMI-1640培养液)。
1.2.2 使用ERα抗体染色质免疫共沉淀技术(chromatin-immunoprecipitation,ChIP)处理样品:MCF-7细胞的甲醛交联及细胞团的分离;细胞溶解及MNase消化,每组样品各得到50 μL的MNase消化产物,留取5 μL-20℃保存作为内对照,留取45 μL进行下一步的免疫沉淀处理,免疫沉淀过程中需向每个ChIP样品加入ERα抗体10 μg,实验步骤均按操作手册完成。最终3组MCF-7细胞均获得ChIP得到的DNA及各自的内对照。
1.2.3 实时PCR检测各组p21WAF1/CIP1f1~f10片段的DNA表达:PCR反应体系为25 μL,DNA 1.5 μL,上下游引物各0.75 μL,PCR Master Mix 12.5 μL,ddH2O 9.5 μL。反应条件为50℃2 min,95℃10 min预变性,95℃15 s,60℃1 min,共40个循环。每个样品3个复孔,采用2-ΔΔCt法计算各组DNA的相对表达量。
p21WAF1/CIP1启动子区10个片段的引物序列:f1,上游5’-TCCTCCTGGA GAGTGCCAAC-3’,下游5’-TTGGTGCGCTGGACACATTT-3’;f2,上游 5’-TTCCCGGAAGCATGTGACAA-3’,下游5’-GCACCT GGAGCACCTAGACACC-3’;f3,上游5’-CCC GTTTCCCCAGCAGTGTA-3’,下游5’-GCCAGG AAGGGGAGGAT TG-3’;f4,上游5’-AGGCCAAGGG GGTCTGCTAC-3’,下游5’-CGGGGAGGACAGGCT TCTTT-3’;f5,上游5’-TGAAAGCAGAGGGGCTTCA A-3’,下游5’-ACCATCCAAAGGGCTGGTTG-3’;f6,上游5’-TGTCCTTGGGCTGCCTGTTT-3’,下游5’-AGCCCTGTCGCAAGGATCTG-3’;f7,上游5’-TTCT GCAGCCACCACTGAGC-3’,下游5’-GTGGAGCAG CATGGGGTAGG-3’;f8,上游5’-CCCACCTCAGCCA CCTGAAT-3’,下游5’-GGGCAGATCACAGGGTCAG G-3’;f9,上游5’-AGTGGGCACATTTAGACATAGCA GGT-3’,下游5’-CCTCCCGGTCATGCCTTTC-3’;f10,上游5’-GTCAGGTGCCACTGGGGTCT-3’,下游5’-CGGTCCCCTGTTTCAATGCT-3’。采用实时PCR筛查调控p21WAF1/CIP1启动子转录功能的ERα反应元件(图1)。
1.3 统计学分析
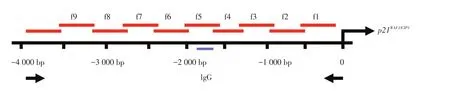
图1 调控p21WAF1/CIP1启动子转录功能的ERα反应元件示意图Fig.1 Schematic diagram of the ERα response element that regulates the transcriptional activity of the p21WAF1/CIP1promoter
2 结果
2.1 对照组MCF-7细胞p21WAF1/CIP1启动子区f1~f10片段ERα高功能结合位点的筛选
对照组MCF-7细胞经ERα抗体ChIP处理后,45 μL样品与5 μL内对照的DNA分别在f1~f10片段的引物作用下进行实时PCR扩增反应,二者Ct值之差为该样品在p21WAF1/CIP1启动子区各自片段的ΔCt值,再以f9片段为对照,其他片段的ΔCt值与其相减,得到对照组样品在p21WAF1/CIP1启动子区f1~f10片段各自ΔΔCt值,采用2-ΔΔCt法计算各片段DNA的相对表达量。对照组f1、f2、f8片段DNA相对表达量较f9片段升高2倍以上(P<0.01),故p21WAF1/CIP1启动子区f1、f2、f8片段是ERα的高功能结合位点。见图2。
2.2 与对照组比较SAHA组及leptin组MCF-7细胞p21WAF1/CIP1启动子区f1~f10片段ERα高功能结合位点的筛选

图2 对照组MCF⁃7细胞p21WAF1/CIP1启动子区f1~f10片段ERα高功能结合位点筛选Fig.2 Screening of high⁃affinity binding sites for ERα in the f1 to f10 fragments of the p21WAF1/CIP1promoter region in MCF⁃7 cells in control group
SAHA组及leptin组MCF-7细胞与ERα抗体进行ChIP处理,并将纯化的DNA组分进行实时PCR检测。结果表明:SAHA组MCF-7细胞的p21WAF1/CIP1启动子区f1~f10片段结合ERα抗体的DNA相对表达量较对照组对应片段均降低,其中f2、f6~f10片段有统计学差异(P<0.05或0.01),f8片段达最低值。leptin组细胞f1~f10片段结合ERα抗体的DNA相对表达量较对照组对应片段均降低,其中f1、f2、f5、f6、f8、f10片段有统计学差异(P<0.05或0.01)。SAHA组及leptin组f8片段结合ERα抗体的DNA相对表达量较对照组对应片段均降低,但SAHA组明显低于leptin组,差异有统计学意义(P<0.01)。见图3。
2.3 以SAHA组及leptin组细胞p21WAF1/CIP1启动子区f1~f10片段中特定片段为对照筛选ERα高功能结合位点
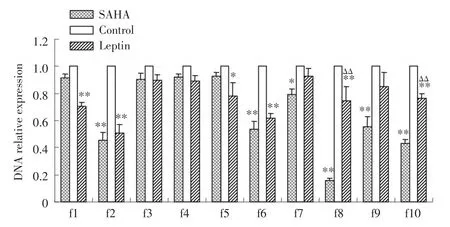
图3 SAHA组及leptin组MCF⁃7细胞p21WAF1/CIP1启动子区f1~f10片段ERα高功能结合位点筛选Fig.3 Screening of high⁃affinity binding sites for ERα in the f1 to f10 fragments of the p21WAF1/CIP1promoter region in MCF⁃7 cells in the SAHA and leptin groups
以SAHA组MCF-7细胞的p21WAF1/CIP1启动子f8片段DNA相对表达量为对照,f1~f7、f9~f10片段DNA相对表达量均较其升高(P<0.05或0.01)。以leptin组MCF-7细胞的p21WAF1/CIP1启动子f8片段DNA相对表达量为对照,f1~f7、f9~f10片段DNA相对表达量均较其降低,除f1片段外均有统计学差异(P<0.01)。见表1。

表1 以f8片段为对照筛选SAHA组及leptin组MCF⁃7细胞p21WAF1/CIP1启动子区f1~f10片段ERα高功能结合位点Tab.1 Screening of high⁃affinity binding sites for ERα in the f1 to f10 fragments of the p21WAF1/CIP1promoter region in MCF⁃7 cells in the SAHA and leptin groups,with f8 fragment as the control
3 讨论
乳腺癌是女性恶性肿瘤之首,其中70%的患者为ERα阳性[4-5]。ERα在乳腺癌的发生发展中至关重要,已成为临床内分泌治疗的金标准,因此深入研究ERα阳性的MCF-7乳腺癌细胞的生物学特性,对完善乳腺癌的治疗方法、抑制其转移和复发有不容忽视的临床价值。近年来,表观遗传学修饰成为乳腺癌研究的热点,组蛋白乙酰化及去乙酰化等共价修饰是主要研究内容。HDAC使组蛋白去乙酰化,增加组蛋白与DNA双链的亲和性,可与一些调控肿瘤发生发展的基因启动子区结合而抑制这些基因的转录。在乳腺癌细胞增殖过程中,细胞增殖信号在p21WAF1/CIP1的启动子区可招募HDAC1转录因子,通过组蛋白去乙酰化表观遗传修饰影响p21WAF1/CIP1表达。ERα是由雌激素激活的转录因子,雌激素应答成分位于雌激素应答靶基因的启动子区,ERα可直接结合到雌激素应答成分或通过与AP1、SP1、MTA1、HDAC1等其他转录因子结合,调控靶基因的转录[6]。
本研究利用DNA-ChIP方法研究发现,对照组MCF-7细胞p21WAF1/CIP1基因转录起始点近端启动子调节区f1、f2和远端调节区f8片段结合ERα抗体的DNA相对表达量较f9片段显著升高。这表明在细胞增殖过程中,ERα可被招募至p21WAF1/CIP1启动子区,f1、f2、f8片段是ERα的高功能结合位点。
研究[7-8]表明,SAHA作为一种广谱的HDAC抑制剂,可以从转录水平抑制ERα合成,同时可以通过增强热休克蛋白90乙酰化修饰而促进ERα经泛素—蛋白酶体通路降解。SAHA作用下的MCF-7细胞,与p21WAF1/CIP1启动子区DNA结合的ERα明显减少,且在f8片段(-2 800 bp~-3 200 bp)处受SAHA影响ERα与p21WAF1/CIP1启动子区DNA的结合量最少。leptin可通过调控细胞周期和凋亡、影响细胞外环境等多重机制促进ERα阳性的MCF-7乳腺癌细胞增殖与转移[9-10]。leptin可提高HDAC1的活性[11],HDAC1与ERα和ERβ均能特异结合,但HDAC1仅能特异地降低ERα蛋白水平,而不影响ERβ蛋白水平[12]。本研究发现,与对照组相应片段比较,leptin作用下的MCF-7细胞p21WAF1/CIP1启动子区f1~f10片段结合ERα的DNA相对表达量均降低。以leptin组自身f8片段DNA相对表达量为对照,其他片段都较之为低。由于leptin可通过促进芳香酶的表达导致雌激素生成增多[13],也可上调乳腺癌MCF-7细胞中ERα的表达水平[14]。故经SAHA、leptin处理后的MCF-7细胞p21WAF1/CIP1启动子区f8片段结合ERα的DNA相对表达量较对照组均降低,但SAHA组明显低于leptin组。这一结果表明:在乳腺癌发生发展过程中,某些细胞增殖信号招募ERα于p21WAF1/CIP1启动子特定区域,调控其转录,f8片段是SAHA、leptin发挥作用的功能敏感区。
综上所述,本研究首先通过ChIP方法筛选出对照组MCF-7细胞p21WAF1/CIP1启动子区ERα的高功能结合位点,再对SAHA及leptin处理后的MCF-7细胞进一步ChIP筛选,明确p21WAF1/CIP1启动子区-2 800 bp至-3 200 bp区域可能是与ERα高度结合的靶功能区。本研究的发现丰富了SAHA和leptin在调节p21WAF1/CIP1启动子功能过程中的分子机制,更为抗乳腺癌的药物研发及靶向治疗奠定了理论和实验基础。
[1]XUE RQ,GU JC,DU ST,et al.Lentivirus-mediated RNA interference targeting the ObR gene in human breast cancer MCF-7 cells ina nude mouse xenograft model[J].Chin Med J(Engl),2012,125(9):1563-1570.DOI:10.3760/cma.j.issn.0366-6999.2012.09.008.
[2]ZHOU W,GUO S,GONZALEZ-PEREZ RR.Leptin pro-angiogenic signature in breast cancer is linked to IL-1 signalling[J].Br J Cancer,2011,104(1):128-137.DOI:10.1038/sj.bjc.6606013.
[3]LEE YJ,WON AJ,LEE J,et al.Molecular mechanism of SAHA on regulation of autophagic cell death in tamoxifen-resistant MCF-7 breast cancer cells[J].Int J Med Sci,2012,9(10):881-893.DOI:10.7150/ijms.5011.
[4]TSUBOI K,KANEKO Y,NAGATOMO T,et al.Different epigenetic mechanisms of ERα implicated in the fate of fulvestrant-resistant breast cancer[J].J Steroid Biochem Mol Biol,2017,167:115-125. DOI:10.1016/j.jsbmb.2016.11.017.
[5]LEI B,PENG W,XU G,et al.Activation of G protein-coupled receptor 30 by thiodiphenol promotes proliferation of estrogen receptor αpositive breast cancer cells[J].Chemosphere,2017,169:204-211. DOI:10.1016/j.chemosphere.2016.11.066.
[6]张佳娜,汪庆余,曾磊,等.乳腺癌细胞中p73α与ERα的相互关系[J].实验与检验医学,2013,31(1):4-6.DOI:10.3969/j. issn.1674-1129.2013.01.002.
[7]YI X,WEI W,WANG SY,et al.Histone deacetylase inhibitor SAHA induces ERalpha degradation in breast cancer MCF-7 cells by CHIP-mediated ubiquitin pathway and inhibits survival signaling[J].Biochem Pharmacol,2008,75(9):1697-1705.DOI:10.1016/j.bcp.2007.10.035.
[8]DE LOS SANTOS M,MARTINEZ-IGLESIAS O,ARANDA A.Antiestrogenic actions of histone deacetylase inhibitors in MCF-7 breast cancer cells[J].Endocr Relat Cancer,2007,14(4):1021-1028. DOI:10.1677/ERC-07-0144.
[9]STRONG AL,OHLSTEIN JF,BIAGAS BA,et al.Leptin produced by obese adipose stromal/stem cells enhances proliferation and metastasis of estrogen receptor positive breast cancers[J].Breast Cancer Res,2015,17:112.DOI:10.1186/s13058-015-0622-z.
[10]FENG X,HAN H,ZOU D,et al.Suberoylanilide hydroxamic acidinduced specific epigenetic regulation controls leptin-induced proliferation of breast cancer cell lines[J].Oncotarget,2017,8(2):3364-3379.DOI:10.18632/oncotarget.13764.
[11]GONZALEZ-PEREZ RR,XU Y,GUO S,et al.Leptin upregulates VEGF in breast cancer via canonic and non-canonical signalling pathways and NF-kappaB/HIF-1alpha activation[J].Cell Signal,2010,22(9):1350-1362.DOI:10.1016/j.cellsig.2010.05.003.
[12]常庆,韩聚强,王晓辉,等.HDAC1对ERα和ERβ蛋白水平的调控[J].军事医学科学院院刊,2006,30(4):329-332.DOI:10.3969/j.issn.1674-9960.2006.04.007.
[13]LIU E,SAMAD F,MUELLER BM.Local adipocytes enable estrogen-dependent breast cancer growth:role of leptin and aromatase[J].Adipocyte,2013,2(3):165-169.DOI:10.4161/adip.23645.
[14]YU W,GU JC,LIUJZ,et al.Regulation of estrogen receptors alpha and beta in human breast carcinoma by exogenous leptin in nude mouse xenograft model[J].Chin Med J(Engl),2010,123(3):337-343.DOI:10.3760/cma.j.issn.0366-6999.2010.03.015.
(编辑 陈 姜)
High⁃affinity Binding Sites for Estrogen Receptor α in the p21WAF1/CIP1Promoter Region in Breast Cancer MCF⁃7 Cells
ZOU Dan1,FENG Xiuyan2,ZHOU Weiqiang2
(1.Department of Pathophysiology,Shenyang Medical College,Shenyang 110034,China;2.Key Laboratory of Environmental Pollution and Microecology of Liaoning Province,Shenyang Medical College,Shenyang 110034,China)
Objective To investigate the specific sites that estrogen receptor(ER)α could be recruited to in thep21WAF1/CIP1promoter region to regulate its transcriptional activity in MCF-7 cells,and to clarify the molecular mechanism of suberoylanilide hydroxamic acid(SAHA)and leptin in the regulation ofp21WAF1/CIP1promoter function.MethodsMCF-7 cells were starved by culturing them in fetal calf serum-free medium for 24 hours,and then treated with 20 μmol/L of 0.88 μL SAHA(SAHA group)or 0.625 nmol/L of 10 μL leptin(leptin group)for 24 hours,or cultured in complete RPMI-1640 medium(control group).Cell lysates were incubated with anti-ERα antibody for ChIP analysis.The relative expression levels of DNA fragments,ranging from the TSS to upstream of thep21WAF1/CIP1promoter region(+2 to-4 000 bp),that bound the antibody were detected by real-time PCR.ResultsIn the control group,the relative expression levels of f1,f2,and f8 DNA fragments that bound the anti-ERα antibody were two-fold higher than the relative expression of the f9 fragment(P<0.01).In the SAHA and leptin groups,the relative expression of f1 to f10 DNA fragment that bound anti-ERα antibody was significantly lower than that of the control.The binding affinity of ERα for the f8 fragment was the lowest(P<0.01)in the SAHA group,and it was significantly lower than that in the leptin group(P<0.01).ConclusionERα could be recruited to thep21WAF1/CIP1promoter via signaling pathways activated during the proliferation of breast cancer MCF-7 cells.Moreover,the DNA fragment ranging from-2 800 to-3 200 bp upstream of thep21WAF1/CIP1promoter is the target functional region for high-affinity binding with ERα.
breast cancer;MCF-7 cell;p21WAF1/CIP1;estrogen receptor α;suberoylanilide hydroxamic acid;leptin
R977.12
A
0258-4646(2017)08-0677-05
10.12007/j.issn.0258-4646.2017.08.002
国家自然科学基金(81172509);辽宁省自然科学基金(201602735);沈阳市科学技术计划(F15-199-1-28)
邹丹(1971-),女,副教授,博士.
周伟强,E-mail:zhouwq@hotmail.com
2016-12-16
网络出版时间:

