纳米二氧化硅固定化脂肪酶改性环氧涂层的耐腐蚀性研究
吕玉翠, 姜国飞, 刘 芳, 王永强, 刘春爽, 孙 娟, 赵朝成
(中国石油大学 化学工程学院, 山东 青岛 266580)
纳米二氧化硅固定化脂肪酶改性环氧涂层的耐腐蚀性研究
吕玉翠, 姜国飞, 刘 芳, 王永强, 刘春爽, 孙 娟, 赵朝成
(中国石油大学 化学工程学院, 山东 青岛 266580)
利用纳米二氧化硅固定化脂肪酶对环氧树脂进行改性。考察涂层中脂肪酶活性变化、改性前后环氧涂层的物理性能变化,以及改性涂层对A3碳钢在循环水中的缓蚀性能影响。结果表明,添加2%质量分数固定化脂肪酶时,涂层中的脂肪酶活性能够达到2300 U/g,涂层硬度为2 H,附着力为3级,用电化学法测得的涂层阻抗值最大,且显著高于未添加固定化脂肪酶的环氧涂层,说明添加固定化脂肪酶后环氧涂层的耐腐蚀性能得到提高。
脂肪酶;固定化;纳米SiO2;环氧涂层;防腐蚀材料
换热器是石化企业的主要设备,约占所有设备总量的1/4。由于存在腐蚀介质浓度大、流体冲刷,以及换热介质易泄漏等问题而使得换热设备的腐蚀比一般设备的腐蚀要严重得多[1]。据统计,炼化企业由于腐蚀造成的经济损失平均约占其产值的6%, 如果采取适当的防护措施,则可以避免30%~40%的腐蚀损失[2]。目前,抑制设备腐蚀的方法主要有涂层防护、添加缓蚀剂和材料升级3种[1,3-6],其中,单一的涂层防护或者添加缓蚀剂的方法不能满足设备防腐的需要。因此向涂层中加入缓蚀剂以达到物理隔离作用和化学缓蚀作用二合一效果的改性涂层是研究热点之一[7-8],即利用纳米多孔粒子对缓蚀剂进行封装固定后添加到涂层中,通过缓蚀剂的释放来达到对金属的缓蚀作用。目前用于涂层改性研究的缓蚀剂可分为无机缓蚀剂和有机缓蚀剂,但针对生物酶缓蚀剂应用于涂层改性的研究国内外还很少有报道。
水性环氧树脂涂料具有环境友好、低毒、低黏度、易清洁、适应性强、操作性好等优点,正在逐渐取代容易引起健康和环境污染问题的挥发性环氧涂层[9-10]。但单一的水性环氧树脂不能满足实际应用环境的需求,这就需要在环氧涂层中添加各种功能的材料,制备复合涂层以满足应用需求。深入探讨具备不同功能的复合涂层作用机理,采取正确的防腐蚀措施减少经济损失,对于提高企业的经济效益、促进可持续发展具有非常重要的意义。
Wang等[11]曾经研究了将固定化α-淀粉酶和葡萄糖氧化酶双酶应用于抗生物黏泥涂层的构建,结果表明,含酶涂层的抗污效果十分显著。笔者所在课题组前期研究发现,脂肪酶具有缓蚀性能[12-14]。但游离脂肪酶在应用方面具有局限性,若采用一定方法和特定载体将游离生物酶固定化并制备防腐蚀涂层,则可以扩大生物酶的应用空间。
笔者以纳米SiO2粒子作为固定化脂肪酶载体,构建固定化酶,制备固定化脂肪酶/环氧复合涂层,考察改性前后环氧涂层的硬度和附着力变化,采用电化学法研究复合涂层的防腐蚀机理。
1 实验部分
1.1 药品
脂肪酶(酶活性>30000 U/g),南京奥多福尼生物科技有限公司产品;纳米SiO2、三丁酸甘油酯(98%质量分数),上海阿拉丁生化科技股份有限公司产品;A3碳钢,50 mm×20 mm×2 mm;水性环氧树脂w1280及其固化剂,广东市红淇洋化工有限公司产品;无水乙醇、甲醇,分析纯,四川西陇化工有限公司产品;丙酮、碳酸氢钠、七水合硫酸镁、氯化钙、氢氧化钠、硅烷偶联剂KH-560、六偏磷酸钠、无水磷酸氢二钠、磷酸二氢钾,分析纯,国药集团化学试剂有限公司产品。
1.2 实验方法
1.2.1 纳米SiO2固定化脂肪酶的制备
将纳米SiO2在真空干燥箱中干燥1 h后,取1.5 g干燥SiO2加入0.8 g/L脂肪酶溶液,于振荡器中震荡8 h进行脂肪酶的装载。取出后抽滤,用200 mL Na2HPO4-KH2PO4缓冲液(pH=8)洗涤数次,最后于30℃干燥箱内烘干得固定化脂肪酶。
1.2.2 脂肪酶涂层的制备
称取不同质量分数(占水性环氧树脂质量)的固定化脂肪酶粉末。采用机械搅拌和超声分散的方法分散在水中,并加入一定量的分散剂进行分散改性,然后加入5 g水性环氧树脂,2000 r/min转速下机械搅拌30 min,再超声波分散30 min。于机械搅拌状态下滴加固化剂,10 min后涂覆于经丙酮和乙醇处理过的A3碳钢上,悬挂于30℃烘箱中固化72 h。其制备流程如图1所示。
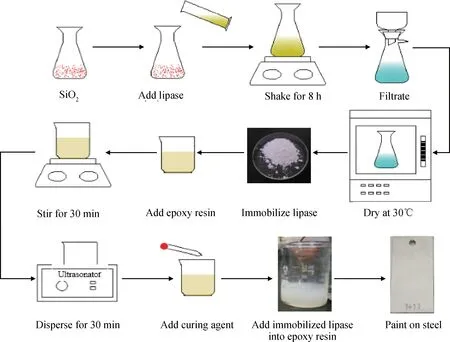
图1 纳米SiO2固定化脂肪酶涂层制备流程图Fig.1 Process flow diagram of epoxy resin coating modified by lipase immobilized on nano-silica
1.2.3 测试与表征
采用扫描电子显微镜(日本日立公司产品)观察纳米SiO2的微观形貌;采用透射电子显微镜(日本电子(JEOL)产品)观察纳米SiO2的孔道结构;采用介孔物理吸附仪(美国 Micromeritics 公司产品)对纳米SiO2进行孔容、孔径和比表面积的表征;采用FT-IR(美国尼高力公司产品)对纳米SiO2、脂肪酶以及固定化脂肪酶进行化学组成的定性分析。
采用滴定法测定固定化脂肪酶及其涂层的酶活性[15]。具体步骤如下:以三丁酸甘油酯为底物,将50 μL三丁酸甘油酯加入到6.0 mL、25 mmol/L、pH值8.0的Na2HPO4-KH2PO4缓冲溶液中,然后加入一定量的游离或固定化酶, 整个反应体系置于37℃的恒温水浴中剧烈搅拌15 min后加入10 mL的95%质量分数甲醇终止反应,然后用 0.05 mol/L NaOH中和反应中生成的酸,以酚酞为指示剂。定义在40℃、pH=7.5、1 g脂肪酸每分钟水解释放出 1 μmol游离有机酸所需的脂肪酶的量为一个活力单位,用E表示,单位U/g,计算方法见式(1)。
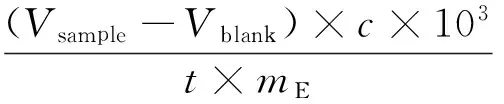
(1)
式(1)中,c为NaOH的摩尔浓度,mol/L;Vsample为添加脂肪酶后滴定所消耗的NaOH的体积,mL;Vblank为空白滴定所消耗的NaOH的体积,mL;t为反应时间,min;mE为加入酶量,mg。
试样处理:将试样用丙酮除油、乙醇清洗、冷风吹干后放置在干燥器中备用。用刷涂法将制备的固定化脂肪酶/环氧复合涂层均匀涂刷在试样上,涂层厚度(30±5) μm。
利用电化学工作站CHI660E(上海华辰仪器公司产品)对试样进行电化学阻抗和极化曲线的测试。采用三电极体系测量,以处理后的试样为工作电极(工作面积9.54 cm2),饱和甘汞电极为参比电极,铂丝电极为辅助电极。电解质体系为配制的循环冷却水,其水质分析如表1所示。体系稳定后进行测试,电化学阻抗测试频率范围为100 kHz~10 mHz,激励信号幅值为5 mV,极化曲线扫描电压范围为开路电压±300 mV,扫描速率1 mV/s。

表1 试验用循环冷却水水质分析Table 1 The analysis of circulating water quality index in experiment ρ/ (mg·L-1)
根据GB/T 6739-1996标准,采用铅笔硬度法手动测定涂层的硬度。根据ISO-2409标准,使用附着力测试仪采用划格法进行附着力测定。
2 结果与讨论
2.1 纳米SiO2和固定化脂肪酶的表征分析
2.1.1 纳米SiO2扫描电镜和透射电镜分析
图2为纳米SiO2的SEM图和TEM图。从图2(a)可以看出,纳米SiO2颗粒细小,颗粒之间有较为严重的团聚现象。因此需要对其进行分散性改性。从图2(b)可以看出,该纳米SiO2粒径分布在20~30 nm,有较为丰富的间隙孔。
2.1.2 纳米SiO2氮气吸附-脱附实验
图3为纳米SiO2的氮气吸附-脱附等温线和孔径分布图。从图3可以看出,纳米SiO2的氮气吸附-脱附等温线属于IUPAC定义的Langmuir IV型,在相对压力约为0.9处吸附曲线有明显突变,且在吸附分支与脱附分支产生了H1型滞后环,说明有圆柱状孔存在,这是由N2在孔道中产生的毛细凝聚现象引起的[16]。经计算此纳米SiO2比表面积为184.18 m2/g,孔容0.65 cm3/g,孔径13~19 nm,同时具有小孔、介孔等不同规格的孔洞,可以作为固定化脂肪酶的载体。

图2 纳米SiO2的SEM图和TEM图Fig.2 SEM image and TEM image of nano-silica(a) SEM image; (b) TEM image
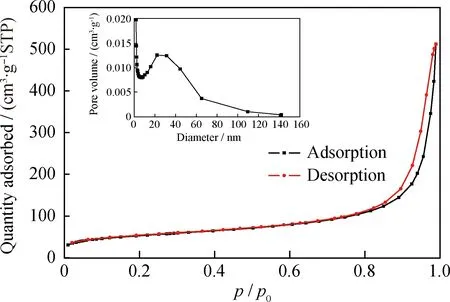
图3 纳米SiO2的氮气吸附-脱附等温线和孔径分布图Fig.3 N2 adsorption desorption isotherms and pore size distribution of nano-silica microspheres sample
2.1.3 纳米SiO2分散性分析
从图3可以看出,颗粒之间有较为严重的团聚现象。六偏磷酸钠((NaPO3)6)吸附在颗粒表面能提高颗粒间的静电排斥作用能和位阻排斥作用能[17],是一种较为常用的纳米粉体分散剂。硅烷偶联剂(KH-560)可在无机物和有机物之间形成架桥作用,广泛应用于纳米SiO2在环氧涂层中的分散改性。因此笔者分别选用六偏磷酸钠和硅烷偶联剂对纳米SiO2进行分散实验,结果分别如图4所示。
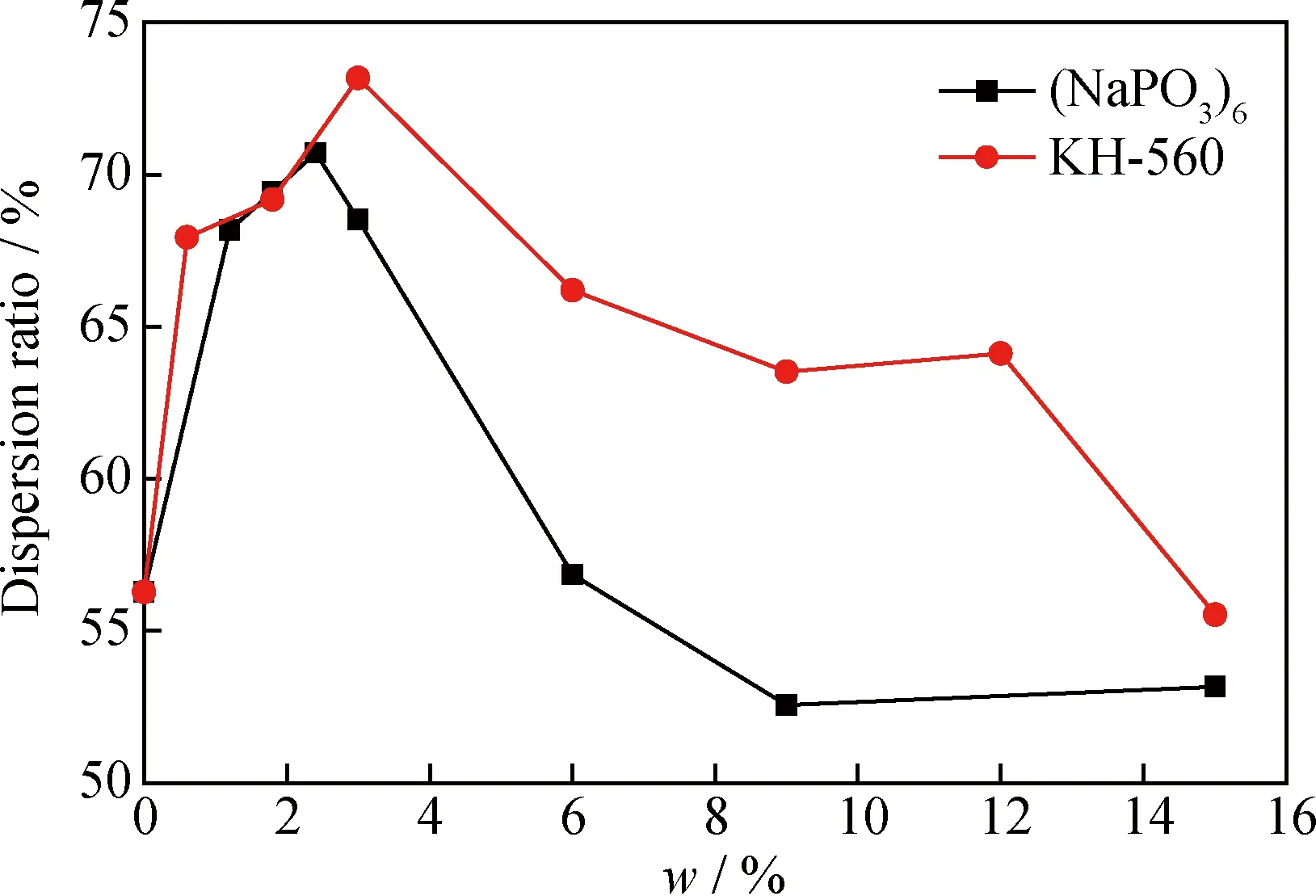
图4 六偏磷酸钠和硅烷偶联剂质量分数对分散率的影响Fig.4 Effect of the type and mass fraction of dispersants on the influence of slurry’s stability
从图4可以看出,随着六偏磷酸钠质量分数的增加,纳米SiO2分散率呈现先增大后减少的趋势。在六偏磷酸钠加入质量分数为2.4%时,SiO2的分散率最大,为70.71%,此时分散效果最好。与六偏磷酸钠相同,随着硅烷偶联剂质量分数的增加,纳米SiO2分散率同样呈现先增大后减少的趋势,在硅烷偶联剂加入质量分数为3%时,SiO2的分散率最大,为73.17%,此时分散效果最好。根据童剑[18]对纳米材料的分散性研究,实验所得趋势与其结果相同,即随着分散剂含量的增加,分散率先增加后减小。从图4还可以看出,硅烷偶联剂的最大分散率要高于六偏磷酸钠,并且质量分数在 1.8%~3%之间的分散率也都要高于六偏磷酸钠。因此笔者在下文采用3%质量分数硅烷偶联剂对纳米SiO2进行分散。
2.1.4 固定化脂肪酶涂层表征
将固定化脂肪酶进行红外分析,结果如图5所示。从图5可以看出,在1647 cm-1和1541 cm-1区间存在蛋白质的特征吸收峰,分别属于酰胺Ⅰ带和酰胺Ⅱ带,其中酰胺Ⅰ带特征吸收峰是在1600~1700 cm-1区间,包括蛋白质的α-螺旋结构角、β-折叠、β-转角以及无规则卷曲[19]。酰胺Ⅱ带特征吸收峰是在1500~1600 cm-1,主要是蛋白质分子中的C—N伸缩振动峰和N—H弯曲振动峰。纳米SiO2谱图中,在472 cm-1、802 cm-1、1106 cm-1处分别是Si—O—Si弯曲振动、对称伸缩振动和反对称伸缩振动,1641 cm-1和3437 cm-1处是H—O—H弯曲振动和—OH基团伸缩振动[20]。固定化脂肪酶谱图中,存在上述的蛋白质酰胺Ⅰ带和酰胺Ⅱ带,也存在Si—O—Si的特征吸收峰。因此说明脂肪酶已经被装载在纳米SiO2上。
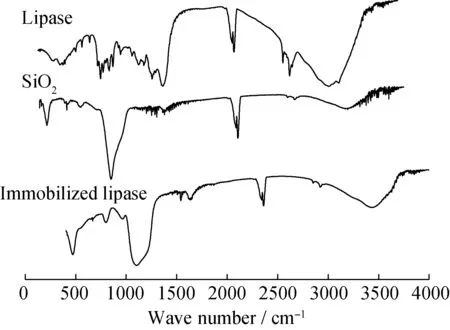
图5 纳米SiO2、脂肪酶及固定化脂肪酶的红外光谱图Fig.5 FTIR spectra of lipase, nano-silica and immobilized lipase
2.2 固定化脂肪酶活性分析
按照1.2.3节的方法测定固定化脂肪酶活性,结果如图6所示。从图6可以看出,随着涂层中固定化脂肪酶含量的增加,表现出来的酶活性呈现先增加后降低的趋势,当向涂层中添加质量分数为2%的固定化脂肪酶时,表现出来的酶活性最高。
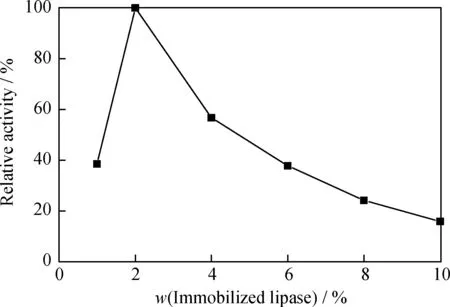
图6 添加不同质量分数固定化脂肪酶的涂层相对酶活性Fig.6 Effect of the mass fraction of immobilized lipase on the activity of lipase in coatings
为了进一步验证水性环氧树脂对脂肪酶生物活性的影响,将游离脂肪酶、固定化脂肪酶及涂层脂肪酶表现出来的最大酶活性作对比。结果显示,游离性脂肪酶的活性为6670 U/g,固定化脂肪酶的活性为480 U/g,而将固定化脂肪酶添加到水性环氧树脂后,其活性反而升高,达到了2300 U/g。分析原因,水性环氧树脂涂层中的活性环氧基团与脂肪酶蛋白质分子链上的氨基、巯基等发生反应,使得
原本被覆盖的脂肪酶分子能够重新发挥活性[21]。
2.3 固定化脂肪酶环氧涂层硬度和附着力分析
表2为添加不同质量分数固定化脂肪酶的涂层硬度和附着力。从表2可以看出,涂层的铅笔硬度在1 H、2 H之间,并且随着固定化脂肪酶添加量的增加,硬度呈现出先增大后减小的趋势。过少或者过多的固定化脂肪酶都会使涂层硬度降低,固定化脂肪酶添加质量分数在1%~6%之间时,涂层有较高的硬度。这是因为所添加的纳米SiO2是具有刚性特征的粒子,可以使涂层的有机相与无机粒子之间形成致密网状结构[22],从而增强了其硬度。但是添加量过多时,由于其团聚现象反而影响了涂层的致密性,使其硬度下降。图7为添加不同质量分数固定化脂肪酶涂层附着力测试照片。

表2 添加不同质量分数固定化脂肪酶的涂层硬度和附着力Table 2 The hardness and adhesion of coatings with different immobilized lipase mass fractions
1)GB/T6739-1996; 2)ISO-2409

图7 添加不同质量分数固定化脂肪酶涂层附着力测试照片Fig.7 The graphs of coatings with different immobilized lipase mass fractions after the testing of adhesion forcew(Immobilized lipase)/%: (a) 0;(b) 1;(c) 2;(d) 4;(e) 6;(f) 8
根据表2和图7,涂层附着力等级在1~5之间,并且随着固定化脂肪酶含量增加,附着力等级呈现逐渐增大的趋势。当固定化脂肪酶的添加质量分数为2%时,涂层的附着力最佳。这是因为纳米粒子巨大的表面能提高了涂层与金属之间不饱和键的结合强度,增大了涂层与基体金属的结合力[22]。
2.4 固定化脂肪酶/环氧复合涂层电化学性能测定
图8给出了添加不同量的固定化脂肪酶的环氧复合涂层浸泡24 h后的电化学阻抗谱。由图8可以看出,经过24 h浸泡后,腐蚀介质已经渗透到金属基底表面,并生成腐蚀产物。添加不同固定化脂肪酶的涂层,其容抗弧不同,当添加2%质量分数固定化脂肪酶时,容抗弧达到最大。这可能是2%纳米粒子增强了杂化涂层的交联度和致密度。同时,释放出的脂肪酶分子由于存在N、O杂原子,容易与Fe的空轨道形成配位键,又由于脂肪酶分子的疏水性,使得金属基体表面形成了一层疏水保护膜,从而增强了涂层的防护性能。
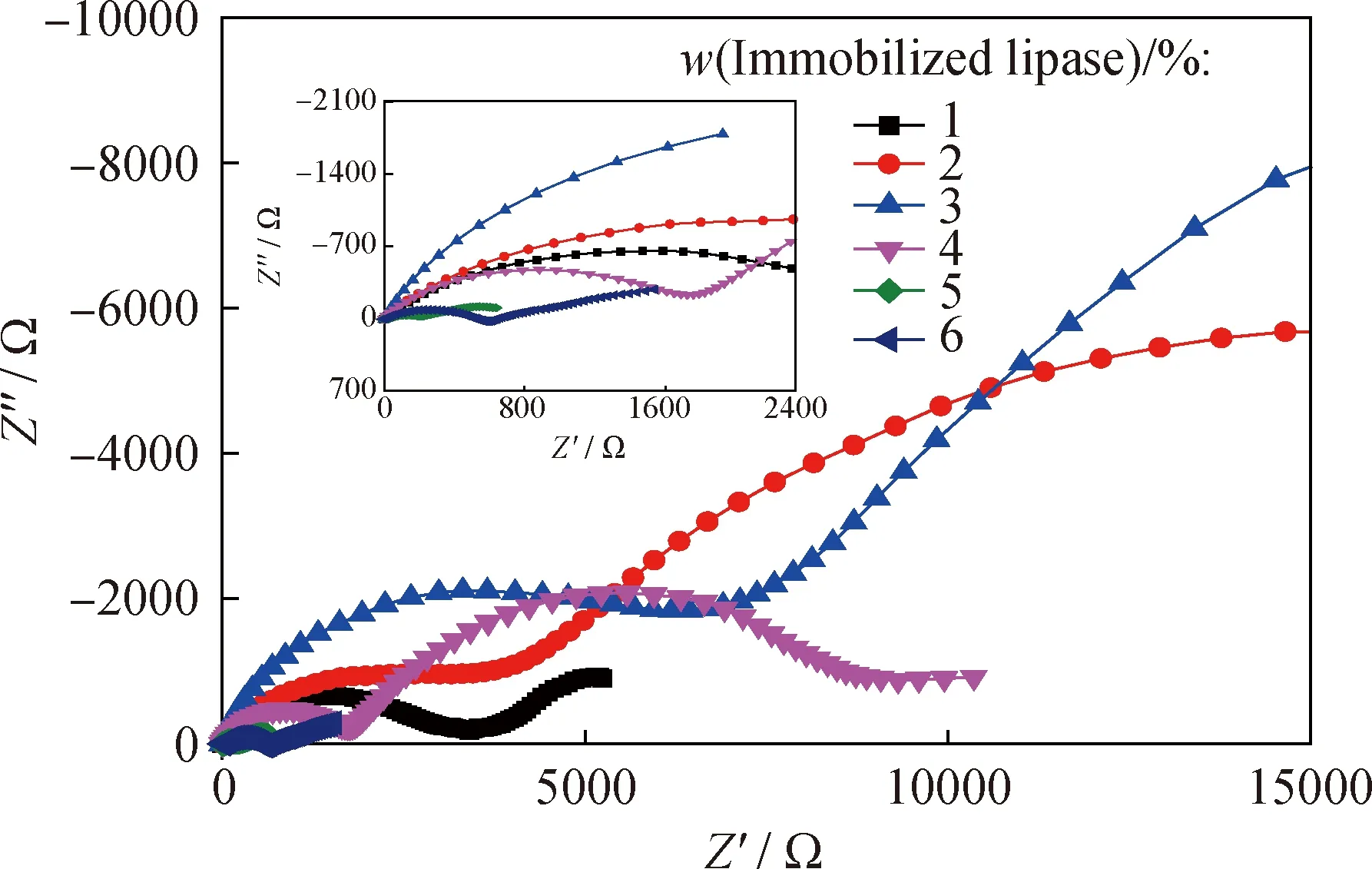
图8 添加不同质量分数固定化脂肪酶的环氧复合涂层浸泡24 h后其电化学阻抗谱图Fig.8 EIS plots for steel after 24 h immersion in circulating cooling water of epoxy resin coatings with different immobilized lipase mass fractionsZ’—Real part of impedance; Z”—Imaginary part of impedance
在阻抗模值与频率关系图(即Bode图)中,低频处的电阻对应的是涂层电阻,其反映的是涂层的抗腐蚀能力大小[10]。高频处的电阻对应溶液电阻,反映的是体系导电能力大小[16]。图9为添加不同质量分数固定化脂肪酶的环氧复合涂层浸泡24 h的波特图。从图9可以看出,添加1%和2%质量分数固定化脂肪酶的涂层在低频区的阻抗值较高,达到105Ω,而未添加固定化脂肪酶的涂层在低频处的阻抗值仅为103Ω。
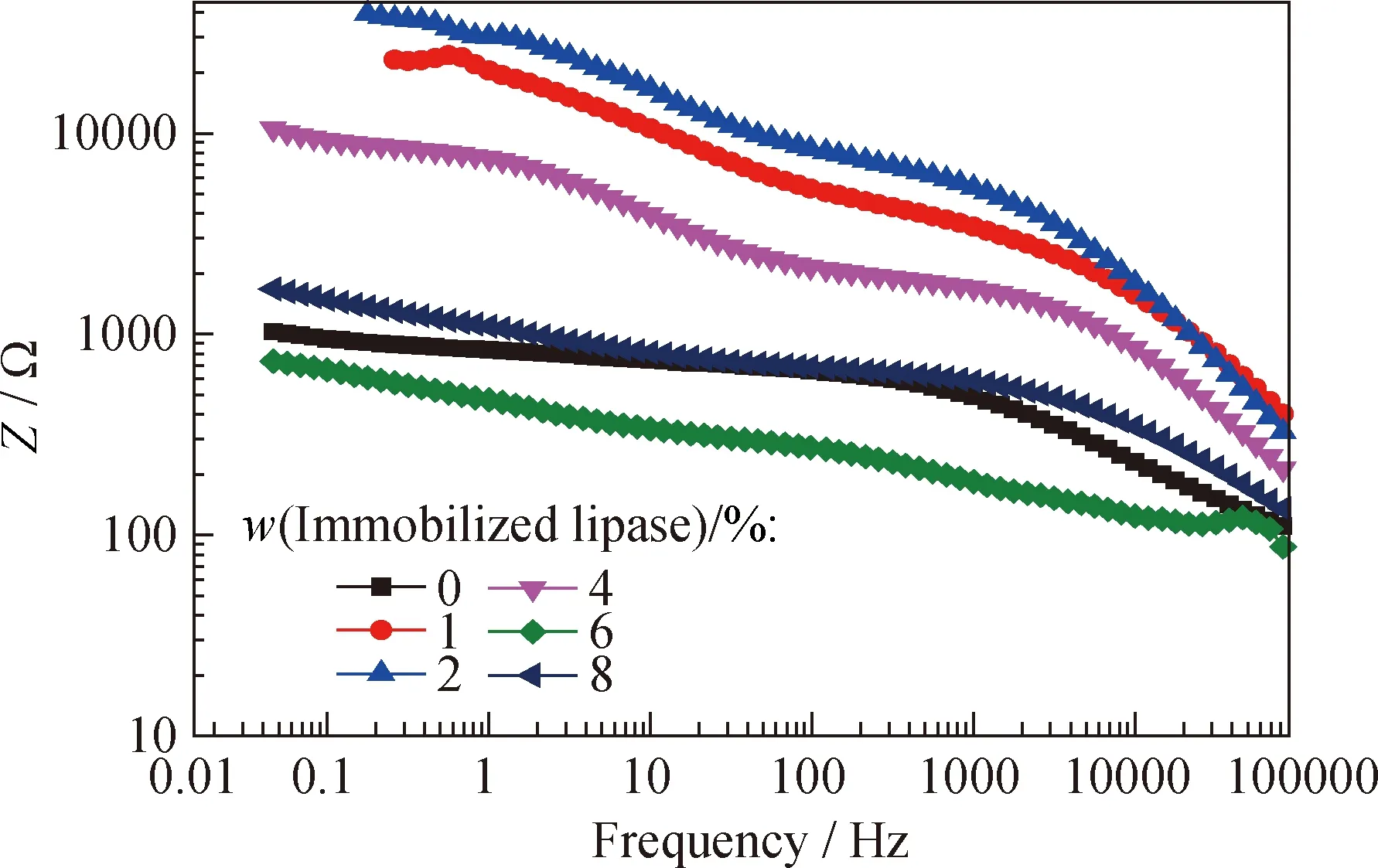
图9 添加不同质量分数固定化脂肪酶的环氧复合涂层浸泡24 h的波特图Fig.9 Bode plots at 24 h immersion in circulating cooling water of epoxy resin coatings with different immobilized lipase mass fractionsZ—Impedance
图10为添加不同质量分数固定化脂肪酶的环氧复合涂层浸泡24 h的塔菲尔图。由图10可以看出,相比于单一环氧涂层,添加了固定化脂肪酶的涂层腐蚀电位明显发生了正移,且腐蚀电流密度下降。尤其是添加了2%质量分数固定化脂肪酶涂层的腐蚀电流密度下降至最低。根据图10的塔菲尔曲线,由塔菲尔外延交点法得出腐蚀电流密度,并按照式(2),计算涂层中添加不同质量分数固定化脂肪酶时,碳钢的年腐蚀速率。计算结果见表3。
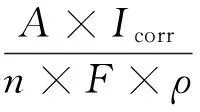
(2)
式(2)中,R为年腐蚀速率,mm/a;A为相对原子质量;Icorr为自腐蚀电流密度,A/cm2;n为电化学转移的电子数,n=2;F为法拉第常数(1F=26.8 A·h);ρ为金属的密度,本文中ρ=7.85 g/cm3。
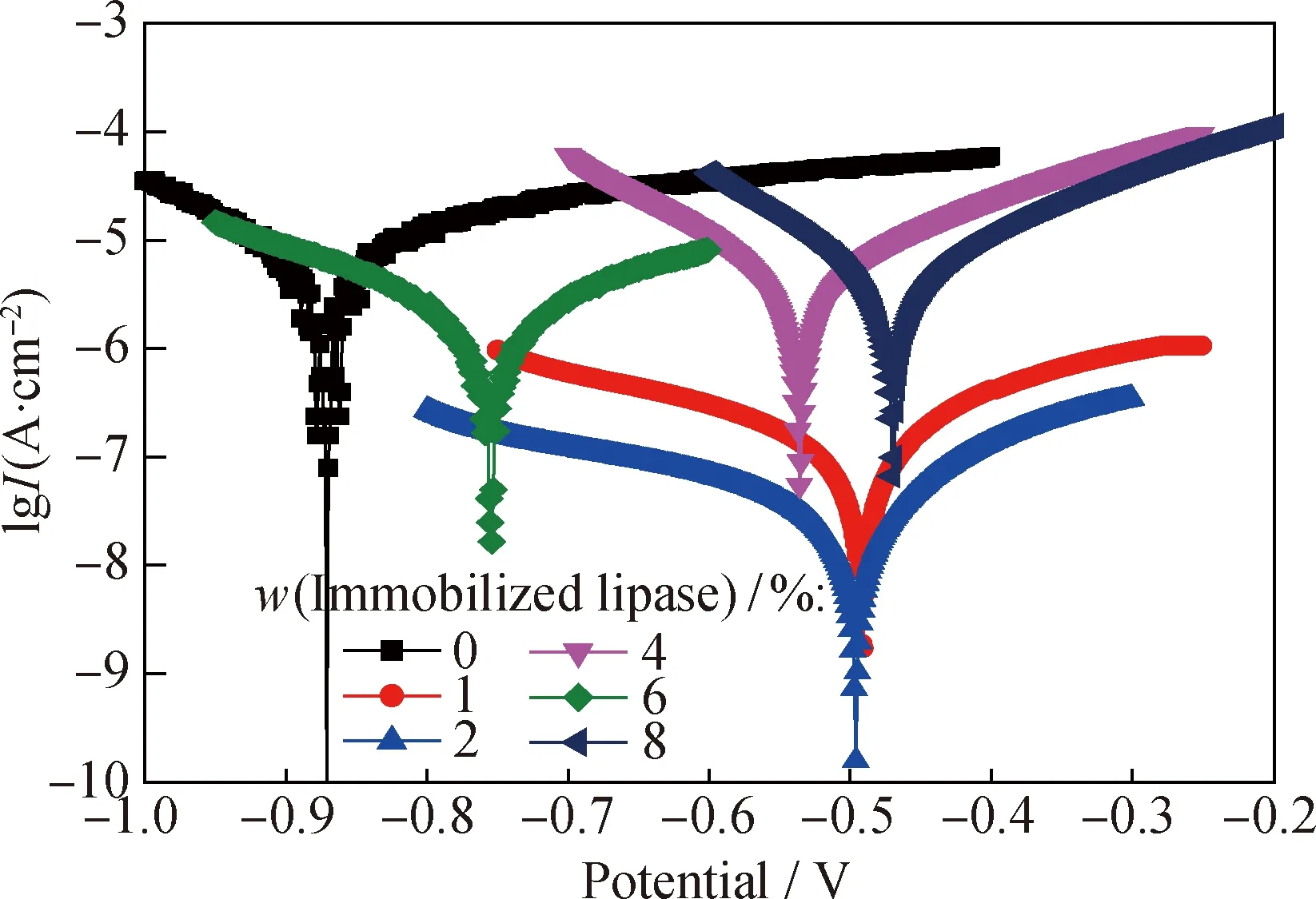
图10 添加不同质量分数固定化脂肪酶的环氧复合涂层浸泡24 h的塔菲尔图Fig.10 Tafel plots after 24 h immersion in circulating cooling water of epoxy resin coatings with different immobilized lipase mass fractions
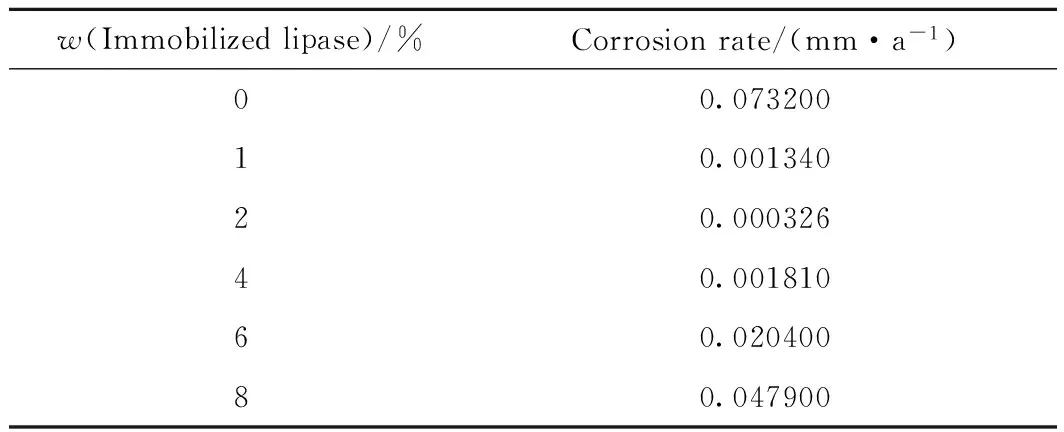
w(Immobilizedlipase)/%Corrosionrate/(mm·a-1)00.07320010.00134020.00032640.00181060.02040080.047900
由表3可见,随着涂层中固定化脂肪酶含量的增加,碳钢的腐蚀速率呈现出先减小后增大的趋势。固定化脂肪酶质量分数为2%时,碳钢的年腐蚀速率最低,涂层的防腐蚀效果最好。
2.5 固定化脂肪酶环氧涂层浸泡实验分析
将涂覆2%质量分数固定化脂肪酶涂层的碳钢片在循环水中浸泡30 d,期间间隔一定时间测其电化学阻抗谱,结果见图11。
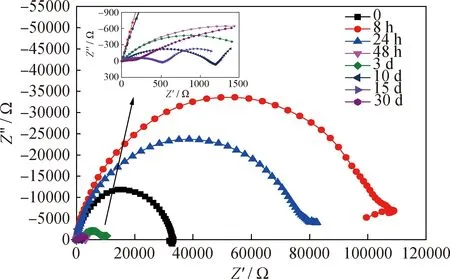
图11 2%质量分数固定化脂肪酶环氧涂层在循环水中浸泡不同时间的交流阻抗谱图Fig.11 EIS plots for steel in circulating cooling water with 2% mass fraction of immobilized lipase in epoxy resin at different immersion timeZ’—Real part of impedance; Z”—Imaginary part of impedance
从图11可以看出,随着浸泡时间的延长,容抗弧先增大后减小,即涂层的防腐蚀性能先增强后减弱。初期阶段,浸泡8 h后,容抗弧最大,涂层的阻抗达到最大;而浸泡48 h时,在阻抗谱图低频区出现了扩散过程引起的扩散阻抗[23-24],说明此时电解质溶液已经穿透涂层到达金属基体的表面;浸泡10 d容抗弧继续减小,腐蚀加剧;浸泡30 d后,涂层阻抗降到最低,涂层有明显的起泡现象,碳钢腐蚀严重,涂层基本失效。
2.6 单一环氧树脂涂层浸泡实验分析
为了进一步证明固定化脂肪酶在环氧涂层中的作用,与2.5节作对照试验,将单一环氧树脂涂覆在碳钢片上,测其在循环水中浸泡不同时间的交流阻抗谱图,结果如图12。
从图12可以看出,随着浸泡时间的延长,单一环氧树脂涂层的容抗弧呈现逐渐减小的趋势,涂层的缓蚀性能逐渐减弱。对比图11和12可以看出,相比于添加了2%质量分数固定化脂肪酶的环氧涂层,单一环氧树脂涂层的最大容抗弧要小得多,且脂肪酶涂层的失效速率明显低于单一环氧涂层。说明固定化脂肪酶的存在增强了环氧树脂的防腐蚀性能。
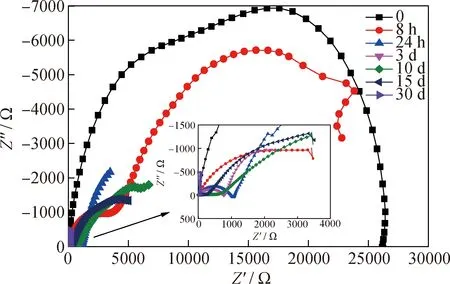
图12 单一环氧树脂涂层在循环水中浸泡不同时间的交流阻抗谱图Fig.12 EIS plots for steel in circulating cooling water with single epoxy resin coating at different immersion time
2.7 比较不同配方涂层保护下碳钢的腐蚀速率
表4为两种涂层浸泡不同时间挂片的年腐蚀速率。由表4可以看出,在相同浸泡时间下,添加2%质量分数固定化脂肪酶/环氧复合涂层,挂片的年腐蚀速率均低于单一环氧树脂涂层。浸泡大约10 d 后,单一环氧涂层腐蚀严重,而2%固定化脂肪酶/环氧复合涂层仍具有一定的防腐蚀能力。
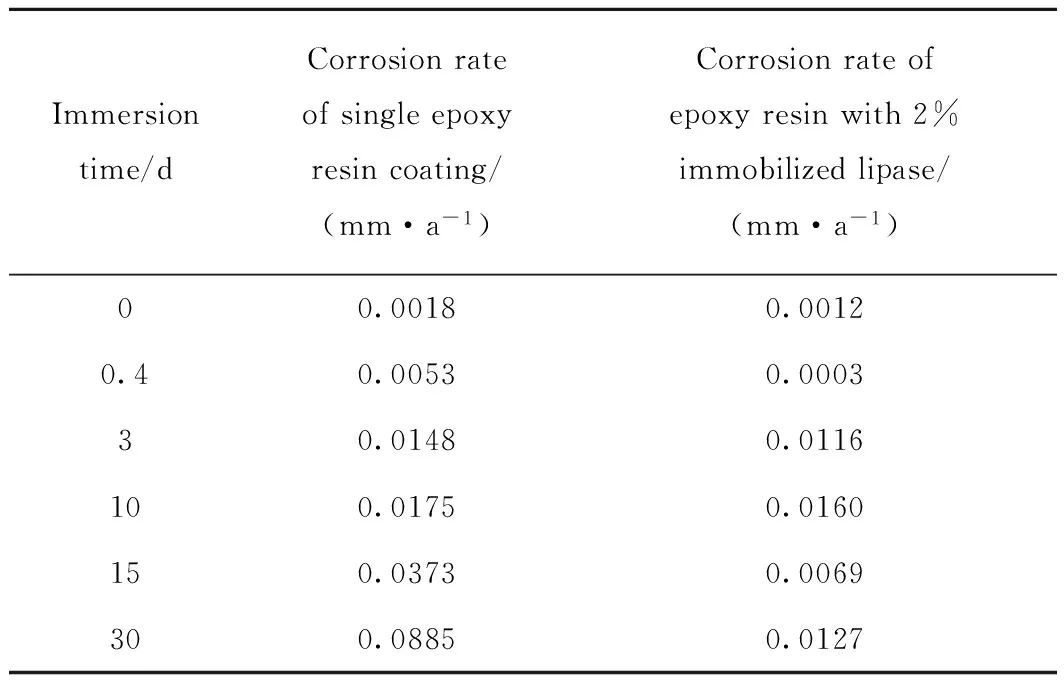
表4 两种涂层浸泡不同时间挂片的年腐蚀速率Table 4 Corrosion rate of steel implied epoxy resin coatings with and without immobilized lipase at different immersion time
3 结 论
用SiO2为载体固定化脂肪酶,制备了固定化脂肪酶环氧复合涂层,并通过固定化脂肪酶添加量的变化,分析复合涂层的各种性能。具体结论如下:
(1)随着涂层中固定化脂肪酶含量的增加,表现出来的酶活性呈现先增加后降低的趋势,且环氧树脂不会降低固定化脂肪酶的酶活性。
(2)当添加2%质量分数的固定化脂肪酶时,涂层的硬度与附着力性能最佳。
(3)环氧树脂中加入不同质量分数的固定化脂肪酶时表现出的涂层耐腐蚀性不同。当添加2%质量分数的固定化脂肪酶时,涂层防腐蚀效果最好,此时涂层可以维持48 h防腐特性,而单一环氧涂层下浸泡8 h后涂层阻抗值就发生明显下降。且复合涂层保护下的金属腐蚀率低于单一环氧涂层保护下的金属。
[1] XU X Q, MIAO J, BAI Z Q, et al. The corrosion behavior of electroless Ni—P coating in Cl-/H2S environment[J].Applied Surface Science, 2012, 258(22): 8802-8806.
[2] 伊帆, 李德豪, 郎春燕, 等. 炼油厂循环冷却水的腐蚀机理及缓蚀技术综述[J].广东石油化工学院学报, 2011, 21(6): 12-15. (YI Fan, LI Dehao, LANG Chunyan, et al. Review of erosive mechanism and inhibitory technology of circulating wastewater from oil refinery[J].Journal of Guangdong University of Petrochemical Technology, 2011, 21(6): 12-15.)
[3] ZHAO Q, WANG X. Heat transfer surfaces coated with fluorinated diamond-like carbon films to minimize scale formation[J].Surface and Coatings Technology, 2005, 192(1): 77-80.
[4] XU X Q, BAI Z Q, FANG Y R, et al. The influence of temperature on the corrosion resistance of 10#carbon steel for refinery heat exchanger tubes[J].Applied Surface Science, 2013, 280: 641-645.
[5] ZHAO X H, HAN Y, BAI Z Q, et al. The experiment research of corrosion behaviour about Ni-based alloys in simulant solution containing H2S/CO2[J].Electrochemical Acta, 2011, 56(22): 7725-7731.
[6] GOGOI P K, BARHAI B. Corrosion inhibition of carbon steel in open recirculating cooling water system of petroleum refinery by a multi-component blend containing zinc(II) diethyldithiocarbamate[J].Indian J Chem Technol, 2010, 17(4): 291-295.
[7] WILSON S A, JOURDAIN R P J, ZHANG Q I, et al. New materials for micro-scale sensors and actuators: An engineering review[J].Materials Science and Engineering: R: Reports, 2007, 56(1-6): 1-129.
[8] VOEVODINN N, GREBASCH N T, SOTO W S, et al. Potentiodynamic evaluation of sol-gel coatings with inorganic inhibitors[J].Surface and Coatings Technology, 2001, 140(1): 24-28.
[9] LIU S, GU L, ZHAO H, et al. Corrosion resistance of graphene-reinforced waterborne epoxy coatings[J].Journal of Materials Science & Technology, 2016, 32(5): 425-431.
[10] RAHMAN O U, KASHIF M, AHMAD S. Nanoferrite dispersed waterborne epoxy-acrylate: Anticorrosive nanocomposite coatings[J].Prog Org Coat, 2015, 80: 77-86.
[11] WANG H, JIANG Y, ZHOU L. Bienzyme system immobilized in biomimetic silica for application in antifouling coatings[J].Chin J Chem Eng, 2015, 23(8): 1384-1388.
[12] LIU F, ZHANG L, YAN X. Effect of diesel on corrosion inhibitors and application of bio-enzyme corrosion inhibitors in the laboratory cooling water system[J].Corrosion Science, 2015, 93: 293-300.
[13] 夏璐, 刘芳, 薛松, 等. 复合型杀菌剂对生物粘泥处理效果的研究[J].环境工程学报, 2011, 5(10): 2215-2220. (XIA Lu, LIU Fang, XUE Song, et al. Research on compound type biocides in biofouling control[J].Chinese Journal of Environment Engineering, 2011, 5(10): 2215-2220.)
[14] LU X H, LIU F, LU J J. The biological enzyme corrosion inhibitors in the circulating water system with diesel leak[J].Acta Petrolei Sinica (Petroleum Processing Section), 2013, 29(6): 1090-1095.
[15] YANG Y, BAI Y X, LI Y F, et al. Characterization of Candida rugosa lipase immobilized onto magnetic microspheres with hydrophilicity[J].Process Biochemistry, 2008, 43(11): 1179-1185.
[16] 孙伟, 尹桂来, 刘福春, 等. 装载缓蚀剂的纳米SiO2对环氧涂层耐腐蚀性的影响[J].中国腐蚀与防护学报, 2015, 35(5): 447-454. (SUN Wei, YIN Guilai, LIU Fuchun, et al. Influence of corrosion inhibitor carriered Nano-SiO2on corrosion resistance of epoxy coating[J].Journal of Chinese Society for Corrosion and Protection, 2015, 35(5): 447-454.)
[17] 龙涛, 冯其明, 卢毅屏. 六偏磷酸钠在硫化铜镍矿浮选中的分散机理[J].中国有色金属学报, 2012, 22(6): 1763-1769. (LONG Tao, FENG Qiming, LU Yiping. Dispersive mechanism of sodium hexametaphosphate on flotation of copper-nickel sulphide[J].The Chinese Journal of Nonferrous Metals, 2012, 22(6):1763-1769.)
[18] 童剑. 纳米浆料的制备及其在水性防腐涂料中的应用[D].广州: 华南理工大学, 2010.
[19] 周朋, 陶玉贵, 曹宁, 等. 纳米TiO2固载脂肪酶及其固载界面表征[J].安徽工程大学学报, 2014, 29(2): 9-12. (ZHOU Peng, TAO Yugui, CAO Ning, et al. Study of nano-TiO2immobilized lipase[J].Journal of Anhui Polytechnic University, 2014, 29(2): 9-12.)
[20] 徐勇. 环氧系纳米水性重防腐涂料的研究[D].长沙: 湖南农业大学, 2009.
[21] 雷青娟, 高保娇, 张正国. 阴离子型双功能含环氧基团酶固定化载体的制备及其固定辣根过氧化酶[J].过程工程学报, 2012, 12(5): 828-833. (LEI Qingjuan, GAO Baojiao, ZHANG Zhengguo. Preparation of anion-type bifunctional carrier with epoxy group and its immobilization of horseradish peroxidase[J].The Chinese Journal of Process Engineering, 2012, 12(5): 828-833.)
[22] 高伟. 纳米改性环氧防腐涂料的制备与性能评价[D].南充: 西南石油大学, 2012.
[23] 崔晓莉, 江志裕. 交流阻抗谱的表示及应用[J].上海师范大学学报(自然科学版), 2001, 30(4): 53-61. (CUI Xiaoli, JIANG Zhiyu. The plot formats and applications of electrochemical impedance spectroscopy[J].Journal of Shanghai Teachers University(Natural Science), 2001, 30(4): 53-61)
[24] 张鉴清, 曹楚南. 电化学阻抗谱方法研究评价有机涂层[J].腐蚀与防护, 1998, 19(3): 99-104. (ZHANG Jianqing, CAO Chunan. Study and evaluation on organic coatings by electrochemical impedance spectroscopy[J].Corrosion & Protection, 1998, 19(3): 99-104.)
Corrosion Resistance of Epoxy Resin Coating Modified by Lipase Immobilized on Nano-Silica
LÜ Yucui, JIANG Guofei, LIU Fang, WANG Yongqiang,LIU Chunshuang, SUN Juan, ZHAO Chaocheng
(CollegeofChemicalEngineering,ChinaUniversityofPetroleum,Qingdao266580,China)
The lipase was immobilized on nano-silca and used as a modifying agent for epoxy resin. The effect of modification was evaluated by measuring the enzyme activity, physical properties and corrosion inhibition of coatings. As a result, the activity of lipase reached 2300 U/g, the hardness of coating reached level two and the adhesive force reached level three. The resistance reached the highest and was significantly higher than unmodified epoxy resin when 2% mass fraction immobilized lipase was added, which indicated that the immobilized lipase improved corrosion inhibition of epoxy resin.
lipase; enzyme immobilization; nano-silica; epoxy coating; anticorrosive material
2016-09-07
中国石油大学(华东)拔尖人才资助项目和中国石油大学(华东)研究生创新工程项目(YCXJ2016039)资助
吕玉翠,女,硕士研究生,从事水污染控制及水资源回用方面的研究
刘芳,女,教授,博士,从事水污染控制及水资源回用方面的研究;Tel:0532-86980608;E-mail:liufangfw@163.com
1001-8719(2017)04-0684-09
TG179
A
10.3969/j.issn.1001-8719.2017.04.012

