低强度脉冲超声波在牵张成骨中对新生骨形成的实验研究
于乃超,任志勇,宋君,王辉,魏长月
(1.阳光融和医院 骨科,山东 潍坊 261000;2.中国人民解放军第89医院 全军创伤骨科研究所创伤骨科,山东 潍坊 261021)
Ilizarov外固定架由前苏联医学专家Gavriil Ilizarov于1952年在西伯利亚库尔干设计[1],该技术可用于解决骨折延迟愈合、骨矫形康复、肢体短缩等多个方面的难题。然而牵拉成骨技术也会产生一些令人头疼的临床问题,比如针道感染、术后护理程序繁琐、周期长、新生骨质量差以及再次骨折需重新手术内固定等弊端。在Ilizarov技术中,怎么保证截骨延长区的成骨质量及成骨速度,大量学者做了相关的实验研究。安全、有效地加快牵拉成骨的矿化进程成为该领域目前研究的热点和焦点。EI-Bialy等曾做过系列研究报道,骨再生、新生骨形成在经过系统的低强度脉冲超声波 (Low-Intensity Pulsed Ultrasound Stimulation,LIPUS)治疗后,具有显著的促进愈合作用。自上个世纪80年代,Duarte研究了多种超声频率信号对骨折愈合速度及新生骨形成质量的影响,结果证明所有对骨愈合有效的均为低强度脉冲超声波,并且证实了每天15 min低强度的治疗显著提高了骨折愈合部位的骨强度[2]。近年来国外创伤研究学者对LIPUS引起了高度重视,这方面的基础研究和临床实验取得一些进展,尽管国外有些学者研究超声治疗骨延长的临床效果,但是时间较短,多为4~6周[3,4],长时间的愈合情况随访结果以及生物力学方面的研究评价鲜有报道。
1 材料与方法
1.1 动物分组及材料
中国成年家兔60只,体重1.5~2.0 kg,雌雄不限,由菏泽医专动物实验室提供。采用标准化单笼饲养管理,统一饲料喂养,同等采光通风条件,自由饮水。随机分两组:实验组:低强度脉冲超声波治疗;对照组:不做干预。
低强度超声骨折治疗仪:Smith&Nephew低强度超声骨折治疗仪,其强度为30 mw/cm2,工作频率为1.5 MHz,脉冲宽度为200 μs,重复频率为l kHz。
1.2 动物模型的制作
动物禁食水,用常规脱毛剂将左小腿脱毛,测量左小腿初始长度,精确测量胫骨初始全长。无菌条件下进行,两组均采用氯胺酮肌注麻醉。麻醉起效后术区常规消毒铺单。取左胫前内侧入路,于左胫骨中上1/3处作纵行切口,依次切开,钝性分离胫前肌,将肌层牵向两侧予以保护,暴露胫骨。先在胫骨粗隆下约1.0 cm处纵向将胫前骨膜作一长约1.0 cm切口,在此平面向远近端适当游离,暴露胫骨,将线锯由腓侧穿入自胫侧穿出,在干骺端行骨膜外截骨。为了方便放入外固定架,暂时保留胫骨前外侧1/3骨皮质不被锯断以维持截面稳定性及下肢力线。将外固定架套入兔左下肢,分别在截骨面上下各1.0 cm处垂直打入两组平行克氏针,用双边外固定架固定。固定结束后将胫骨近端截骨面完全锯断,旋紧螺丝帽分别加压。在胫骨截骨线以远0.5 cm水平将腓骨截断,碘伏、生理盐水冲洗创口,缝合后包扎固定。术后连续5 d注射抗生素预防感染,于术后第8天起开始延长外固定架近端,2次/d,每次牵张0.5 mm,牵张总长度为1.0 cm(共牵张10 d),随后固定。骨牵张结束后固定期第2天,实验组行低强度脉冲超声波治疗;对照组则不予处理。
1.3 观察指标
X线摄片观察:分别于固定期第28天,第56天,第84天拍摄两组实验动物左侧胫骨全长X线片,仔细观察不同时相段延长区的成骨情况。
HE染色组织学检查:固定期第28天,第56天,第84天分别于两组中随机抽取8只实验动物,在牵张成骨区内取材,HE染色,光镜下观察组织学变化。
骨密度测定:于固定期第84天将两组处死的8只动物取标本,用Hologic QDR-2000双能X线骨密度仪(中国人民解放军第89医院实验中心)进行骨密度测定。
扭转实验:在固定期第84天,每组随机抽取8只行力学实验,测量最大扭矩,扭转角,计算抗扭强度及刚度:Tb(抗扭强度)=Mn(最大扭矩)/Wn(抗扭截面模量),GJP(抗扭刚度)=Mn·l(长度)/θ(扭转角)。
2 结果
2.1 X线摄片观察
固定期第28天:X线示两组延长区均可见少量模糊低密度骨痂影,实验组较对照组骨痂密度略高(图 1)。
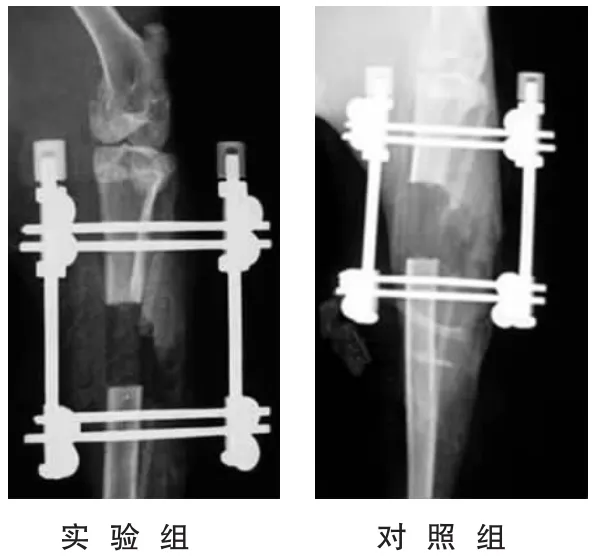
图1,2两组固定期第28天X线片

图3,4两组固定期第56天X线片

图5,6两组固定期第84天X线片

图7,8两组固定期第28天牵张间隙新生骨组织(HE 染色×100)
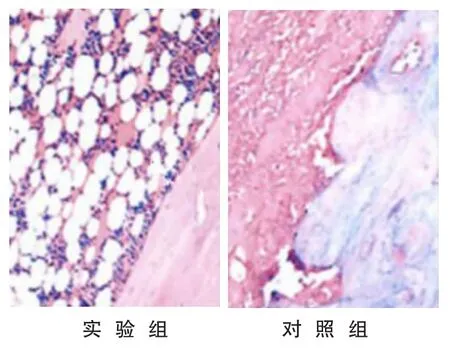
图9,10两组固定期第56天牵张间隙新生骨组织(HE 染色×100)

图11,12两组固定期第84天牵张间隙新生骨组织(HE 染色×200)
固定期第56天:X线示两组新骨密度及数量均增加并充填于整个延长区,延长区内出现少量纵行排列的条索状或片状新骨影,骨延长区新生骨骨痂影由截骨断端向中央生长,远近截骨断端有模糊的新生皮质骨征象。实验组较对照组放射状透光区减弱(图 2)。
固定期第84天:实验组髓腔通畅,骨折线消失,骨皮质完整,相比之下对照组骨折线稍显模糊,部分皮质骨发育不良(图3)。
2.2 HE染色观察
固定期第28天:对照组可见炎性细胞减少,破骨细胞减少;实验组可见炎性细胞减少,破骨细胞减少,少量纤维软骨骨痂形成(图4)。
固定期第56天:实验组较对照组软骨骨痂向骨性骨痂转变明显,骨细胞较肥大,钙盐沉积均匀(图5)。
固定期第84天:实验组新生骨组织主要以板层骨为主,骨痂形成改建过程成熟;对照组主要以编织骨为主,骨髓腔进一步改建,相对实验组落后(图6)。
2.3 骨密度测定
骨密度测定结果用SPSS 18.0统计程序在电子计算机上行统计学分析,实验组较对照组差异有显著性(P<0.05)。两组骨密度值排列顺序为:实验组>对照组(表1)。

表1 两组骨密度测试结果比较(配对t检验)
2.4 生物力学测试
在固定期第84天,每组随机抽取8只行力学实验,测量最大扭矩,扭转角计算抗扭强度及刚度。结果各项指标用SPSS 18.0统计程序在电子计算机上行统计学分析。实验组与对照组有统计学意义(P<0.05),实验组载荷强度较大(表2)。
实验结果的统计学分析,实验组的相对骨密度显著高于对照组(P<0.05),差别有统计学意义。说明超声治疗可以明显提高骨密度,促进骨折愈合。
表2 两组扭力测试结果比较±s)

表2 两组扭力测试结果比较±s)
Group Mn(kg·cm) Tb(g/mm2) GJP(gcm2/ 度) θ(度 /cm)(最大扭矩) (抗扭强度) (抗扭刚度) (单位长度扭转角)对照组 10.05±0.65 1543.54±10.62 3345.13±506.64 1.8630±0.25实验组 14.13±0.47 1924.23±11.19 5213.00±537.28 3.2066±0.26
3 讨论
3.1 低强度超声促进骨折修复的作用及其机制
超声波穿过和进入生物组织是由机械能量形式实现的,被作为诊断和治疗工具广泛应用于医学领域中。最新研究表明,当机械负荷在低能量(5microstrain)高频(30 Hz)的时候对骨组织可产生应答[5]。此外低强度脉冲超声波引起的机械负荷不能诱导正常骨产生适应性效应[6,7]。但迄今为止低强度脉冲超声波可促进骨折愈合及新生骨形成的生物学原理和机制仍不是很清楚。认为与超声波可能导致骨质中静态压力变化有关。本研究是LIPUS模型在兔下肢骨建立,操作并不复杂,但是也受能量限制和多方面参数影响。另外我们发现经过LIPUS治疗后BMP-2信使核糖核酸和蛋白质的表达增加,可以促进成骨作用和增强生物力学强度、刚度。实验证明可以增强成骨细胞活动及骨形成,此外,矿物附着率增加,类骨质厚度和小脂肪细胞表达显著增加,成骨细胞的活动以及骨组织分化,新骨生成和新生血管分化在骨愈合中发挥着重要作用。因此,加大LIPUS的应用能为现有的实验及研究提供更有力的说服力。
3.2 低强度脉冲超声对新生骨形成的影响
LIPUS能够显著促进骨延长区新骨形成和骨痂改建,当骨折或外伤导致的骨缺损后形成于骨折端的复合组织,在经过一系列的转变,直至恢复原有的强度、刚度。LIPUS还能够促进骨膜增生,形成骨膜新生骨,其X线上显示为骨皮质外面局限性或广泛性的层状、带状、放射状的高密度影。LIPUS能产生机械应力,它对骨的形成影响较大,反复承受高应力时,骨的大小、形状和结构可因机械应力的变化而改变,骨密度可以增加,反之骨量将减少。骨折愈合过程中,压应力和张应力将有助于骨的形成,而LIPUS能够持续缓慢地施加这种压力。除了促进骨折愈合外还可以检测骨痂形成,形成系统的评估参数,超声的传播速度对新生骨形成骨痂的反射性结构改变是最灵敏的。骨密度扫描仪和X射线分析结果表明骨矿物质沉积的情况,说明LIPUS可以促进新生骨形成的矿物质沉积以及骨痂塑形改建,被逐渐骨化是一个非常重要的进程,实验结果表明超声可以促进骨密度钙质沉积,并加速向正常骨密度恢复。
3.3 低强度超声治疗应用的研究进展
在过去的十多年中,大量的研究已经证实低强度脉冲超声波对于新鲜骨折、延迟愈合和骨不连不愈合以及大段骨质缺损 (如截骨术后)均能促进愈合。通过有效的超声波治疗,17 d即可恢复骨的正常功能,而对侧无超声波治疗恢复至正常骨的功能一般在损伤后的28 d左右[8]。Heckman等率先报道,利用低强度脉冲超声波治疗下肢骨折,与未经超声处理对照组相比,骨折愈合的平均时间缩短了58 d[9]。Kristiansen(克里斯坦森)等发现,与对照组相比,结合临床有效的低强度脉冲超声波治疗,能够使桡骨远端骨折的影像学和临床愈合时间平均缩短37 d[10]。近年来,Mayr(迈尔)等证实治疗舟状骨骨折运用低强度脉冲超声波可提前19 d治愈[11]。对这些临床实验结果进行比较,表明低强度脉冲超声波能使胫骨、桡骨和舟状骨骨折的临床愈合时间缩短30%~38%。LIPUS是一种非侵入的治疗方式,呈现低毒性、低免疫性,而且具有高度针对选择性,且在实验中可被反复使用,尽管LIPUS疗法已经广泛应用在医学等领域,比如外科手术和骨创伤修复,其潜在可用性仍在初始阶段,似乎LIPUS在骨组织的影响很好理解,但是文字资料仍匮乏。
许多研究已经表明,LIPUS有其独特的优势,这主要体现在以下几个方面:⑴超声波具有穿透性且不形成创伤,可进入和穿过生物组织,也可体外进行。⑵有效性:具有较好的临床效果,本实验可证实。⑶安全性:局部和全身治疗均无损害。⑷操作方便,操作时间短。除了以上应用外,低强度脉冲超声具有在运动损伤康复中的应用潜力。发现合适的超声频率、强度及范围,并采取相应的处理,将更大程度地发挥超声波的治疗作用,减少副作用,是实验研究的关键。治疗期间,单次持续时间不同的条件下,取得骨折愈合良好的效果才是推广超声的基础。超声促进骨折愈合的作用机制至今还不是很清楚,但这一结论和超声强度、频率、治疗方案是否有关,或合并有其他因素仍有待证实。自LIPUS首次被报道用于治疗骨不连、骨缺损成功案例之后并在临床应用,取得了一定疗效,治愈率显著提高。本研究的意义在于:⑴LIPUS可以促进骨折生物力学特性的恢复,在牵张成骨应用中可促进新生骨形成,提供了超声治疗的实验室依据。⑵为骨矫形、大段骨缺损、骨不愈合的治疗提供了一个新的方法。
[1]Kessler T,Winkler H,Weiss c,et a1.Ultrasound diagnosis of the elbow joint in fracture of the head of the radiusOrmopade(Germany)[J].Mar 2002,31(3),268-270.
[2]Allen MR,Hock JM,Burr DB.Periosteum:Biology,regulation,and response to osteoporosis therapies[J].Bone,2004,35(5):l003-1012.
[3]Reuter U,Strempel F,John F,et al.Modifocatlon of bone fracture healing by ultrasound in an animal experiment model[J].Z Exp Chir Transplant Kunstliche Organe,1984,17:290-297.
[4]Reuter U,Strempel F,John F,et al.Modification of bone fracture healing by ultrasonics in an animal model:Radioligic and histologic results[J].Z Exp Chir Transplant Kunstliche Organe,1987,20:294-302.
[5]Chang WH,Sun JS,Chang SP,et al.Study of the thermal effects of ultrasound stimulation on fracture healing[J].Bioelectromagnetics,2002,23:256-263.
[6]Heckman JD,Ryaby JP,McCabe J,et al.acceleration of tibial fracture-healing by non-invasive,low-intensity pulsed ultrasound[J].Bone Joint Surg Am,2004,76(1):26-34.
[7]Kristiansen TK,Rysby JP,McCabe J,et al.Accelerated healin of distal radius fractures with the use of specific,low-intensity ultrasound[J].J Bone Joint Surg Am,2007,79(7):961-973.
[8]Aynaci O,Onder C,Piskin A,et al.The effect of ultrasuound on the healing of muscle-pediculated bone graft in spinal fusion[J].Spine,2002,27(14):1531-1535.
[9]Rubbin C,Turner AS,Bain S,et al.Low mechanical.signals strengthen long bones[J].Nature,2001,412(6847):603-604.
[10]Warden SJ,Bennel KL,Forwood MR,et al.Skeletal effects of Iow-intensity pulsed ultrasound on the ovariectomized rodent[J].Ultrasound Med Biol,2001,27(7):989-998.
[11]Nyborg WL.Biological effects pf ultrasound:development.of safety guidelines,PartⅡ;general review[J].Ultrasound Med Biol,2001,27:301-333.

