玉米须药材质量标准研究*
王众宽,明孟碟,石 磊,杨红兵
(湖北中医药大学药学院,湖北 武汉 430065)
·实验研究·
玉米须药材质量标准研究*
王众宽,明孟碟,石 磊,杨红兵△
(湖北中医药大学药学院,湖北 武汉 430065)
目的 修订玉米须药材现有的质量标准。方法 观察玉米须药材的性状及显微特征,测定其水分、灰分、浸出物、多糖及木犀草素的含量。结果 在玉米须药材现有质量标准中,其性状特征需要修正,可增加显微鉴别、检查及含量测定等项目。结论 应更新有效的鉴别项目和内容,补充和完善玉米须药材的质量标准。
玉米须;质量标准;修订
玉米须,别名玉麦须、棒子毛等,为禾本科植物玉蜀黍 Zea maysL.的花柱和柱头[1]。玉米须入药始载于《滇南本草》,性平、味甘,主要活性成分为多糖、黄酮等[2-3],具有降血糖、降血压、利尿、利胆等作用,民间常用作治疗高血压、高血脂、糖尿病的辅助药物[4-8]。1977年版《中国药典(一部)》[9]及1992年版《卫生部药品标准·中药材(第一册)》[10]均有收录,含来源、性状、鉴别、性味、功能与主治、用法与用量、贮藏等项目。由于这些标准的内容比较简略,时间也比较久远,有必要重新修订,以适应市场经济发展的需要,保障临床用药的安全、有效。对此,本研究中观察了市售玉米须药材的性状及显微特征,并测定了其水分、灰分、浸出物、多糖及木犀草素的含量,现报道如下。
1 仪器与试药
1.1 仪器
Dionex P680型高效液相色谱仪(戴安中国有限公司);UV-1800型分光光度计(岛津企业管理有限公司);BM1000型生物显微镜(江南永新光学有限公司);AL104型电子分析天平(梅特勒-托利多仪器有限公司);DGB/20-002A型电热干燥箱(重庆银河试验仪器有限公司);SK250H型超声波清洗器(上海科导超声仪器有限公司)。
1.2 试药
玉米须药材10批,分别购自湖北蕲春、安徽亳州及重庆;木犀草素对照品(批号为PS1032-0025,成都普思生物科技有限公司);甲醇为色谱纯,水为娃哈哈纯净水,其余试剂均为分析纯。
2 方法与结果
2.1 性状特征观察
通过对10批玉米须药材的形状、长度、直径、颜色、表面特征、质地及气味等方面的特征进行细致观察、研判,同时对比观察玉米原植物及新鲜玉米须的外观性状,归纳出玉米须有以下性状特征:呈细长条形或须状,边缘被茸毛,常卷曲成团;完整者可长达30 cm,宽约0.5 mm;黄棕色至棕红色,柱头部位常呈黑褐色;质柔软;气微,味淡。
2.2 粉末显微特征观察
将玉米须药材打粉过4号筛,制作水合氯醛透化装片,置显微镜下观察。本品粉末呈黄棕色至棕褐色。非腺毛多列性,长约500 μm;花粉粒完整者呈类球形,多数干瘪呈不规则形;直径80~120 μm;单个萌发孔明显。环纹或螺纹导管较细,直径约10 μm,周围薄壁组织含棕色物质。详见图1。

图1 玉米须粉末特征
2.3 检查项目指标测定
依照2015年版《中国药典(一部)》方法,分别对10批玉米须药材的水分、总灰分和水溶性浸出物进行测定,结果见表1。根据测定结果,结合药材的生产、贮存与销售情况,拟订玉米须药材的水分不得超过14.0%,总灰分不得超过7.0%,水溶性浸出物不得少于8.0%。
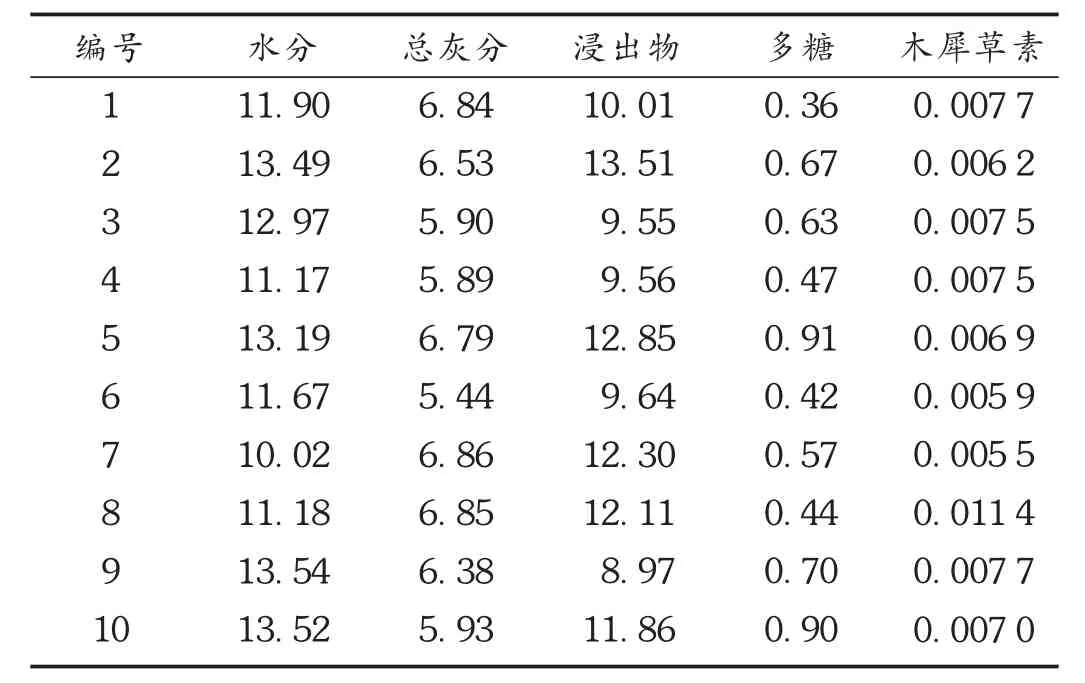
表1 玉米须样品水分、总灰分、浸出物及含量测定结果(%,n=10)
2.4 多糖含量测定
2.4.1 测定方法
采用硫酸-苯酚比色法测定。
2.4.2 葡萄糖贮备液及供试品溶液制备
葡萄糖贮备液:称取105℃干燥至恒重的葡萄糖50 mg,精密称定,加水溶解,并定容至50 mL,即得。
供试品溶液:取玉米须粉末(过3号筛)约1 g,精密称定,置圆底烧瓶中,加水30 mL,浸泡1 h,然后置水浴锅中冷凝回流1 h,趁热过滤,滤渣中加水30 mL,重复上述过程,提取2次合并滤液。所得滤液采用Seveg法[11]除去蛋白,离心,取上清液,加入活性炭脱色,置90℃水浴加热10 min,过滤,定容至250 mL,即得。
2.4.3 线性关系考察
精密吸取葡萄糖贮备液1,2,4,6,8,10 mL,分别置100 mL容量瓶中,加水至刻度,摇匀。精密吸取上述溶液1 mL,置10 mL具塞试管中,加入5%苯酚溶液1 mL,混合后迅速加入浓硫酸5 mL,摇匀,于40℃水浴30 min,在490 nm波长处测定吸光度。以溶液吸光度(X)为横坐标、质量浓度(Y)为纵坐标进行线性回归,得回归方程 Y=0.081 2 X+0.001 4,r=0.999 4(n=6)。结果表明,多糖质量浓度在0.01~0.10 g/L范围内与吸光度线性关系良好。
2.4.4 样品含量测定
精密吸取供试品溶液1 mL,分别置10 mL具塞试管中,加入苯酚溶液 1 mL,混合后迅速加入浓硫酸5 mL,摇匀,于40℃水浴30 min,在490 nm波长处测定吸光度,计算多糖含量,结果见表1。根据测定结果,结合药材的生产、贮存与销售情况,拟订玉米须药材多糖含量不得少于0.30%。
2.5 木犀草素含量测定
2.5.1 测定方法
采用高效液相色谱法测定。
2.5.2 色谱条件
色谱柱:Dionex C18柱(250 mm×4.6 mm,5 μm),流动相:甲醇-0.1%磷酸水溶液(55∶45);流速:1 mL/min;检测波长:254 nm;柱温:25℃;进样量:20 μL。
2.5.3 溶液制备
对照品溶液:称取木犀草素对照品适量,精密称定,加甲醇制成质量浓度为20 μg/mL的溶液,即得。
供试品溶液:取玉米须粉末(过3号筛)约3 g,精密称定,置具塞锥形瓶中,加入甲醇25 mL,称定质量,静置过夜,超声提取2 h,冷却后称定质量,用甲醇补足减失的质量,摇匀,过滤,取续滤液,即得。
2.5.4 方法学考察
线性关系考察:分别精密吸取木犀草素对照品溶液2,5,10,15,20 μL,注入液相色谱仪,测定木犀草素峰面积。以木犀草素进样量(μg,X)为横坐标,峰面积值(Y)为纵坐标进行线性回归,得回归方程 Y=1.062 1 X-0.101 3,r=0.999 4(n=5)。结果表明,木犀草素质量浓度在2.12~21.20 μg/mL范围内与峰面积线性关系良好。
精密度试验:精密吸取同一木犀草素对照品溶液20 μL,重复进样5次,测定木犀草素峰面积。结果的RSD=1.37%(n=5),表明仪器精密度良好。
稳定性试验:取同一供试品溶液,分别于0,2,4,6,8 h时各进样 20 μL,测定木犀草素峰面积。结果的RSD=1.80%(n=5),表明供试品溶液在8 h内稳定。
重复性试验:分别称取同批玉米须样品5份,约3 g,精密称定,按2.5.3项下方法制备供试品溶液,测定木犀草素峰面积,计算木犀草素含量。结果的 RSD=1.49%(n=5),表明方法重复性良好。
加样回收试验:分别称取已知含量的同批玉米须样品5份,约1.5 g,精密称定,加入对照品溶液适量,按2.5.3项下方法制备供试品溶液,测定木犀草素含量,计算加样回收率。结果平均加样回收率为98.95%,RSD=2.00%(n=5),表明方法回收率良好。
2.5.5 样品含量测定
分别称取不同批次的玉米须粉末约3 g,精密称定,按2.5.3项下方法制备供试品溶液,测定木犀草素含量,结果见表1。根据测定结果,结合药材的生产、贮存与销售情况,并参考文献[12],拟订玉米须药材木犀草素含量不得少于0.005 0%。
3 讨论
本研究中拟订的玉米须药材新质量标准中保留了现有质量标准中的所有项目,同时对现有标准的性状特征进行了修正,并增加了显微鉴别、检查(水分、灰分、浸出物)及含量测定(多糖、木犀草素)等项目,更切合实际,可有效引导药材的规范生产和交易。
性状特征的修订共有4处:1)药典描述玉米须“呈线状”,部标“呈绒状”,实际药材(花柱)除柱头部位卷曲呈须状以外,主体呈扁平的细长条形,明显有一定宽度;2)药典及部标描述玉米须“呈淡黄色至棕红色”,实际上只有部分药材样品带有少数淡黄色部分,且活性成分(黄酮类)含量深色(黄棕色至棕红色)玉米须较高,浅色玉米须(淡黄色)较低;3)药典及部标描述玉米须“柱头短,2裂”,实际上在药材柱头的分裂情况多无法分辨;4)药典及部标描述玉米须“味微甜”,实际药材并无甜味。
药典无鉴别项,部标则收载了理化鉴别(颜色反应),新标准增加了粉末显微特征。经反复观察,花粉粒与非腺毛(多列性)是玉米须粉末的主要显微特征,另外可见环纹或螺纹导管及其周围薄壁组织含有棕色物质。结果与文献[13]一致。
此外,本研究中试图用薄层色谱法对玉米须中黄酮类成分进行鉴别。参考文献[14],以甲醇为溶剂,分别采用超声提取法、索氏提取法,对玉米须供试品进行提取和浓缩,得供试品溶液;另取木犀草素、刺芒柄花素、芹菜素对照品,分别加甲醇制成每1 mL含0.5 mg的对照品溶液;照薄层色谱法[2015年版《中国药典(四部)》通则0502]试验,吸取对照品溶液5 μL、供试品溶液10~20 μL分别点于同一硅胶G薄层板上,以氯仿-甲醇(15∶1)为展开剂,展开,取出,晾干,喷以3%氯化铝溶液显色,晾干后置紫外光灯(365 nm)下检视;结果对照品显示黄色及蓝色荧光斑点清晰,但供试品溶液在与对照品溶液色谱相应位置上未见斑点。通过加大供试品取样量,提高供试品溶液浓度,以及加大点样量等,供试品溶液仍无斑点出现。结合含量测定结果,可认为玉米须中相关成分的含量低于薄层色谱法的检测限,故在新标准中不采用此鉴别方法。
在进行黄酮类成分的定量研究时,由于上述3种成分含量偏低,只有木犀草素的含量相对较高,重复性、稳定性及峰形也较好,故将木犀草素作为定量指标。
[1]江苏新医学院.中药大辞典(上册)[M].上海:上海人民出版社,1979:555.
[2]胡瑛瑛,楼肖成,郭 勇,等.玉米多糖的研究进展[J].安徽农学通报,2009,15(8):36-37.
[3]任顺成,丁霄霖.气相色谱-质谱法分析玉米须中的有机酸[J].无锡轻工学报,2003,22(6):89-91.
[4]陈艳军,高旭珍,关大勇,等.玉米须醇提物对肝纤维化大鼠药效学研究 [J].中国实验方剂学杂志,2012,18(11):195-199.
[5]杨灵玲,农绍庄,崔 瑾,等.玉米须多糖的降血糖作用研究[J].食品科技,2011,36(3):152-154.
[6]黄晓巍,王晓婷,衣春光,等.玉米须总黄酮对糖尿病合并心肌缺血大鼠血清中乳酸及糖化血红蛋白含量的影响[J].吉林中医药,2009,29(1):75-76.
[7]赵 强,赵二劳,赵 昀,等.玉米须中黄酮类化合物的抗氧化活性研究[J].食品工业,2011(1):36-38.
[8]郑鸿雁,闵伟红,昌友权,等.玉米须多糖调节免疫功能研究[J].食品科学,2004,25(10):291-293.
[9]中华人民共和国卫生部药典委员会.中华人民共和国药典(一部)[M].北京:人民卫生出版社,1978:126.
[10]中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准·中药材(第一册)[M].北京:人民卫生出版社,1992:25.
[11]周鸿立,张 艳,金海甲,等.玉米须多糖药理作用及提取纯化研究进展[J].吉林化工学院学报,2009,26(1):23-26.
[12]董金香,梁 东,丘智东.玉米须黄酮类成分的含量比较[J].中国药房,2012,23(11):1002-1004.
[13]吕晓琼.番红花及其伪品玉米须的鉴别[J].基层中医药杂志,1992,6(14):12-13.
[14]余婷婷,鲁晓翔,连喜军,等.玉米须黄酮类化合物的薄层层析及紫外光谱研究[J].食品科学,2008,29(11):477-481.
Quality Standard of Maydis Stigma
Wang Zhongkuan,Ming Mengdie,Shi Lei,Yang Hongbing
(School of Pharmacy,Hubei College of Traditional Chinese Medicine,Wuhan,Hubei,China 430065)
Objective To revise the existing quality standard of Maydis Stigma.Methods The characters and microscopic characteristics of Maydis Stigma were observed,and the contents of water,ash,extract,polysaccharide and luteolin were determined.Results In the existing quality standard ofMaydis Stigma,the characters and characteristics need to be revised,and the microscopic identification,inspection and content determination should be added.Conclusion The valid identification items and contents should be updated so as to supplement and perfect the quality standards of Maydis Stigma.
Maydis Stigma;quality standard;revision
R282.5
A
1006-4931(2017)14-0001-03
2017-03-10)
10.3969/j.issn.1006-4931.2017.14.001
湖北省食品药品监督检验研究院项目[2016湖北省中药材质量标准]。
王众宽(1994-),男,硕士研究生,研究方向为中药品种、质量与资源,(电话)027-68890106(电子信箱)1339418733@qq.com。
△通讯作者:杨红兵(1963-),男,教授,研究方向为中药品种、质量与资源,(电子信箱)yanghb321@126.com。

