CuO/ZnO纳米复合物的制备及其光催化脱汞的评价
周瑞兴, 张 静, 吴 江, 田 欢, 孙小明, 张文博, 张进京
(上海电力学院 能源与机械工程学院, 上海 200090)
CuO/ZnO纳米复合物的制备及其光催化脱汞的评价
周瑞兴, 张 静, 吴 江, 田 欢, 孙小明, 张文博, 张进京
(上海电力学院 能源与机械工程学院, 上海 200090)
采用均相沉淀法制备CuO/ZnO纳米金属氧化物光催化剂,并用X射线衍射、比表面积测试和紫外-可见漫反射光谱对其进行了表征.结果表明,CuO/ZnO纳米复合物的比表面积比纯ZnO的比表面积大,而且CuO/ZnO吸光强度增强,在可见光区域表现出微弱的吸收,说明CuO/ZnO纳米复合物出现了红移现象.研究表明,CuO/ZnO的掺杂摩尔比为0.2时光催化活性最好.另外,分析了CuO/ZnO的脱汞机理.
CuO/ZnO纳米复合物; 改性; 光催化
当前,全球因人为活动引起的汞排放总量每年约为2 000~6 000 t,其中中国每年汞排放量约为600 t,中国的能源和工业结构决定了约有50%以上的汞排放来自于煤的燃烧[1-2].汞的形态主要有元素态汞(Hg0)、氧化态汞(Hg2+)和颗粒态汞(HgP)3种[3].其中,元素态汞为主要形态.由于元素态汞性质较为稳定,易挥发、不溶于水,在生态环境中停留时间较长,较难除去,因而它对生态环境造成的污染已逐渐引起各国环保部门的重视.2011年,我国环保部门发布了新的火电厂大气污染物排放标准GB13223—2011,规定了燃煤机组汞及其化合物的排放量限制在0.03 mg/m3[4],限制燃煤工业的汞污染物排放已是大势所趋.
由于元素汞具有挥发性和不溶于水的特性,使得其很难利用电厂现有的设备进行脱除.目前,元素汞脱除的关键技术均是将元素态汞转化为易脱除的氧化态汞,其中光催化氧化法是一种新型的脱汞技术.金属氧化物是良好的光催化剂,在众多金属氧化物中氧化锌(ZnO)是近来的研究热点[5],它具有稳定的化学性质和量子尺寸效应,未来有望广泛应用于光催化氧化等领域.但ZnO属于n型宽禁带半导体氧化物,对光流子的利用率较低,因此光流子的利用率直接影响着ZnO的光催化效果.研究表明,掺杂不同类型金属氧化物形成的异质结结构可以改善金属氧化物的光流子利用率,从而提高金属氧化物的光催化氧化性能.因此,可选取p型窄宽带半导体金属氧化物与ZnO进行改性.由于氧化铜(CuO)既属于p型半导体,又是窄宽带半导体,所以选取CuO改性ZnO.
1 实验部分
1.1 实验仪器
制备CuO/ZnO样品所需主要实验仪器如表1所示.
1.2 实验试剂
制备CuO/ZnO样品所需的主要实验试剂为二水乙酸锌、一水乙酸铜和25%氨水.以上试剂的纯度均为分析纯,生产厂家为国药集团化学试剂有限公司.
1.3 样品制备
采用均相共沉淀法制备CuO/ZnO金属氧化物.首先,将80 mL乙酸锌(7 mmol)溶液和80 mL乙酸铜(7 mmol)溶液掺杂在250 mL烧杯中.然后,将10 mL氨水缓慢滴入上述混合溶液中,在水浴80 ℃下持续磁力搅拌2 h.反应中形成棕色沉淀,抽滤并用去离子水洗3次以除去其他杂质,并转移至烘箱中80 ℃烘干.将得到的粉末在马弗炉中350 ℃(加热速率为1 ℃/min)下煅烧2 h.然后,制备不同摩尔比例的CuO/ZnO纳米金属氧化物,摩尔比分别为0.01,0.02,0.1,0.2,0.5,1,2,根据CuO/ZnO的摩尔比分别命名为ZnO,0.01-CuO/ZnO,0.02-CuO/ZnO,0.1-CuO/ZnO,0.2-CuO/ZnO,0.5-CuO/ZnO,1-CuO/ZnO,2-CuO/ZnO和CuO.

表1 实验所需主要仪器
主要反应方程式为:
7Cu(CH3COO)2+7Zn(CH3COO)2+
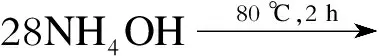
26CH3COO+26NH4++8H2O
(1)

6CuO/ZnO+6H2O
(2)

(3)
1.4 样品表征与测试
采用日本Rigaku公司Dmax-2550VBPC型X射线衍射仪(CuKα作为放射源,其波长为0.154nm,扫描速度为2°/min)测试样品的晶体结构.采用美国麦克仪器公司生产的ASAP2020型物理吸附仪测量比表面积.以高纯N2为样品的吸附气体,样品在100 ℃下脱气预处理5h,采用液氮温度(77.3K)下的N2吸附法测定比表面积和孔径分布.紫外可见吸收光谱采用日本Hitachi公司的U-3600型紫外光可见分光光度计测试,测试波长为250~1 000nm,将BaSO4作为对照标准.
1.5 光催化实验
元素汞的光催化氧化实验系统如图1所示.由气体汞系统、光催化反应器和汞分析装置3部分组成,所有的管路均采用特氟龙管.氮气分成两路,流量分别由两个质量流量控制器(CS200型)控制,总路流量控制在1.2L/min.其中一路气体作为载气进入U型玻璃管,气体流量为0.2L/min,将汞渗透管挥发出的元素汞携带出来,元素汞的挥发温度设定为50 ℃.另一路为主路气体,气体速度为1.0L/min,两股气体在混气罐中充分混合.从混气罐出来的气体经阀门的调节可分别进入光催化反应器和旁路,反应后的气体或旁路气体经过硅胶瓶吸水的干燥后,进入RA-915A型烟气在线测汞仪(俄罗斯LUMEX),以测定汞的气相浓度.最后,尾气经过吸收装置吸收过滤后排空.
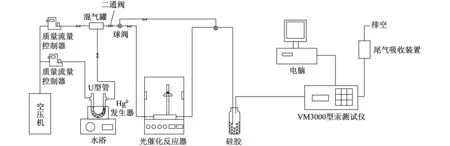
图1 元素汞光催化脱除实验系统示意
称取0.05 g样品,将其溶解在30 mL无水乙醇中,并用超声波震荡器处理20 min.并用注射器将震荡好的溶液均匀滴涂到玻璃片上,并在烘箱中烘干.重复以上步骤,直到将溶液全部用完.将涂覆有样品的玻璃片装入光催化反应器中,在320 nm波长的紫外灯照射下进行脱除元素汞的实验.
为了详细地阐述脱汞效果,实验中Hg0的脱除效率η定义如下:
(4)
式中:Cin——反应器进口浓度,μg/m3;Cout——反应器出口浓度,μg/m3.
光催化反应器如图2所示.光催化反应器是脱除烟气中汞的主体部分,该反应器为不锈钢腔体密封装置,由进气口、出气口、过渡区、反应区和石英玻璃透光窗口组成.反应区内置有物料架,高度为5 mm,用于放置负载有光催化剂的玻璃片.反应区上方为石英玻璃盖板,紫外光可穿过盖板到达催化剂表面.光源采用紫外灯管,灯管周围配置反光装置,使光能够均匀照射到反应区.

图2 光催化反应器示意
2 结果与讨论
2.1 X射线衍射分析
图3为CuO,ZnO,0.01-CuO/ZnO,0.02-CuO/ZnO,0.1-CuO/ZnO,0.2-CuO/ZnO,1-CuO/ZnO,2-CuO/ZnO光催化剂的X射线粉末衍射图谱.该图谱表明,最终制备的样品为CuO/ZnO混合金属氧化物.与标准卡片对比,CuO为单斜晶体(JCPDS file no.89-5895),ZnO的衍射峰能够与六方晶系ZnO(JCPDS file no.36-1451)的标准峰很好地吻合.CuO的(110)衍射峰(2θ≈32.73)在CuO/ZnO中向着小角度偏移,随着摩尔比的增大,偏移角度先变大后变小,在摩尔比为0.2时偏移角度最大.
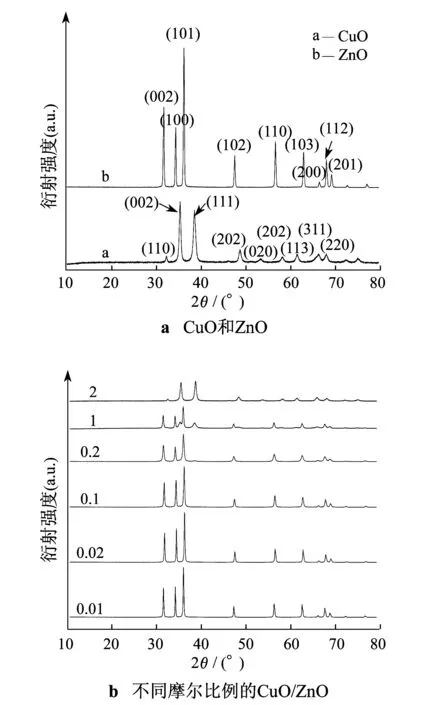
图3 不同光催化剂的X射线衍射图谱
2.2 紫外可见漫反射吸光光谱分析
图4为纯ZnO,CuO,CuO/ZnO金属氧化物的紫外可见光吸收光谱.
由图4可以看出,纯ZnO的特征吸收边界约为400 nm,CuO的特征吸收边界较广.掺杂了CuO的ZnO的光吸收强度随着掺杂摩尔比的增大而增强,而且在可见光区域光敏性增强,这说明掺杂CuO的ZnO出现了红移现象,可以响应可见光区域[6].这可能是由于CuO/ZnO异质结构的形成,降低了金属氧化物的费米能级,抑制了光流子的复合,从而增强了光催化性能.

注:图中数字为CuO/ZnO的摩尔比例.
图4 不同样品的紫外可见吸收光谱
2.3 BET分析结果
通过美国麦克研究级超高性能全自动气体吸附仪ASAP©2020 HD88测得不同样品的比表面积,如表2所示.由表2可以看出,纯ZnO在掺CuO后比表面积相对增大,在摩尔比为0.2时比表面积最大,这种差异可能是由CuO/ZnO金属氧化物微孔结构的形成所造成的.比表面积越大,则烟气与光催化剂的接触面积越大,而大的比表面积则会使催化剂的光催化反应效率提高[7],这也与最后的实验结果相吻合.

表2 不同样品的比表面积参数
2.4 光催化脱汞

由图5可以看出,在紫外光条件下,催化剂的脱汞效率分别为15.47%,12.98%,14.48%,34.19%,14.36%,57.4%,18.53%,12.45%,26.54%.CuO/ZnO摩尔比为0.2时,脱汞效果最佳.
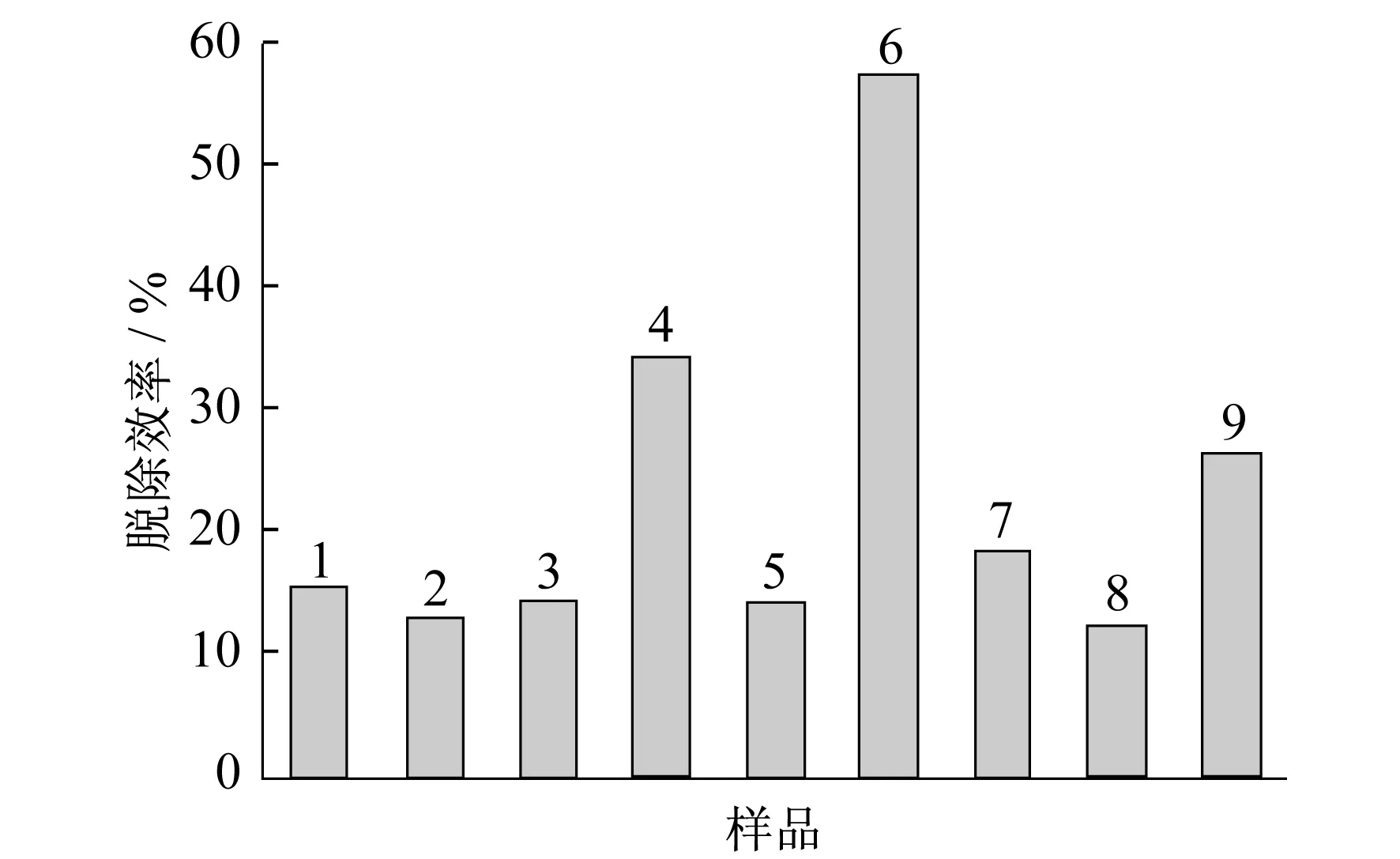
注:1—ZnO;2—CuO;3—0.01-ZnO/CuO;4—0.02-ZnO/CuO;5—0.1-ZnO/CuO;6—0.1-ZnO/CuO;7—0.5-ZnO/CuO;8—1-ZnO/CuO;9—2-ZnO/CuO.
图5 不同摩尔比例样品的脱汞效率
改性后的ZnO大大提高了光催化效果,主要是因为CuO/ZnO在其纳米复合物表面形成了异质结结构,阻碍了光生电子和空穴的复合,提高了光流子的利用率[8],如图6所示.

图6 CuO/ZnO异质结结构
光生电子从高电位的ZnO导带跃迁到低电位的CuO导带,而光生空穴则从CuO禁带跃迁至ZnO禁带,从而在很大程度上抑制了光流子的复合,提高了光催化效果.
光催化反应方程式如下[9-12]:

(5)
(6)
(7)
(8)
(9)
(10)
(11)
(12)
(13)
(14)
3 结 论
(1) 本文成功制备了不同摩尔比例的CuO/ZnO纳米复合物光催化剂,大大提高了ZnO的光催化性能.其中,CuO/ZnO摩尔比为0.2时光催化效果最佳.
(2) CuO/ZnO形成异质结结构,光生电子从ZnO的导带跃迁到CuO的导带,而光生空穴则从CuO的禁带跃迁至ZnO的禁带,从而在很大程度上抑制了光子的复合,提高了光流子的利用率,使光催化效果得到了改善.
[1] HE P,WU J,JIANG X M,etal.Mercury adsorption on sulfuric acid-impregnated carbonaceous surface:theoretical study[J].Surface review and letters,2014(21):1 142-1 143.
[2] CAI Y R,XU W F,WU J,etal.Experimental study of mercury releasing characteristics of coal fly ash under mild thermal condition[J].Advanced Materials Research,2012(424-425):1 258-1 261.
[3] GALE T K,LANI B W,OFFEN G R.Mechanisms governing the fate of mercury in coal fired power systems,fuel process[J].Techonol,2008(89):139-151.
[4] Ministry of Environmental Protection (MEP) of China.GB 13223-2011 Emission standard of air pollutants for thermal power plants[S].Beijing:MEP of China,2011:1-10.
[5] 张立德,方明.纳米颗粒材料研究的新进展[J].材料导报,2010(9):60-78.
[6] MOHAMED R M,AAZAM E S.Novel Ag/YVO4nanoparticles prepared by a hydrothermal method for photocatalytic degradation of methylene-blue dye[J].Journal of Industrial and Engineering Chemistry,2014(20):4 377-4 381.
[7] 倪补,李超恩,赵丽丽,等.YVO4基纳米光催化剂制备及其光催化脱汞性能评价[J].上海电力学院学报,2015(5):434-438.
[8] 张雯,张华集,彭亦如.TiO2半导体光催化剂的改性技术[J].福建师范大学学报:自然科学版,2005(4):113-123.
[9] YUAN Y,ZHANG J,LI H,etal.Simultaneous removal of SO2,NO and mercury using TiO2-aluminum silicate fiber by photocatalysis[J].Chemical Engineering Journal,2012(92):21-28.
[10] SJOTROM S,DURHAM M,BUSTARD C J,etal.Activated carbon injection for mercury control:overview[J].Fuel,2010,89(6):1 320-1 322.
[11] JIANG Y,ZHANG P,LIU Z,etal.The preparation of porous nano-TiO2with high activity and the discussion of the cooperation photocatalysis mechanism[J].Materials Chemistry and Physics,2006,99(2-3):498-504.
[12] WANG Z H,JIANG S D,ZHU Y Q,etal.Investigation on elemental mercury oxidation mechanism by non-thermal plasma treatment[J].Fuel Processing Technology,2010,91(11):1 395-1 400.
(编辑 白林雪)
Study on the Preparation of CuO/ZnO Nano Composite and its Photocatalytic Removal of Gas Mercury
ZHOU Ruixing, ZHANG Jing, WU Jiang, TIAN Huan, SUN Xiaoming, ZHANG Wenbo, ZHANG Jinjing
(SchoolofEnergyandMechanicalEngineering,ShanghaiUniversityofElectricPower,Shanghai200090,China)
CuO/ZnO nano metal oxide photocatalysis is prepared by homogeneous precipitation method,and is characterized by X-ray diffraction and ultraviolet visible diffuse reflectance spectroscopy.The results show that the special surface area of CuO/ZnO nano composites is larger than that of pure ZnO.The absorption intensity of CuO/ZnO is enhanced and CuO/ZnO shows a weak absorption in the visible light region,which indicates that the CuO/ZnO appears red shift.It is showed that the photocatalytic activity is the highest when the doping ratio of CuO/ZnO is 0.2,and the mercury removal mechanism of CuO/ZnO is analyzed.
CuO/ZnO nano composite; modification; photocatalytic
10.3969/j.issn.1006-4729.2017.03.015
2016-06-27
吴江(1974-),男,博士,教授,江苏建湖人.主要研究方向为污染物控制.E-mail:wjcfd2002@sina.com.
O643.36;X701.2
A
1006-4729(2017)03-0289-06

