N-[2-(2-吡啶基)-6-(1,2,4,5-四氢-3H-3-苯并氮杂卓-3-基)-4-嘧啶基]-β-丙氨酸的合成
田兆勇,徐博
(淮南师范学院,安徽 淮南 232038)
N-[2-(2-吡啶基)-6-(1,2,4,5-四氢-3H-3-苯并氮杂卓-3-基)-4-嘧啶基]-β-丙氨酸的合成
田兆勇,徐博
(淮南师范学院,安徽 淮南 232038)
以2-脒基吡啶盐酸盐为原料,通过成环、氯化、取代、水解反应,经过五步反应,合成了目标化合物,其结构经1H-NMR和MS确证。
2-脒基吡啶盐酸盐;抑制剂;氯化;取代;合成;表征
N-[2-(2-吡啶基)-6-(1,2,4,5-四氢-3H-3-苯并氮杂卓-3-基)-4-嘧啶基]-β-丙氨酸(GSK-J1)是一个高效和选择性的H3K27去甲基化酶抑制剂,抑制JMJ家族的去甲基化酶活性①Kruidenier L,etal.A selective jumonji H3K27 demethylase inhibitor modulates the proinflammatory macrophage response.Nature,2012,488(7411),pp.404-408.,体外对人源JMJD3的IC50值为60 nM。
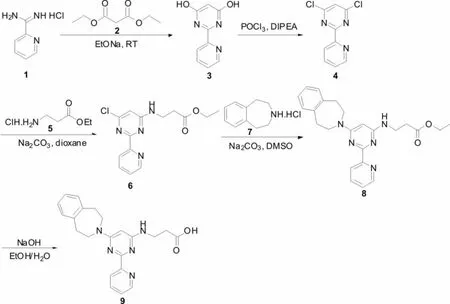
近年来,对该类抑制剂的合成鲜有报道。本文在已有文献工作的基础上,设计出一种操作简便易行的合成方法,合成目标产物。采用在新制的乙醇钠催化条件下,2-脒基吡啶盐酸盐(1)与丙二酸二乙酯(2)反应②Zhang,N.,Ayral-K.S.,Nguyen,T.,Hernandez,R.,Lucas,J.,Discafani,C.,Beyer,C.Synthesis and SARof 6-chloro-4-fluoroalkylamino-2-heteroaryl-5-(substituted)phenyl-pyrimidines as anti-cancer agents.Bioorganic and Medicinal Chemistry,Vol.17,No.1,2009,pp.111-118.Dürrenberger,F.,Burckhardt;Susanna,Geisser,Peter O.,Buhr,Wilm,Funk,Felix,Bainbridge,Julia M.,Corden,Vincent A.,Courtney, Stephen M.,Davenport,Tara,Jaeger,Stefan,Ridgill,Mark P.,Slack,Mark,Yarnold,Christopher J.,Yau,WeiT..Novel Pyrimidine-AndTriazine-HepcidineAntagonists.US2012/202806A1,2012.合成2-(吡啶-2-基)嘧啶-4,6-二醇(3),再进行氯化得到4,6-二氯-2-(2-吡啶)嘧啶(4)。在碳酸钠作用下,4,6-二氯-2-(2-吡啶)嘧啶与乙基-β-丙氨酸盐酸盐(5)亲核取代③Atkinson,Stephen J.,Barker,Michael D.,Campbell,Matthew,Humphreys,Philip,Liddle,John,Sheppard;Robert J.,Wilson D.N-2-(2-pyridinyl)-4-pyrimidinyl-beta-alanine derivatives as inhibitors of histone demethylase JMJD3.WO2012/52390A1,2012.,得到N-[6-氯-2-(2-吡啶基)-4-嘧啶基]-β-丙氨酸(6),该中间体在碳酸钠作用下与2,3,4,5-四氢-1H-3-苯并氮杂盐酸盐(7)④Fabrizio M.,Giorgio B.,Frank E.B.,Simone B.,Anna M.C.,Anna C.,Ornella C.,Federica D.,Romano D.F., Daniele D.,Gabriella G.,Andy G.,et al.1,2,4-Triazol-3-yl-thiopropyl-tetrahydrobenzazepines:A series of potent and selective dopamine D3receptor antagonists.J.Med.Chem.,2007,50,pp.5076-5089.亲核取代,得到乙基-N-[2-(2-吡啶基) -6-(1,2,4,5-四氢-3H-3-苯并氮杂卓-3-基)-4-嘧啶基]-β-丙氨酸(8)。最后,在氢氧化钠催化条件下,水解①得到目标化合物(9)。利用质谱、核磁氢谱等方法对其结构进行了表征。合成路线如下图。
1实验部分
1.1主要仪器与试剂
实验中用到的主要仪器:RE-522A型旋转蒸发仪(上海亚荣生化仪器厂);AL204型分析天平(梅特勒-托利多仪器(上海)有限公司);ZF-I型三用紫外分析仪(上海顾林电光仪器厂);安捷伦1260型HPLC;安捷伦7820A型GC;岛津2020型LC-MS;Bruker AVANCE 400MHz核磁共振仪(TMS为内标)。
实验所用化学试剂和生产厂家包括:乙醇钠(98%,安耐吉),2-脒基吡啶盐酸盐(98%,安耐吉),丙二酸二乙酯(AR,阿拉丁),三氯氧磷(AR,阿拉丁),N,N-二异丙基乙胺(AR,阿拉丁),乙基-β-丙氨酸盐酸盐(99%,阿拉丁),2,3,4,5-四氢-1H-3-苯并氮杂盐酸盐(97%,Sigma-Aldrich),碳酸钠(AR,阿拉丁),氢氧化钠(AR,江苏永丰化学试剂厂),二甲基亚砜(AR,上海晶纯试剂有限公司);其余所用试剂均为分析纯。
1.2 2-(吡啶-2-基)嘧啶-4,6-二醇(3)的合成
在250 mL三口烧瓶中分别加入无水乙醇(40 mL)和乙醇钠(2.76 g,40.56 mmol),室温搅拌全溶后,再慢慢向混合溶液中依次加入2-脒基吡啶盐酸盐(3.14 g,20 mmol)与丙二酸二乙酯(3.84 g,24 mmol),于室温下反应8 h。TLC点板确认反应完全后,向反应液中滴加1M冰盐酸,调节反应液pH= 5。减压浓缩除去有机溶剂得到棕黄色固体粗品3 (4.78 g,包含氯化钠固体)。未经纯化直接用于下一步反应。ESI-MS(negative):m/z 187.9[M-H]。
1.3 4,6-二氯-2-(2-吡啶)嘧啶(4)的合成
在2L三口烧瓶中,将化合物3(53.78 g,粗品)溶于甲苯(374 mL)溶液中,逐步降温至0℃,向其中依次滴加三氯氧磷(350 mL,3.76 mol)和N,N-二异丙基乙胺(254.9 mL,1.47 mol)。滴加完毕后升温至80℃,反应5 h。TLC点板确认反应完全后,减压蒸馏除去有机溶剂,倒入冰水(1200 mL)淬灭反应。乙酸乙酯萃取(3×1200 mL),分液,有机相分别用饱和碳酸钠溶液(1000 mL)和饱和食盐水(1000 mL)各洗涤一次,无水硫酸钠干燥,过滤,减压浓缩除去有机溶剂得到黄色固体粗品。柱层析纯化(洗脱剂:乙酸乙酯/石油醚=1:3),得到黄色固体4(56.41 g),纯度98.90%,收率87.67%。1H NMR(400 MHz,CDCl3): δ 8.86(d,J=4.68 Hz,1H),8.50(d,J=7.96 Hz, 1H),7.85(t,J=9.48 Hz,1H),7.45(t,J=3.84 Hz, 1H),7.41(s,1H)。ESI-MS(positive):m/z 226.2[M+ H]。
1.4 N-[6-氯-2-(2-吡啶基)-4-嘧啶基]-β-丙氨酸(6)的合成
室温条件下,在1L三口烧瓶中,将化合物4 (14.80 g,65.5 mmol)溶于1,4-二氧六环(150 mL)溶液中,向其中依次加入碳酸钠(34.60 g,327.5 mmol)和乙基-β-丙氨酸盐酸盐(16.61 g,108.03 mmol)。加料完毕后升温至70℃,反应6 h。TLC点板确认反应完全后,逐步降至室温,向反应液中依次加入水(300 mL)和二氯甲烷(300 mL)。萃取,分液,无水硫酸钠干燥,过滤,减压浓缩除去有机溶剂得到棕色油状物粗品。柱层析纯化(洗脱剂:乙酸乙酯/石油醚=1:1),得到棕色固体6(15.23 g),纯度99.24 %,收率76%。1H NMR(400 MHz,CDCl3):δ 8.75 (d,J=3.96 Hz,1H),8.39(d,J=7.76 Hz,1H),7.79 (t,J=7.40 Hz,1H),7.35(t,J=5.04 Hz,1H),6.37 (s,1H),5.93(s,1H),4.16-4.10(dd,J 1=7.08 Hz,J 2=6.44 Hz,2H),3.73-3.68(m,2H),2.63(t,J= 5.96 Hz,2H),1.23(t,J=7.16 Hz,3H)。ESI-MS (positive):m/z 307.2[M+H]。
1.5乙基-N-[2-(2-吡啶基)-6-(1,2,4,5-四氢-3H-3-苯并氮杂卓-3-基)-4-嘧啶基]-β-丙氨酸(8)的合成
室温条件下,在100mL三口烧瓶中,将化合物6(3.0 g,9.80 mmol)溶于二甲基亚砜(30 mL)溶液中,向其中依次加入碳酸钠(5.20 g,49 mmol)和2,3,4,5-四氢-1H-3-苯并氮杂盐酸盐(2.70 g,14.70 mmol)。加料完毕后升温至180℃,反应10 h。TLC点板确认反应完全后,逐步降至室温,向反应液中依次加入水(20 mL)淬灭反应。二氯甲烷萃取(3×30 mL),萃取,分液,无水硫酸钠干燥,过滤,减压浓缩除去有机溶剂得到棕黄色固体粗品。柱层析纯化(洗脱剂:二氯甲烷/甲醇=40:1),得到黄色固体8 (2.48 g),纯度99.30%,收率60.6%。1H NMR(400MHz,CDCl3):δ 8.77(d,J=3.92 Hz,1H),8.42(d,J= 7.92 Hz,1H),7.80(t,J=9.52 Hz,1H),7.34(t,J= 5.84 Hz,1H),7.33-7.14(m,4H),5.54(s,1H),4.17-4.14(dd,J 1=7.16 Hz,J 2=6.54 Hz,2H),3.95-3.93 (m,4H),3.64-3.60(m,2H),3.02-2.98(m,4H),2.66(t, J=6.64 Hz,2H),1.27(t,J=7.12 Hz,3H)。ESI-MS (positive):m/z 418.5[M+H]。
1.6 N-[2-(2-吡啶基)-6-(1,2,4,5-四氢-3H-3-苯并氮杂卓-3-基)-4-嘧啶基]-β-丙氨酸(9)的合成
在100 mL三口烧瓶中,依次加入乙醇(40 mL),水(10 mL),和化合物6(2.55 g,6.11 mmol),室温搅拌溶解,向反应液中加入氢氧化钠(244.4 mg, 6.11 mmol),室温反应12h。TLC点板确认反应完全后,减压浓缩除去乙醇,向反应液中滴加1M冰盐酸,调节反应液pH=5,反应液中析出固体,抽滤,55℃真空干燥6h,得到黄色固体目标化合物9(2.24 g),纯度99.46%,收率94.11%。1H NMR(400 MHz, d6-DMSO):δ 8.65(d,J=4.16 Hz,1H),8.23(d,J= 8.16 Hz,1H),7.87(t,J=7.88 Hz,1H),7.41(t,J= 7.12 Hz,1H),7.22-7.07(m,4H),6.81(s,1H),5.71 (s,1H),3.83-3.79(m,4H),3.51-3.48(m,2H),2.92-2.89(m,4H),2.52(t,J=6.84 Hz,2H)。ESIMS(positive):m/z 390.3[M+H]。
2结果与讨论
2.1 2-(吡啶-2-基)嘧啶-4,6-二醇的合成
一般文献报道嘧啶环的合成方法都是在有机碱的催化下,脒基与丙二酸二乙酯①Jun-ichi Tamura;Junko Nishihara.Synthesis of Phosphorylated and Sulfated Glycosyl Serines in the Linkage Region of the Glycosaminoglycans.J.Org.Chem.,2001,66,pp.3074-3083.Kuo-Long Yu;Bert Fraser-Reid. A novel reagent for the synthesis of myo-inositol phospates:N,N-diisopropyl dibenzyl phosphoramidite.Tetrahedron Letters,Vol.29,No.9,1988,pp.979-982.关环形成,但是因为底物反应活性的差异,副反应和收率会产生较大的差异。基于此,本文中采用高活性的有机碱,尽可能提高催化效率,提高产率,具有反应迅速、后处理简便等特点。
2.2 4,6-二氯-2-(2-吡啶)嘧啶的合成
氯化反应常用的氯化试剂包括氯气、氯化氢、次氯酸②Farard,J.,Loge,C.,Pfeiffer,B.,Lesur,B.,Duflos,M.Aconvenientsynthesisof5-arylamino-4H-pyran-4-onesusing palladium-catalyzedamination.TetrahedronLetters,2009,50(41),pp.5729-5732.、次氯化碳、光气(碳酰氯)③Jones J.D.,Bowden M.C.,Brown S.M.Process for the preparation of 4,6-dichloropyrimi-dine, US5750694 A1,1998.、硫酰氯、三氯化磷④Epple R.,Azimioara M.,Russo R.,Bursulaya B.,Tian S.,Gerken A.,Iskandar Maya.1,3,5-Trisubstituted aryls as highly selective PPAR agonists.Bioorganic and Medicinal Chemistry Letters,Vol.29,No.9,2006,16(11),pp. 2969-2973.、五氯化磷⑤Weber C.,Demeter A.;Greiner I.An efficient solid-phase synthesis of 2-alkyl-4,6-diaminopyrimidines and 2,4,6-triaminopyrimidines.Tetrahedron,Vol.62,No.10,2006,pp.2304-2312.、三氯氧磷⑥Allentoff A.J.,Lago M.W.,Ogan M.,Chen B.C.,Zhao R.l.,Iyer R.A.;et al.Synthesis of 14C-labeled and 13C-,15N-labeled dasatinib and its piperazineN-dealkyl metabolite.Journal of Labelled Compounds and Radiopharmaceuticals,Vol.51,No.1,2008,pp.41-47.等,一般都具有有毒、腐蚀性强、后处理复杂等特点。基于此,本文中在采用三氯氧磷的情况下,选择催化活性更高的N,N-二异丙基乙胺催化反应,加快反应速度,反应结束后减压蒸馏回收三氯氧磷,避免了后处理难题。
2.3氯代物与有机胺的亲核取代反应的讨论
氯代物与有机胺的亲核取代反应⑦Zdzis1aw B.,Jaros1aw S.,Daniela V.,Claudiu T.S.Carbonic anhydrase inhibitors.Regioselective synthesis of novel series 1-substituted 1,4-dihydro-4-oxo-3-pyridinesul-fonamides and their inhibition of the human cytosolic isozymes I and II and transmembrane cancer-associated isozymes IX and XII.European Journal of Medicinal Chemistry,pp.2012,56,282-291.Prathap R.M.,Rishi K.G.;Komal S.,Chilappa R.,Kolupula S., Durga P.M.,Surendar R.B.Anticancer siRNA delivery by new anticancer molecule:A novel combination strategy for cancer cell killingq.European Journal of Medicinal Chemistry,2012,56,pp.282-291.一般都是在碱的催化作用下进行,反应条件相对温和。碱的类型包括有机碱和无机碱,有机碱的催化活性相对较高,但无机碱的成本要低很多,本文中采用碳酸钠催化反应在保证催化效率的前提下,又很大程度上降低了工艺成本,提高了工艺放大的可能性。
2.4水解反应的讨论
酯水解的反应条件相对简单易行,酸碱都可以催化⑦反应进行。考虑到目标化合物自身结构的特殊性(含有易于酸成盐的游离胺基),本文中采用最常见的无机碱催化的方式进行,而且是定量反应,在保证反应进行程度的前提下,尽最大可能减少了产物损失,降低了工艺成本,从根本上提高了反应收率。
本文合成路线通过简便易行的合成方法,成功合成了一个高效和选择性的H3K27去甲基化酶抑制剂N-[2-(2-吡啶基)-6-(1,2,4,5-四氢-3H-3-苯并氮杂卓-3-基)-4-嘧啶基]-β-丙氨酸。另外,此方法也适用于合成其它的类似衍生物,并实现了工艺路线的低成本,提高了工业化生产的可能性。
The synthesis of N-[2-(2-pyridinyl)-6-(1,2,4,5-tetrahydro-3H-3-benzazepin-3-yl)-4-pyrimidinyl]-β-alanine
TIAN Zhaoyong,XU Bo
With2-amidino-pyridinehydrochlorideastherawmaterial,throughcyclization, chlorination,substitution,and hydrolysis reaction,the target compound was synthesized,and its structure was characterized by 1H-NMR and MS.
Pyridine-2-carboximidamide hydrochloride;inhibitor;chlorination;substitution;synthesis; characterization
O621.3
A
1009-9530(2017)03-0095-04
2016-06-24
田兆勇(1980-),男,淮南师范学院助教。徐博(1972-),男,淮南师范学院实验师。

