HPLC 法测定D-色氨酸甲酯盐酸盐中的左旋异构体
夏星雅, 韩承刚, 郑 枫
他达拉非是环磷酸鸟苷特异性磷酸二酯酶5(PDE5)的选择性可逆抑制剂[1-2], 可用于治疗男性勃起功能障碍(Erectile Dysfunction, 简称ED)和肺动脉高压等疾病[3-4]。 当性刺激导致局部释放一氧化氮时, PDE5 受到他达拉非抑制, 使阴茎海绵体内环磷酸鸟苷(cGMP)水平提高, 可导致平滑肌松弛, 血液流入阴茎组织, 产生勃起[5-7]。 此外, 他达拉非也可通过减少cGMP 的降解而舒张肺动脉血管平滑肌, 降低肺血管阻力[8]。 他达拉非作为目前世界上公认的最有效的ED 治疗特效药之一, 在治疗ED 人群中的表现已远远超过其他同类型的药物, 具有很强的市场优势。 调查显示, 该产品化合物专利于2015 年到期, ED 适应症专利2020 年到期, 工艺专利将于2023 年到期[4,9], 所以研发突破专利的新工艺成为目前仿制药的研究热点, 这对于他达拉非仿制药尽快在中国上市具有重要的价值, 因此, 在他达拉非合成工艺中对其的质量控制与杂质研究也是不可或缺。
D-色氨酸甲酯盐酸盐作为合成他达拉非原料药的起始物料之一(常用合成路线见图1), 在制备过程中, 会引入其左旋异构体杂质L-色氨酸甲酯盐酸盐[10-12](结构式见图2), 且会伴随合成工艺路线存在而产生影响他达拉非质量的副产物。 药物中异构体杂质如果控制不当, 可能会产生临床隐患[13], 因此,在药物的生产过程中, 采用合适的分析方法对异构体杂质进行控制非常重要[14]。 目前作者未见D-色氨酸甲酯盐酸盐与其左旋异构体分离与分析的相关报道, 本文建立了一种手性高效液相色谱方法对D-色氨酸甲酯盐酸盐中L-色氨酸甲酯盐酸盐进行分离与检测, 该方法具有良好的分离效果及重现性, 能从源头上对他达拉非的质量进行控制。

图1 他达拉非常用合成路线Fig.1 Common synthetic route of Tadalafil
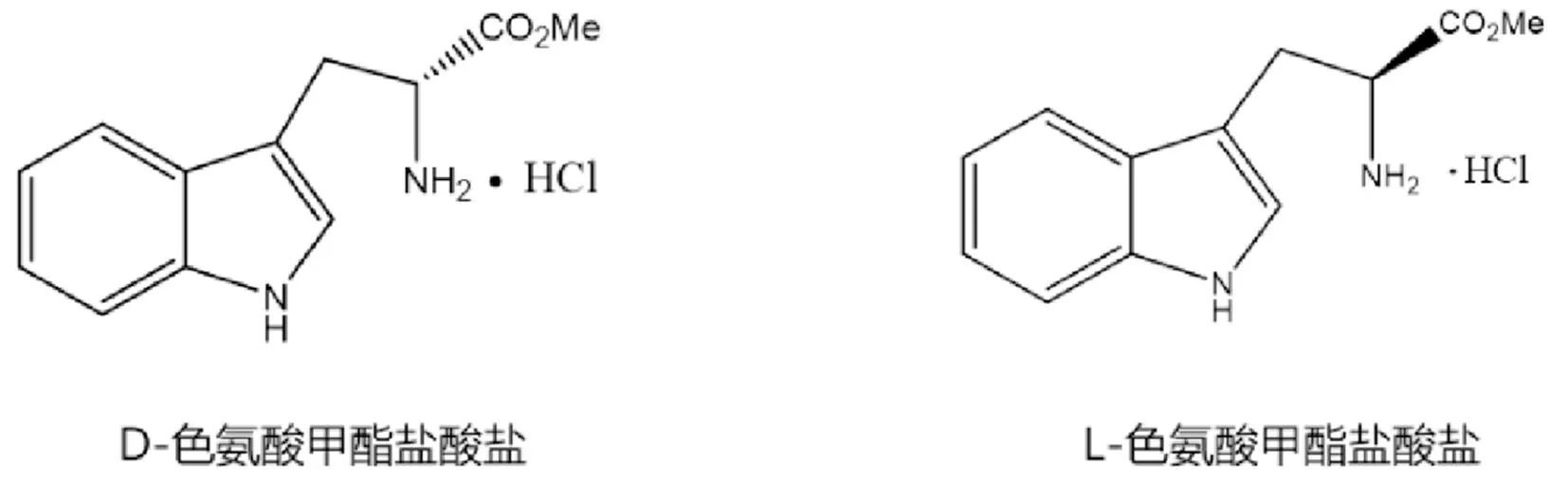
图2 D-色氨酸甲酯盐酸盐及其左旋异构体的化学结构式Fig.2 Structure of D-tryptophan methyl ester hydrochloride and its L-isomer
1 仪器与试药
1.1 仪 器
LC-20AT 高效液相色谱仪(SPD-M20A 紫外检测器、LabSolutions 色谱工作站), 日本岛津有限公司; SQP 电子分析天平(d=0.01 mg), 德国赛多利斯公司。
1.2 试 药
D-色氨酸甲酯盐酸盐对照品(批号: 5ARP981, 纯度:98.00%), 加拿大TRC; L-色氨酸甲酯盐酸盐对照品(批号:13ABY1521, 纯度: 99.27%), 加拿大TRC; D-色氨酸甲酯盐酸盐供试品(批号: 010327-2020011201), 四川同晟生物医药有限公司; 正己烷(批号: 20210406, 纯度: 色谱纯), 永华化学股份有限公司; 无水乙醇(批号: E2107166, 纯度: 色谱纯), 阿拉丁; 二乙胺(批号: L17005094, 纯度: 色谱纯), 阿拉丁。
2 方法与结果
2.1 色谱条件
色谱柱: EnantioPak Y5 色谱柱(4.6×250 mm, 5 μm); 流动相: 正己烷(含0.1%二乙胺): 无水乙醇=80∶20(V/V);流速: 1.0 mL·min-1; 检测波长: 280 nm; 柱温: 25 ℃; 进样量: 10 μL。
2.2 溶液配制
2.2.1 D-色氨酸甲酯盐酸盐储备液
精密称取D-色氨酸甲酯盐酸盐对照品10 mg, 置于10 mL量瓶中, 加乙醇溶解并稀释至刻度, 摇匀, 即得浓度约为1.0 mg·mL-1的D-色氨酸甲酯盐酸盐储备液。
2.2.2 L-色氨酸甲酯盐酸盐储备液
精密称取L-色氨酸甲酯盐酸盐对照品10 mg, 置于10 mL量瓶中, 加乙醇溶解并稀释至刻度, 摇匀, 即得浓度约为1.0 mg·mL-1的L-色氨酸甲酯盐酸盐储备液。
2.2.3 L-色氨酸甲酯盐酸盐工作溶液
精密移取 “2.2.2” 项下L-色氨酸甲酯盐酸盐储备液2.5 mL, 置于50 mL 量瓶中, 加乙醇稀释至刻度, 摇匀, 即得浓度约为50 μg·mL-1的L-色氨酸甲酯盐酸盐工作溶液。
2.2.4 混合对照工作溶液
精密移取“2.2.1” 和“2.2.2” 项下D-色氨酸甲酯盐酸盐与L-色氨酸甲酯盐酸盐储备液各2.5 mL 至同一50 mL 量瓶中, 加乙醇稀释至刻度, 摇匀, 即得浓度约为50 μg·mL-1的混合对照工作溶液。
2.2.5 L-色氨酸甲酯盐酸盐对照溶液
精密移取“2.2.3” 项下L-色氨酸甲酯盐酸盐工作溶液1.0 mL, 置于10 mL 量瓶中, 加乙醇稀释至刻度, 摇匀, 即得浓度约为5.0 μg·mL-1的L-色氨酸甲酯盐酸盐对照溶液。
2.2.6 混合对照溶液
精密移取“2.2.4” 项下混合对照工作溶液1.0 mL, 置于10 mL 量瓶中, 加乙醇稀释至刻度, 摇匀, 即得浓度约为5.0 μg·mL-1的混合对照溶液。
2.2.7 D-色氨酸甲酯盐酸盐供试品溶液
精密称取D-色氨酸甲酯盐酸盐供试品(批号: 010327-2020011201)10 mg, 置于10 mL 量瓶中, 加乙醇溶解并稀释至刻度, 摇匀, 即得浓度约为1.0 mg·mL-1的D-色氨酸甲酯盐酸盐供试品溶液。
2.2.8 系统适用性溶液(供试品加样溶液)
精密称取D-色氨酸甲酯盐酸盐供试品(批号: 010327-2020011201)10 mg, 置于10 mL 量瓶中, 精密移取“2.2.3”项下L-色氨酸甲酯盐酸盐工作溶液1.0 mL, 加乙醇溶解并稀释至刻度, 摇匀, 即得系统适用性溶液。
2.3 系统适用性和专属性
取空白溶剂(乙醇)、 L-色氨酸甲酯盐酸盐对照溶液、 混合对照溶液, 供试品溶液和系统适用性溶液各10 μL 依次进样分析, 记录色谱图, 结果见图3。 空白溶剂和D-色氨酸甲酯盐酸盐供试品均不干扰L-色氨酸甲酯盐酸盐的测定; 各色谱图中D-色氨酸甲酯盐酸盐色谱峰与L-色氨酸甲酯盐酸盐的分离度均大于1.5, 符合要求。

图3 系统适用性和专属性HPLC 色谱图Fig.3 HPLC chromatograms of system suitability and specificity test
2.4 检测限和定量限试验
取“2.2.4” 项下混合对照工作溶液逐级稀释后进样分析,以信噪比约为3∶1 和10∶1 的溶液浓度作为D-色氨酸甲酯盐酸盐及其左旋异构体的检测限与定量限。 结果得L-色氨酸甲酯盐酸盐的检测限浓度为0.4964 μg·mL-1(0.05%), 定量限浓度为0.9927 μg·mL-1(0.1%),D-色氨酸甲酯盐酸盐的检测限浓度为0.4920 μg·mL-1(0.05%), 定量限浓度为0.9839 μg·mL-1(0.1%)。 取定量限对应浓度溶液连续进样6 针, L-色氨酸甲酯盐酸盐峰面积RSD 为3.45%, D-色氨酸甲酯盐酸盐峰面积RSD 为3.40%。
2.5 线性试验
精密移取 “2.2.4” 项下混合对照工作溶液0.2、 0.5、0.8、 1.0、 1.5 和3.0 mL, 分别置于六个10 mL 量瓶中, 加乙醇稀释至刻度, 得系列浓度混合对照溶液, 取上述线性测试溶液各10 μL 依次进样分析, 记录色谱图, 以峰面积为纵坐标,浓度为横坐标绘制标准曲线, 进行线性回归, 结果见表1。 同时计算得出L-色氨酸甲酯盐酸盐得校正因子为1.03, 在0.9 ~1.1 范围内。

表1 线性试验结果Table 1 Results of linearity test
2.6 进样精密度与重复性试验
按“2.2.6” 项下方法配制浓度约为5.0 μg·mL-1混合对照溶液。 取上述溶液10 μL 连续进样6 次, L-色氨酸甲酯盐酸盐和D-色氨酸甲酯盐酸盐峰面积的RSD 分别为1.25%、1.41%; 保留时间的RSD 分别为0.07%和0.07%, 进样精密度良好。 另按“2.2.8” 项下方法平行配制六份含杂质L-色氨酸甲酯盐酸盐约5 μg·mL-1的D-色氨酸甲酯盐酸盐供试品加样溶液, 取上述溶液各10 μL 进样分析, 得L-色氨酸甲酯盐酸盐含量的RSD 为1.42%(n=6), 表明方法重复性良好。
2.7 稳定性试验
按“2.2.5”、 “2.2.7” 和“2.2.8” 项下方法分别配制L-色氨酸甲酯盐酸盐对照溶液、 D-色氨酸甲酯盐酸盐供试品溶液和供试品加样溶液, 于室温放置0 h、 2 h、 4 h、 6 h、 8 h 和12 h 后, 分别进样分析, 对照溶液中L-色氨酸甲酯盐酸盐峰面积变化率低于3.64%(<10.0%); 供试品和供试品加样溶液中L-色氨酸甲酯盐酸盐含量的变化率分别低于7.04% 和2.33%(<10.0%), 表明上述各溶液在12 h 内稳定。
2.8 准确度试验
取D-色氨酸甲酯盐酸盐供试品9 份, 每份约10 mg, 置于10 mL 量瓶中, 用适量乙醇溶解, 分为三组, 每组分别加入0.2、 1.0 和1.5 mL “2.2.3” 项下L-色氨酸甲酯盐酸盐工作溶液, 乙醇稀释至刻度, 摇匀即得每组三份的定量限准确度、100%准确度和150%准确度溶液; 另按“2.2.5” 项下方法配制L-色氨酸甲酯盐酸盐对照溶液, 按“2.2.7” 项下方法平行配制两份D-色氨酸甲酯盐酸盐供试品溶液。 取上述溶液10 μL分别进样分析, 结果见表2, 该方法准确度良好。
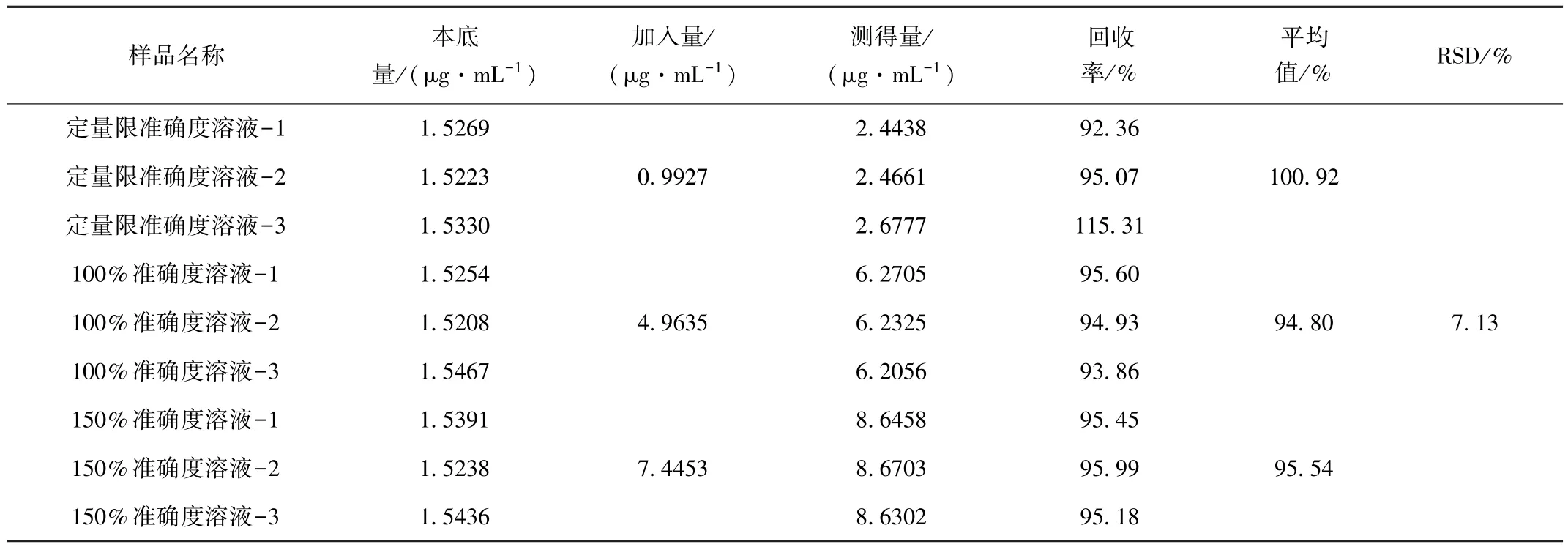
表2 准确度试验结果Table 2 Results of recovery test
2.9 耐用性考察试验
在柱温(±2 ℃)、 流速(±0.1 mL·min-1)、 流动相比例(±2%)的范围内变动色谱条件, 按“2.2.5” 和“2.2.8” 项下配制L-色氨酸甲酯盐酸盐对照溶液与系统适用性溶液, 分别在不同条件下进样分析, 结果表明, 各组分色谱峰与相邻峰之间的分离度符合要求(>1.5), 系统适用性溶液中L-色氨酸甲酯盐酸盐的含量在不同条件下与原条件相比变化率低于2.54%(<10.0%), 该方法耐用性良好。
2.10 样品检测
取D - 色氨酸甲酯盐酸盐供试品(批号: 010327 -2020011201), 按“2.2.7” 项下方法配制供试品溶液, 另按“2.2.5” 项下配制L-色氨酸甲酯盐酸盐对照溶液。 取上述溶液10 μL 分别进样分析, 结果表明D-色氨酸甲酯盐酸盐供试品(批号: 010327-2020011201)中含有0.17% L-色氨酸甲酯盐酸盐异构体杂质, 未超过0.5%限度。
3 讨 论
3.1 色谱柱的筛选
采用多糖衍生物正相涂敷型CHIRALPAK AD-H 手性色谱柱、 键合型CHIRAL ART Cellulose-SZ 手性色谱柱和多糖衍生物反相涂敷型CHIRALCEL OJ-RH 手性色谱柱, 不同流动相及配比, 均未能达到D-色氨酸甲酯盐酸盐与其左旋异构体的分离。 但EnantioPak Y5(硅胶表面涂敷有纤维素-三(3-氯-4-甲基苯基氨基甲酸酯))手性色谱柱可以有效分离分析D-色氨酸甲酯盐酸盐中的L-色氨酸甲酯盐酸盐, 故选用EnantioPak Y5色谱柱(4.6 mm×250 mm, 5 μm)为本实验的手性分析柱。
3.2 溶剂的选择
色氨酸甲酯盐酸盐在正己烷、 异丙醇及乙腈中均不溶, 而在水、 甲醇和乙醇中有较好的溶解度。 由于在正相手性色谱柱上进行分离, 水和甲醇不适用于该体系, 故经过优化后选用乙醇作为溶剂。
3.3 检测波长的选择
本实验采用DAD 检测器对D-色氨酸甲酯盐酸盐和L-色氨酸甲酯盐酸盐在190 ~800 nm 波长进行紫外光谱扫描, 结果表明待测物在222 nm 和280 nm 左右具有最大吸收。 由于在222 nm 波长下, 基线不平稳影响测定, 故选择280 nm 为最终检测波长。
3.4 流动相的选择
由于色氨酸甲酯盐酸盐结构中含有氨基, 可以加入少量胺类添加剂二乙胺进行调节。 当流动相仅为正己烷-乙醇而无碱性调节剂时, 两对映体难以洗脱分离, 因此最终选择正己烷-乙醇-二乙胺流动相体系, 可有效改善待测物峰形及分离度。
4 结 论
本文建立了一种测定D-色氨酸甲酯盐酸盐中L-色氨酸甲酯盐酸盐的手性高效液相色谱法。 该方法分离度、 灵敏度和耐用性良好; 经过方法学验证, 表明该方法可以用于他达拉非起始物料D-色氨酸甲酯盐酸盐中左旋异构体杂质的质量研究。

