双柏膏微生物限度检查方法适用性试验
钟柳芳 肖文可 孙树周 温颖婉
·实验研究·
双柏膏微生物限度检查方法适用性试验
钟柳芳 肖文可 孙树周 温颖婉
目的建立双柏膏的微生物限度检查方法, 并进行适用性实验。方法按照中国药典(2015年)对双柏膏进行微生物限度检查适用性试验。双柏膏可溶于十四烷酸异丙酯, 溶解后薄膜过滤,并在水相冲洗液中加入乳化剂聚山梨酯80, 控制菌检查采用薄膜法。结果需氧菌总数计数、真菌和酵母菌总数计数适用性实验中的回收率比值均在 0.5~2 内, 控制菌生长良好, 符合《中国药典》2015年版规定。结论该方法有效可行, 可用于双柏膏的微生物限度检查。
双柏膏;微生物限度;适用性试验;薄膜过滤
双柏膏是广州市番禺区中医院制剂, 处方来源于85年版医院制剂规范中的双柏膏。处方主要成分为黄柏、侧柏叶、冰片、凡士林组成的一种外用中药复方膏剂, 具有清热、消炎、祛瘀、止痛的功效[1-3]。临床上用于跌打损伤、疮痛肿毒、消炎等症, 是现代骨伤科中药治疗的主要药物。为了提高双柏膏质量标准, 更准确地反映该制剂质量真实状况, 确保医院制剂的用药安全, 本文根据《中国药典》2015年版四部[3]微生物限度检查法中的相关规定, 双柏膏微生物限度检查法进行了重新修订并进行了适用性试验。在适用性试验过程中,发现该制剂处方中黄柏[1]、侧柏叶[2]、冰片[3]对微生物限度检查造成严重干扰, 常规平皿法、稀释法检查需氧菌总数计数真菌和酵母菌总数计数适用性实验中的回收率比值均不在 0.5~2 内。利用双柏膏可溶于十四烷酸异丙酯后, 置于在含有0.5%的吐温80的pH=7.0无菌蛋白胨-氯化钠缓冲液至100 ml分液漏斗中充分振摇、萃取, 静置, 取下层液作为(1∶10)供试液, 用薄膜过滤法可以有效地去除抑菌成分, 达到满意的效果, 现对研究作如下汇报分析。
1 仪器与材料
1.1 仪器 全自动电热压力蒸汽灭菌器(型号:YM30Z, 上海三申医疗设备公司);霉菌培养箱(型号:LRH-150, 上海一恒科学仪器有限公司);生化培养箱(型号:SPX-150B, 上海悦丰仪器表有限公司);电热恒温水浴箱WBK-4A, 广东环凯微生物科技有限公司);无菌检查仪(型号:WJ-6, 天津市罗根科技有限公司);快速混合仪(型号:SZ-1, 江苏金坛市金城国胜实验仪器厂);生物安全柜(型号:BHC-1300ⅡA2,苏净集团苏册安泰空气技术有限公司)。
1.2 供试药品 双柏膏(批号:20160911、201601007、20161116,广州市番禺区中医院制剂室)。
1.3 培养基 胰酪大豆胨琼脂培养基(批号:20160816)、沙氏葡萄糖琼脂培养(批号31105120)、胰酪大豆胨液体培养基(TSB)(批号:3104880)、甘露醇氯化钠琼脂培养基(批号:3102307)、pH=7.0无菌氯化钠蛋白冻缓冲液(3104875)、溴化十六烷基三甲铵琼脂培养基(批号:3104874), 以上培养基均由广东环凯微生物科技有限公司生产, 均按照《中国药典》2015版第四部通则有关规定配制并验证。
1.4 菌株 金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌和白色念珠菌均由中国医学细菌保藏中心提供, 黑曲霉由中国药品生物制品检定所提供, 用于菌液制备的工作菌株均为第3代。
1.5 方法
1.5.1 菌液的制备 按照中国药典 2015 年版要求, 将金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌分别接种于新鲜培养物, 然后至胰蛋白胨大豆肉汤培养基(TSB)中, 金黄色葡萄球菌、铜绿假单胞菌的TSB于33℃环境中培养 18 h;枯草芽孢杆菌的TSB在33℃环境中培养 24 h;接种白色念珠菌的新鲜培养物至沙氏葡萄糖液体培养基中, 23℃环境中培养48 h(菌液a)。用 0.9%无菌氯化钠溶液将金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌、枯草芽孢杆菌的培养物制成每1 ml含菌数≤100 cfu 的菌悬液。接种黑曲霉的新鲜培养物培养 120 h, 用 5 ml 0.9%无菌氯化钠溶液(含 0.05%聚山梨酯 80)将孢子洗脱, 再用无菌毛细吸管吸出孢子悬液至无菌试管内, 用含 0.05%聚山梨酯 80 的0.9%无菌氯化钠溶液制成孢子悬液(每 1 ml含孢子数≤100 cfu)。
1.5.2 供试液制备
1.5.2.1 供试液的制备 取10 g双柏膏可溶于20 m l十四烷酸异丙酯后, 置于在含有0.5%的吐温80的p H=7.0无菌蛋白胨-氯化钠缓冲液至100 m l分液漏斗中充分振摇、萃取,静置, 取下层液作为(1∶10)供试液(供试液a)。
1.5.2.2 试验组 取供试液a 1 m l, 加入 100 m l p H =7.0 无菌氯化钠蛋白胨缓冲液中, 同时加入1 m l菌液a, 摇匀后薄膜过滤, 每膜用上述缓冲液600 m l 分次冲洗过滤, 取出滤膜贴至相应的琼脂平皿, 按中国药典2015 年版规定培养。真菌和酵母菌总数计数为白色念珠菌和黑曲霉, 培养基为沙氏葡萄糖琼脂培养基。总数计数的需氧菌为金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌、白色念珠菌和黑曲霉, 培养基为T S B, 每种试验菌株的试验组过滤、培养2 次。
1.5.2.3 供试品对照组 取供试液a 1 m l, 不加菌液, 根据试验组方法计数菌数。每种试验菌株的供试品对照组同法操作 2 次。
1.5.2.4 菌液对照组 用p H=7.0无菌氯化钠-蛋白胨缓冲液替代供试液, 在100 m l稀释液中加入1 m l试验菌液, 根据试验组方法测定菌数。计数方法适用性试验回收率计算公式:试验组菌回收率比值=试验组菌落数供试品对照组菌落数)/菌液对照组菌落数。
1.5.3 控制菌检查方法适用性试验 取10 g双柏膏可溶于20 ml十四烷酸异丙酯后, 置于在含有0.5%的吐温80的pH=7.0无菌蛋白胨-氯化钠缓冲液至100 ml分液漏斗中充分振摇、萃取, 静置, 取下层液作为(1∶10)供试液(供试液a)。
1.5.3.1 金黄色葡萄球菌检查适用性试验结果 取两份10 ml供试液a薄膜过滤, 用pH=7.0无菌蛋白胨-氯化钠缓冲液至600 ml, 分3次冲洗, 200 ml/次, 在最后一次冲洗液中分别加入铜绿假单胞菌、含菌50~100 cfu的金黄色葡萄球菌悬液1 ml, 过滤, 取出滤膜, 接种100 ml TSB中, 30~35℃环境中培养24 h, 取培养物分别划线接种于溴化十六烷基三甲铵(CTMAB)琼脂培养基和甘露醇氯化钠琼脂培养基的平板,培养18~72 h, 每种菌平行制备2张滤膜。
1.5.3.2 阴性对照组 以稀释剂代替供试液, 不加试验菌,照“1.5.2.2”项中的步骤进行操作。
2 结果
2.1 需氧菌总数计数、真菌和酵母菌总数计数适用性试验结果 试验组菌回收率均在《中国药典》(2015年)中规定的 0.5~2 cfu/皿, 说明薄膜过滤法应用于本品具有可行性。见表1, 表2。
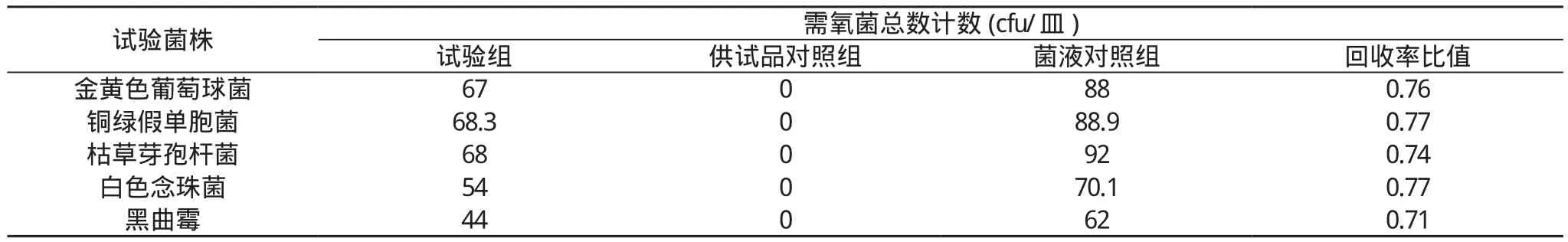
表1 需氧菌总数计数适用性试验结果

表2 真菌和酵母菌总数计数适用性试验结果
2.2 铜绿假单胞菌控制菌及金黄色葡萄球菌控制菌适用性试验结果 两种菌的适用性试验中试验组均为阳性, 对照组均为阴性, 说明此法应用于本品微生物限度控制菌检查具有可行性。见表3, 表4。
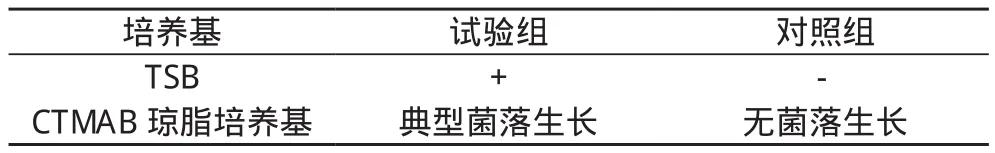
表3 铜绿假单胞菌控制菌适用性试验结果
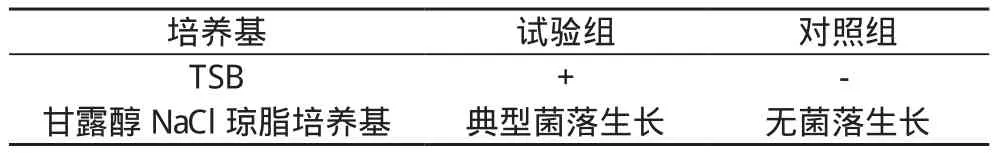
表4 金黄色葡萄球菌控制菌适用性试验结果
3 讨论
双柏膏是《中医伤科学讲义》中的经典处方, 常规检查法[4]会对检查造成干扰。为降低抑菌成分, 消除干扰, 本次研究中采用薄膜过滤法进行检查, 试验中将样品直接溶于无菌十四烷酸异丙酯, 用匀浆仪混匀, 取下清液膜过滤的方法进行实验, 为确保过滤效果良好, 采用含有0.5%乳化剂聚山梨酯 80的pH=7.0无菌蛋白胨-氯化钠缓冲液至100 ml分液漏斗中充分振摇、萃取, 静置, 取下层液作为(1∶10)供试液, 用薄膜过滤法可以有效地去除抑菌成分, 能轻松通过微孔膜过滤, 避免滤膜堵塞。在实验过程中使用微生物限度仪冲洗900 ml, 分析金黄色葡萄球菌、枯草芽孢杆菌试验组回收比值产生的原因可能与冲洗时微生物限度仪底座一直固定, 导致药物无法充分洗脱有关。在冲洗的过程中, 集菌仪边冲洗边振摇则冲洗至900 ml各菌株的回收比值则可达到要求。通过表1、表2可以看出, 试验组菌回收率均在《中国药典》(2015年)中规定的 0.5~2 cfu/皿, 说明薄膜过滤法应用于本品具有可行性。此外, 两种控制菌的适用性试验中试验组均为阳性, 对照组均为阴性, 说明此法应用于本品微生物限度控制菌检查具有可行性。结合工作经验认为试验中的供试液制备较为繁琐复杂, 尤其是非水溶性又具抗菌作用的软膏制剂, 因而建议最好选用能溶解基质的有机溶剂(无菌十四烷酸异丙酯)必要时可加热45℃以下的加入含有0.1%~1%乳化剂聚山梨酯 80的pH=7.0无菌蛋白胨-氯化钠缓冲液100 ml置于分液漏斗中充分振摇、萃取, 静置取下层液作为(1:10)供试液, 这样可直接用薄膜过滤法进行微生物限度检查方法, 并能通过适用性试验, 本方法验证结果准确、可靠、重现性好。
[1] 吴嘉瑞, 张冰, 张光敏.黄柏药理作用研究进展.亚太传统医药, 2009, 5(11):160-162.
[2] 张俊飞, 孙广璐, 张彬, 等.侧柏叶药理作用的研究进展.时珍国医国药, 2013, 24(9):2231-2233.
[3] 姜建昌, 曹雷, 姚瑜洁, 等.冰片的临床应用研究概况.现代中西医结合杂志, 2013, 22(2):221-223.
[4] 国家药典委员会.中国药典(2015年版四部).北京:中国医药科技出版社, 2015:附录1105-1106.
Applicability test of microbial limit test for Shuangbai ointment
ZHONG Liu-fang, XIAO Wen-ke, SUN Shu-zhou, et al.
Guangzhou City Panyu District Institute of Food and Drug Control, Guangzhou 511400, China
ObjectiveTo establish microbial limit test for Shuangbai ointment, and perform applicability test.MethodsApplicability test of microbial limit test was made on Shuangbai ointment according to Chinese Pharmacopoeia (2015).Shuangbai ointment was soluble in isopropyl myristate.After dissolution, the membrane was filtered and emulsifier 80 was added into aqueous washing solution.The control bacteria were examined by membrane method.ResultsThe recovery ratio of aerobic bacteria count, fungi and yeasts count in applicability test was all within 0.5-2.The control bacteria grew well and met the requirements of "Chinese Pharmacopoeia" 2015 edition.ConclusionThis method is reliable and feasible, and it can be used in microbial limit test of Shuangbai ointment.
Shuangbai ointment; Microbial limit; Applicability test; Membrane filtration
10.14164/j.cnki.cn11-5581/r.2017.14.114
2017-03-22]
511400 广州市番禺区食品药品检验所

