氧化偶氮苯双席夫碱化合物对Cu2+的比色识别
吕 蕾, 盛 野, 郑松志, 苏 冉, 安胜姬
(吉林大学 化学学院, 吉林 长春 130012)
氧化偶氮苯双席夫碱化合物对Cu2+的比色识别
吕 蕾, 盛 野, 郑松志, 苏 冉, 安胜姬*
(吉林大学 化学学院, 吉林 长春 130012)
为得到简便地识别Cu2+的传感器,设计合成了氧化偶氮苯双席夫碱化合物。采用紫外吸收光谱法研究了化合物对Cu2+的配合作用及对As3+、Mo6+、Mn2+、Zn2+、Fe3+、Pb2+、Al3+、Hg2+、Ni2+、Pt4+、Mg2+、Be2+、Sr2+、Cs+、Os4+、Cd2+、Se4+、Cr6+、Co2+、Rb+、Ba2+、V6+、Ca2+等23种金属离子的干扰作用。采用等摩尔的连续变化法(Job-plot),研究了化合物与Cu2+形成配合物的配比。用红外光谱法研究了配合机理。同时研究了在EDTA存在时,化合物对Cu2+的“off-on”性质。结果表明,合成的化合物具有大共轭体系,结构新颖且稳定。化合物可以克服23种金属离子的干扰,对Cu2+的选择性很高。化合物与Cu2+形成1∶1型强发光配合物,可以达到比色(裸眼)识别。在1.32~13.0 μmol·L-1范围内,化合物紫外光谱吸光度值与Cu2+浓度呈现良好的线性关系,线性范围宽,最低检出限为2.6×10-7mol·L-1。在EDTA存在时,该配合物释放出Cu2+,表现出对Cu2+的“off-on”模式,红外光谱法研究明确了化合物与Cu2+的结合位点。研究结果表明,所合成的氧化偶氮苯双席夫碱化合物可以对Cu2+实现简便易行的比色(裸眼)识别。
双席夫碱; 氧化偶氮; Cu2+; 比色识别
1 引 言
Cu2+在生命科学和环境科学领域具有重要作用。作为生命体中的基本元素,铜与锌、铁等一样都是大脑神经递质的重要成分,如果摄取不足可致神经系统失调,大脑功能会发生障碍。铜缺乏将使脑细胞中的色素氧化酶减少,活力下降,从而使记忆衰退、思维紊乱、反应迟钝,甚至步态不稳、运动失常等。而人类对铜离子的长期过量使用,又会导致生理受阻、发育停滞。因此,Cu2+的检测、处理成为科学工作者热衷的研究课题[1]。目前,铜离子的检测方法主要有分光光度法、电化学法、原子吸收光谱法、电感耦合等离子体原子发射光谱法和荧光分析法等。紫外探针和荧光探针中的比色(裸眼)识别,因其方法简便明晰更为引人瞩目,成为重要的铜离子传感器研究对象。具有较大共轭基团可作为生色基的一些化合物,因其紫外吸收的特征,成为比色识别研究的重要目标。偶氮苯[2-3]、姜黄素[4]、多苯胺及萘胺等芳香胺[5-6]、罗丹明B[7-13]、荧光素[14]、香豆素[15-16]、芘[17]、苯并噻唑或苯并二唑[18-21]等化合物及其衍生物,都是具有较大共轭基团的重要生色基,是对铜离子比色识别的重要化合物。也有研究者将多个生色基引入到一个分子内,达到增强生色作用的目的,如将罗丹明B和香豆素相连的化合物[22]对铜离子具有较好的识别作用。酰腙、酰亚胺、酰胺、胺、亚胺、硫脲、缩氨基硫脲等胺衍生物[23-28]中的氧原子和氮原子成为Cu2+的有效结合位点,从而形成环状配位化合物;冠醚及杂冠醚[29]等也具有可以成为结合位点的氮原子或氧原子;联吡啶[30]等基团既可成为生色基也可成为结合位点。因此,这些化合物都是良好的识别铜离子的化合物。
本文设计合成含氧化偶氮苯的双席夫碱共轭化合物,旨在增加共轭体系以加强官能团的生色作用。分子中引入酚羟基与席夫碱基团成为Cu2+的结合位点,实现对Cu2+的高选择性比色识别。研究了氧化偶氮苯双席夫碱化合物对Cu2+的络合能力及其对Cu2+的检测灵敏度,化合物在多种阳离子存在下的抗干扰能力即化合物对Cu2+是否具有高选择性单一比色识别能力,以及在EDTA存在时,该化合物是否表现出对Cu2+的“off-on”模式。
2 实 验
2.1 仪器与试剂
所用阳离子的高氯酸盐及六氯锇氨购自Alfa Aesar公司,无水甲醇等其他试剂均购自国药集团化学试剂有限公司,以上试剂均为分析纯试剂。光谱测试用甲醇、乙腈为购自Dikma Technologies Inc.的色谱纯试剂。
实验中使用的仪器主要有UV-2450紫外分光光度计(日本岛津公司)、Vario EL cube CHNSO元素分析仪(德国艾力蒙塔公司)、Varian Unity-300核磁共振仪(美国瓦里安公司)、Agilent1290-micrOTOF Q Ⅱ高分辨液相色谱质谱联用仪(美国布鲁克·道尔顿公司)、NiCOLET iS5 傅里叶变换红外光谱仪(美国尼高力仪器公司)等。
2.2 合成
2.2.1 氧化偶氮苯双席夫碱化合物1的合成
氧化偶氮苯双席夫碱化合物1是课题组在抗肿瘤化合物结构设计及合成研究[31]时发现其离子识别特性的。在研究其离子识别特性时,改进了合成方法,结果产率提高且产物熔点范围变得更窄。在125 mL三颈烧瓶中,加入1.20 g邻氨基苯酚和60 mL无水四氢呋喃,加入5 mL冰醋酸,缓慢滴加溶解有0.50 g 氧化偶氮双醛的甲醇溶液,TLC监测反应进程。回流3.5 h,浓缩反应液至一半体积,冷却,有黄色针状晶体生成。固体产物用乙醇和乙酸乙酯重结晶,得浅黄色针状晶体0.78 g。产率:91%。m.p.:100.4~100.8 ℃

2.2.2 氧化偶氮苯双席夫碱化合物1与铜的配合物2的合成
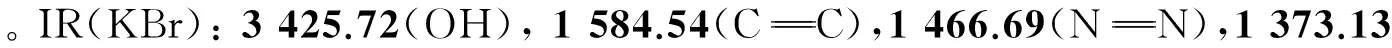
2.3 紫外吸收光谱滴定
配制化合物1的甲醇溶液和金属离子的水溶液,用微量注射器精确移取金属离子试液加入到化合物1的甲醇溶液中,于室温下测定紫外吸收光谱。
3 结果与讨论
3.1 氧化偶氮苯双席夫碱化合物的合成及光异构化分析
氧化偶氮苯双席夫碱化合物1结构如图1所示。

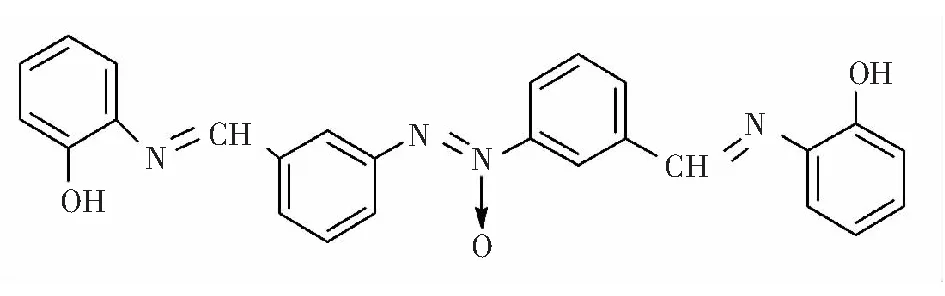
图1 化合物1的结构式
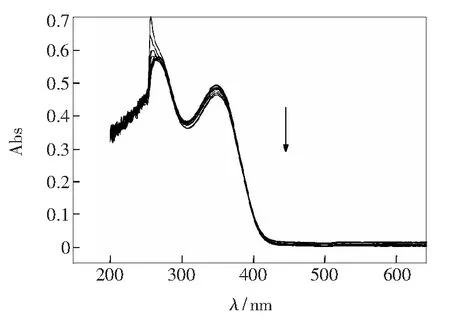
图2 化合物1(9 μmol·L-1,甲醇中)的紫外光谱
Fig.2 Absorption spectra of Compound 1 (9 μmol·L-1) in CH3OH
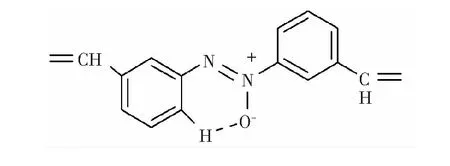
图3 化合物1的部分氢键
3.2 化合物1对Cu2+的识别
取1×10-4mol·L-1化合物1的甲醇溶液300 μL和1×10-3mol·L-1Cu2+的水溶液30 μL,用甲醇稀释至3 mL。混合均匀后,发现混合溶液呈亮黄色,而化合物1与As3+、Mo6+、Mn2+、Zn2+、Fe3+、Pb2+、Al3+、Hg2+、Ni2+、Pt4+、Mg2+、Be2+、Sr2+、Cs+、Os4+、Cd2+、Se4+、Cr6+、Co2+、Rb+、Ba2+、V6+、 Ca2+等23种与 Cu2+相同浓度的金属离子分别混合则无此现象,从而可以实现Cu2+的比色识别。
为考察溶剂体系pH值对化合物1与Cu2+络合的影响,配制了pH值分别为6,7,8,9,10,11,12的化合物1与Cu2+混合物甲醇溶液(pH值更小会影响席夫碱的稳定性故不考虑),测定其紫外光谱,如图4所示。随着体系pH值的增大,紫外光谱吸收峰的强度不断下降,最后趋于平稳,由此可见,pH值会影响化合物1与Cu2+的络合,因此我们选择影响较小的pH值为6~8的甲醇溶液进行以下实验。
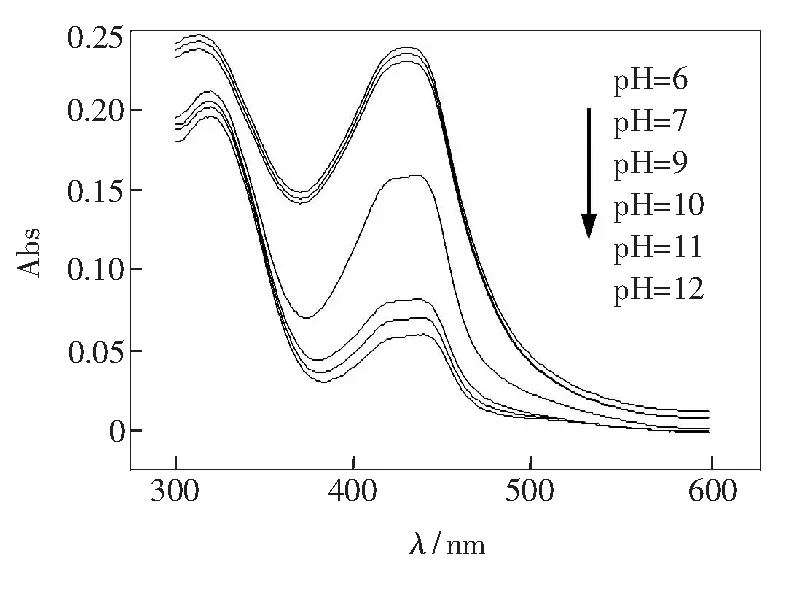
图4 pH值对加入Cu2+(8.7 μmol·L-1)后的化合物1(8.7 μmol·L-1)的紫外吸收光谱的影响(甲醇溶剂)
Fig.4 Absorption spectra of Compound 1(8.7 μmol·L-1) upon the addition of Cu2+( 8.7 μmol·L-1) in different pH value solutions(CH3OH)
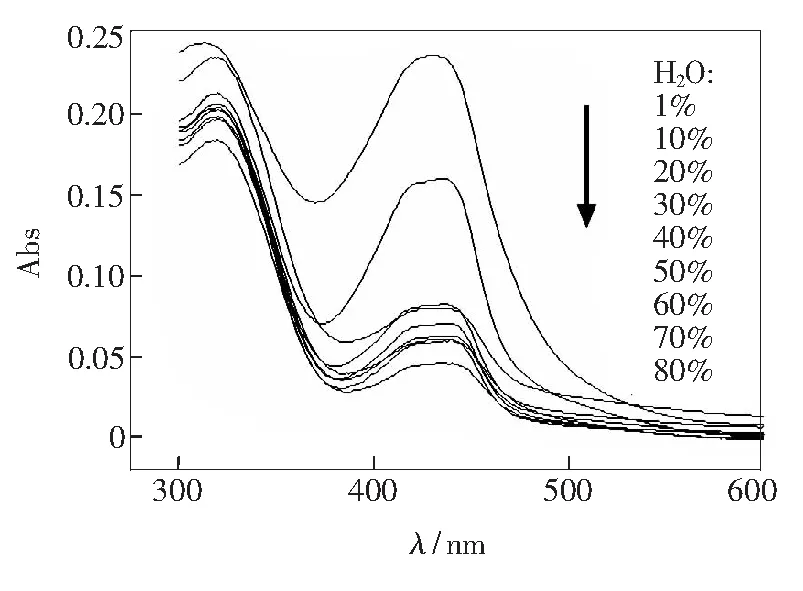
图5 含水率对加入Cu2+(8.7 μmol·L-1)后的化合物1(8.7 μmol·L-1)的紫外光谱的影响
Fig.5 Absorption spectra of Compound 1(8.7 μmol·L-1) upon the addition of Cu2+(8.7 μmol·L-1) with different water content in CH3OH
为了验证体系含水量对化合物1与Cu2+络合的影响,配置了含水率分别为1%、10%、20%、30%、40%、50%、60%、70%、80%的化合物1与Cu2+混合物的甲醇水溶液,测定混合体系的紫外光谱,如图5所示。随着体系含水量的增多,紫外光谱吸收峰的强度不断下降,最后趋于平稳。由此可见,水的存在会影响化合物1与Cu2+的络合,因此我们选择含水率不超过1%的甲醇溶液进行以下实验。
测定pH值为7、含水率为1%以下的化合物1与Cu2+混合物甲醇溶液的紫外吸收光谱,如图6所示。347 nm处的吸收峰明显蓝移至323 nm,且在435 nm处出现一个新的吸收峰。其他金属离子与化合物1作用以后,也可以使化合物1的吸收峰蓝移,但在435 nm左右没有新的吸收峰产生。化合物1对Cu2+有很强的络合能力,显示出显著的高选择性识别作用。
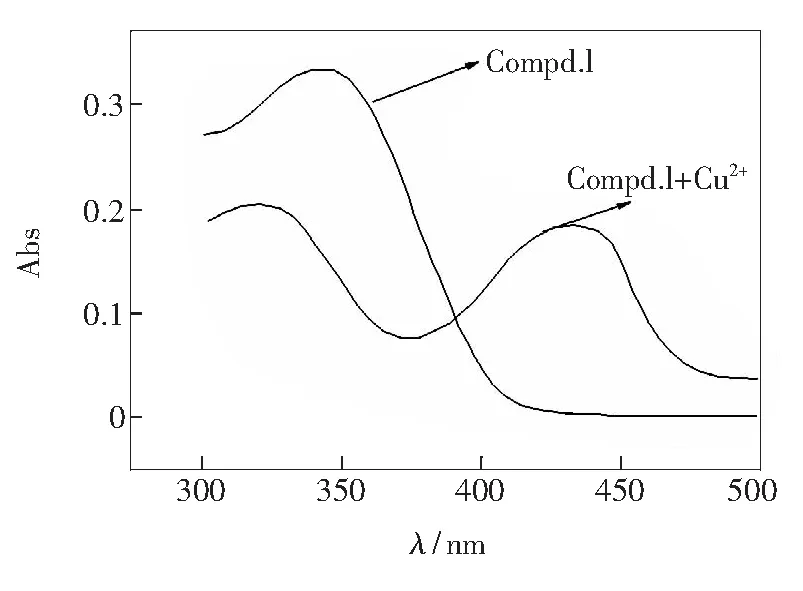
图6 加入Cu2+(7 μmol·L-1)后的化合物1(7 μmol·L-1)的紫外光谱(甲醇中,pH=7)
Fig.6 Absorption spectra of Compound 1(7 μmol·L-1) upon the addition of Cu2+(7 μmol·L-1) in CH3OH(pH=7)
3.3 干扰实验
实验还考察了其他金属离子对于化合物1对Cu2+识别的干扰作用,见图7。
当化合物1的甲醇溶液中分别加入7 μmol·L-1浓度的As3+、Mo6+、Mn2+、Zn2+、Fe3+、Pb2+、Al3+、Hg2+、Ni2+、Pt4+、Mg2+、Be2+、Sr2+、Cs+、Os4+、Cd2+、Se4+、Cr6+、Co2+、Rb+、Ba2+、V6+、Ca2+等23种金属离子后,435 nm处没有明显的吸收峰出现,而加入7 μmol·L-1的Cu2+后在435 nm处有新的吸收峰出现,说明其他金属离子对于化合物1对Cu2+的识别没有干扰。

图7 不同金属离子对加入Cu2+(7 μmol·L-1)后的化合物1(7 μmol·L-1)的紫外吸收光谱的影响(λ=435 nm,甲醇溶剂)
Fig.7 Absorption spectra of Compound 1(7 μmol·L-1) in the presence of Cu2+(7 μmol·L-1) and miscellaneous cations in CH3OH at 435 nm
3.4 Cu2+浓度对化合物1的紫外吸收光谱的影响
为了验证不同浓度的Cu2+对化合物1的紫外吸收光谱的影响,控制化合物1的浓度为 1.38×10-5mol·L-1,Cu2+与化合物1的浓度比从0.01增加到2,测定混合溶液的紫外光谱,如图8所示。从图8可以看出,随着体系中Cu2+含量的增大,325 nm左右的吸收峰变化不大,435 nm处的吸收峰值不断增大。图8插图表示,随着Cu2+含量的增大,在1.32~13.0 μmol·L-1范围内,吸光度值与离子浓度呈现良好的线性关系;当铜离子浓度达到17.5 μmol·L-1时,化合物1-Cu2+配合物的配位-解离达到平衡。线性拟合得到方程为A=0.01246 + 0.0196C,A为吸光度,C为Cu2+的浓度(μmol·L-1),R为0.999 8,根据线性方程的斜率及8次测量平均标准偏差,得出检出限为2.6×10-7mol·L-1。
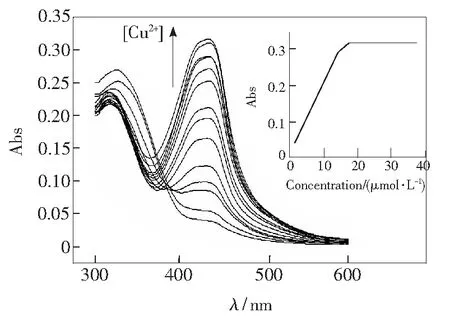
图8 Cu2+浓度对化合物1(13.8 μmol·L-1)的紫外吸收光谱的影响(甲醇溶剂)
Fig.8 Absorption spectra of Compound 1(13.8 μmol·L-1) in CH3OH in the presence of Cu2+with different concentration
.
(1)
用等摩尔的连续变化法(Job-plot)测定了化合物1与Cu2+的配合比。分别控制Cu2+和化合物1的总浓度为 0.02 mmol·L-1,在化合物1中滴加Cu2+测定吸收光谱,并绘制Job-plot,如图9所示。测得化合物1与Cu2+的配合比为1∶1。Cu2+与化合物1的结合常数Kα可由Benesi-Hildebrand 方程确定[32]。式中A0和A分别为加入Cu2+前后体系的吸光度,Amax为加入过量Cu2+时化合物1的饱和吸光度。由式(1)得结合常数Kα为1.0×105L·mol-1。
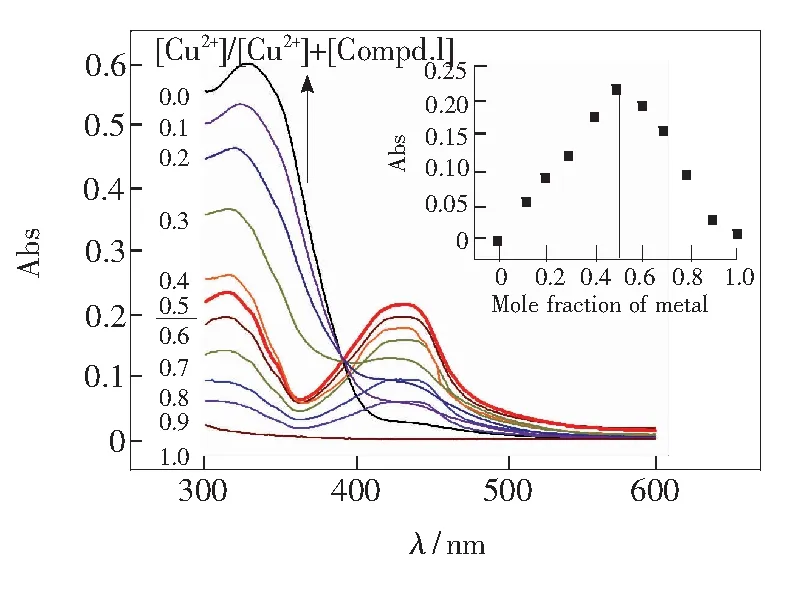
图9 向化合物1的甲醇溶液中滴加Cu2+(总浓度为0.02 mmol·L-1)时的紫外光谱(插图:用1滴定Cu2+的Job-plot)
Fig.9 Absorbance spectra of Compound 1 on titration with Cu2+in CH3OH (inset: Job-plot of Compound 1 with Cu2+in CH3OH). The total mole fraction of Compound 1 and Cu2+is 0.02 mmol·L-1.
3.5 化合物1对Cu2+的“off-on”性质实验
为验证化合物1对Cu2+识别的可逆性,将同倍量的EDTA加入到含有等摩尔化合物1和Cu2+的混合溶液中,溶液的吸光度值基本恢复至未加入Cu2+时化合物1的数值,如图10所示。图10表明,化合物1对Cu2+的光谱响应来自于化合物1和Cu2+的配合物的形成,因此化合物1是具备“off-on”性质的紫外Cu2+分子开关。
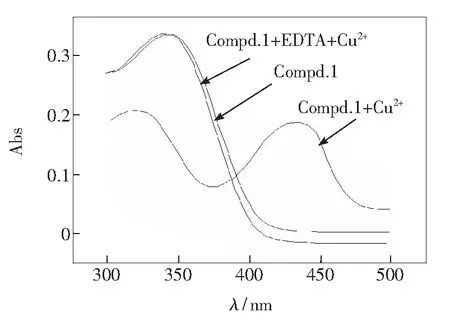
图10 EDTA对化合物1(7 μmol·L-1)与Cu2+(7 μmol·L-1)混合物的紫外吸收光谱(甲醇溶剂)的影响
Fig.10 Absorbance spectra of Compound 1(7 μmol·L-1) upon the addition of Cu2+(7 μmol·L-1) and EDTA
3.6 化合物1对Cu2+的识别机理
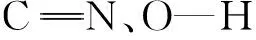
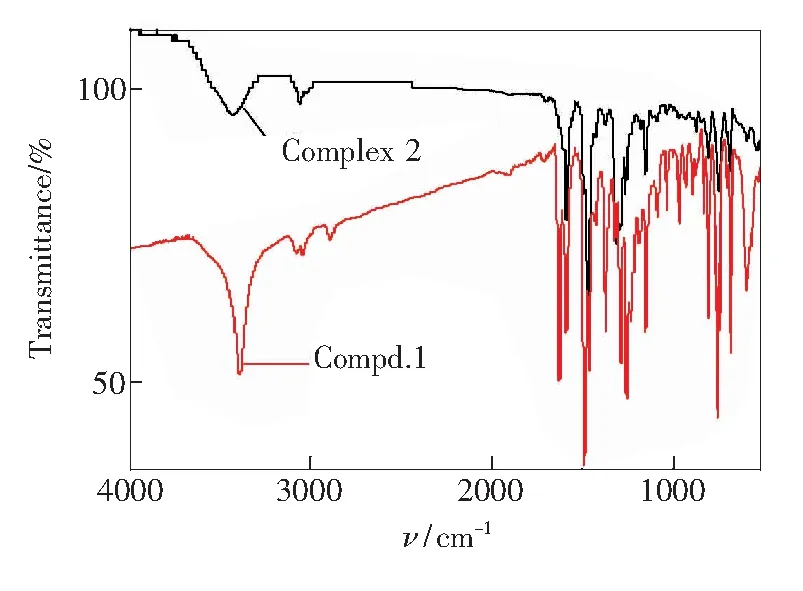
图11 化合物1与配合物2的红外光谱
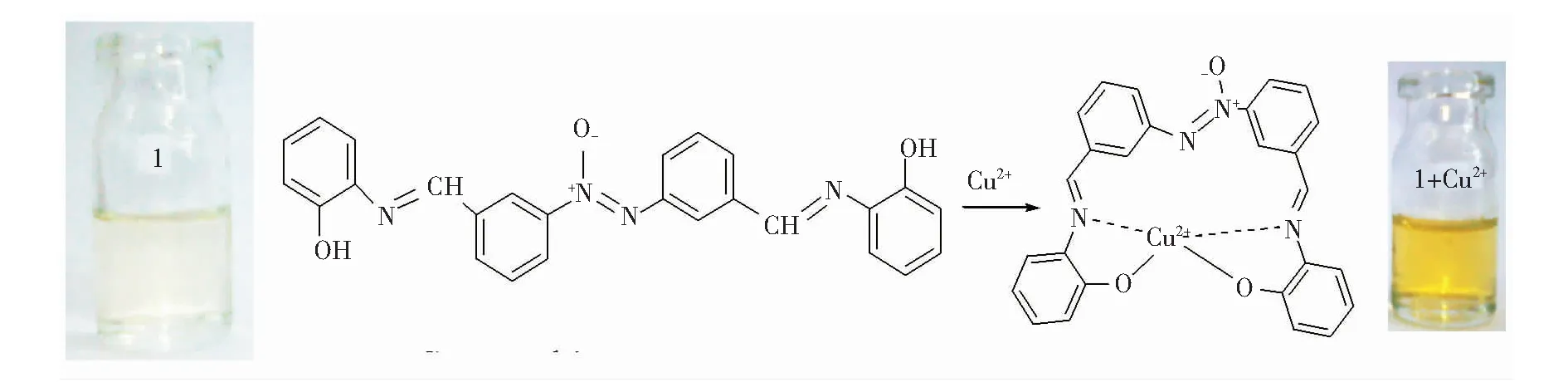
图 12 化合物1与Cu2+在甲醇中的配合机理
4 结 论
设计合成了一种具有稳定大共轭体系的结构新颖的含氧化偶氮苯双席夫碱化合物,考察了其对Cu2+等24种金属离子的识别作用。结果表明,该化合物可专一选择性比色识别Cu2+。化合物与Cu2+形成了1∶1型强发光配合物,在1.32~13.0 μmol·L-1范围内,化合物紫外光谱吸光度值与Cu2+浓度呈现良好的线性关系,线性范围宽,最低检出限为2.6×10-7mol·L-1。同时,在EDTA存在时,该配合物释放出Cu2+,表现出对Cu2+的“off-on”模式。因此,化合物1是可在不需要仪器的情况下很简便地肉眼检测Cu2+的高选择性铜离子紫外探针。用红外光谱法研究了氧化偶氮苯双席夫碱化合物与Cu2+的配合机理,明确了氧化偶氮苯双席夫碱化合物与Cu2+的结合位点。
[1] 王夏芳. 铜离子对环境危害现状及对策研究 [J]. 国土与自然资源研究, 2015(1):55-57. WANG X F. The dangers of copper ions on the environment and research on countermeasure [J].TerritoryNat.Res.Study, 2015(1):55-57. (in Chinese)
[2] GUNNLAUGSSON T, LEONARD J P, MURRAY N S. Highly selective colorimetric naked-eye Cu(Ⅱ) detection using an azobenzene chemosensor [J].Org.Lett., 2004, 6(10):1557-1560.
[3] JO J, LEE H Y, LIU W J,etal.. Reactivity-based detection of copper(Ⅱ) ion in water: oxidative cyclization of azoaromatics as fluorescence turn-on signaling mechanism [J].J.Am.Chem.Soc., 2012, 134(38):16000-16007.
[4] POURREZA N, GOLMOHAMMADI H. Green colorimetric recognition of trace sulfide ions in water samples using curcumin nanoparticle in micelle mediated system [J].Talanta, 2014, 119:181-186.
[5] MALKONDU S, ERDEMIR S. A triphenylamine based multi-analyte chemosensor for Hg2+and Cu2+ions in MeCN/H2O[J].Tetrahedron, 2014, 70(35):5494-5498.
[6] GOSWAMI S, SEN D, DAS N K. A new highly selective, ratiometric and colorimetric fluorescence sensor for Cu2+with a remarkable red shift in absorption and emission spectra based on internal charge transfer [J].Org.Lett., 2010, 12(4):856-859.
[7] FAN J L, ZHAN P, HU M M,etal.. A fluorescent ratiometric chemodosimeter for Cu2+based on TBET and its application in living cells [J].Org.Lett., 2013, 15(3):492-495.
[8] XIANG Y, TONG A J, JIN P Y,etal.. New fluorescent rhodamine hydrazone chemosensor for Cu(Ⅱ) with high selectivity and sensitivity [J].Org.Lett., 2006, 8(13):2863-2866.
[9] DONG M, MA T H, ZHANG A J,etal.. A series of highly sensitive and selective fluorescent and colorimetric “off-on” chemosensors for Cu (Ⅱ) based on rhodamine derivatives [J].DyesPigm., 2010, 87(2):164-172.
[10] HUANG L, CHEN F J, XI P X,etal.. A turn-on fluorescent chemosensor for Cu2+in aqueous media and its application to bioimaging [J].DyesPigm., 2011, 90(3):265-268.
[11] XU Z H, ZHANG L K, GUO R,etal.. A highly sensitive and selective colorimetric and off-on fluorescent chemosensor for Cu2+based on rhodamine B derivative [J].Sens.ActuatorsB:Chem., 2011, 156(2):546-552.
[12] ZHANG J, YU C W, QIAN S Y,etal.. A selective fluorescent chemosensor with 1, 2, 4-triazole as subunit for Cu (Ⅱ) and its application in imaging Cu (II) in living cells [J].DyesPigm., 2012, 92(3):1370-1375.
[13] 陈稼轩, 田怡, 向清祥, 等. 罗丹明B衍生物的合成及其对Cu2+, Hg2+的识别研究 [J]. 有机化学, 2012, 32(10):1930-1935. CHEN J X, TIAN Y, XIANG Q X,etal.. Synthesis and properties of rhodamine B derivative for recognition of Cu2+and Hg2+[J].Chin.J.Org.Chem., 2012, 32(10):1930-1935. (in Chinese)
[14] SEO S, LEE H Y, PARK M,etal.. Fluorescein-functionalized silica nanoparticles as a selective fluorogenic chemosensor for Cu2+in living cells [J].Eur.J.Inorg.Chem., 2010, 2010(6):843-847.
[15] YANG M D, WANG H Z, HUANG J,etal.. Highly sensitive and selective colorimetric and fluorescent off-on probe for copper (Ⅱ) based on unique addition reaction and its imaging in living cells [J].Sens.ActuatorsB:Chem., 2014, 204:710-715.
[16] JO H Y, PARK G J, NA Y J,etal.. Sequential colorimetric recognition of Cu2+and CN- by asymmetric coumarin-conjugated naphthol groups in aqueous solution [J].DyesPigm., 2014, 109:127-134.
[17] BHORGE Y R, TSAI H T, HUANG K F,etal.. A new pyrene-based Schiff-base: a selective colorimetric and fluorescent chemosensor for detection of Cu(Ⅱ) and Fe(Ⅲ) [J].Spectrochim.ActaPart A:Mol.Biomol.Spectrosc., 2014, 130: 7-12.
[18] TAN J, YAN X P. 2, 1, 3-Benzoxadiazole-based selective chromogenic chemosensor for rapid naked-eye detection of Hg2+and Cu2+[J].Talanta, 2008, 76(1):9-14.
[19] YE H, GE F, ZHOU Y M,etal.. A new Schiff base fluorescent probe for imaging Cu2+in living cells [J].Spectrochim.ActaPart A:Mol.Biomol.Spectrosc., 2013, 112:132-138.
[20] LIU M X, WEI T B, LIN Q,etal.. A novel 5-mercapto triazole Schiff base as a selective chromogenic chemosensor for Cu2+[J].Spectrochim.ActaPart A:Mol.Biomol.Spectrosc., 2011, 79(5):1837-1842.
[21] PENG Y, DONG Y M, DONG M,etal.. A selective, sensitive, colorimetric, and fluorescence probe for relay recognition of fluoride and Cu(Ⅱ) ions with “off-on-off” switching in ethanol-water solution [J].J.Org.Chem., 2012, 77(20):9072-9080.
[22] YUAN L, LIN W Y, CHEN B,etal.. Development of FRET-based ratiometric fluorescent Cu2+chemodosimeters and the applications for living cell imaging [J].Org.Lett., 2012, 14(2):432-435.
[23] KAO S L, LIN W Y, VENKATESAN P,etal.. Colorimetric detection of Cu(Ⅱ): Cu(Ⅱ)-induced deprotonation of NH responsible for color change [J].Sens.ActuatorsB:Chem., 2014, 204:688-693.
[24] LI W, ZHANG Y, GAN X P,etal.. A triphenylamine-isophorone-based “off-on” fluorescent and colorimetric probe for Cu2+[J].Sens.ActuatorsB:Chem., 2015, 206:640-646.
[25] XI W G, GONG, Y M, MEI B,etal.. Schiff base derivatives based on diaminomaleonitrile: colorimetric and fluorescent recognition of Cu(Ⅱ), cell imaging application, polymorph-dependent fluorescence and aggregation-enhanced emission [J].Sens.ActuatorsB:Chem., 2014, 205:158-167.
[26] 魏太保, 李军舰, 林奇, 等. N-芳基香豆素甲基酮缩氨基硫脲对Cu2+的选择性比色识别 [J]. 高等学校化学学报, 2012, 33(11):2452-2456. WEI T B, LI J J, LIN Q,etal.. Highly selective colorimetric recognition of copper ions based on N-Aryl coumarin methyl ketone thiosemicarbazone receptors [J].Chem.J.Chin.Univ., 2012, 33(11):2452-2456. (in Chinese)
[27] WANG W J, CHEN Q H, LI Q,etal.. Ligand-structure effect on the formation of one-dimensional nanoscale Cu(Ⅱ)-schiff base complexes and solvent-mediated shape transformation [J].Cryst.GrowthDes., 2012, 12(5):2707-2713.
[28] 张鹏, 张有明, 林奇, 等. 金属离子响应型荧光传感分子的设计原理及研究进展 [J]. 有机化学, 2014, 34(7):1300-1321. ZHANG P, ZHANG Y M, LIN Q,etal.. Principle and the research progress of fluorescent chemosensors for cations recognition [J].Chin.J.Org.Chem., 2014, 34(7):1300-1321. (in Chinese)
[29] ZHOU H P, WANG J Q, CHEN Y X,etal.. New diaminomaleonitrile derivatives containing aza-crown ether: selective, sensitive and colorimetric chemosensors for Cu(Ⅱ) [J].DyesPigm., 2013, 98(1):1-10.
[30] ZHENG C H, LIU G, PU S Z. A sensitive sensor for Cu(Ⅱ) based on a novel diarylethene with a bipyridyl moiety [J].TetrahedronLett., 2013, 54(43):5791-5794.
[31] SU R, LÜ L, ZHENG S Z,etal.. Synthesis and characterization of novel azo-containing or azoxy-containing schiff bases and their antiproliferative and cytotoxic activities [J].Chem.Res.Chin.Univ., 2015, 31(1):60-64.
[32] TANG L J, LI F F, LIU M H,etal.. Single sensor for two metal ions: colorimetric recognition of Cu2+and fluorescent recognition of Hg2+[J].Spectrochim.ActaPart A:Mol.Biomol.Spectrosc., 2011, 78(3):1168-1172.

吕蕾(1965-),女,吉林长春人,学士,工程师,1988年于长春卫生学校本科班获得学士学位,主要从事药物合成的研究。

E-mail: lvlei@jlu.edu.cn 安胜姬(1965-),女,吉林图们人,博士,教授,2000年于吉林大学获得博士学位,主要从事有机合成及其应用方面的研究。
E-mail: anshengji@jlu.edu.cn
Highly Selective Colorimetric Recognition of Copper Ions Based on Bis-Schiff Base Containing An Azoxy Group
LYU Lei, SHENG Ye, ZHENG Song-zhi, SU Ran, AN Sheng-ji*
(CollegeofChemistry,JilinUniversity,Changchun130012,China) *CorrespondingAuthor,E-mail:anshengji@jlu.edu.cn
In order to obtain copper ion sensors, a bis-Schiff base containing an azoxy group was synthesized. The complexation effect of the compound on Cu2+was studied, and the interference of 23 metal ions such as As3+, Mo6+, Mn2+, Zn2+, Fe3+, Pb2+, Al3+, Hg2+, Ni2+, Pt4+, Mg2+, Be2+, Sr2+, Cs+, Os4+, Cd2+, Se4+, Cr6+, Co2+, Rb+, Ba2+, V6+, Ca2+was also studied in MeOH-H2O by UV-Vis spectroscopy. Job-plot method was used to study the ratio of the Cu2+complex with the compound. The cooperation mechanism was studied by infrared spectrometry, and the “off-on” nature of the compound with copper ion was studied in EDTA. The results indicate that the bis-Schiff base has a large conjugated system, the structure is novel and stable. The bis-Schiff base shows a highly selective response to Cu2+. A clear color change from colorless to yellow is observed upon the addition of Cu2+to the solution of the receptor in MeOH by naked-eyes and a single selectivity colorimetric recognition. The Job-plot shows that the bis-Schiff base coordinates with Cu2+to form 1∶1 stable luminescent complex. The UV absorbance of the system shows a good linear relationship with Cu2+concentration within 1.32-13.0 μmol·L-1, and the detection limit is 2.6×10-7mol·L-1. The sensing of Cu2+by this sensor is found to be reversible with the Cu2+induced color being lost upon the addition of EDTA. The process of titrating Compound 1 with Cu2+is reversible, and Compound 1 can be used as an off-on switch chemosensor. The complexation mechanism of Compound 1 and Cu2+was studied by IR spectroscopy, and the binding sites of compound 1 and Cu2+were identified.
bis-Schiff base; azoxy; copper ion; colorimetric recognition
2017-01-05;
2017-02-13
国家自然科学基金国家基础科学人才培养基金(J1103302)资助项目 Supported by National Science Foundation for Fostering Talents in Basic Research of The National Natural Science Foundation of China(GJ1103302)
1000-7032(2017)08-1109-08
O657.3; O626.32
A
10.3788/fgxb20173808.1109

