ZnS∶Cu-罗丹明B的荧光共振能量转移性质
翟英歌, 楚学影, 徐铭泽*, 李金华, 金芳军, 王晓华
(1. 长春理工大学 理学院, 吉林 长春 130022; 2. 长春理工大学 国际教育与交流学院, 吉林 长春 130022)
ZnS∶Cu-罗丹明B的荧光共振能量转移性质
翟英歌1, 楚学影1, 徐铭泽1*, 李金华1, 金芳军1, 王晓华2
(1. 长春理工大学 理学院, 吉林 长春 130022; 2. 长春理工大学 国际教育与交流学院, 吉林 长春 130022)
为了解决现有的基于量子点荧光共振能量转移体系的生物毒性问题,选用无毒的ZnS∶Cu量子点与罗丹明B构建新型荧光共振能量转移体系。通过共沉淀法成功制备了形貌均一的ZnS∶Cu纳米晶量子点。在此基础上,测试了不同掺杂浓度的ZnS∶Cu量子点及罗丹明B的荧光光谱。然后,通过对ZnS∶Cu量子点的表面修饰构建了以ZnS∶Cu量子点为供体、罗丹明B为受体的荧光共振能量转移体系。实验结果表明:ZnS∶2%Cu量子点的发光光谱与罗丹明B的吸收光谱在481 nm处有较大重合,说明构建荧光共振能量转移的最佳铜掺杂摩尔分数为2%。通过计算发现以ZnS∶2%Cu量子点为供体、罗丹明B为受体的荧光共振能量转移体系的能量转移效率为25.8%。进一步实验结果表明,罗丹明B浓度也能够影响能量转移。
ZnS∶Cu; 罗丹明B; 荧光共振能量转移
1 引 言
荧光共振能量转移(FRET)现象是发生在两个不同发光基团所构成的体系内部的一种非辐射能量转移。当供体分子的荧光光谱与受体分子的激发光谱相重叠时,供体荧光分子的激发能诱发受体分子发出荧光,同时供体荧光分子自身的荧光强度衰减的现象即为荧光共振能量转移[1]。荧光共振能量转移技术是一种高效的光学分子尺,在免疫分析、核酸检测、生物大分子检测等方面都有着广泛的应用[2-5]。传统的荧光共振能量转移体系多是基于荧光染料分子的发光,它会受到染料分子的吸收光谱窄、发射光谱宽、光漂白现象严重等问题的制约,因此在实际应用中受到了一定程度的限制[6]。所以寻找新型的能够构建荧光共振能量转移体系的能量供体及受体是一种新的研究思路。近年来人们广泛研究的量子点[7]比传统的有机染料更加具有优势,由于量子点的发射光谱较窄、红色光谱较多且具有一定的对称性,使得量子点能够作为供体更好地满足荧光共振能量转移条件。所以,量子点在日后探究荧光共振能量转移方面有着广阔的应用前景[8-10]。目前,已有文章报道了一些基于量子点的荧光共振能量转移体系能够在免疫测定、生物医学传感器等方面应用[11-14]。但在量子点的选择方面多数采用CdTe、CdSe或稀土掺杂的NaYF4作为能量供体[15-16],然而Cd2+、Se2-和Te2-等重金属离子具有生物毒性,对肺和肾脏都有严重的危害[17],所以随着量子点在生物学研究中的广泛应用,与此密切相关的药物毒性问题以及对人类环境可能产生的污染问题都日渐引起研究者的高度重视。
寻找没有生物毒性且光学性质较好的量子点来构建荧光共振能量转移体系成为近年来人们的研究热点。在众多可选择的材料中,宽带隙直接带隙半导体ZnS基量子点备受关注[18-19]。由于它无生物毒性、晶体结构可调、发光波长可调和荧光寿命相对较长等特点,使其能够成为构建荧光共振能量转移体系的能量供体。本文选择安全性较佳且发光性能较好的ZnS基纳米材料(ZnS∶Cu)及罗丹明B来构建荧光共振能量转移体系,能够进一步拓展荧光共振能量转移体系的应用领域与限度。
2 实 验
2.1 药剂和仪器
二水合乙酸锌产自天津市科密欧化学试剂研究所,九水合硫化钠、醋酸铜购于汕头市西陇化工股份有限公司,氢氧化钠购于国药集团化学试剂有限公司,3-巯基丙酸(MPA) 购于ALDRICH 化学试剂公司,实验用水为自制的高纯去离子水。
样品的晶体结构由X射线衍射仪(Rigaku D/max2500型)测得,微观形貌由透射电子显微镜(JEM-2010型)测得,紫外吸收光谱和荧光光谱利用SHIMADZU公司的光谱仪测得(紫外光谱:UV-2450、荧光光谱:RF-5301pc)。
2.2 实验过程
ZnS∶Cu纳米微粒通过 Zn2+、Cu2+离子和 S2-离子共沉淀反应得到。首先,将5 mL 0.1 mol/L 乙酸锌溶液和20 mL 0.1 mol/L MPA溶液相混合,加水稀释到 44 mL,通氮除氧 15 min。然后,添加不同体积的0.01 mol/L 的醋酸铜溶液(如2%Cu掺杂需1 mL),充分搅拌后,用 2 mol/L 的氢氧化钠溶液调节溶液pH值为10,继续通氮气除氧20 min。充分搅拌下,用注射针管迅速向反应溶液中添加5 mL 0.1 mol/L的硫化钠溶液,在通氮气条件下反应 15 min,随后所得溶液放入温度为50 ℃的摇床中陈化2 h,即可得到 ZnS∶Cu 纳米晶的水溶胶。将2 mL ZnS∶Cu量子点水溶液放在反应瓶内,添加CTAB缓冲液,再加入2 mL罗丹明B水溶液,把反应瓶置于恒温振荡器内振荡,充分反应后再进行光学性质测试。
3 结果与讨论
3.1 ZnS∶Cu的晶体结构和形貌
为了研究所制备样品的基本结构及形貌,对样品进行了X射线衍射(XRD)测试及透射电子显微镜(TEM)测试,如图1所示。将ZnS∶Cu纳米晶的XRD图谱与PDF标准卡(No. 050566)对比发现,图1中28.5°、47.9°、56.5°的衍射峰分别对应于闪锌矿ZnS的 (111)、(220)、(311)晶面,说明所得到的样品是立方闪锌矿结构的ZnS纳米晶,没有明显的杂质。因为Cu2+离子半径(0.073 nm)与Zn2+离子半径(0.074 nm)相差无几,在铜离子少量掺杂时,不会引起ZnS的晶格畸变,所以在XRD图谱中衍射峰并没有明显的移动。从图1中的插图所显示的TEM图片可以看出,ZnS∶Cu纳米晶的尺寸很小,平均尺寸为3 nm左右,说明我们成功制备了ZnS∶Cu量子点。

图1 ZnS∶Cu纳米晶的XRD图谱及其TEM图片
3.2 荧光共振能量转移的构建
荧光共振能量转移的构建需要供体和受体的荧光光谱满足以下条件:(1)能量供体和受体的激发光谱要足够分得开;(2)能量供体的发光光谱和能量受体的激发光谱要重叠;(3)能量供、受体的发射光谱不能互相干扰。所以,为了构建荧光共振转移体系,我们需要对所选择的供体(ZnS∶Cu)和受体(罗丹明B)进行荧光光谱测试。
图2为ZnS∶Cu及罗丹明B的激发光谱,可以看到ZnS∶Cu量子点与罗丹明B荧光强度激发波长各自位于351 nm、481 nm位置处。该现象充分说明能量供、受体间的激发光谱之间的距离足够大,这是成功构建荧光共振能量转移体系必须满足的条件之一。由于罗丹明B的激发光谱约位于481 nm处,要构建荧光共振能量转移体系,需要供体ZnS∶Cu的发光光谱与其有较大的重合。Cu的掺杂浓度会对ZnS∶Cu的发光产生较大影响。图3是用351 nm的激发波长对浓度不同的ZnS∶Cu进行激发并得到的荧光光谱,可以看出,不同铜掺杂浓度的样品的发射波长就会存在差异。根据荧光共振能量转移所需满足的条件,我们发现掺杂摩尔分数为2%的ZnS∶Cu的发射光谱位于480 nm处,与罗丹明B的激发光谱重合最大。所以我们选用ZnS∶2%Cu作为供体。将供体与受体的荧光激发光谱及发射光谱对比(图4)可以发现,供体受体二者的发射光谱分别位于480 nm及590 nm处,也没有相互干扰。综上所述,ZnS∶2%Cu与罗丹明B的荧光光谱能够满足上述的3个条件,具备了构建荧光共振能量转移的基本条件。
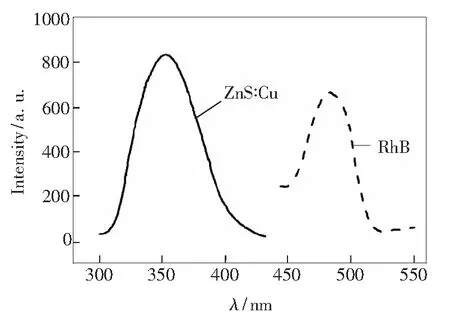
图2 ZnS∶Cu与罗丹明B的激发光谱
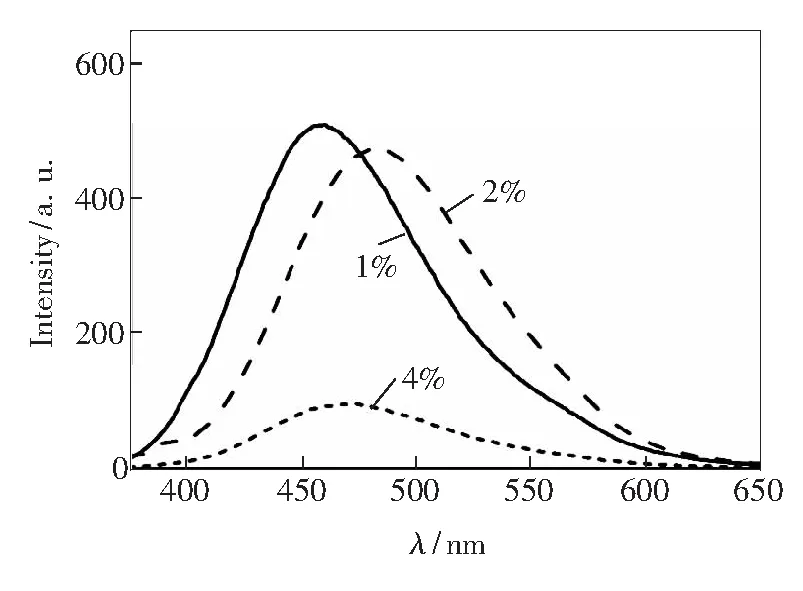
图3 不同掺杂浓度的ZnS∶Cu量子点的发射光谱
Fig.3 Emission spectra of ZnS∶Cu QDs with different Cu concentration
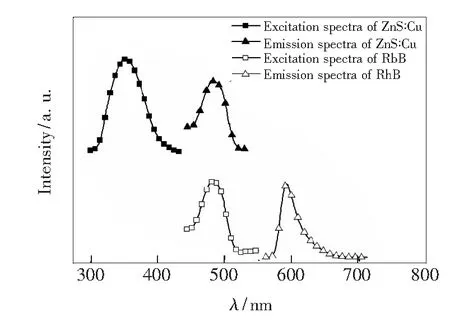
图4 ZnS∶Cu与罗丹明B的激发光谱及发射光谱
Fig.4 Excitation and emission spectra of ZnS∶Cu and Rhodamine B
对于构建荧光共振能量转移体系来说,择优选择能量给予者与能量接受者的材料是首要条件,但供体及受体之间的距离也能够对荧光共振能量转移体系的构建产生极大的影响。虽然ZnS∶Cu量子点的发光光谱与罗丹明B的激发光谱能够大面积重合,但是量子点荧光强度较低,需要二者距离较近时才能发生荧光共振能量转移。我们利用3-巯基丙酸对ZnS∶Cu 量子点表面进行修饰而使其带负电,阳离子CTAB作为表面活性剂时带正电,利用静电作用结合,从而产生CTAB修饰的ZnS∶Cu量子点。利用分子作用力将CTAB分子中的烃基与罗丹明B分子结合在一起,减小两者之间的分子距离,使二者之间能够发生共振能量转移。
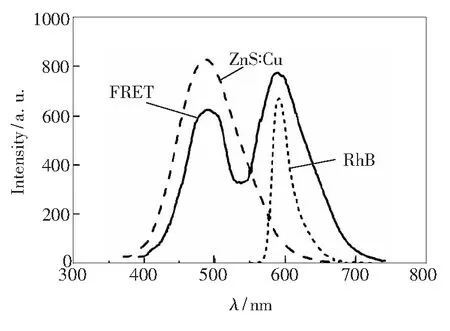
图5 ZnS∶Cu-RhB的FRET体系的发射光谱
为了分析荧光共振能量转移现象,我们测试了ZnS∶Cu量子点、罗丹明B等体积混合溶液(即ZnS∶Cu-RhB体系)的荧光光谱,并将其与ZnS∶Cu量子点及罗丹明B溶液在325 nm紫外激发下的发射光谱进行了对比。由制备过程可知QDs-RhB体系中对应的ZnS∶Cu量子点及罗丹明B的浓度是原浓度的1/2。而二者的荧光光谱也在各自初始溶液浓度的1/2处得到。从图5所示的三者的荧光光谱图中可以看出,混合液同时拥有ZnS∶Cu量子点及罗丹明B的发光,但其强度不同于同浓度的单独量子点或罗丹明B的发光强度。量子点的发光变弱,但罗丹明B的发光变强,说明二者之间发生了能量转移。荧光共振能量转移的效率可以用如下公式计算:
(1)
其中,E代表荧光共振能量转移效率,FDA和FD分别代表无供体存在时受体的荧光强度及供体存在时受体的荧光强度。通过公式计算得到,由ZnS∶Cu量子点与罗丹明B构建的荧光共振能量转移体系的能量转移效率是25.8%,有望应用于大分子细胞的检测。
受体浓度也会影响荧光共振能量转移的程度。这里,我们将ZnS∶Cu的浓度固定,改变罗丹明B的浓度,使ZnS∶Cu与其浓度比分别为4∶1、2∶1及1∶1。研究了受体浓度对荧光共振能量转移体系的影响。从图6可以看到,罗丹明B浓度逐渐增大时,供体ZnS∶Cu的荧光强度逐渐下降,受体罗丹明B的荧光强度逐渐升高,也就是说罗丹明B的浓度能够促进荧光共振能量转移的发生。所以在实际应用中,选择适当的供体受体浓度也极为重要。
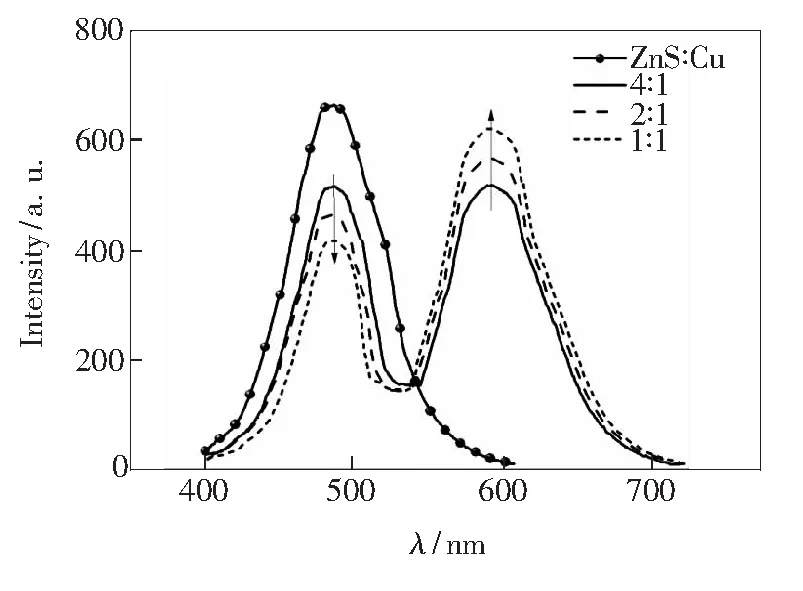
图6 不同浓度罗丹明B构建的FRET体系发光光谱
Fig.6 Emission spectra of FRET system based on different concentrations of RhB
4 结 论
通过不同掺杂浓度的ZnS∶Cu纳米晶量子点的制备及其荧光特性分析,发现了铜掺杂摩尔分数为2%的ZnS∶Cu纳米晶的发射峰与罗丹明B的吸收峰在481 nm处有着最大重叠。以ZnS∶Cu量子点为供体及罗丹明B为受体成功构建了能量转化效率为25.8%的荧光共振能量转移体系。该体系有望应用于生物分子的检测。
[1] FÖRSTER T. Zwischenmolekulare energiewanderung und fluoreszenz [J].Ann.Phys., 1948, 437(1-2):55-75.
[2] VANOAICA L, BEHERA A, CAMARGO S M R,etal.. Real-time functional characterization of cationic amino acid transporters using a new FRET sensor [J].PflügersArch., 2016, 468(4):563-572.
[3] WANG Y, LIU K, LIU X M,etal.. Critical shell thickness of core/shell upconversion luminescence nanoplastform for FRET application [J].J.Phys.Chem.Lett., 2011, 2(17):2083-2088.
[4] COST A L, RINGER P, CHROSTEK-GRASHOFF A,etal.. How to measure molecular forces in cells: a guide to evaluating genetically-encoded FRET-based tension sensors [J].Cell.Mol.Bioeng., 2015, 8(1):96-105.
[5] VAN DER KROGT G N M, OGINK J, PONSIOEN B,etal.. A comparison of donor-acceptor pairs for genetically encoded FRET sensors: application to the Epac cAMP sensor as an example [J].PLoSOne, 2008, 3(4):e1916.
[6] KEDZIORA K M, JALINK K.FluorescenceResonanceEnergyTransferMicroscopy(FRET) [M]. VERVEER P J. Advanced Fluorescence Microscopy: Methods and Protocols. New York: Springer, 2015:67-82.
[7] KERSHAW S V, SUSHA A S, ROGACH A L. Narrow bandgap colloidal metal chalcogenide quantum dots: synthetic methods, heterostructures, assemblies, electronic and infrared optical properties [J].Chem.Soc.Rev., 2013, 42(7):3033-3087.
[8] MATTSSON L, WEGNER K D, HILDEBRANDT N,etal.. Upconverting nanoparticle to quantum dot FRET for homogeneous double-nano biosensors [J].RSCAdv., 2015, 5(18):13270-13277.
[9] DENNIS A M, RHEE W J, SOTTO D,etal.. Quantum dot-fluorescent protein FRET probes for sensing intracellular pH [J].ACSNano, 2012, 6(4):2917-2924.
[10] LI L, LIU J B, YANG X H,etal.. Quantum dot/methylene blue FRET mediated NIR fluorescent nanomicelles with large Stokes shift for bioimaging [J].Chem.Commun., 2015, 51(76):14357-14360.
[11] DOS SANTOS M C, HILDEBRANDT N. Recent developments in lanthanide-to-quantum dot FRET using time-gated fluorescence detection and photon upconversion [J].TrACTrendsAnal.Chem., 2016, 86:60-71.
[12] ALIVISATOS A P, GU W W, LARABELL C. Quantum dots as cellular probes [J].Annu.Rev.Biomed.Eng., 2005, 7:55-76.
[13] LEI Y, XIAO Q, HUANG S,etal.. Impact of CdSe/ZnS quantum dots on the development of zebrafish embryos [J].J.Nanopart.Res., 2011, 13(12):6895-6906.
[14] LI J L, ZHANG Y H, AI J J,etal.. Quantum dot cluster (QDC)-loaded phospholipid micelles as a FRET probe for phospholipase A2 detection [J].RSCAdv., 2016, 6(19):15895-15899.
[15] WANG S Z, ZHANG J G, CHEN H G,etal.. An optical FRET inhibition sensor for serum ferritin based on Mn2+-doped NaYF4∶Yb, Tm NIR luminescence up-conversion nanoparticles [J].J.Lumin., 2015, 168:82-87.
[16] 高桂园, 刘璐, 付璇, 等. CdTe量子点-罗丹明B荧光共振能量转移法测定溶菌酶 [J]. 发光学报, 2012, 33(8):911-915. GAO G Y, LIU L, FU X,etal.. Fluorescence resonance energy transfer between CdTe QDs and rhodamine B with its application in the determination of lysozyme [J].Chin.J.Lumin., 2012, 33(8):911-915. (in Chinese)
[17] HABEEBU S S M, LIU J, KLAASSEN C D. Cadmium-induced apoptosis in mouse liver [J].Toxicol.Appl.Pharmacol., 1998, 149(2):203-209.
[18] GESZKE-MORITZ M, PIOTROWSKA H, MURIAS M,etal.. Thioglycerol-capped Mn-doped ZnS quantum dot bioconjugates as efficient two-photon fluorescent nano-probes for bioimaging [J].J.Mater.Chem. B, 2013, 1(5):698-706.
[19] DAS U. Development of ZnS nanostructure based luminescent devices [J].ImperialJ.Interdiscip.Res., 2016, 2(6): 627-630.

翟英歌(1989-),女,吉林长春人,硕士,2016年于长春理工大学获得硕士学位,主要从事纳米材料制备及光学性质的研究。

E-mail: 187149072@qq.com 徐铭泽(1988-),女,吉林长春人,博士,讲师,2014年于吉林大学获得博士学位,主要从事纳米材料的研究。
E-mail: llmingze@foxmail.com
Properties of Fluorescence Resonance Energy Transfer of ZnS∶Cu-Rhodamine
BZHAI Ying-ge1, CHU Xue-ying1, XU Ming-ze1*, LI Jin-hua1, JIN Fang-jun1, WANG Xiao-hua2
(1.SchoolofScience,ChangchunUniversityofScienceandTechnology,Changchun130022,China; 2.InternationalEducationandExchangeCollege,ChangchunUniversityofScienceandTechnology,Changchun130022,China)
*CorrespondingAuthor,E-mail:llmingze@foxmail.com
In order to solve the biological toxicity of fluorescence resonance energy transfer (FRET) system based on quantum dots, non-toxic ZnS∶Cu quantum dots and Rhodamine B were chosen to construct FRET system. ZnS∶Cu nanocrystalline quantum dots with good morphology were successfully prepared by precipitation method. On this basis, the fluorescence spectra of ZnS∶Cu quantum dots with different concentration of copper and fluorescence spectra of Rhodamine B were tested. Then, FRET system with ZnS∶Cu quantum dots as donor and Rhodamine B as acceptor was successfully constructed by the surface modification. Experimental results indicate that the emission spectrum of ZnS∶2%Cu matches the excitation spectrum of Rhodamine B most in 481 nm. So the optimum copper doping mole fraction for the construction of FRET system is 2%. The energy transfer efficiency of ZnS∶Cu quantum dots as donor and Rhodamine B as acceptor is 25.8%. Further experimental results indicate that the concentration of Rhodamine B also can affect the energy transfer.
ZnS∶Cu; Rhodamine B; fluorescence resonance energy transfer
1000-7032(2017)08-1028-05
2017-01-23;
2017-02-22
国家自然科学基金(61205193); 吉林省科技发展计划(20140520107JH,20140204025GX); 长春理工大学青年科学基金(XQNJJ-2015-03)资助项目 Supported by National Natural Science Foundation of China (61205193); Project of Science and Technology of Jilin Province(20140520107JH,20140204025GX); Science Foundation for Young Scientists of Changchun University of Science and Technology(XQNJJ-2015-03)
O482.31
A
10.3788/fgxb20173808.1028

