高效液相色谱法测定牛奶中安赛蜜、苯甲酸和山梨酸含量
文/吴 腾 何 瑛 杨爱君 纪坤发 杨美丰
高效液相色谱法测定牛奶中安赛蜜、苯甲酸和山梨酸含量
文/吴 腾 何 瑛 杨爱君 纪坤发 杨美丰
(广东燕塘乳业股份有限公司)
建立采用高效液相色谱法测定牛奶中安赛蜜、苯甲酸和山梨酸含量的方法。试验采用C18柱,以甲醇∶乙酸铵溶液(0.02 mol/L)=5∶95(V/V)为流动相进行分离,检测波长230 nm,流速1 mL/min,柱温25 ℃,进样量10 μL。结果表明,样品中的安赛蜜、苯甲酸和山梨酸的最低检出限均为1 mg/kg,平均加标回收率分别为93.03%、94.56%、90.71%。
牛奶;安赛蜜;苯甲酸;山梨酸;高效液相色谱法
食品添加剂是为改善食品色、香、味等品质,以及为防腐和加工工艺的需要而加入食品中的人工合成或者天然物质。随着经济的发展,在食品生产过程中过量添加食品添加剂的现象越来越普遍,因而我国制定了国家强制标准GB 2760-2014《食品国家安全标准 食品添加剂使用标准》[1],规定了2 000 种以上的食品添加剂限量要求。
苯甲酸和山梨酸是目前食品中使用范围最广的防腐剂。依据相关规定,苯甲酸和山梨酸不允许在牛奶中添加[1],但是牛奶本身含有微量的苯甲酸,为0.40~1.02 mg/kg[2],而在发酵过程中,牛奶中的马尿酸脱甘氨酸生成苯甲酸,酸牛乳中天然苯甲酸含量有所增加[3]。
安赛蜜是食品中常用的人工合成甜味剂,其甜度约为蔗糖的200倍,甜觉快,味质好,不增加血糖含量,适合于糖尿病患者食用[4]。但经常食用合成甜味剂超标的食品会对人体的肝脏和神经系统造成危害,如果短时间内大量食用,会引起血小板减少导致急性大出血。
为了防止以上3 种物质在食品中超量使用,需要对其进行监控,检验其在食品中的含量,保障消费者的身体健康。目前,食品中安赛蜜的检测方法有高效液相色谱法[5]、液相色谱-串联质谱法[6]、离子色谱法[7]、毛细管电泳法[8]等,苯甲酸和山梨酸的检测方法有高效液相色谱法[9]、薄层色谱法[10]、毛细管电泳法[11]、气相色谱法[12]等。2016年国家颁布GB 5009.28-2016《食品安全国家标准 食品中苯甲酸、山梨酸和糖精钠的测定》[13],在采用该标准对牛奶中的安赛蜜、苯甲酸和山梨酸检验的过程中,发现加标回收率偏低且不稳定,为此,对检验条件进行反复研究,建立采用高效液相色谱法测定牛奶中安赛蜜、苯甲酸和山梨酸含量的方法,通过验证,该方法回收率高,重复性良好,试剂污染少,适合企业日常检验使用。
1 试验材料与方法
1.1 材料
1.1.1 样品
生乳:采自广东、福建、广西等地的奶牛场。
1.1.2 试剂
除非另有说明,本方法所用试剂均为分析纯,水为GB/T 6682-2008《分析试验室用水国家标准》规定的一级水。
亚铁氰化钾溶液(92 g/L):称取106 g亚铁氰化钾,加入适量水溶解,定容至1 000 mL。
乙酸锌溶液(183 g/L):称取220 g乙酸锌溶于少量水中,加入30 mL冰乙酸,用水定容至1 000 mL。
乙酸铵溶液(20 mmol/L):称取1.54 g乙酸铵,加入适量水溶解,定容至1 000 mL,经0.22 μm水相微孔滤膜过滤后备用。
安赛蜜标准储备液(2 000 mg/L):准确称取干燥后的安赛蜜标准品0.1000 g于50 mL棕色容量瓶中,用甲醇溶解并定容至50 mL,混匀后置于4 ℃避光保存。
苯甲酸标准储备液(500 mg/ L):准确称取干燥后的苯甲酸标准品0.0250 g于50 mL棕色容量瓶中,用甲醇溶解并定容至50 mL,混匀后置于4 ℃避光保存。
山梨酸标准储备液(500 mg/ L):准确称取干燥后的山梨酸标准品0.0250 g于50 mL棕色容量瓶中,用甲醇溶解并定容至50 mL,混匀后置于4 ℃避光保存。
安赛蜜、苯甲酸和山梨酸混合标准中间液:分别吸取安赛蜜标准储备液0.5 mL,苯甲酸、山梨酸标准储备液各2 mL于50 mL棕色容量瓶,用纯水定容至50 mL,配制成浓度均为20 mg/L的标准中间液,混匀后置于4 ℃避光保存。
1.1.3 仪器
Agilent 1200液相色谱仪-DAD检测器(美国安捷伦科技公司),电子分析天平(感量0.1 mg,瑞士梅特勒-托利多仪器上海有限公司),离心机(德国希格玛公司),超纯水系统(德国默克密理博公司),超声波清洗器(上海科导公司),电热恒温鼓风干燥箱(上海一恒科学仪器有限公司),涡旋振荡器(广州海太光电生物科技有限公司),移液枪(德国普兰德(Brand)公司);0.22μm水相微孔滤膜,50 mL具塞离心管。
1.2 方法
1.2.1 样品前处理
准确称取2 g(精确到0.001 g)样品于50 mL具塞离心管中,加水约15 mL,涡旋混匀,于50℃水浴超声20 min,冷却至室温后加亚铁氰化钾溶液和乙酸锌溶液各2 mL,混匀,于8 000 r/min离心5 min,将水相转移至50 mL具塞离心管中;于残渣中加水10 mL,涡旋混匀后超声5 min,于8 000 r/ min离心5 min,将水相转移到同一50 mL具塞离心管中,重复操作2次;将萃取液用水定容至40 mL,混匀。取适量萃取液过0.22 μm滤膜待测。
1.2.2 色谱条件
色谱柱:C18柱(Waters HSS T3,5 μm×4.6 mm×150 mm);
流动相:甲醇∶乙酸铵(0.02 mol/L)=5∶95(V/V);
检测波长:230 nm;
柱温:25 ℃;
流速:1 mL/min;
进样量:10 μL 。
1.2.3 标准曲线
取10 mL比色管5 支,分别吸取0.025、0.050、0.500、2.000、4.000 mL安赛蜜、苯甲酸和山梨酸混合标准工作液,用水定容至10 mL,配制成浓度为0.05、0.10、1.00、4.00、8.00 mg/L的标准工作液(现配现用),通过液相色谱分析,以标准溶液浓度为横坐标,峰面积为纵坐标绘制标准曲线。
1.2.4 样品测定
将待测溶液上机测定,根据计算公式得到样品中安赛蜜、苯甲酸和山梨酸的含量。
1.2.5 计算公式
样品中的安赛蜜、苯甲酸和山梨酸的含量按以下公式计算:

X—样品中安赛蜜、苯甲酸、山梨酸的含量,mg/kg;
A—样品中各检测物质峰面积;
C—标样中各检测物质浓度,mg/L;
V—样品最终定容体积,mL;
As—标样中各检测物质峰面积;
m—样品取样量,g。
2 分析与讨论
试验从样品的萃取次数、定容体积及萃取溶剂三方面进行调整,最后根据交叉试验结果选择最优的试验条件。mL,每个加标水平重复5 次,得出样品的平均加标回收率和相对标准偏差(RSD值),试验结果如表1所示。
从表1可以看出,三次萃取时各组分的加标回收率均优于二次萃取,且三次萃取时回收率的RSD值小于两次萃取,重复性较好,因而选择萃取次数为三次。1.2.1的步骤进行,分别使用45、35、25 mL的水对加标样品进行二次萃取,最后用水定容至50、40、30 mL,每个加标水平重复5 次,试验结果如表2所示。
从表2可以看到,最终定容体积分别为50 mL和40 mL时,各组分加标回收率相对较好,但山梨酸的加标回收率仍不理想,保留这两个试验条件待下一步的试验研究。
2.2 定容体积的选择
2.3 萃取溶剂的选择
2.1 样品萃取次数的选择
试验按1.2.1的步骤进行,使用45 mL水分别对加标样品进行二次和三次萃取,最后用水定容至50
为了在充分提取样品的同时尽量减少样品稀释带来的试验误差,试验比较最终定容体积分别为50、40、30 mL时,样品中安赛蜜、苯甲酸及山梨酸的平均加标回收率,以选择最佳的定容体积。试验按
从以上试验可以发现山梨酸的加标回收率并不理想,山梨酸微溶于水,能溶于有机溶剂,因此将萃取溶剂进行调整,分别比较用水和50%甲醇水(V/V)进行萃取时,样品中安赛蜜、苯甲酸及山梨酸的平均加标回收率,选择最佳的萃取溶剂。试验按1.2.1的步骤进行,分别使用45 mL水和50%甲醇水对加标样品进行二次萃取,最后定容至50 mL,每个加标水平重复5 次,试验结果如表3所示。
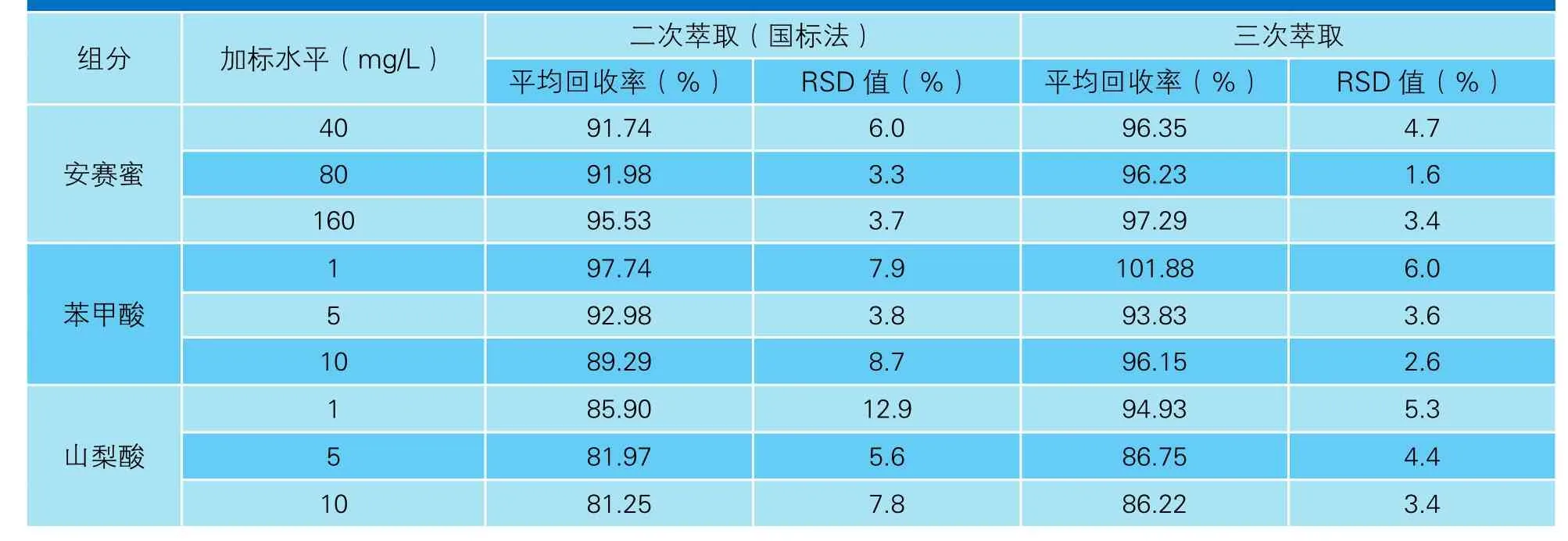
表1 不同萃取次数的样品加标回收率
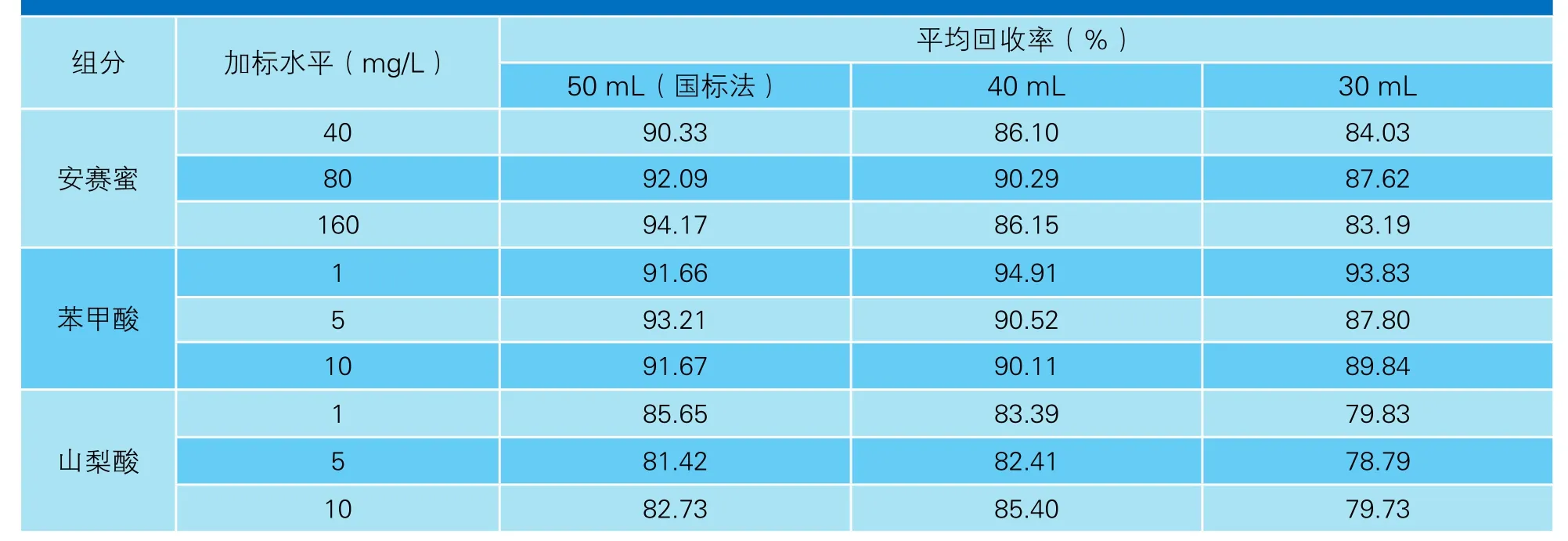
表2 不同定容体积的样品加标回收率
从表3可以看出,使用50%甲醇水提取时,山梨酸的加标回收率有所提高,而安赛蜜和苯甲酸的加标回收率变化不大,可能是由于安赛蜜和苯甲酸均能溶于水和有机试剂。
2.4 交叉试验
综合上述试验结果,选择萃取次数为三次,最终定容体积分别为50 mL和40 mL,萃取溶剂分别为水和50%甲醇水几个条件进行交叉试验,和国标法(二次水萃取、最终定容至50 mL)对比,得出样品的平均加标回收率,同时计算出RSD值,以选择出最优的试验方法。试验按1.2.1中的步骤进行,分别对样品萃取次数、最终定容体积及萃取溶剂进行调整,每个加标水平重复5 次,试验结果如表4和表5所示。
从表4和表5可以看出:(1)各方法的安赛蜜回收率差别不大,均在90%~100%,其中使用50 mL 50%甲醇水三次萃取及使用40 mL水三次萃取的回收率RSD值较小,均低于2%;(2)苯甲酸回收率普遍较好,均在90%~110%,其中使用40 mL水和50%甲醇水三次萃取这两种方法的RSD值较小,均低于5%;(3)使用50%甲醇水萃取时山梨酸的回收率较高,在89%~100%,使用40 mL水三次萃取时山梨酸的回收率次之,在88%~96%,其中使用50 mL 50%甲醇水三次萃取及40 mL水三次萃取这两种方法的回收率RSD值较小,均低于5%。
综合各方法回收率及RSD值,考虑到减少稀释倍数带来的试验误差及试剂污染等因素,选择分别使用15、10、10 mL水三次萃取样品,最后用水定容到40 mL为最终试验方案。该试验方案与国标法相比较,回收率较高,重复性良好。

表3 不同萃取溶剂的样品加标回收率
3 结果与验证
3.1 标准曲线的绘制
在试验选定的色谱条件下,将1.2.3中所配制的标准工作液依次上机测定,以标准溶液浓度为横坐标,峰面积为纵坐标绘制标准曲线,如图1所示。制得的标准曲线相关系数R2值分别为安赛蜜0.9999,苯甲酸0.9999,山梨酸0.9999。

表4 交叉试验的样品加标回收率

表5 交叉试验样品加标回收率的RSD值

图1 标准曲线

表6 重复试验样品加标回收率及RSD值
3.2 检出限和回收率
使用选定的试验方法进行6 次重复试验,得出方法中安赛蜜、苯甲酸和山梨酸的最低检出限均为1 mg/kg,各组分平均加标回收率分别为99.29%、90.46%、95.96%,RSD值分别为3.4%、3.9%、2.4%,回收率高,重复性良好,试验结果如表6所示。
4 小结
4.1使用本方法测得生乳样品中苯甲酸含量均低于1.38 mg/kg,与相关文献报道结果一致[2];巴氏杀菌乳样品中苯甲酸含量均低于1.09 mg/kg,发酵乳样品中苯甲酸含量为4.20~5.45 mg/kg,灭菌型含乳饮料样品中苯甲酸含量均低于1.73 mg/kg;各样品中均未检出山梨酸;测得含乳饮料样品中安赛蜜含量为137.62~155.24 mg/ kg,符合GB 2760-2014《食品国家安全标准 食品添加剂使用标准》中的规定。
4.2本方法与国标法相比较,回收率高,重复性良好,适用于牛奶中安赛蜜、苯甲酸和山梨酸含量的日常监测。
[1] 国家卫生和计划生育委员会. GB 2760-2014食品安全国家标准 食品添加剂使用标准[S].北京:中国标准出版社,2014.
[2] 曹燕,刘昊. 原料乳中苯甲酸质量分数的影响因素和控制初探[J]. 生命科学仪器,2010(8):58-60.
[3] 吴丽莉. 发酵乳制品中苯甲酸的来源及水平[J]. 中国乳品工业,2007(35):3.
[4] 阮春梅. 食品添加剂应用技术[M]. 北京:中国农业出版社,2008.
[5] 刘峰. 食品中安赛蜜的两种快速检测方法比较[J]. 湖州师范学院学报,2017,39(2):27-30.
[6] 邵明媛. 液相色谱-串联质谱法同时测定调制乳制品中5种人工合成甜味剂[J]. 分析试验室,2017,36(1):96-99.
[7] 赵士权,查河霞. 离子色谱法测定食品中的安赛蜜含量[J]. 食品安全质量检测学报,2016,7(5):1840-1843.
[8] 张静. 毛细管电泳法同时测定饮料中的阿斯巴甜、糖精钠和安赛蜜[J]. 现代预防医学,2014,41(20):3768-3770.
[9] 王克新. HPLC法测定乳制品中的苯甲酸和山梨酸含量[J]. 中国乳品工业,2006,3 4(4):54-55.
[10] 柳毅. 牛乳中掺防腐添加物的检验及评价[J].畜牧兽医科技信息,2016(10):23.
[11] 曾暖茜,谢天尧. 食品中苯甲酸和山梨酸的毛细管电泳-电导法分离测定[A]. 第三届全国微全分析系统学术会议文集[C]. 武汉:武汉大学,2005:248-249.
[12] 李林,汪书红. 3种食品防腐剂的气相色谱法检测研究[J]. 现代预防医学,2009,36(17):3342-3345.
[13] 国家卫生和计划生育委员会、国家食品药品
监督管理总局. GB 5009.28-2016食品安全国家标准食品中苯甲酸、山梨酸和糖精钠的测定[S]. 北京:中国标准出版社,2016.
Determination of Acesulfame,Benzoic Acid and Sorbic Acid in Milk by High Performance Liquid Chromatography
WU Teng,HE Ying,YANG Ai-jun,JI Kun-fa,YANG Mei-feng
(Guangdong Yantang Dairy Corporation Ltd.)
A method for detecting acesulfame,benzoic acid and sorbic acid in milk by high performance liquid chromatography(HPLC)was built. A C18column was used,and methanol∶ammonium acetate(0.02 mol/L)= 5∶95(V/V) as mobile phase(1 mL/min) to separate. The detector wave was at 230 nm,the flow rate was 1 mL/min,the column temperature was 25 ℃and the sample quantity was 10 μL. Results showed the minimum detectable value of acesulfame,benzoic acid and sorbic acid is 1 mg/kg,and the average recovery rates are 93.03%,94.56%,90.71%.
milk;acesulfame;benzoic acid;sorbic acid;HPLC
吴腾(1989-),女,食品助理工程师,广东燕塘乳业股份有限公司品控部检验员,主要从事乳制品检测工作。
2017-06-15)

