硫酸催化竹粉新型基碳材料的制备
王 澍,王 杰
(黄山学院 化学化工学院,安徽 黄山 245041)
硫酸催化竹粉新型基碳材料的制备
王 澍,王 杰
(黄山学院 化学化工学院,安徽 黄山 245041)
利用硫酸催化竹粉制备新型基碳材料,通过调节反应时间、反应温度、硫酸的浓度,获得硫酸催化竹粉制备新型基碳材料的最佳工艺条件。 结果表明 90%的硫酸在 90℃下催化竹粉 6h, 其碳化率可高达54%。 为竹材资源特别是短纤维竹粉(竹屑)等的生态高值化理论和应用提供了新的途径。
竹粉;催化;基碳材料
随着能源短缺和环境问题的日益突出,进行清洁可再生能源的开发以满足人类社会生存和发展需要已成为全世界关注的热点。基碳材料具有广泛的潜在优越性,在机械、化学、物理、医药及材料等领域具有广阔的应用前景,尤其是其在材料方面的应用 ,正 受到越来越 多的关注[1-3]。 利用大自然中 可再生的,拥有大量有机碳的生物质成为人类未来首选资源[4]。 传统 生 物质 利 用 技术 需对原料 进行干 燥 ,增加 了 设 备 成 本 和 能 耗 , 制 约 了 生 物 质 能 的 发 展[5,6]。而将水作为反应介质,在一定温度和催化作用下将生物质转化为基碳材料,廉价易得,理化特性简单。 基碳 材 料 应 用 广 泛 , 如 : 催 化[7]、 储 氢[8]、 生 物 医 学[9]、 水处 理[10]、二 氧 化 碳 吸 附[11]、甲 醇 燃 料 电 池[12]、电 容 器[13]等,因此这种理想的制备基碳材料的方法为生物质能的发展提供新的有利途径。
我国江南地区竹材资源丰富,国家对竹材资源的综合开发利用也逐步展开,特别是竹质工程材料。 主要的产品有竹集成材、竹层积材和分级竹丝等复合材料。而在竹材加工的下脚料的化学综合利用方面,还鲜有研究报道。
本文通过对获得的短纤维竹粉(竹屑)进行硫酸催化处理,以获得廉价易得,理化特性简单的基碳材料。旨在为最终实现竹材剩余物的全效(100%)利用提供应用的理论依据,也为竹材资源的生态高值化理论和应用提供新的途径。
1 实验部分
1.1 实验用试剂
竹粉:黄山市金泰竹业有限公司提供,将竹材加工的下脚料过 10 目筛网,放入 105℃电热鼓风干燥 2 小时后放入干燥器中备用;硫酸 :A.R.级,由西陇化工股份有限公司提供。
1.2 实验主要仪器
巩义市予华仪器有限责任公司 HH-S恒温水浴锅, 上海博迅实业有限公司 GZX-9030 电热鼓风干燥箱, 巩义市予华仪器有限责任公司 SHZ-D (Ⅲ)循 环 水式真 空水泵, 美 国 Nicolet (尼 高 力 ) 公 司Nicolet380 红外光谱仪,珀金埃尔默仪器有限公司TGA4000 热重分析仪。
1.3 实验方法
1.3.1 竹粉基碳材料的制备
(1)称取竹粉 6.00g,按照固液比为 1:15,依次取30%,40%,50%,60%,70%,80%,90%,95%浓度的新制硫酸溶液混合均匀,75℃的恒温水浴加热 6h,自然冷却至室温, 洗涤、 真空抽滤至滤液 pH= 7,120℃真空干燥 10h,即得产品。
(2)称取竹粉 6.00g,按照固液比为 1:15,取(1)中胶体碳产率最高浓度的新制硫酸溶液混合均匀,分别置于 75℃,80℃,85℃,90℃,95℃的恒温水浴加热 6h,自然冷却至室温,洗涤、真空抽滤至滤液 pH= 7,120℃真空干燥 10h,即得产品。
(3)称取竹粉 6.00g,按照固液比为 1:15,取上述(1) 中胶体碳产率最高浓度的新制硫酸溶液混合均匀,置于(2)中胶体碳产率最高温度下的恒温水浴加热 1h,2h,4h,6h,8h,10h,自然冷却至室温,洗涤、真空抽滤至滤液 pH=7,120℃真空干燥 10h,即得产品。
1.3.2 竹粉基碳材料热重分析检测
采用珀金埃尔默仪器有限公司 TGA4000 热重分析仪对样品进行热失重分析,温度范围 50-850℃,升温速率 10℃/min。
1.3.3 竹粉基碳材料红外光谱分析
采用美国 Nicolet(尼高力)公司 Nicolet380 红外光谱仪,用 KBr压片法测定,扫描速度为 32 次/秒,分辨率为 4cm-1。
2 结果与讨论
2.1 碳化产率的分析
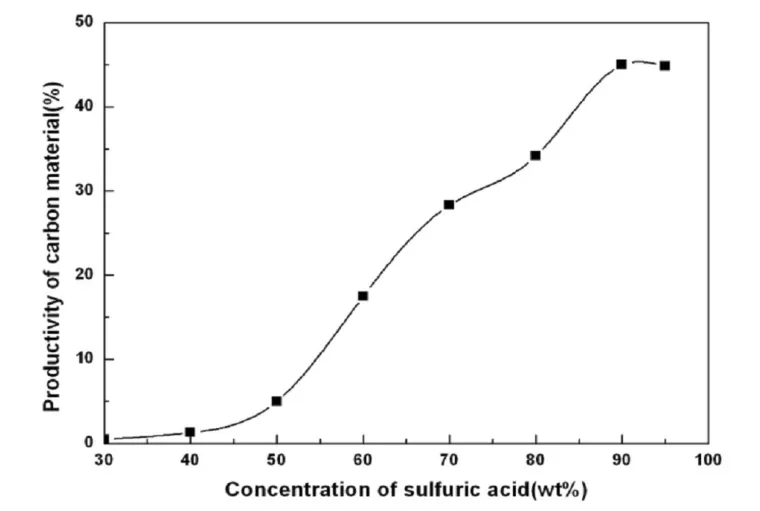
图1 硫酸浓度对碳化产率的影响
图1 为 分 别 取 30% ,40% ,50% ,60% ,70% ,80%,90%,95%浓度的新制硫酸溶液与 6.00g 竹粉按照固液比为 1:15 混合均匀,75℃的恒温水浴加热6h,自然冷却至室温,洗涤、真空抽滤至滤液 pH= 7,120℃真空干燥 10h,所得基碳材料产率与硫酸浓度的关系图。
由图1可以看出竹粉基碳产率随着硫酸浓度的增加而增加,当硫酸浓度达到 90%时基碳产率达到最高点,继续增大硫酸浓度,基碳产率略有下降。
图2 为浓度为 90%的新制硫酸溶液与 6.00g 竹粉按照固液比为 1:15 混合均匀, 分别置于 75℃,80℃,85℃,90℃,95℃的恒温水浴加热 6h,自然冷却至室温,洗涤、真空抽滤至滤液 pH=7,120℃真空干燥 10h,所得基碳材料产率与温度的关系图。
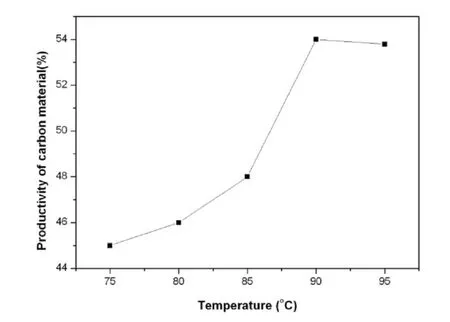
图2 温度对碳化产率的影响
由图2可以看出竹粉基碳产率随着水浴温度的增加而增加,当水浴温度达到 90℃时基碳产率达到最高点,继续提高水浴温度,基碳产率略有下降。
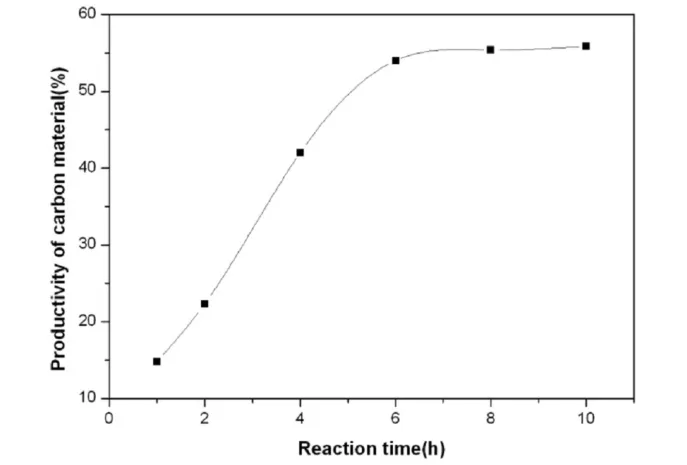
图3 反应时间对碳化产率的影响
图3 为浓度为 90%的新制硫酸溶液与 6.00g 竹粉按照固液比为 1:15 混合均匀,置于 90℃的恒温水浴加热 1h,2h,4h,6h,8h,10h, 自然冷却至室温,洗涤、真空抽滤至滤液 pH=7,120℃真空干燥 10h,所得基碳材料产率与反应时间的关系图。
由图 3可以看出在反应时间低于 6h时, 竹粉基碳产率随着反应时间的增加而显著增加,而当反应时间继续增加时,竹粉基碳产率随反应时间的增加基本趋于不变。
2.2 竹粉基碳材料的结构和性能测试
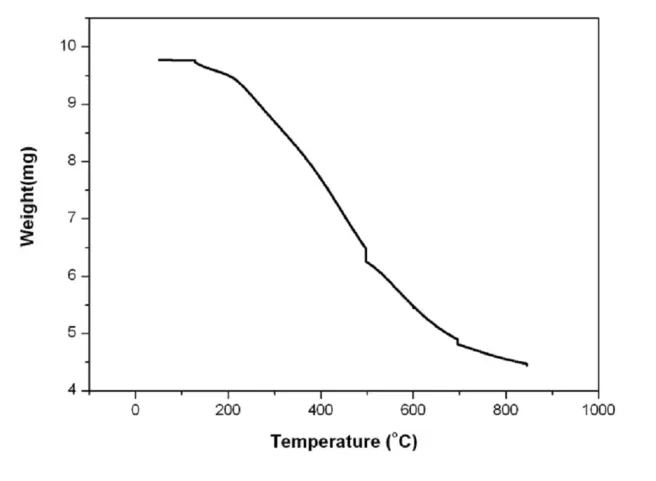
图4 竹粉基碳材料热重分析图谱
图4为竹粉基碳材料的热重分析图谱。从图中可以看出,120℃之前无失重现象, 说明基碳材料中无结合水等挥发性物质,200-845℃均匀失重,说明基碳材料结构均一。
图5为竹粉基碳材料的红外光谱图。从图中可以看出, 在 3414cm-1处的峰属于 O-H 基伸缩振动产生的吸收峰,2500-1900cm-1区域为叁键和累积双键区, 主要包括-C≡C、-C≡N 等叁键的伸缩振动,以及-C=C=C、-C=C=O 等累积双键的不对称性伸缩振动。 1900-1200cm-1范围主要是 C=O 和 C=C 键的伸缩振动。 1000-1300cm-1主要是 C-O 的伸缩振动。400-900cm-1区域是一些重原子伸缩振动和一些变形振动。 由图可见,竹粉基碳材料中丰富的 O-H 基等官能团为该基碳材料的综合利用提供了契机。
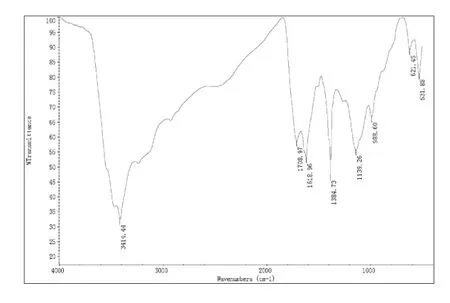
图5 竹粉基碳材料的红外光谱
3 结 论
实验利用硫酸催化竹粉来制备新型基碳材料,通过调节反应时间、反应温度、硫酸的浓度,获得硫酸催化竹粉制备新型基碳材料的最佳的工艺条件,为生物质能的发展提供新的有利途径。
产品竹粉基碳材料通过红外光谱和热重手段分析,可知其中不含结合水等挥发性物质,结构均一,且含有丰富的羟基、醚基、酯基、碳碳双键等官能团,从结构上为它在染料吸附、催化剂载体、电化学等方面的综合利用提供了依据,有利于我国江南地区丰富竹材资源的生态高值化。
[1]孙 振 钧 .中 国 生 物 质 产 业 及 发 展 取 向 [J].农 业 工 程 学 报 ,2004,20(5):1-5.
[2]周 中 仁 ,吴 文 良.生 物 质 能 研 究 现 状 及 展 望[J].农 业 工 程 学报,2006,21(12):12-15.
[3]王泽,林伟刚,宋文立,等.生物质热化学转化制备生物燃料及化学品[J].化学进展,2007,19(7/8):1190-1197.
[4]王 霞 ,汪 春.稻 草 纤 维 素 的 提 取 及 其 结 构 表 征 [J].黑 龙 江 八一农垦大学学报,2010,22(1):68-73.
[5]Gao Y,Chen H,Wang J,et al.Characterization of products from hydrothermal liquefaction and carbonation of biomass model compounds and real biomass[J].Journalof Fuel Chemistry and Technology,2011,39(12):893-900.
[6]Gao Y,Wang X H,Yang H P,et al.Characterization of products from hydrothermal treatments of cellulose[J].Energy, 2012,42(1):457-465.
[7]Upare D P,Yoon S,Lee C W.Nano-structured porous carbon materials for catalysis and energy storage[J].Korean J. Chem.Eng.,2011,28:731-743.
[8]Yang S J,Jung H,Kim T, et al.Recent advances in hydrogen storage technologies based on nanoporous carbon materials [J].Progress in NaturalScience:Materials International,2012,22 (6):631-638.
[9]Michel M,Buszewski B.Porous graphitic carbon sorbents in biomedical and environmental applications[J].Adsorption,2009,15:193-202.
[10]Nunell G V,Fernandez M E,Bonelli P R,et al.Conversion ofbiomass from an invasive species into activated carbons for removal of nitrate from wastewater[J].Biomass and Bioenergy,2012,44:87-95.
[11]Dobele G,Dizhbite T,Gil M V,et al.Production of nanoporouscarbonsfrom wood processing wastesand their use in supercapacitors and CO2capture[J].Biomass and Bioenergy,2012,46:145-154.
[12]Lee J,Park Y,Yang O,et al.Synthesis of porous carbons having surface functional groups and their application to direct-methanol fuel cells[J].Journal of Power Sources,2006,158:1251-1255.
[13]Yamadaa H,MorlguchiI,KudoT.Electricdoublelayer capacitance on hierarchical porous carbons in an organic electrolyte[J].Journal of Power Sources,2008,175:651-656.
责任编辑:胡德明
A New Carbon Material Preparation with Bamboo Powder Using Sulfuric Acid as the Catalyst
Wang Shu,Wang Jie
(College of Chemistry and Chemical Engineering,Huangshan University,Huangshan 245041,China)
Sulfuric acid is used as the catalyst to prepare a new carbon material with bamboo powder. The most favorable conditions of the preparation are obtained by controlling reaction time,temperature and sulfuric acid concentration.The results indicate that the carbonation rate of bamboo powder can reach 54% after a 6-hour reaction in 90%sulfuric acid concentration at 90℃ ,which provides a new method to the study and maximum use of bamboo resources(short fiber bamboo powder in particular).
bamboo powder;catalyze;carbon mate,lial
O69
:A
:1672-447X(2017)03-0047-03
2016-12-06
安徽省大学生创新创业计划项目(AH201310375051);黄山学院自然科学研究项目(2011xkj014)
王澍(1979-),安徽歙县人,黄山学院化学化工学院讲师,研究方向为天然产物提取与纳米催化。

