重组人血管内皮抑素联合放化疗治疗高级别人脑胶质瘤的临床疗效
靳彩玲 赵树鹏 杨 军 陈美玲 亢晓春 牛红蕊 张 敏△
新乡医学院第一附属医院 1)肿瘤科 2)神经外科 卫辉 453100
重组人血管内皮抑素联合放化疗治疗高级别人脑胶质瘤的临床疗效
靳彩玲1)赵树鹏2)杨 军1)陈美玲1)亢晓春1)牛红蕊1)张 敏1)△
新乡医学院第一附属医院 1)肿瘤科 2)神经外科 卫辉 453100
目的 探讨重组人血管内皮抑素联合放化疗治疗高级别胶质瘤的临床疗效及安全性。方法 回顾性分析新乡医学院第一附属医院2012-01—2014-12收治的80例高级别人脑胶质瘤患者,其中40例采取放疗联合替莫唑胺化疗的患者为对照组,40例在对照组的基础上加用重组人血管内皮抑素治疗的患者为观察组。治疗后随访2 a并进行实体肿瘤客观疗效、药物安全性的评定。结果 对照组和观察组的有效率分别为45.0%和70.0%,差异有统计学意义(P<0.05)。1 a、2 a存活率分别为50.0%、35.0%和72.5%、62.5%,差异有统计学意义(P<0.05)。本组病例不良反应多为Ⅰ~Ⅱ级,无Ⅲ级以上的反应,不良反应差异无统计学意义(P>0.05)。结论 重组人血管内皮抑素联合放化疗治疗高级别胶质瘤能显著提高近远期临床疗效,安全性高,值得进一步临床研究。
胶质瘤;调强放疗;重组人血管内皮抑素;替莫唑胺
高级别脑胶质瘤是指颅内WHO分级为Ⅲ~Ⅳ级的高度恶性肿瘤,呈浸润性生长,手术不易全切,复发率及病死率较高,主要包括间变性星形细胞瘤和多形性胶质母细胞瘤。近年来,替莫唑胺联合放疗对高级胶质瘤的治疗已取得较好的疗效,但预后仍不满意,平均生存时间约为14.6个月[1]。研究发现,肿瘤的生长、浸润和转移与肿瘤的血管形成密切相关,抑制肿瘤新生血管的生长能减少肿瘤的复发率。恩度(重组人血管内皮抑素)是我国自主研发的新型抗血管生长药物,可通过调控下游靶基因,如VEGF等的表达及蛋白水解酶的活性,多靶点发挥抗血管生成作用[2]。本研究回顾性分析2012-01—2014-12新乡医学院第一附属医院肿瘤科收治的80例高级别胶质瘤患者的临床资料,探讨重组人血管内皮抑素联合放化疗治疗高级别胶质瘤的近远期疗效和不良反应。
1 资料与方法
1.1 一般资料 本组80例患者中男42例,女38例,年龄18~70岁,平均45.4岁,生活质量功能状态评分(KPS评分)均>60分。术后病理结果均证实WHO分级为Ⅲ~Ⅳ级脑胶质瘤,其中Ⅲ级34例(包括21例间变型星形细胞瘤,9例间变型少突-星形细胞瘤,4例间变少突胶质细胞瘤),多形性胶质母细胞瘤46例。肿瘤部位:额叶25例,颞叶22例,顶枕叶15例,岛叶12例,脑干4例,丘脑2例。80例患者分为对照组(40例)和观察组(40例),对照组采取替莫唑胺联合放疗,观察组在替莫唑胺联合放疗的基础上加用重组人血管内皮抑素。
入组标准:(1)病理诊断明确为脑胶质瘤Ⅲ~Ⅳ级;(2)年龄18~70岁;(3)KPS评分>60分,预计生存期>3个月,无明显放、化疗禁忌;(4)本次治疗前后未接受过其他放、化疗;(5)磁共振上有可测量的病灶;(6)均签署知情同意书。
1.2 治疗方法 放疗:对照组采取同期放化疗,放疗采用CT模拟定位调强放射治疗技术,患者仰卧位,并用热塑头颈罩进行固定,激光灯摆位。从颅顶至下颌边缘行CT连续扫描,层厚3 mm,采集影像资料。在MRI 指导下,进行靶区勾画,勾画肿瘤靶区(GTV),高危CTV1为T1加权像肿瘤增强区域+外放2 cm,低危CTV2为T1加权像肿瘤增强区域+FLAIR/T2加权像上的异常区域+外放2 cm。计划靶区(PTV)为CTV 外放0.5 cm,GTV 、CTV1和CTV2均需要外扩处理5 mm,分别将其定义为PGTV、PTV1 和PTV2。处方剂量:PGTVnx 63 Gy/30次,PTV1 60 Gy/30次,PTV2 54 Gy/30次。采用6 MV X线,每周5次。
化疗:在放疗期间按75 mg/(m2·d)口服替莫唑胺,同步放化疗结束后4周进行6个周期的替莫唑胺辅助治疗,第1周期的剂量150 mg/(m2·d),连续口服5 d,然后停药23 d,第2周期200 mg/(m2·d)。观察组在同步放化疗第1天给予重组人血管内皮抑素15 mg/d,加入生理盐水500 mL中缓慢静脉滴注,连续14 d,21 d为1周期,共4个周期。依据2组患者治疗期间的病情给予激素、脱水、止吐、护胃、保肝等对症治疗。
治疗期间,每周复查血常规,肝肾功电解质、心电图等,评价其不良反应。第1年内每3个月复查1次,1 a后每半年复查1次,均行头颅增强MRI检查,评价疗效。末次随访时间2016-10。其中对照组2例失访,观察组1例失访,失访时间按死亡时间计算。
1.3 评价标准 近期疗效评价依据新的实体瘤疗效评价标准(RECIST)[3]:完全缓解(CR):全部病灶消失,至少维持4周;部分缓解(PR):缩小至少30%,至少维持4周;稳定(SD):介于PR和PD之间;进展(PD):增加超过20%,或出现新的病灶。有效率(RR)=CR+PR。不良反应评估参照美国国家癌症研究所不良事件常用术语评定标准(CT-CAE)4.0版进行评价。
1.4 统计学方法 采用SPSS 20.0软件进行统计学分析,定性资料以率或百分比表示,2组间比较采用四格表χ2检验,多组比较采用行×列表的χ2检验。检验水准α=0.05,P<0.05为差异有统计学意义。
2 结果
2.1 治疗完成情况 80例高级别人脑胶质瘤患者均完成放疗,随访中1例因替莫唑胺的骨髓抑制行3周期辅助化疗后未再继续化疗,其他患者均未因治疗的不良反应中断TMZ辅助治疗。随访中若出现可复发及进展,则不再继续进行TMZ的后续治疗。
2.2 2组近期疗效比较 治疗前行颅脑MRI增强扫描判断肿瘤大小,放疗结束后4周行MRI增强扫描。观察组总有效率70.0%,对照组为45.0%,2组比较差异有统计学意义(P<0.05)。见表1。
2.3 2组远期疗效比较 2组1 a、2 a总生存率比较差异有统计学意义(P<0.05)。见表2。
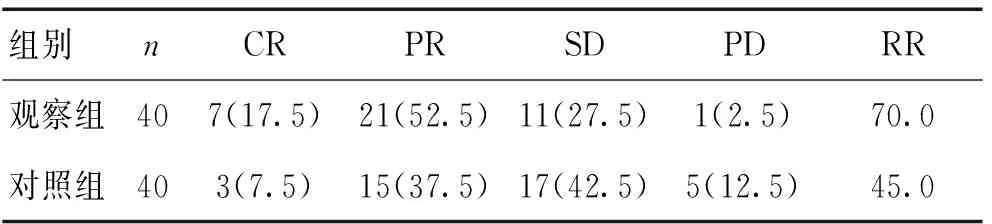
表1 2组近期疗效比较 [n(%)]

表2 2组远期疗效比较 [n(%)]
2.4 2组不良反应比较 2组近期不良反应主要是骨髓抑制、消化道反应、肝功能异常等,多为Ⅰ、Ⅱ级,无Ⅲ级以上不良反应。观察组中15例出现恶心,对照组中13例出现恶心,给予护胃、止吐治疗后症状均得到缓解。观察组中15%的患者出现高血压,对照组中5%的患者出现高血压,这种高血压为一过性高血压,是恩度联合替莫唑胺特有的不良反应,停药后血压恢复正常。2组均有轻度肝功损伤,给予异甘草酸镁保肝治疗后,肝功恢复正常。2组胃肠反应、骨髓抑制、肝功异常等不良反应发生率比较差异均无统计学意义(P>0.05,表3),2组均未见心脏、肾脏损伤,未见皮肤过敏反应,未见放射性脑病。

表3 2组不良反应比较 [n(%)]
3 讨论
人脑胶质瘤是颅内常见的恶性肿瘤,呈浸润性生长,恶性程度较高,尤其高级别胶质瘤周围组织浸润广泛,肿瘤无边界,有时肿瘤靠近脑功能区,手术难以完全切除,易复发,治疗效果往往不佳[4]。目前,高级别胶质瘤治疗策略是首选在安全范围内尽可能手术切除肿瘤,术后应常规辅以放疗和化疗,以减少肿瘤复发,延长患者的生存周期。
术后替莫唑胺化疗并同步放疗是目前公认的高级别胶质瘤最佳辅助治疗手段。替莫唑胺是第二代口服烷化剂类抗肿瘤药物,完全亲脂性,在体内可不通过肝脏代谢,易透过血脑屏障,在脑肿瘤中的浓度高于正常脑细胞,可作用于肿瘤细胞各个分裂时期,使肿瘤细胞DNA烷基化,为细胞周期非特异性药物,具有广谱抗肿瘤活性。同时替莫唑胺还具有放疗增敏作用,调强放疗联合替莫唑胺化疗可以增强肿瘤细胞对射线的敏感性,同时也可减少肿瘤耐药,从而提高治疗效果[5]。宗庆华等[6]对37例脑间变性星形细胞瘤术后患者进行调强放疗并联合替莫唑胺化疗,结果显示,该治疗方法可在一定程度上改善脑间变性星形细胞瘤术后患者的预后。我们对40例高级别胶质瘤术后常规行替莫唑胺并同步放疗,治疗后总有效率为45.0%,1、2 a总生存率分别为62.5%和35.0%,与文献[7]报道一致。然而,在此种治疗模式下患者的复发率仍较高,替莫唑胺能提高多形性胶质母细胞瘤和间变性星形细胞瘤患者无病生存率,但总体生存时间未明显延长。
研究表明,肿瘤的复发与瘤体内含有乏氧细胞密切相关,肿瘤细胞在快速增殖过程中消耗大量氧,缺氧是恶性肿瘤内部普遍存在的现象[8]。乏氧细胞及其受体能够促进肿瘤新生血管形成,导致肿瘤的侵袭及播散。Seiz等[9]研究认为,低剂量抗血管靶向治疗可能是一种新的辅助治疗手段。恩度是我国自主研制的肿瘤血管内皮增生抑制剂,能通过调控下游靶基因,如血管内皮细胞生长因子(VEGF)及其受体的转录,特异性地抑制血管内皮细胞增殖,从而减少肿瘤新生血管的生成,其对食管癌、宫颈癌、肺癌、大肠癌等多种肿瘤细胞有明显抑制作用[10]。与其他肿瘤一样,在常规放化疗的基础上加用重组人血管内皮抑素不仅能够改善高级别胶质瘤内部的缺氧环境,提高其对放疗的敏感性,且能使肿瘤血管结构暂时正常化,使化疗药物更易进入肿瘤内部,提高肿瘤内部的血药浓度,对放化疗起到协同作用,更加有效地抑制肿瘤的生长,减少复发。李岩等[11]对74例复发性高级别胶质瘤进行临床研究,其中37例恩度联合替莫唑胺联合化疗的患者比单用替莫唑胺化疗的患者有更好的客观疗效,相对延长患者中位无进展生存期。本组结果显示,重组人血管内皮抑素联合放化疗与单纯替莫唑胺联合放疗治疗高级别人脑胶质瘤相比,在治疗初期加入重组人血管内皮抑素,观察组患者治疗有效率、1 a生存率和2 a生存率均显著高于对照组,说明在放化疗的基础上加用恩度能够显著改善脑胶质瘤患者的近期和远期临床疗效,具有协同作用,与相关研究结果一致[12-13]。
恩度常见的药物不良反应主要有心脏不良反应,少见的不良反应主要有消化系统反应、皮肤及附件的过敏反应。观察组患者1~2级胃肠反应发生率为37.5%,无3~4级胃肠反应发生;1~2级骨髓抑制发生率为30.0%,无3~4级骨髓抑制反应发生。观察组与对照组间胃肠反应发生率、骨髓抑制、肝功异常发生率比较差异无统计学意义(P>0.05),2组均未见心脏损伤,未见皮肤过敏反应。本研究显示,在放化疗基础上加用重组人血管内皮抑素,不良反应无明显增加,与文献[14]结果一致。在替莫唑胺化疗并同步放疗治疗高级别胶质瘤的基础上加用重组人血管内皮抑素具有一定的安全性,近、远期疗效好,值得临床推广。
[1] Modrek AS,Bayin NS,Placantonakis DG.Brain stem cells as the cell of origin in glioma[J].World J Stem Cells,2014,6(1):43-52.
[2] Ling Y,Yang Y,Lu N,et al.Endostar,a novel recombinant humanendostatin,execs antiangiogenie effect viablockin VEGF-induced tyrosine phosphorylation of KDR/Flk-1 of endothelial cells[J].Biochem Biophys Res Commun,2007,361(1):79-84.
[3] 石元凯,孙燕.临床肿瘤内科手册[M].6版.北京:人民卫生出版社,2015:136-137.
[4] 王振华,王建华,郭小奇,等.调强放疗联合替莫唑胺胶囊治疗成人Ⅲ~Ⅳ级胶质瘤术后残留临床疗效观察[J].中国全科医学,2013,16(11):3 962-3 964.
[5] 王家清,于云龙,王慧星,等.调强放疗联合替莫唑胺治疗脑胶质瘤术后残余病灶的疗效观察[J].中国实用神经疾病杂志,2016,19(15):55-56.
[6] 宗庆华,闵有会,张辉,等.脑间变性星形细胞瘤术后患者调强放疗联合替莫唑胺化疗临床效果评价及影响因素[J].中国实用神经疾病志,2016,19(2):44-46.
[7] 徐宜全,黄生富.调强放疗联合替莫唑胺胶囊治疗成人Ⅲ~Ⅳ级胶质瘤残留的临床研究[J].医学综述,2016,22(9):1 805-1 807.
[8] 赵树鹏,靳彩玲,赵新利,等.星形细胞瘤组织中生长抑制因子4和缺氧诱导因子-1α的表达及其临床意义[J].中华医学杂志,2015,95(43):3 533-3 536.
[9] Seiz M,Kohlhof P,Brockmannm A,et al.First experiences with low-dose anti-angiogenic treatment in gliomatosis cerebri with signs of angiogenic activity[J].Anticancer Res,2009,29(8):3 261-3 267.
[10] 王慧敏,戈伟,草德东,等.重组人血管内皮抑素联合放疗对Leiwis肺癌小鼠肿瘤生长季VEGF 表达的影响[J].微循环学杂志,2010,20(4):19-21.
[11] 李岩,张俊平,王仲伟,等.重组人血管内皮抑制素联合替莫唑胺治疗复发高级别胶质瘤的临床研究[J].中华脑科疾病与康复杂志:电子版,2014,4(2):8-11.
[12] 白雪红,闫钢,郭艳红.脑胶质瘤术后患者调强放疗联合替莫唑胺治疗的临床疗效观察[J].宁夏医学杂志,2016,38(6):565-567.
[13] 陈卫峰,吴倩岚,莫立根,等.高级别脑胶质瘤术后3D-CRT与替莫唑胺同步放化疗Meta分析[J].中华肿瘤防治杂志,2014,21(7):543-551.
[14] 樊锐太,王书君,王瑞.重组人血管内皮抑素联合放化疗治疗大脑胶质瘤病的效果[J].广东医学,2015, 36(9):1 435-1 437.
(收稿2016-12-08)
Clinicaleffect of recombinant human endostatin combined radiotherapy and chemotherapy for high-grade gliomas
Jin Cailing﹡,Zhao Shupeng,Yang Jun,Chen Meiling,Kang Xiaochun,Niu Hongrui,Zhang Min
﹡Department of Oncology,the First Hospital of Xinxiang Medical College,Weihui 453100,China
Objective To investigate the clinical efficacy and safety of recombinant human endostatin combined radiotherapy and chemotherapy for high-grade gliomas.Methods Totally 80 cases of brain glioma from January 2012 to December 2014 in the First Hospital of Xinxiang Medical College were divided into control group and observation group,40 cases in each group.The control group adopted radiotherapy combined with temozolomide chemotherapy,observation group applied recombinant human endostatin based on the control group.The patients were followed up for 2 years,and the objective curative effect and the safety of drugs were evaluated.Results The effective rate of the control group and the observation group were 45% and 70%,respectively,the difference was statistically significant (P<0.05).The one-year and two-year survival rate was 50%,35% and 72.5%,62.5%,respectively.The difference of survival rate between two groups was statistically significant (P<0.05).The adverse reactions were mostly from gradeⅠto grade Ⅱ.No grade Ⅲ or more adverse reactions were observed.There was no significant difference on adverse reactions (P>0.05).Conclusion Recombinant human endostatin combined radiotherapy and chemotherapy for high grade gliomas can significantly improve the short- and long-term clinical efficacy with a certain safety.It was worth for further clinical study.
Glioma;Intensity modulated radiothempy;Recombinant human endostatin;Temozolomide capsule
R730.264
A
1673-5110(2017)11-0024-04
△通讯作者:张敏,女,副教授,博士,研究方向:肿瘤内科

