271例药品不良反应报告分析
张新毅,刘晓燕
(包头市肿瘤医院,内蒙古 包头 014030)
271例药品不良反应报告分析
张新毅,刘晓燕
(包头市肿瘤医院,内蒙古 包头 014030)
目的:了解肿瘤医院药品不良反应(ADR)发生的特点及规律,为临床合理用药和ADR监测工作提供参考。方法:对我院2014年1月 - 2016年4月上报的ADR进行统计,分析ADR涉及的患者性别、年龄、药品种类、给药途径、累及器官/系统、报告人职业等信息。结果:共报告ADR 271例,女性报告多于男性(60.9% vs. 39.1%);年龄≥50且<70岁患者ADR报告最多(60.1%);静脉给药致ADR发生率最高(94.4%);抗肿瘤药物引起的ADR数居于首位(196例,72.3%);累及器官/系统主要是血液系统毒性(51.7%);严重ADR报告率较高(52.8%);报告人职业中,医师与药师上报例数相近(50.6% vs. 48.3%)。结论:临床治疗中应该加强抗肿瘤药物ADR的监测,以提高患者用药的安全性和治疗依从性。
药品不良反应;分析;抗肿瘤药物;合理用药
随着近年来新上市及新获批的临床药物种类的增加,各类药物不良反应(adverse drug reaction,ADR)发生率也相应升高[1]。ADR监测对药品安全性评价,保障患者用药安全等方面具有重要意义。近年来ADR监测工作受到药品监管部门的重点关注,并于2015年拨付了专项资金对ADR上报人员进行奖励。我院作为肿瘤专科医院,抗肿瘤药物应用非常广泛,相应这类药物引起的ADR也较为常见。本研究对我院2014年 1月 - 2016年4月报告的ADR进行回顾性分析,以期为临床合理用药提供参考依据。
1 资料与方法
选取我院2014年1月 - 2016年4月上报的ADR报告的271例。按照ADR涉及的患者性别、年龄、给药途径、药品种类、累计器官/系统、临床表现及报告人员等情况进行统计分析。
2 结果
2.1 发生ADR患者的性别与年龄分布
271例ADR报告,其中男106例(39.1%),女165例(60.9%)。ADR发生率最高的人群是≥50且<60岁的患者,其次是≥60且<70岁的患者,两个年龄段ADR发生率占60.1%。发生ADR患者的性别与年龄分布见表1。
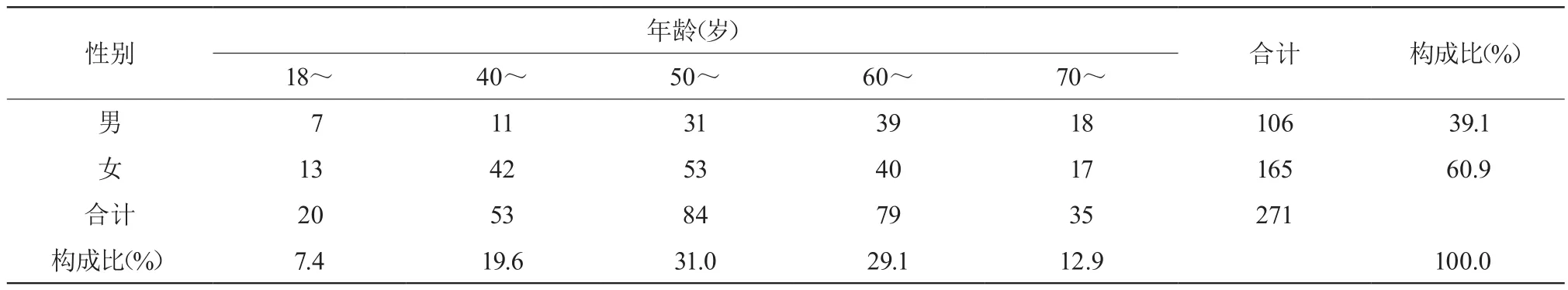
表1 发生ADR患者的性别与年龄分布
2.2 引发ADR的给药途径分布
不同给药途径引起ADR中,以静脉滴注为主,占94.4%。引发ADR的给药途径分布见表2。
2.3 引发ADR的药品种类分布
271例ADR共涉及82种药,其中抗肿瘤药34种(41.5%),其次为抗菌药12种(14.6%);抗肿瘤药引起的ADR共计196例(72.3%)。引发ADR的药品种类分布情况见表3。
2.4 ADR累及器官/系统及临床表现
所有ADR中血液系统反应居首位(占51.7%),主要表现为骨髓抑制,如白细胞、中性粒细胞或血小板降低。其次有全身损害、消化系统反应等。ADR累及器官/系统及临床表现见表4。
2.5 ADR的分级、构成比及转归
271例报告中,一般ADR有128例(47.2%),严重ADR有143例(52.8%)。在ADR结果方面,大部分ADR经过治疗后都能好转或治愈。ADR的分级、构成比、转归见表5。
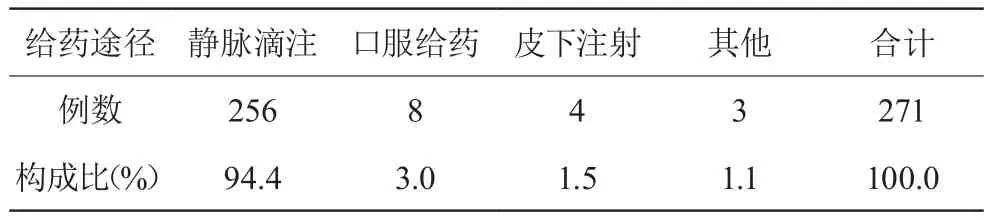
表2 引发ADR的给药途径分布
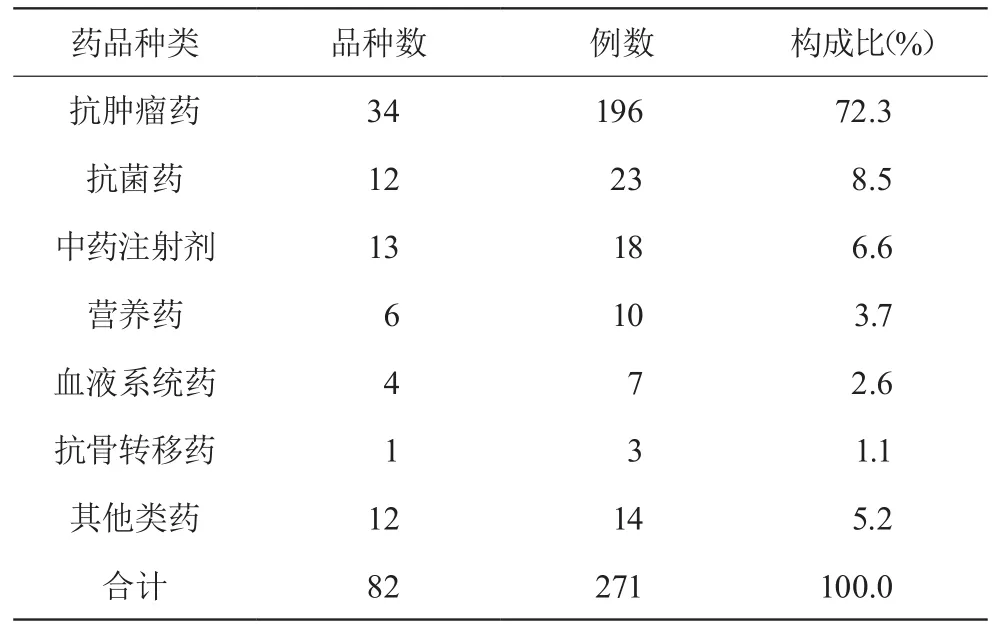
表3 引发ADR的药品种类分布
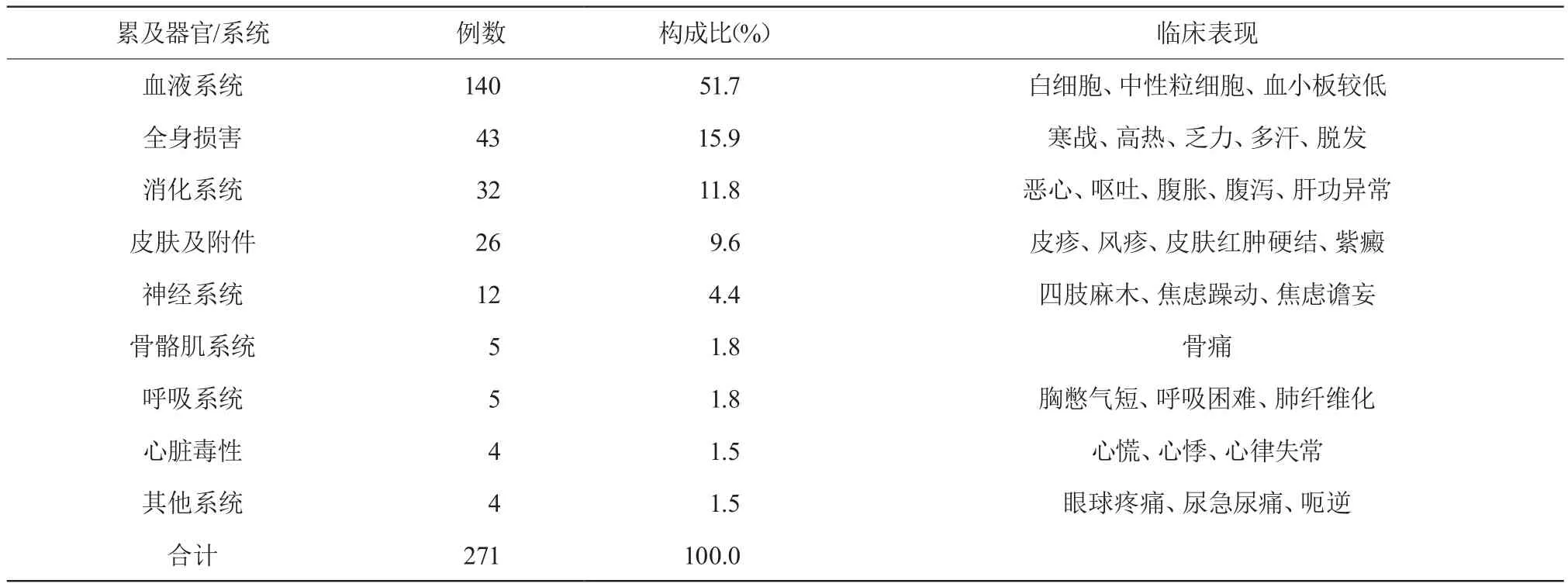
表4 ADR累及器官/系统及临床表现
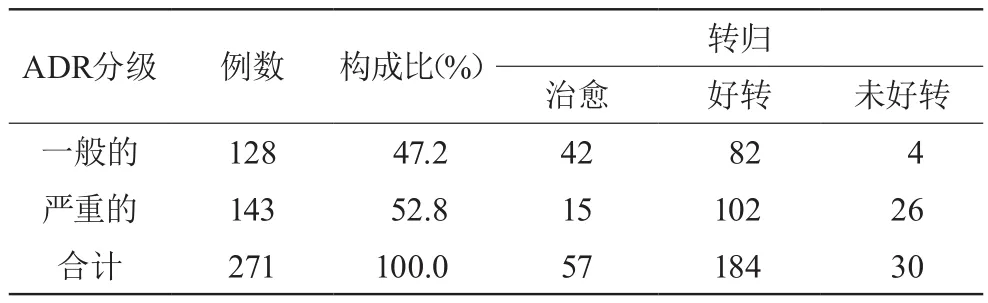
表5 ADR的分级、构成比及转归
2.6 上报ADR人员的职业及构成比
在上报ADR人员中,医师报告的例数最多,有137例(50.6%),其中严重ADR的报告中,药师上报例数最多,占严重ADR报告的62.2%。上报ADR人员的职业及构成比见表6。
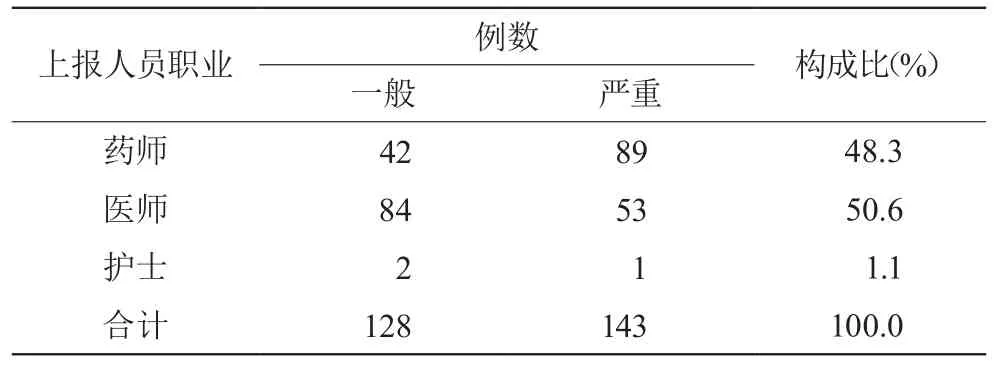
表6 上报ADR人员的职业及构成比
3 讨论
3.1 一般情况分析
表1可见,271例ADR报告中,男女比例为1∶1.56,女性高于男性,与于海燕等[2]报道的结果相似。在发生ADR患者年龄方面,最小为18岁,最大为89岁,≥50且<70岁ADR发生率最高,占60.1%。与我院实际收治的患者情况相符。由表2可见,在引起ADR的给药途径中,静脉给药比例最高,高达94.4%,这与我院门诊患者较少,住院患者大多采用静脉给药治疗的现状相一致。
3.2 引起ADR的药品种类分析
由表3可见,所有药品中,抗肿瘤药物引起的ADR最多,占73.4%。这与我院是肿瘤专科的特点相一致,抗肿瘤药物应用广泛,且这类药品大多数是细胞毒药物,选择性差、治疗窗窄,在杀死肿瘤细胞的同时对人体正常细胞也有杀伤作用,ADR发生率高[3]。此外,肿瘤治疗经常需联合用药,这也进一步增加了ADR的发生率。因此,在使用抗肿瘤药物时,应给予高度重视,积极预防化疗相关不良反应。其他ADR发生率较高的药物有抗菌药物和中药注射剂。
3.3 ADR累及器官/系统及临床表现分析
由表4可见,我院各类ADR中累及血液系统损害的最常见,占51.7%,主要表现为白细胞减少、中性粒细胞减少及血小板减少,这与抗肿瘤药物对生长较快的骨髓造血细胞无选择性杀灭有关。其次ADR累及的器官较多的是全身损害和消化系统反应,分别表现为高热、寒战、发力、多汗等症状和恶心、呕吐、腹泻等症状。全身损害与静脉给药易引起全身各种过敏反应[4]有关;消化系统反应与消化道黏膜细胞增殖活跃,对细胞毒类药物敏感相关[5]。
3.4 严重ADR分析
由表5可见,我院上报的ADR以严重反应为主,占52.8%。其中又以Ⅲ~Ⅵ度骨髓抑制报告最多。这是由于抗肿瘤药物大多具有明显骨髓抑制作用,治疗时经常需要联合用药[6];且化疗期间需经常检查血细胞,数据体现较为直观,严重骨髓对患者影响较大,也较易引起医师、药师及患者的重视。因此在肿瘤治疗过程中应给予高度重视,积极做好预防化疗相关ADR的预防工作,以降低治疗费用并提高患者依从性。
3.5 ADR报告人员职业分析
由表6可见,271例ADR中,医师报告比例占50.6%,药师报告比例占48.3%,护士报告比例仅占1.1%。而在严重ADR报告中,临床药师报告比例占62.2%,体现出在ADR监测中,临床药师对严重ADR更为关注,对ADR分析更为深入。提示临床药师在工作中可以帮助医师,做好ADR的预防与监测,以减少ADR发生率,降低患者经济负担。表6数据也反映出,护士上报的ADR较少,实际工作中护士是用药的一线人员,与患者接触较多,可以在第一时间发现ADR。应加强对护士的培训,提高其对ADR监测重要性的认识,鼓励护士积极上报ADR。
综上所述,我院严重ADR的报告率高于其他医院,引起严重ADR的药物以抗肿瘤药物为主,报告人员以医师和药师为主,报告质量较高。我院的ADR监测工作得到了包头市药品不良反应监测中心的肯定和表彰。在今后的工作中,应进一步加强医师、药师和护士的密切配合,继续加强对合理用药和ADR监测工作的宣传,充分发挥临床药师作用,同时调动临床医师和护士的积极性,加强ADR的监测工作,进而促进临床用药安全、有效、合理。
[1] 荀艳.我院2014年上报的520例药物不良反应报告分析[J].中国临床药学杂志,2016,25(3):191-192.
[2] 于海燕,何粤红,胥小叶.729例临床药品不良反应报告分析[J].中国药物评价,2016,33(1):44-46.
[3] 党和琴,苏风云,尹玲,等.278例药品不良反应报告分析[J].中国医院药学杂志,2015,35(12):1126-1129.
[4] 刘平,徐国防,刘长缨,等.我院368例药品不良反应报告分析[J].中国药房,2015,26(35):4955-4957.
[5] 刘加涛,金亮,汪燕燕,等.我院中肿瘤及辅助治疗药物不良反应164例分析[J].中国药物警戒,2012,9(3):184-186.
[6] 吴颖其,刘琳琳,李青,等.2005-2013年某三甲医院血液系统损害相关药品不良反应报告分析[J].安徽医药,2016,19(12):2435-2437.
本文编辑:苏日力嘎
Analysis of 271 Cases of Adverse Drug Reactions
Zhang Xin-yi, Liu Xiao-yan
(Baotou Tumor Hospital, Inner Mongolia Baotou 014030, China)
Objective:To investigate the characteristics of adverse drug reactions (ADRs) occurred in a tumor hospital and provide a reference for rational drug use and monitoring of ADRs. Methods:The ADRs reported in Baotou Tumor Hospital from January 2014 to April 2016 were analzyed, including the genders and ages of patients as well as the durg species, route of administration, involved organs or systems and report personnel’s career. Results:A total of 271 cases of ADRs were reported, which was more in female than in male (60.9% vs. 39.1%). Most of the ADRs were reported in the patients at ages not less than 50 but less than 70 years (60.1%) and induced by intravenous administration (94.4%). The case number of ADRs induced by anti-tumor drugs (196, 72.3%) ranked the first. The ADRS mainly involved with blood system (51.7%). The reproted incidence of severe ADRs was 52.8%. However, the case numbers reported by physician was similar to that by pharmacists (50.6% vs. 48.3%). Conclusion:The monitoring on ADRs induced by anti-tumor drugs should be strengthened in clinic so as to improve the compliance of patients and safety of drugs.
Adverse Drug Reaction (ADR); Analysis; Anti-tumor Drug; Rational Drug Use
R95
A
10.3969/j.issn.2096-3327.2017.03.013
2016 - 12 - 15
张新毅,男,硕士,主管药师。研究方向:临床药学。通讯作者E-mail:neimengzxy@sian.com

