利塞膦酸钠关键中间体3-乙酰基吡啶的合成
管月清,章鹏飞
(1.台州职业技术学院 医学与制药工程学院,浙江 台州 318000; 2.杭州师范大学 材料与化学化工学院,浙江 杭州 310036)
利塞膦酸钠关键中间体3-乙酰基吡啶的合成
管月清1*,章鹏飞2
(1.台州职业技术学院 医学与制药工程学院,浙江 台州 318000; 2.杭州师范大学 材料与化学化工学院,浙江 杭州 310036)
3-乙酰基吡啶是合成利塞膦酸钠的关键中间体. 室温下,以3-乙炔基吡啶在CF3SO3H/CF3CH2OH(n(CF3SO3H)/n(CF3CH2OH)=20%)催化体系中顺利进行马氏水合反应,反应收率较高,环境友好,该方法同时具有原料易得、反应条件温和、操作简便、适合工业化生产等优点.
利塞膦酸钠;关键中间体;3-乙酰基吡啶;合成;环境友好
骨质疏松症(Osteoporosis,OP) 是一种以骨量低下,骨微结构破坏,导致骨脆性增加,易发生骨折为特征的全身性骨病[1]. 根据病因,可分为原发性和继发性两种. 其中,原发性骨质疏松症多发于老年人群及绝经后妇女,是随着年龄的增长必然发生的一种生理退行性病变,严重威胁老年人的健康和生活质量,也给家庭和社会带来沉重的负担. 随着人类寿命延长和老龄化社会的到来,骨质疏松症已成为全人类的重要健康问题,中国也不例外. 2006年中国50岁以上的骨质疏松患者约为6 944万人,目前有8 400万人患有不同程度的骨质疏松症,预计到2020年将增至2.866亿人,到2050年上升至5.333亿人[2].
目前,治疗和预防骨质疏松症主要依靠补充钙剂和维生素D类产品,但骨质疏松症是钙的沉积和流失不平衡所致,单纯补钙并不能有效治疗和预防骨质疏松症,因此,需要应用一些防止钙流失的药物进行治疗. 双膦酸盐类药物是迄今为止临床上应用时间最长的抗骨吸收药物,其疗效确切,且可根据患者依从性选择不同的类型. 其中,利塞膦酸钠(Risedronate sodium,图1)是新一代双膦酸盐类药物的杰出代表,由美国宝洁(Procter & Gamble)公司开发,于1998年同时在美国和欧洲上市,属于第三代双膦酸盐. 与其他同类药相比,利塞膦酸钠抗吸收作用增强且毒副作用小,已成为目前防治骨质疏松症最主要药物之一[3-4].
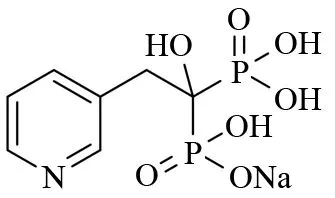
图1 利塞膦酸钠的结构式Fig.1 Chemical structure of risedronate sodium
3-乙酰基吡啶是合成利塞膦酸钠的重要中间体,其合成工艺已有文献报道[5-9](图 2),但现有工艺大多存在催化剂昂贵、反应条件苛刻、反应时间长、试剂毒性大、收率低、环境污染严重等问题. 因此,开发一种高效、易于工业化合成3-乙酰基吡啶的新方法已成为当前研究的重点课题之一.
近些年来,炔烃水合反应在现代大规模化工生产和精细化学品制备中备受关注[10-15]. 炔烃水合制备羰基化合物的原子经济性可达100%,且炔烃原料易得,产物附加值较高是该反应的显著优势,但与此同时该反应也存在一些不足:如传统的炔烃水合反应多采用剧毒Hg盐和过量的硫酸为催化剂环境污染严重;后续开发的低毒过渡金属及金属/Bronsted acid共组催化剂催化水合反应时存在反应温度高、催化剂昂贵、三废量大等不足. 本文在前人研究的基础上[16],首次将无过渡金属参与的CF3SO3H/CF3CH2OH催化体系应用于3-乙炔基吡啶的水合反应,并高产率得到利塞膦酸钠的关键中间体3-乙酰基吡啶,产物经核磁、质谱等进行了结构确认,其具体合成路线见图 2.
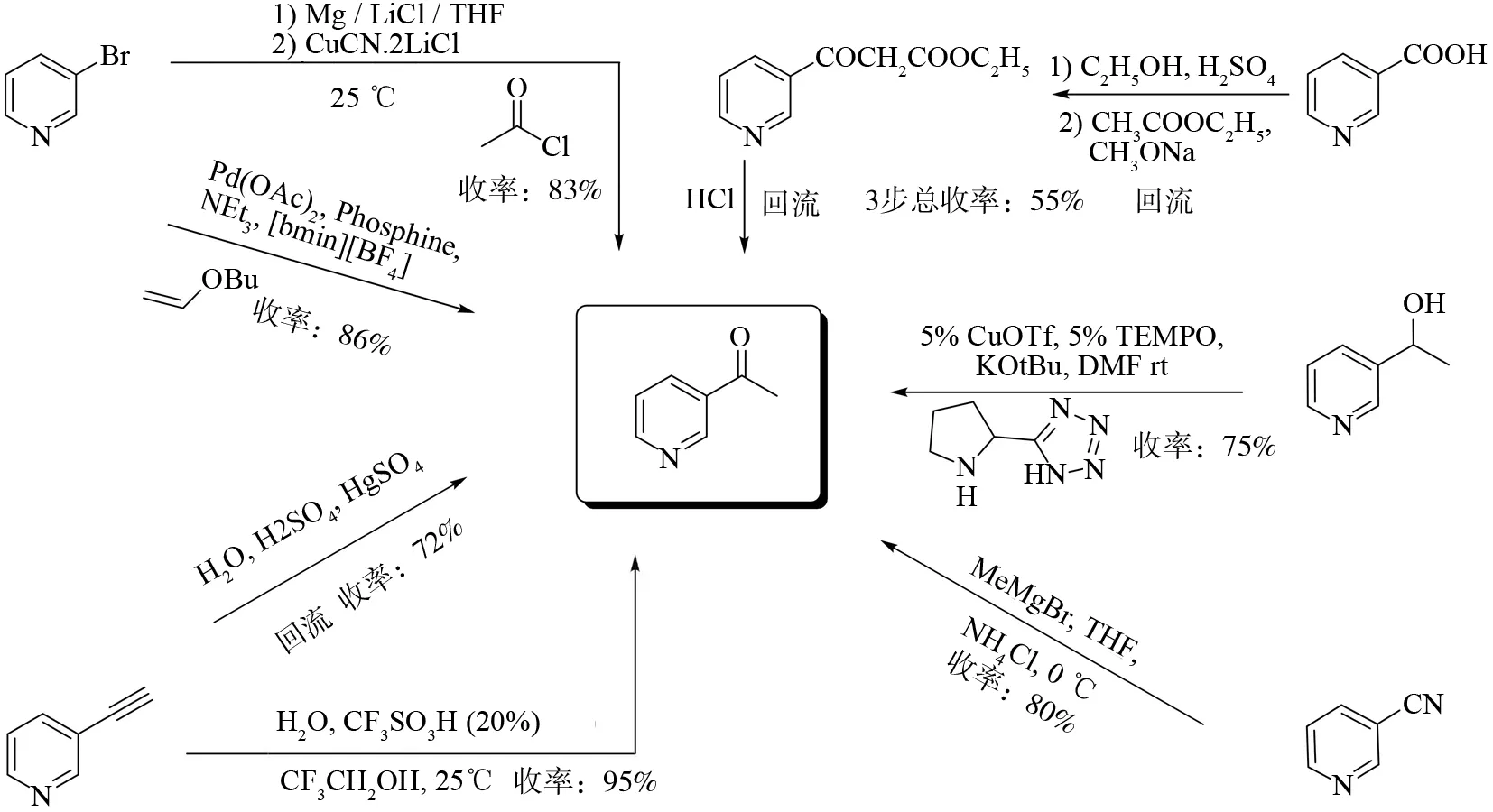
图2 3-乙酰基吡啶的合成路线Fig.2 Synthesis route of 3-acetylpyridine
1 实验部分
1.1 主要仪器与试剂
Bruker-500型核磁共振仪,Thermo Scientific LCQ质谱仪. 3-溴吡啶、乙炔基三甲基硅烷、二异丙胺、碘化亚铜、无水硫酸镁、氢氧化钾、三氟甲磺酸,三氟乙醇、无水硫酸钠、碳酸氢钠、二氯甲烷、甲醇、乙酸乙酯、正己烷均为分析纯.
1.2 实验步骤
1.2.1 3-乙炔基吡啶的合成[17]
在1 000 mL三颈圆底烧瓶中先加入3-溴吡啶49.8 g(0.31 mol),Pd(PPh3)Cl25.4 g和 CuI 1.5 g,加完后进行氮气置换,在控温(30 ℃)及搅拌下再依次加入二异丙胺 510 mL和乙炔基三甲基硅烷34.2 g(0.34 mol),加完后保温反应约3 h,反应结束后依次加水淬灭,二氯甲烷萃取及MgSO4干燥,减压蒸馏得到浓缩物;接着,在氮气保护的1 000 mL三颈圆底烧瓶中依次加入上述浓缩物,KOH 19.2 g(0.62 mol),甲醇570 mL和二氯甲烷300 mL. 加完后保温反应约3 h,反应结束后依次加水淬灭,二氯甲烷萃取,MgSO4干燥,减压蒸馏得到3-乙炔基吡啶黄色固体产物30.3 g,收率93%,mp 38.5~39.5 ℃(ref. [18], 39~40 ℃).
1.2.2 3-乙酰基吡啶的合成
在250 mL圆底烧瓶中依次加入3-乙炔基吡啶28.8 g(0.28 mmol),水10.2 g(0.56 mmol),三氟甲磺酸8.4 g (0.56 mmol),三氟乙醇100 mL,加完后进行瓶口密封,在室温搅拌反应约45 h. 反应结束后,将反应液倒入500 mL分液漏斗中,然后加入250 mL的乙酸乙酯,混合物先后分别经100 mL 1mol/L 碳酸氢钠和100 mL氯化钠溶液洗涤,所得有机层经无水硫酸镁干燥、过滤、减压浓缩,最后经蒸馏得到无色油状液体32.19 g,收率为95%,bp 218~219 ℃;1H NMR (500 MHz, CDCl3):δ9.18 (d, 1H), 8.90~8.68 (m, 1H), 8.25 (d, 1H), 7.44(dd, 1H), 2.66 (s, 3H);13C NMR (126 MHz CDCl3):δ196.63, 153.40, 149.80, 135.35, 132.15, 123.53, 26.60. MS (ESI):m/z122.06 [M + H]+.
2 结果与讨论
本研究主要考察了CF3SO3H与CF3CH2OH体系及用量、水的用量、反应温度和反应时间对3-乙炔基吡啶水合化反应的影响. 实验结果表明3-乙炔基吡啶在CF3SO3H/CF3CH2OH催化体系下进行炔烃的水合反应,该体系无需任何过渡金属的参与,克服了传统工艺中剧毒Hg盐和贵重金属盐的使用所带来环境污染严重、生产成本过高等不足. 反应过程中只需加入催化量的CF3SO3H和等物质量的水,从而大大减少了三废的排放. 反应在室温下反应就能顺利进行,且以较高产率(95%)得到目标产物3-乙酰基吡啶. 总之,该工艺与现有文献报道的工艺相比,具有反应条件温和、操作简单、三废排放少、收率高、生产成本低等优点,具有非常好的工业化生产应用前景.
3 结论
本文通过对3-乙炔基吡啶的无金属参与催化的马氏水合反应的研究,在高产率获得利塞膦酸钠关键中间体3-乙酰基吡啶的同时,为其建立了一种高效的合成新方法,该工艺具有原料易得、反应条件温和、操作简便、产率高、环境友好、适合工业化生产等特点.
[1] 中华医学会. 临床诊疗指南·骨质疏松症和骨矿盐疾病分册[M]. 北京: 人民卫生出版杜, 2006: 44-47.
Chinese Society of Osteoporosis and Bone Mineral Disease, Chinese Medical Association. Clinical practice guidelines: osteoporosis [M]. Beijing: People’s Medical Publishing House, 2006: 44-47.
[2] 中华医学会. 原发性骨质疏松症诊治指南(2011年)[J]. 中华骨质疏松和骨矿盐疾病杂志, 2011, 4(1): 2-17.
Chinese Medical Association. Guidelines for diagnosis and treatment of primary osteoporosis [J]. Chinese Journal of Osteoporosis & Bone Mineral Research, 2011, 4(1): 2-17.
[3] CART A J, THOMPSON P W, COOPER C. Factors associated with adherence and persistence to bisphosphonate therapy in osteoporosis: a cross-sectional survey [J]. Osteoporosis International, 2006, 17(11): 1638-1644.
[4] MCCLUNG M R, ZANCHETTA J R, RACEWICZ A, et al. Efficacy and safety of risedronate 150-mg once a month in the treatment of postmenopausal osteoporosis: 2-year data [J]. Osteoporosis International, 2013, 24(1): 293-299.
[5] KARIMI F, BARLETTA J, LÅNGSTRÖM B. Palladium-mediated 11C-carbonylative cross-coupling of alkyl/aryl iodides with organostannanes: An efficient synthesis of unsymmetrical alkyl/aryl [11C-carbonyl]ketones [J]. Journal of Organometallic Chemistry, 2005, 2005(11): 2374-2378.
[6] PEI W, MO J, XIAO J L. Highly regioselective Heck reactions of heteroaryl halides with electron-rich olefins in ionic liquid [J]. The Journal of Organic Chemistry, 2005, 690(15): 3546-3551.
[7] XU D, LIU Z H, TANG W J, et al. Palladium-catalyzed regiocontrolled internal heteroarylation of electron-rich olefins with heteroaryl halides [J]. Tetrahedron Letters, 2008, 49(42): 6104-6107.
[8] PILLER F M, APPUKKUTTAN P, GAVRYUSHIN A, et al. Convenient preparation of polyfunctional aryl magnesium reagents by a direct magnesium insertion in the presence of LiCl [J]. Angewandte Chemie International Edition, 2008, 47(36): 6802-6806.
[9] LIU Y Y, XIE A, LI J J, et al. Heterocycle-substituted tetrazole ligands for copper-catalysed aerobic oxidation of alcohols [J]. Tetrahedron, 2014, 70(52): 9791-9796.
[10] XU Y, HU X B, SHAO J, et al. Hydration of alkynes at room temperature catalyzed by gold(I) isocyanide compounds [J]. Green Chemistry, 2015, 17(1): 532-537.
[11] XU C X, DU W Y, ZENG Y, et al. Reactivity switch enabled by counterion: highly chemoselective dimerization and hydration of terminal alkynes [J]. Organic Letters, 2014, 16(3): 948-951.
[12] HERZON S B, LI L, ZENG M S. A highly active and air-stable ruthenium complex for the ambient temperature anti-markovnikov reductive hydration of terminal alkynes [J]. Journal of the American Chemical Society, 2014, 136 (19): 7058-7067.
[13] HASSAM M, LI W S. Copper-catalyzed Markovnikov hydration of alkynes [J]. Tetrahedron, 2015, 71(19): 2719-2723.
[14] BAQUERO E A, SILBESTRI G F, FLORES J C. Sul-fonated water-soluble N-heterocyclic carbene silver(I) complexes: Behavior in aqueous medium and as NHC-transfer agents to platinum(II) [J]. Organometallics, 2013, 32(9): 2814-2826.
[15] CORDON J, JIMENEZ O G, JOSE M L, et al. Experimental and theoretical study of gold(III)-catalyzed hydration of alkynes [J]. Organometallics, 2014, 33(14): 3823-3830.
[16] LIU W B, WANG H N, LI C J. Metal-free Markovnikov-type alkyne hydration under mild conditions [J]. Organic Letters, 2016, 18(9): 2184-2187.
[17] HOLMES B T, PENNINGTON W T, HANKS T W. Efficient synthesis of a complete donor/acceptor bis(aryl)diyne family [J]. Synthetic Communications, 2003, 33(14): 2447-2461.
[18] RODRIGUEZ J G, MARTIN-VILLAMIL R, CANO F H, et al. Synthesis of 1,4-di(n-pyridyl)buta-1,3-diyne and formation of charge-transfer complexes. X-ray structure of 1,4-di(3-pyridyl)buta-1,3-diyne [J]. Journal of the Chemical Society, Perkin Transactions, 1997, 5(5): 709-714.
[责任编辑:张普玉]
Synthesis of 3-acetylpyridine as a key intermediate for risedronate sodium
GUAN Yueqing1*, ZHANG Pengfei2
(1.DepartmentofMedicalandPharmaceuticalEngineering,TaizhouVocational&TechnicalCollege,Taizhou318000,Zhejiang,China; 2.CollegeofMaterial,ChemistryandChemicalEngineering,HangzhouNormalUniversity,Hangzhou310036,Zhejiang,China)
3-Acetylpyridine is a key intermediate for risedronate sodium. A highly improved and environmentally benign methodology with the advantages of simple materials, simple operation, high yield and suitable for scale-up, has been developed for the synthesis of 3-acetylpyridine from the metal-free Markovnikov-type hydration of 3-ethynylpyridine by using CF3SO3H/CF3CH2OH (n(CF3SO3H)/n(CF3CH2OH)=20%) as the catalyst under mild conditions.
risedronate sodium; key intermediate; 3-acetylpyridine; synthesis; environmental friendship
2017-01-07.
国家自然科学基金 (21376058),台州市科技计划项目(131KY07),台州市博士后科研基金项目(2013BSH01).
管月清(1976-),女,高级工程师,主要从事药物合成及分析.*
,E-mail:gbzhou_zju@126.com.
TQ463.2
A
1008-1011(2017)02-0191-04