电感耦合等离子体原子发射光谱法测定废蓄电池硫酸铅及其脱硫物中的硫*
刘泽斌,刘守廷,蒋天成,吴婷,文艳,黄龙龙,徐婵,苏云鹏
(1.广西辐射环境监督管理站,南宁 530022; 2.广西分析测试研究中心,南宁 530022;3.广西卫生职业技术学院,南宁 530023; 4.广西金秀瑶族自治县农业局,广西来宾 545799)
电感耦合等离子体原子发射光谱法测定废蓄电池硫酸铅及其脱硫物中的硫*
刘泽斌1,刘守廷2,蒋天成2,吴婷2,文艳3,黄龙龙4,徐婵2,苏云鹏2
(1.广西辐射环境监督管理站,南宁 530022; 2.广西分析测试研究中心,南宁 530022;3.广西卫生职业技术学院,南宁 530023; 4.广西金秀瑶族自治县农业局,广西来宾 545799)
建立废蓄电池硫酸铅及其脱硫物可硫含量的测定方法。样品采用硝酸、盐酸消解样品,电感耦合等离子体原子发射光谱法测定废蓄电池硫酸铅及其脱硫物可硫的含量。在选定的仪器工作条件下,大量Pb,Al,Fe等基体元素的存在不影响硫的测定。硫的质量浓度在0.00~80.00 mg/L范围内与其光谱强度具有良好的线性关系,线性相关系数为0.999 9,检出限为0.14 mg/L。测定结果的相对标准偏差为2.18%~5.22%(n=11),样品加标回收率在95.0%~104.2%之间。该方法的测定结果与重量法测定结果一致。该方法简单易行,测定结果准确可靠,重复性好,可用于废蓄电池硫酸铅及其脱硫物可硫的测定。
废蓄电池;硫酸铅;脱硫物;硫;电感耦合等离子体原子发射光谱法
目前汽车和电动自行车已成为人们出行的主要交通工具。推广废铅蓄电池铅膏脱硫是国家“十二五”节能环保产业发展规划中列为资源循环利用产业重点领域节能减排项目[1-2],其回收利用的关键在于把蓄电池中的PbSO4脱硫成无硫、冶炼温度相对较低的PbCO3脱硫物[3-6],从而大大降低冶炼能耗,大幅减少因Pb的挥发和SO2排放而造成的环境污染[7-10]。废蓄电池脱硫过程中一般要对脱硫后的沉淀物进行脱硫率的测定,即测定脱硫前废铅蓄电池中的硫含量和脱硫后沉淀物中的硫含量,借以检验脱硫过程是否将废铅蓄电池PbSO4转变成PbCO3沉淀物。PbSO4中硫含量的测定通常采用硫酸钡重量法[11-13]、高频红外吸收法[14-15]和燃烧-酸碱滴定中和法[16]。硫酸钡重量法分析过程手续繁锁,分析时间冗长,需要高温熔融和高温灼烧及长时间沉淀;高频红外吸收法能快速测定硫含量,其称样量少,需要样品均匀性很好,否则测定结果重复性较差;燃烧-酸碱滴定中和法较难达到1 300℃以上的温度,使得PbSO4中SO42-不易完全转化成SO2逸出而造成硫测定结果偏低,且分析操作繁锁,试剂消耗量大。笔者采用ICP-AES法测定废蓄电池硫酸铅及其脱硫后沉淀物中硫含量,该方法简单快速,测量线性范围宽,结果准确,重复性好,与重量法测定结果吻合,特别适用于大批量样品的测定。
1 实验部分
1.1 主要仪器与试剂
电感耦合等离子体原子发射光谱仪:ICAP 6300DUO型,美国热电仪器公司;
氩气:纯度为99.99%;
盐酸:1.19 g/mL,分析纯;
硝酸:1.42 g/mL,分析纯;
无水硫酸钠:优级纯;
硫标准储备溶液:1 000 mg/L,称取4.430 3 g(精确至0.00 01 g)于105~110℃烘至恒重的无水硫酸钠,置于300 mL烧杯中,用适量水溶解,移入1 000 mL容量瓶中,用水稀释至标线,摇匀,备用;
实验所用其它试剂均为分析纯;
实验用水为实验室二级水。
1.2 仪器工作条件
高频入射功率:1 170 W;工作频率:27.12 MHz;冷却气:氩气,流量为12 L/min;辅助气:氩气,流量为0.5 L/min;雾化气:氩气,流量为0.75 L/min;冲洗泵转速:75 r/min;分析泵速:50 r/min;泵稳定时间:5 s;积分时间:5 s;积分次数:2次;硫的分析谱线:182.0 nm。
1.3 硫系列标准工作溶液的配制
分别移取硫标准储备溶液0.00,0.25,0.50,1.00,2.00,3.00,4.00 mL于7只50 mL容量瓶中,各加入2.5 mL盐酸,用水稀释至标线,摇匀,配制成硫含量为0.00,5.0,10.0,20.0,40.0,60.0,80.0 mg/L的硫系列标准工作溶液。
1.4 样品前处理
将利用NaOH脱硫处理后的样品标记为1#,利用(NH4)2CO3脱硫处理后的样品标记为2#,未脱硫的PbSO4样品标记为3#。分别称取1#,2#,3#样品0.2 g(精确至0.000 1 g)于125 mL高型三角烧杯中,用少量水润湿,加入9 mL硝酸、3 mL盐酸,盖上表面皿,在电热板上于160~180℃加热溶解,若样品消化不完全可适当补充硝酸和盐酸,待试样蒸至近干,取下,稍冷。向1#样品、2#样品中加入5 mL盐酸,用少量水冲洗表面皿及杯壁,温热溶解盐类,取下,冷却至室温,移入100 mL容量瓶中;向3#样品中加入12.5 mL盐酸,温热溶解盐类,移入250 mL容量瓶中。3种样品均用水稀释至标线,摇匀,静置,澄清,取上清溶液或过滤后进行测定。同时作空白试验。
1.5 样品测定
根据试液中待测元素的大致浓度范围,导入硫标准工作溶液,用电感耦合等离子体原子发射光谱仪测定标准工作曲线的谱线强度,以硫的质量浓度为横坐标,谱线强度为纵坐标,绘制标准工作曲线。确定标准工作曲线后,先测定样品空白溶液,再测定样品溶液,利用标准工作曲线计算空白溶液与试样溶液中待测元素的浓度。按式(1)计算试样中硫的含量X:
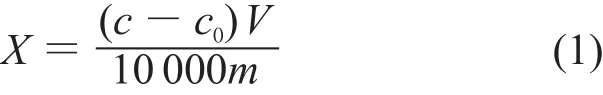
式中:c——从标准工作曲线上得到的试液中硫的含量,µg/mL;
c0——从标准工作曲线上得到的试剂空白液中硫的含量,µg/mL;
V——试样溶液定容体积,mL;
m——试样的质量,g。
2 结果与讨论
2.1 检测波长与干扰试验
PbSO4及其脱硫后的沉淀物主要基体为铅,同时在沉淀物粉碎和脱硫过程中会引入Al,Fe,Ca,Mg,K,Na,P,Mn等元素。为了考察这些元素对硫测定的影响,进行了对应元素的干扰试验。选择加入不同量的Al,Fe,Ca,Mg,K,Na,P,Mn,考察以上元素对10 mg/L SO42-标准溶液测定结果的影响,干扰试验结果见表1。从表1可以看出,基体元素对波长为182.0 nm的分析谱线几乎没有干扰影响,因此选择检测波长为182.0 nm。
2.2 线性方程
在1.2仪器工作条件下,分别测定1.3配制的硫系列标准工作溶液,以硫标准工作溶液的质量浓度X为横坐标,光谱强度Y为纵坐标,绘制标准工作曲线,结果见表2。由表2可知,在0.00~80.00 mg/L范围内,硫的质量浓度与光谱强度线性相关,相关系数为0.999 9。
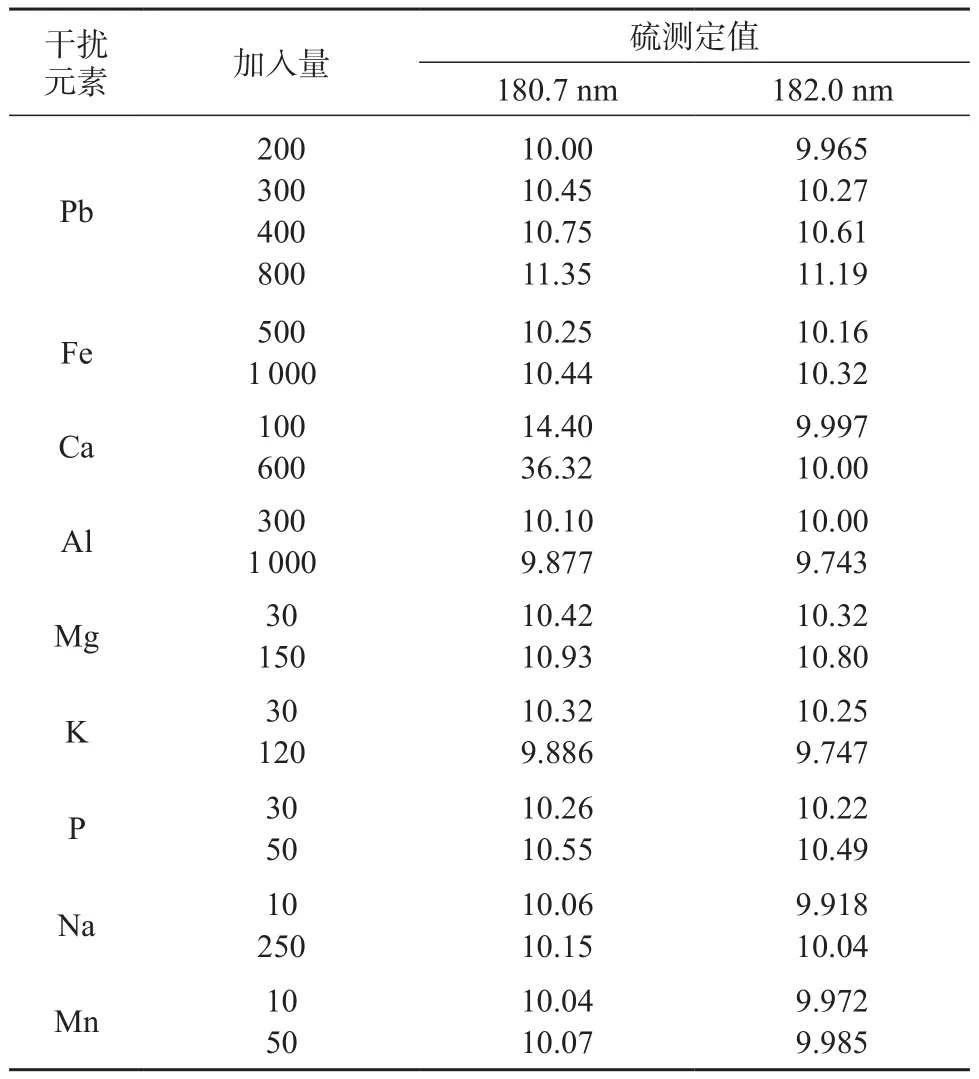
表1 干扰试验结果 mg/L

表2 标准曲线及相关系数
2.3 检出限
对样品空白连续测定11次,以测定结果标准偏差的3倍作为硫的检出限,计算得硫的检出限为0.14 mg/L。
2.4 精密度试验
选取1#,2#,3#三个样品进行硫含量测定,每个样品称取11个平行样,按实验方法进行消解测定,结果见表3。由表3可知,本方法具有良好的精密度。
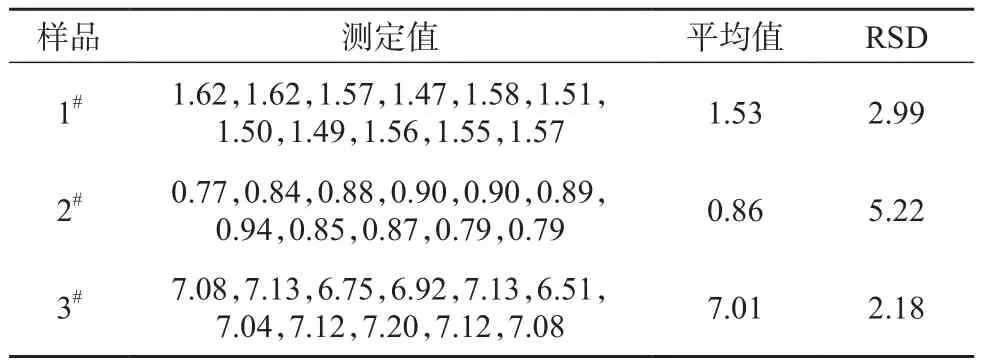
表3 样品测定结果 %
2.5 回收试验
选取1#,2#,3#三个样品,分别加入不同量的硫标准储备溶液,按照实验方法进行消解测定,加标回收试验结果见表4。由表4可知,该方法具有较高的准确度。
2.6 比对试验
按实验方法对样品进行消解处理,用BaSO4重量法和本方法对1#,2#,3#三个样品的硫含量进行测定,结果见表5。由表5可知,本法与BaSO4重量法测定结果基本一致。

表4 回收试验结果

表5 比对试验结果 %
3 结语
采用硝酸、盐酸消解样品,以电感耦合等离子体原子发射光谱法测定铅蓄电池铅膏及其脱硫物中的硫含量。该方法精密度好,线性范围宽,测定结果准确可靠。大量Pb,Al,Fe等基体元素的存在对硫的测定结果无影响。该方法可满足铅蓄电池铅膏及其脱硫物中的硫含量的测定要求。
[1] 环境保护部环境工程评估中心.环境影响评价相关法律法规汇编增补本2013[ M].北京:中国环境出版社,2013: 35.
[2] 国务院关于印发“十二五”节能环保产业发展规划的通知,国发[2012]19[ Z/OL]. http://www.gov.cn/zwgk/2012-06/29/ content_2172913.htm.
[3] 吴广龙,张正洁,刘俐媛,等.废铅膏冶炼工艺比较分析研究[J].蓄电池,2015,52(5): 209-211.
[4] 王学健,沈海泉.废铅酸蓄电池回收处理技术现状及发展趋势[J].科技创新与应用,2015(9): 66-69.
[5] 汪振忠,柯昌美,王茜.废铅酸蓄电池铅膏脱硫工艺的研究进展[J].无机盐工业,2013,45(1): 60-62.
[6] 邱德芬,柯昌美,王茜,等.从废铅膏中回收铅及铅的化合物的方法[J].无机盐工业,2014,46(7): 16-20.
[7] 李金惠,聂永丰.中国废铅蓄电池回收利用现状及管理对策[J].环境保护,2000(4): 40-42.
[8] 刘建斌,黄志明,许民,等.废铅酸蓄电池渣泥湿法脱硫和还原新工艺[J].无机盐工业,2004, 36(1): 47-49.
[9] 孙晓娟,李卉,朱新锋,等.复合脱硫剂对废铅酸蓄电池铅膏脱硫影响的研究[J].蓄电池,2013,50(4): 147-152.
[10] 徐新.铅酸蓄电池生产过程中废铅膏的再生铅利用[J].广东化工,2015,42(4): 31-34.
[11] 岩石矿物分析编写组.岩石矿物分析(第一册)[M].北京:地质出版社,1991: 188.
[12] 北京矿冶研究总院分析室编.矿石及有色金属分析手册[M].北京:冶金工业出版社,2006: 132.
[13] 陈梅,柯昌美,邱德芬,等.废铅酸蓄电池铅膏中各成分含量的测定方法研究[J].无机盐工业,2015,47(11): 69-74.
[14] 王宝玲.高频红外吸收法快速测定硫精矿中高含量[J].冶金分析,2013,33(8): 52-54.
[15] 刘守廷,蒋天成,罗平,等.高频红外碳硫分析仪快速测定废蓄电池硫酸铅及其脱硫后沉淀物中硫[C].北京:中国金属学会第十三届分析测试学术年会,2006: 241-244.
[16] 《有色金属工业分析从书》编辑委员会.重金属冶金分析[M].北京:冶金工业出版社,1994: 119.
Determination of Sulfur in Waste Battery Lead Sulfate and its Desulfurization Product by ICP-AES
Liu Zebin1, Liu Shouting2, Jiang Tiancheng2, Wu Ting2, Wen Yan3, Huang Longlong4, Xu Chan2, Su Yunpeng2
(1. Guangxi Radiation Environment Supervision and Managemental Station, Nanning 530022, China; 2. Guangxi Center of Analysis and Test Research, Nanning 530022, China; 3. Guangxi Medical College, Nanning 530023, China; 4. Agriculture Bureau of Jinxiu Yao Autonomous County , Laibin 545799, China)
The method for determination of sulfur in lead-acid battery lead sulfate and its desulfurization product was established. The sample was dissolved by nitric acid and hydrochloric acid, the content of sulfate was detected by ICP-AES. At the selected instrument operating conditions, the existence of a large amount of Pb, Al, Fe matrix elements, etc., did not interfere with the determination of sulfur. The mass concentration of sulfate has good relationship with the spectral intensity in the range of 0.00-80.00 mg/L, the linear correlation coefficient was 0.999 9, the detection limit was 0.14 mg/L. The relative standard deviation of determination results was 2.18%-5.22%(n=11), and the recovery was 95.0%-104.2%. The determination result of this method was consistent with the result determined by gravimetric method. The method is simple, accurate and reliable with good repeatability, it can be used for determination of sulfur in waste battery lead sulfate and its desulfurization product.
waste batteries; lead sulfate; desulfurization; sulfur; ICP-AES
O657.3
:A
:1008-6145(2017)02-0038-04
10.3969/j.issn.1008-6145.2017.02.010
*广西壮族自治区直属公益性科研院所基本科研业务费专项(2015ACZ09)
联系人:刘守廷;E-mail: Liushouting@163.com
2017-01-10

