桑叶水提液体外清除亚硝酸盐作用研究
徐 娟,汪 滔,付雪薇,刘兰萍,李 静
(安徽科技学院 动物科学学院,安徽 凤阳 233100)
桑叶水提液体外清除亚硝酸盐作用研究
徐 娟,汪 滔,付雪薇,刘兰萍,李 静*
(安徽科技学院 动物科学学院,安徽 凤阳 233100)
目的:对桑叶水提液的降低亚硝酸盐作用进行研究,确定清除的最佳条件。方法:采用水浸提法,考察提取温度、提取时间、反应时间、反应用量4个因素对桑叶水提液的降低亚硝酸盐作用的影响,用正交试验法优化最佳清除条件。结果:4个因素的影响的次序为提取温度>反应用量>反应时间>提取时间,最佳清除条件为提取温度30 ℃,提取时间1.5 h,反应时间15 min,反应用量15 mL,清除率可达49.71 %。结论:桑叶水提液在体外对亚硝酸盐具用一定的消除作用,可作为桑叶新功效加以开发。
正交试验;桑叶;盐酸萘乙二胺法;亚硝酸盐;清除率
XU Juan, WANG Tao, FU Xue-wei, LIU Lan-ping, LI Jing*
(College of Animal Science, Anhui Science and Technology University, Fengyang 233100, China)
亚硝酸盐具有一定的毒性,一方面,大剂量的亚硝酸盐进入机体内会造成中毒,另一方面,部分亚硝酸盐在一定条件下会转化为亚硝胺,而亚硝胺是一种强致癌物质[1]。在蔬菜、肉类食品中常含有亚硝酸盐[2],由于氮肥施用的增加、设施技术应用及环境污染的影响,使亚硝酸盐的含量呈增加趋势[3],成为影响食品安全的重要因素,将食品和膳食中的亚硝酸盐的含量降低到安全水平是保证人体安全的重要举措。据悉,食用各种新鲜水果和蔬菜可以一定程度地抑制亚硝酸盐转化为亚硝胺。果蔬中还原性成分的种类、含量及其氧化还原特性是果蔬对亚硝酸盐的消除能力的关键。桑叶是桑科植物桑的干燥叶,具有散风热、清肺润燥、清肝明目等功效,可治疗头晕头痛,目赤昏花等病症,其富含黄酮、多糖和生物碱等生物活性成分[4],桑叶总黄酮含量较多[5],可以作为食品中黄酮来源的主要方面。桑叶的抗衰老,抗突变的作用与含有大量的黄酮有密切关系。研究证明,植物黄酮能有效抑制亚硝化反应[6]。桑叶在中国拥有药物使用的悠久历史,且资源丰富,是国家认证的药食同源的食品,可长期代茶饮用。桑叶在生活中的应用主要是用水冲泡代茶饮,所以本试验中采用水提法进行研究。目前在桑叶提取物对清除亚硝酸的研究报道很少,本试验从提取温度,提取时间,反应时间与反应量四个方面,确定桑叶提取液在清除亚硝酸盐过程中的影响因素,用正交试验确定清除亚硝酸盐的最佳条件,可作为对今后桑叶功效的深入研究提供参考。
1 材料与方法
1.1 试验材料
桑叶(MorusalbaL),生产许可证号:皖Y20050050,桑叶产地:安徽,批号:151227,生产日期:2015.12.27,生产厂家:亳州市永刚饮片厂有限公司,经安徽科技学院食品药品学院时维静教授鉴定为正品;氨基苯磺酸,分析纯,国营上海第一制药厂,批号 H41023771;盐酸萘乙二胺,分析纯,天津市光复精细化工研究所,批号:H31021689;盐酸,分析纯,蚌埠化学试剂厂,批号:H41020227;亚硝酸钠,分析纯,国药集团化学试剂有限公司,批号:H41020228。
1.2 试验仪器与器材
L-16C台式离心机,上海安亭科学仪器厂生产;紫外、可见分光光度计,日本岛津公司生产,(苏)制(05000111)号;HH-S恒温水浴锅,江苏国胜实验仪器厂生产;YD-6000电子分析天平,上海精科天平生产;FA-1004电子天平,上海精密科学仪器科学有限公司生产;XW-80A微型漩涡混合仪,上海分析仪器厂有限公司生产;可调移液器等。
1.3 药品的制备
桑叶,去除杂质后,放入粉碎机中1800 r/min进行3 min的粉碎。每份提取液均用10 g桑叶,加入100 mL蒸馏水,在不同条件(温度、时间)下提取,然后用3000 r/min离心10 min,取上清液备用。
亚硝酸钠标准储备液:准确称取0.1 g的亚硝酸钠,移入250 mL容量瓶中进行加水溶解,加水稀释至刻度,混匀。此溶液为亚硝酸钠储备液(400 μg/mL)。亚硝酸钠标准使用液:临用前,吸取亚硝酸钠标准溶液1.25 mL,置于100 mL容量瓶中,加水稀释至刻度,混匀。此溶液为亚硝酸盐使用液(5 μg/mL)。
准确吸取5 μg/mL 标准液0、0.5、1.0、2.0、3.0、4.0、5.0 mL于25 mL量瓶中,加入0.4 %的对氨基苯磺酸溶液1 mL,摇匀静置5 min。再加入0.2 %的盐酸萘乙二胺0.5 mL,加水至刻度,摇匀,放置15 min,以不加NaNO2(亚硝酸钠)标准液作参比,在最大吸收波长538 nm处测定吸光度,以吸光度值A为纵坐标,NaNO2浓度C(μg/mL)为横坐标,绘制标准曲线。
1.4 亚硝酸盐清除率的测定
亚硝酸盐含量用盐酸萘乙二胺比色法[7]测定。准确吸取5 μg/mL NaNO2两份各2 mL分别置于10 mL试管中,其中一份加入5 mL 提取液,摇匀反应5 min,另一份加蒸馏水作空白对照。两份都加入0.4%对氨基苯磺酸1 mL,摇匀静置5 min。再都加入0.2 %盐酸萘乙二胺0.5 mL,混匀,静置15 min,用2 cm 比色皿于538 nm 处测定吸光度,分别为A1、A2。按下式计算桑叶提取液对亚硝酸盐的清除率。
清除率(%)=(A2-A1)/A2×100%
A1—— 加桑叶提取液测得值
A2—— 未加桑叶提取液测得值
1.5 试验设计
1.5.1 桑叶的提取温度对亚硝酸盐的清除作用 各称取桑叶样品10 g于6个烧杯中,分别加入100 mL蒸馏水。分别在不同温度(30 ℃、42 ℃、54 ℃、66 ℃、78 ℃、90 ℃)下水浴浸提0.5 h,然后用纱布过滤,静置,取上清液3000 r/min离心10 min取上清液用滤纸过滤,取滤液5 mL,均加入5 μg/mL的亚硝酸钠2 mL,反应5 min,另作空白。测得对亚硝酸盐的清除率。试验重复三次,取平均值,确定出最佳提取温度。
1.5.2 桑叶的提取时间对亚硝酸盐的清除作用 各称取桑叶10 g于5个烧杯中,分别加入100 mL蒸馏水。在1.5.1步骤确定的最佳浸提温度下分别浸提(0.5 h、1.0 h、1.5 h、2.0 h、2.5 h),然后用纱布过滤,静置,取上清液,3000 r/min离心10 min,取5 mL桑叶提取液于10 mL试管中,加入5 μg/mL的亚硝酸钠2mL,反应5 min然后均加入对氨基苯磺酸,盐酸萘乙二胺,显色。测得提取液对亚硝酸盐的清除率,试验重复3次,取平均值,确定出最佳提取时间。
1.5.3 桑叶提取液的反应时间对亚硝酸盐的清除作用 称取桑叶样品10 g于烧杯中,加入100 mL蒸馏水。在1.5.1步骤确定的最佳浸提温度下提取,提取时间为1.5.2步骤确定的最佳提取时间,然后用纱布过滤,静置,取上清液3000 r/min离心10 min。取上清液用滤纸过滤,取5 mL提取液,均加入5 μg/mL 的亚硝酸钠2 mL,反应不同的时间(1 min、5 min、15 min、25 min、35 min)。均加入对氨基苯磺酸,盐酸萘乙二胺,显色。测得提取液对亚硝酸盐的清除率,试验重复3次,取平均值。
1.5.4 桑叶提取液的用量对亚硝酸盐的清除作用 各称取桑叶样品10 g于5个烧杯中,分别加入100 mL蒸馏水。在1.5.1步骤确定的最佳浸提温度下,提取时间为1.5.2步骤确定的最佳提取时间,然后用纱布过滤,静置,取上清液 ,3000 r/min离心10 min。取上清液用滤纸过滤,分别取不同计量(1 mL、5 mL、10 mL、15 mL、20 mL)的滤液,均加入5 μg/mL的亚硝酸钠2 mL反应15 min,然后均加入对氨基苯磺酸、盐酸萘乙二胺,显色。测得提取液对亚硝酸盐的清除率,试验重复3次,取平均值。
1.5.5 正交试验设计 采用正交试验优选提取和反应条件,根据单因素试验结果,选择提取温度、提取时间、反应时间、反应用量为影响因素,进行四因素三水平的正交试验设计,见表 1。

表1 因素水平表
2 结果与分析
2.1 亚硝酸盐标准曲线

表2 亚硝酸钠浓度与吸光度
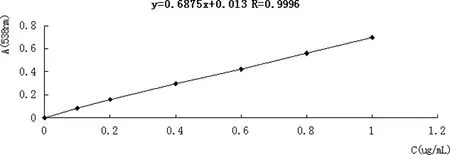
图1 亚硝酸钠的浓度与吸光度

图2 不同温度浸提的桑叶提取液对亚硝酸盐的清除率
由表2及图1可知,吸光度与亚硝酸钠的浓度呈线性关系。
2.2 桑叶的提取温度对亚硝酸盐的清除作用的影响
由图2可见,在一定条件下,伴随提取温度的升高,桑叶提取液对亚硝酸盐的清除率逐渐降低。清除率在30 ℃时达到最大。在温度为90 ℃时,几乎没有清除率。本试验表明,只有较低的温度才能促使桑叶中清除亚硝酸盐的有效成分释放,当温度过高后可能造成桑叶有效成分失活,从而无法对亚硝酸盐进行消解作用。
2.3 桑叶的提取时间对亚硝酸盐的清除作用的影响
由图3可见,在提取时间0.5 h到1.5 h时间段,清除率与提取时间成正比关系。在桑叶水浴提取1.5 h时,对亚硝酸盐的清除率达到最大,在提取时间继续增大到2.0 h到2.5 h时,其清除率反而减小。表明浸提1.5 h时,桑叶中清除亚硝酸盐的有效成分基本上已全部溶出。在1.5 h以后消除率下降明显,表明在长时间的浸提过程中桑叶的有效成分有所减少。
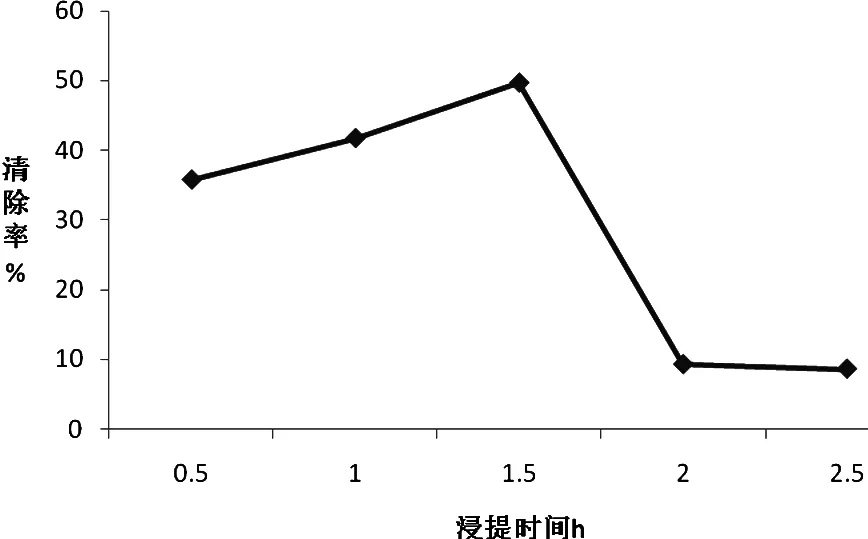
图3 不同浸提时间的桑叶提取液对亚硝酸盐的清除率
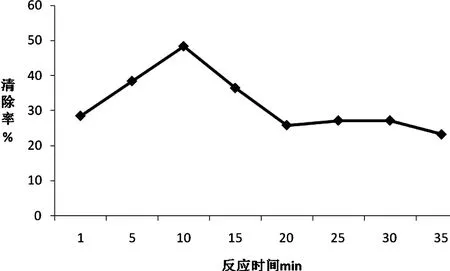
图4 不同反应时间对亚硝酸盐清除作用的影响
2.4 桑叶提取液的反应时间对亚硝酸盐的清除作用的影响
由图4可见,在30 ℃下,提取时间1.5 h下,在桑叶提取液与亚硝酸盐的反应时间在1 min到10 min时,清除率与反应时间成正比,反应10 min时达到最大,以后,随着时间的延长,清除率与反应时间成反比。表明此条件下桑叶提取液对亚硝酸盐的清除在10 min左右全部完成,而后在反应时间的延长过程中可能由于黄酮的水溶性较强造成产物的分解,从而使消解率下降。
2.5 桑叶提取液的用量对亚硝酸盐的清除作用的影响
由图5可见,在30 ℃下,提取时间1.5 h下,在桑叶提取液用量在1 mL到10 mL之间时,亚硝酸盐的清除率与提取液的用量之间成正比关系,以后随着用量的增加,清除率与提取液用量成反比,在提取液10 mL时消除率最高。表明当桑叶提取液的用量在增加到一定量之后,桑叶类的其他物质会对还原性物质的还原性活性有灭活作用。
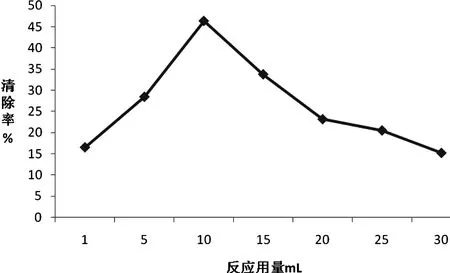
图5 桑叶提取液用量对亚硝酸盐的清除率的影响
2.6 正交试验结果
由表3可知,各因素影响桑叶水提液清除亚硝酸盐作用的主次因素为: 提取温度>反应用量>反应时间>提取时间,最佳提取条件为A1B3C3D3,即提取温度 30 ℃,提取时间1. 5 h,反应时间 15 min,反应用量15 mL,清除率可达49.71%。由表4方差分析可知,提取温度、提取时间、反应时间、反应用量均为显著因素。
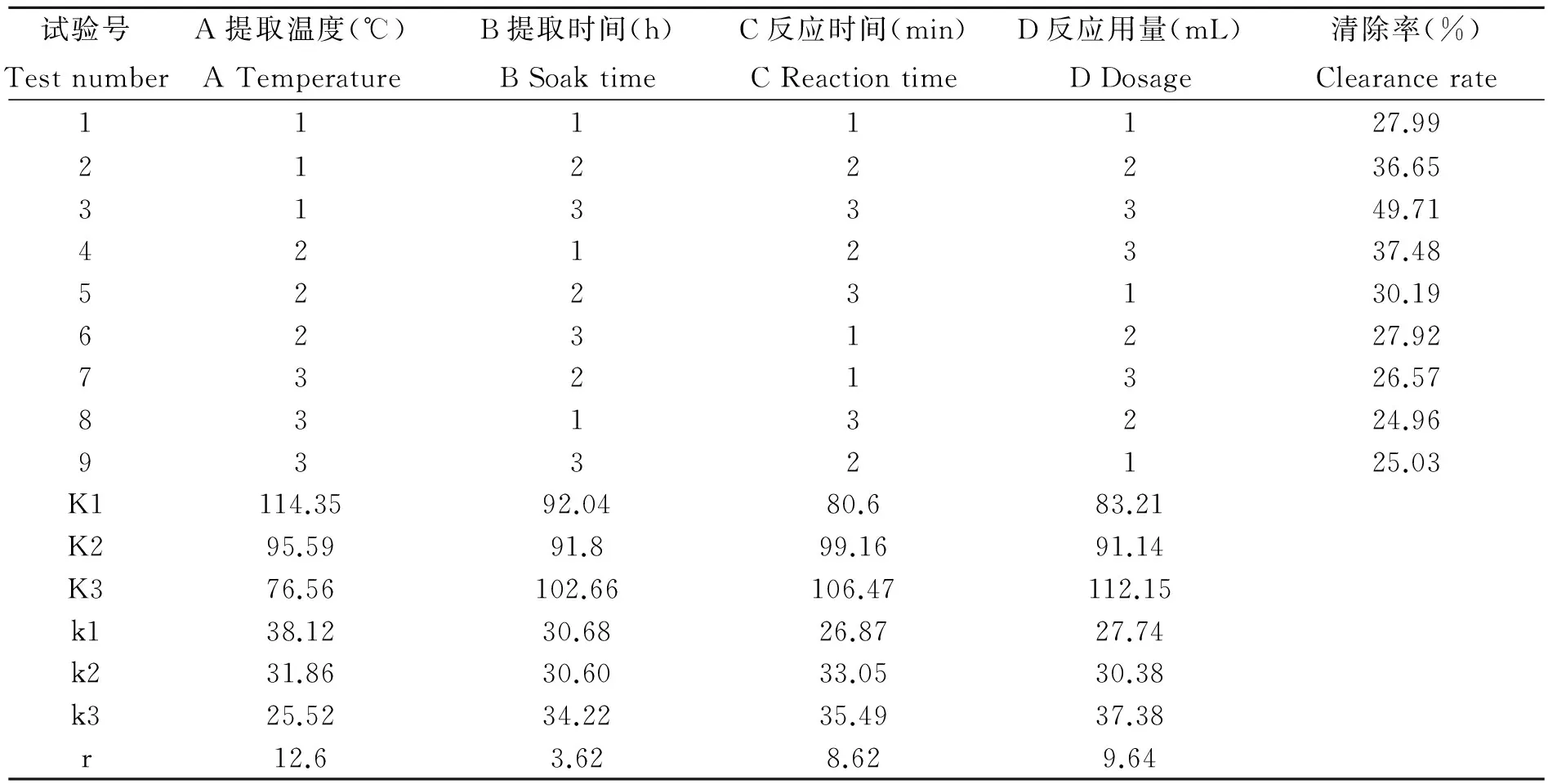
表3 L9(3)4正交试验设计及结果

表4 方差分析
3 结论与讨论
桑叶主要成分黄酮类、生物碱、桑叶多糖等[8],因为黄酮类是大多数氧自由基的清除剂,所以能阻断亚硝胺的合成,达到清除亚硝酸盐的作用[9-10]。
本试验结果表明,桑叶提取液对亚硝酸盐具有一定的的清除作用。不同条件下如浸提温度、浸提时间、反应时间、反应用量,均对亚硝酸盐的清除率都有一定的影响。胡利[11]的研究表明,桑叶黄酮在较高温度下对亚硝酸盐表现更大的清除作用,清除机理可能与其抗氧化活性有关。而本试验的结果表明在30 ℃条件下清除率最高,说明水提方法中提取出的是多种成分,推测桑叶中除黄酮发挥分解亚硝酸盐作用。硝酸盐和亚硝酸盐是自然界氮素循环的必然产物。正常情况下,植物将体内的硝酸盐和亚硝酸盐不断地合成蛋白质,但当蔬菜收获以后,合成代谢下降,一部分硝酸盐残留在植物体内[12]。自然界能使亚酸盐还原的菌有100多种,纪淑娟[13]等对大白菜泡菜发酵过程中亚硝酸盐消长规律的研究吋,发现亚硝酸盐的含量迅速上升的同时,微生物也会大量的生长繁殖。而植物本身在浸泡发酵过程中更会产生亚硝酸盐[14]。有研究表明对亚硝酸盐的清除能力与其本身抗氧化能力密切相关[15]。桑叶可消除亚硝酸盐的功效具有新的开发价值,例如桑叶食品添加剂或桑叶茶等。桑叶清除亚硝酸盐具有方便,无害,无残留,价格低廉等优势。本实验也存在一定的不足之处,例如在水提之后,未确定其中具体的物质成分,从而在分析过程中也存在一些不到之处。
在本次试验中首次讨论了桑叶提取液清除亚硝酸盐的影响条件,结果表明不同提取温度,不同提取时间,不同的反应时间和不同的提取液用量对亚硝酸盐的分解都会产生一定的影响。在温度30 ℃,提取1.5 h ,反应15 min,用量15 mL时清除率最高,可达49.71 %。
[1]HOU Jun-cai, JIANG Cheng-gang, LONG Zhong-chen. Nitrite level of pickled vegetables in Northeast China[J]. Food Control, 2013, 29(1): 7-10.
[2]YANG Lei, CHEN Zhong-lin, SHEN Ji-min, et al. Reinvestigation of the Nitrosamine-Formation mechanism during ozonation[J]. Environmental Science & Technology, 2009, 43(14): 5481-5487.
[3]罗晓梅,朱波.蔬菜亚硝酸盐污染现状分析[J].西南农业学报,2003,16(2):79-81.
[4]Masood Sadiq Butt, Akmal Nazir, Morus alba L, et al. Natures functional tonic[J].Trends in Food Science & Tcchnology, 2008,19:505-512.
[5]杨海霞,朱祥瑞,陆洪省.桑叶保健品开发利用研究进展[J].科技通报,2003,19(1):72-76.
[6]吴洪,高平章.18种中草药对亚硝酸盐清除活性与黄酮含量相关性研究[J].安徽农业科学,2011,36(24):14636-14638.
[7]中华人民共和国卫生部,中国国家标准委员会, GB/T5009.33-2003.中华人民共和国国家标准[S]. 2003.
[8]张志海,王彩云,杨天鸣,等.陈皮的化学成分及药理作用研究进展[J].西北药学杂志,2005,20(1):47-48.
[9]高春燕,王竹,卢跃红.薄荷对亚硝酸盐清除作用的研究[J].食品工业科技,2009(4):98-99, 102.
[10]丁之思.亚硝酸盐和亚硝胺在食品中的作用及其机理[J].安徽农业大学学报,1994,7(2):95-96.
[11]胡利,贾冬英,姚开,等.桑叶黄酮对亚硝酸盐的体外清除作用研究[J].中国调味品,2015,40(3):1-5.
[12]Schmkh I, Sliekers O, Schinid M, et al. Aerobic and anaerobic ammonia oxicli/ingbacteria competitors or natural pai1ners[J] .FEMS Microbiology Ecology, 2002,39(3):l75-18l.
[13]纪淑娟,孟宪军.大白菜发酵过程中亚硝酸盐消长规律的研究[J].食品与发酵工业,2001,27(2):42-46.
[14]王树庆,张瑞菊,姜薇薇,等.蔬菜发酵食品中亚硝酸盐含量的控制[J].山东商业职业技术学院学报,2009,9(5):99-100, 106.
[15]张强,王松华,孙玉军,等.10种香辛调味料提取液对亚硝酸盐清除能力的研究[J].食品工业科技,2015,36(17):100-103.
(责任编辑:马世堂)
Study on the Water Extract of Mulberry Leaf Scavenging Effect on Nitrite in Vitro
Objective: To investigate the anti-nitrosation of aqueous extract from mulberry leaf by orthogonal design, and to determine the optimum conditions for nitrite scavenging effect. Methods:The influence of temperature, soak time,reaction time and dosage on anti-nitrosation of aqueous extract of mulberry leaf, the optimum condition for nitrite scavenging effect was optimized by orthogonal test. Results: The primary and secondary were in the model of temperature > dosage >reaction time > soak time, and the optimum condition of the four factors was at 30 ℃, 1.5 h, reaction time 15 min, dosage 15 ml, and the clearance rate can reach to 49.71 %. Conclusion: Mulberry leaf aqueous extract in vitro with nitrite with a certain role in the elimination can be exploited and utilized as another new effect.
Orthogonal design; Mulberry leaf; Hydrochloride naphthyl ethylenediamine law; Nitrite; Clearance rate
2016-07-09
安徽省大学生创新训练项目(S10879CX04);安徽科技学院重点学科基金项目(AKXK20101-2) ;安徽科技学院重点学科基金项目(AKZDXK2015A04)
徐娟(1994-),女,安徽省合肥市人,在读本科生,主要从事兽用中药与饲料开发。*通讯作者:李静,副教授, E-mail:lij@ahsteu.edu.cn。
R932
A
1673-8772(2016)06-0071-06

