PCOS雌性模型大鼠血清、卵巢及肾上腺的雄激素水平*
王厚梅, 黄 林, 肖子文
(贵州医科大学附院 妇产科, 贵州 贵阳 550004)
PCOS雌性模型大鼠血清、卵巢及肾上腺的雄激素水平*
王厚梅, 黄 林, 肖子文**
(贵州医科大学附院 妇产科, 贵州 贵阳 550004)
目的: 探讨多囊卵巢综合征 (PCOS)雌性SD模型大鼠血清、卵巢及肾上腺的雄激素水平。方法: 选取雌性SD大鼠,随机分为对照组和实验组,对照组以基础饲料喂养,自由饮食饮水;实验组进高脂高糖饮食,5%葡萄糖水,第1~42天给予诺和灵N(低精蛋白锌胰岛素NPH-Humulin)股内侧皮下注射,第11~22天同时给予人绒毛膜促性腺激素皮下注射,6周处死大鼠;观察大鼠卵巢组织学及卵巢重量,同时用酶联免疫吸附法(ELISA)法测定血清黄体生成素(LH)、卵泡生成素(FSH)、睾酮(T)、游离睾酮(FT)、硫酸脱氢表雄酮(DHEA-S),同时检测卵巢组织及肾上腺组织匀浆T、FT、DHEA-S表达。结果: 实验组大鼠卵巢组织镜下见囊性扩张的卵泡增多,黄体及各种发育阶段卵泡减少,对照组卵巢镜下见多个黄体及不同发育阶段的卵泡,卵泡内颗粒细胞呈多层,多为8~9层,造模成功;实验组大鼠卵巢重量、血清T、LH、卵巢组织匀浆T均高于对照组,差异有显著性(P<0.05);实验组大鼠血清FSH、FT、DEAH-S与对照比较差异均无显著性(P>0.05);实验组大鼠卵巢组织匀浆FT、DHEA-S及肾上腺组织匀浆T、FT、DEAH-S与对照比较差异均无显著性(P>0.05)。结论: 多囊卵巢综合征雌性SD大鼠模型的高雄激素血症主要表现为高睾酮血症,且卵巢所分泌睾酮影响高雄激素血症发生可能性较大。
多囊卵巢综合症; 卵巢; 肾上腺; 血清; 大鼠,Sprague-Dawley ; 高雄激素症
目前关于多囊卵巢综合症(PCOS)的概念已经超出了妇科内分泌的范畴,它集合了一组多样的、多系统的慢性内分泌紊乱疾病,2003年制定了PCOS鹿特丹标准[1]:(1)稀发排卵,(2)高雄激素血症或高雄激素临床表现,(3)多囊性改变、一侧或双侧卵巢直径2~9 mm的卵泡≥12个、或卵巢体积≥10 mL;上述条件中符合任意2条,并排除其他高雄激素病因(高雄激素的临床和生化表现是PCOS基本特征之一,但并不是所有患者同时具有高雄激素的临床及生化表现,仅有70%~80%患者表现为高雄激素的生化表现[2])。本实验通过建立多囊卵巢综合征雌性SD大鼠模型检测大鼠体内雄激素的分布,对多囊卵巢综合征患者高雄激素来源进行探讨,为更深认识PCOS提供更多的依据。
1 材料与方法
1.1 实验对象
清洁级雌性SD大鼠,体重180~220 g,8~9周龄。
1.2 方法
棉签取大鼠阴道分泌涂片,电子显微镜观察细胞变化,了解动情周期。选择连续两个以上规律动情周期的大鼠60只,按照编号随机分为对照组n=15只与实验组n=45只,每5只1笼;对照组3笼,实验组9笼。对照组以基础饲料喂养,自由饮食饮水;实验组进高脂高糖饮食(基础饲料 73%、猪油 10%、蔗糖15%、胆固醇2%),给药前喂普通饮用水,实验期间喂5%葡萄糖水,第1~10天给予诺和灵N股内侧皮下注射,每日1次,由0.5 IU递增至5.0 IU,第11~22天持续5.0 IU剂量;同时第11~22天给予人绒毛膜促性腺激素皮下注射1.5 IU(溶于0.9%氯化钠注射液0.2 mL),每天 2次;22 天后对照组继续普食喂养,实验组继续进高脂高糖饮食,持续至第6周。
1.3 观察指标
1.3.1 体重 采用USA.HJ&HUAJIE称重仪每周测定1次大鼠体重,称重时间均为早上10点,并记录。
1.3.2 卵巢重量及形态学观察 6周后失血处死大鼠,立即解剖,双侧卵巢离体后采用USA.HJ&HUAJIE称重,然后将一侧卵巢组织浸泡于4%的甲醛中固定、切片、HE染色、组织学观察。
1.3.3 血清促卵泡素(FSH)、黄体生成素(LH)、睾酮(T)、游离睾酮(FT)、硫酸脱氢表雄酮(DHEA-S)测定 处死前采大鼠股静脉血液5 mL,室温血液自然凝固10~20 min,离心20 min左右(3 000 r/min),收集上清液,采用上海基尔顿公司提供的大鼠酶联免疫分析(ELISA)试剂盒测定血清LH、FSH、T、FT、DHEA-S。
1.3.4 卵巢组织匀浆T、FT、DHEA-S测定 处死大鼠后迅速解剖离体双侧卵巢组织,手工将一侧卵巢组织充分匀浆,用上海基尔顿公司提供的大鼠酶联免疫分析(ELISA)试剂盒测定卵巢组织匀浆中T、FT、DHEA-S。
1.3.5 肾上腺组织匀浆T、FT、DHEA-S测定 方法同卵巢组织匀浆。
1.4 统计学处理
2 结果
2.1 卵巢重量及形态学观察
两组大鼠6周后处死,实验组30例,双侧卵巢重量(0.113±0.224)g,对照组10例,双侧卵巢重量(0.096±0.108)g,两组比较差异有统计学意义(P<0.05)。对照组卵巢肉眼观察表面色泽红润,模型组外观苍白,体积增大,可见较多囊状扩张卵泡。模型组卵巢见囊性扩张的卵泡增多,黄体及各种发育阶段卵泡减少,其卵泡内卵母细胞或放射冠消失,颗粒细胞层数减少至2~3层(图1A)。对照组卵巢镜下见多个黄体及不同发育阶段的卵泡,卵泡内颗粒细胞呈多层,多为8~9层(图1B)。

图1 两组大鼠卵巢组织染色(HE,100×)Fig.1 HE staining of ovarian tissue of rats in the two groups
2.2 血清FSH、LH、T、FT、DHEA-S
实验组大鼠血清LH、T值水平高于对照组,P<0.05,实验组FSH、FT、DHEA-S值与对照组相比,差异无统计学意义(P>0.05)。见表1。

表1 两组大鼠血清LH、FSH、T、 FTDHEA-S水平Tab.1 The serum hormone levels of two groups
(1)两组比较P<0.05
2.3 卵巢及肾上腺组织匀浆T、FT、DHEA-S
实验组卵巢组织匀浆T水平较对照组升高,差异有统计学意义;实验组卵巢组织匀浆FT、DEAH-S及肾上腺组织匀浆T、FT、DHEA-S水平比较差异无统计学意义,P>0.05。见表2。
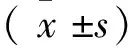
表2 两组大鼠卵巢和肾上腺组织T、 FT、DHEA-S水平Tab.2 The hormone level of two groups' ovarian and adrenal tissue
(1)与对照组比较,P<0.05
3 讨论
目前多囊卵巢综合征病因不清,由于临床表现的复杂性和高度异质性,故病因学一直是研究的热点与难点,关于PCOS病因主要涉及5个方面:(1)GnRH分泌控制异常;(2)卵巢原发障碍;(3)高雄激素分泌;(4)胰岛素抵抗;(5)肥胖因素。GnRH的高频率脉冲可导致LH分泌增加,FSH增加不明显,卵巢局部形成高LH的环境,卵泡发育障碍,卵泡闭锁增加。在卵巢原发障碍中,卵巢卵泡膜细胞表面某些酶表达异常导致雄激素合成增加,因雄激素增多与胰岛素抵抗两者紧密相连,形成雄激素-胰岛素-雄激素的自我延续的“恶性循环”。而对于生化性多囊卵巢综合征患者体内的高雄激素代谢如何,临床上有不同看法。在女性体内雄激素主要有雄烯二酮(A2)、睾酮(T)、脱氢表雄酮(DHEA)、硫酸脱氢表雄酮(DHEA-S)以及双氢睾酮(DHT),正常生理下这些雄激素主要来源于卵巢卵泡膜细胞产物及肾上腺皮质醇合成的中间产物,故有学者认为高雄激素症主要由卵巢引起,而有人认为由肾上腺引起,还有学者认为由外周脂肪组织引起。
本实验中实验组SD大鼠病理可见,卵巢外观体体积增大,白膜增厚,可见较多囊状扩张卵泡,镜下见卵巢间质不同程度增生,颗粒细胞减少,无优势卵泡形成,与PCOS卵巢病理改变相似。对照组大鼠卵巢组织切片见正常结构卵泡,有优势卵泡形成。通过ELISA检查方法检测显示实验组PCOS雌性SD大鼠血液循环中LH、T及卵巢组织匀浆中T水平均出现了明显升高,而血清FSH、FT、DHEA-S,卵巢组织匀浆的FT、DHEA-S及肾上腺组织匀浆的T、FT、DHEA-S与对照组相比升高不明显,差异无统计学意义。LH与FSH协同促进卵泡发育,激发排卵,促进颗粒细胞黄素化;当LH高峰出现促进颗粒细胞分化,同时也抑制颗粒细胞的有丝分裂和增殖,使颗粒细胞过早进入分化状态,导致颗粒细胞增殖终止,最终导致卵泡发育停止在窦卵泡阶段,无优势卵泡形成。另者因FSH和LH结构相似,两者有竞争性,当LH水平升高时,FSH维持在相当于或低于卵泡早期水平,故在PCOS患者中其FSH水平大多都正常或稍微偏低[3]。有学者通过原位杂交方法发现,雄激素受体(AR) mRNA主要在大鼠卵泡膜细胞表达明显,卵巢AR与雄激素结合在卵泡发育局部控制机制上的重要作用[4],主要表现在调控卵泡发育的早期阶段,例如应用抗雄激素抗体可以阻止小鼠的窦前卵泡发展到排卵前卵泡[5]。卵泡膜细胞体外细胞培养实验表示多囊卵巢综合征患者体内合成雄激素过程的酶活性都增强[6],如P450侧链裂解酶、17-α羟化酶(CYP17),生成大量雄激素最终导致高雄激素环境使大量卵泡闭锁。本实验中PCOS雌性SD大鼠卵巢局部高雄激素水平影响了早期卵泡发育,增加卵泡数量及大小,同时促使卵泡闭锁,发生不排卵,肾上腺所分泌睾酮与高睾酮血症发生可能无明显关系。众多学者研究发现约50%患者存在不同程度的胰岛素抵抗及代偿性高胰岛素血症,胰岛素受体可增强LH释放并促进卵巢分娩雄激素,又可抑制性激素结合蛋白(SHGB)的合成[7],减少与睾酮的结合致游离T浓度升高。但是游离睾酮浓度在体内含量较低,很多因素可以影响它与SHBG的亲和力,包括年龄、肥胖、妊娠、雄激素治疗和多囊卵巢综合征,导致总睾酮与游离睾酮部分错配,故对于游离睾酮的测定存在误差可能。硫酸脱氢表雄酮只源于肾上腺,DHEA-S是肾上腺功能标志性检测物,且DHEA-S分泌的增加应该考虑到年龄与种族的关系,DHEA-S会随着年龄增加而减少。有研究表示高剂量外源性睾酮对做过卵巢切除术妇女的影响,发现切除卵巢后,DHEA-S增加不明显[8]。张焰等研究结果显示在PCOS组DHEA-S与对照组中差异无统计学意义[9]。另有研究表示高胰岛素对肾上腺合成的脱氢表雄酮(DHEA)抑制作用[10]。最近有研究提出伴或不伴有高雄激素血症的多囊卵巢综合征患者,其DHEA-S水平无明显变化[11]。本实验结果显示其卵巢组织中DHEA-S含量应该比肾上腺组织含量少,但其两者均值相比较,卵巢含量稍高,这与实验对象的生理性质有关。
综上所述,PCOS雌性SD大鼠血液循环中出现高LH及高T水平,其体内雄激素主要分布在血液中及卵巢中,卵巢卵泡膜细胞与间质细胞分泌过多的雄激素通过血液循环进入体内,产生高雄激素血症,进而出现一系列的临床表现。对于卵泡膜细胞及间质细胞产生高雄激素水平机制及肾上腺分泌的雄激素有没有其他因素间接导致高雄激素血症有待进一步研究。
[1] Gambineri A,Pelusi C,Vicennati V,et al.Obesity and the polycystic ovary syndrome[J].Int J Obes Relat Metab Disord, 2002(7):883-896.
[2] Nisenblat V,Norman RJ.Androgens and polycystic ovary syndrome[J].CurtOpin Endocrinol Diabetes Obes, 2009(3):224-231.
[3] Boomsma CM,Eijkemans MJ.A meta-analysis of pregnancy out-comes in women with polycystic ovary syndrome[J].Hum Reprod Up-date, 2006(6):673-683.
[4] Gill A,Jamnongjit M,Hammes SR.Androgens promote maturation and signaling in mouse oocytes independent of transcription:a release of inhibition model for mammalian oocyte meiosis[J].Mol Endoerinol, 2004(1):97-104.
[5] Orisaka M.Growth differentiation factor 9 promotes rat preantral follicle growth by up-regulating follicular androgen biosynthesis[J].Endocrinology, 2009(6):2740-2748.
[6] Fujita Y,Mori T,Aso T,et al.Sites of androgen overproduction in the polycystic ovary (author's translate)[J].Nihon Sanka Fujinka Gakkai Zasshi, 1980(6):706-712.
[7] Guzick DS.Polycystic ovary syndrome[J].Obstct Gynecol, 2004(1):41-47.
[8] Arlt W,Martens JW,Song M,et al.Molecular evolution of adrenarche:structural and functional analysis of p450c17 from four primate species[J].Endocrinology, 2002(12):4665-4672.
[9] 张焰,袁瑞.多囊卵巢综合征高雄激素血症特性研究[J].中华内分泌外科杂志, 2009(1):8-9.
[10]Vrbikova J,Hill M,Starka L,et al.The effects of long-term metformin treatment on adrenal and ovarian steroidogenesis in women with polycystic ovary syndrome[J].Eur J Endocrinol, 2001( 6):619-628.
[11]韦燕妮,覃爱平.多囊卵巢综合征高雄激素血症相关性研究[D].广西医科大学, 2008.
(2016-09-27收稿,2016-11-09修回)
中文编辑: 刘 平; 英文编辑: 赵 毅
Androgen Levels in Female SD Rats with Polycystic Ovarian Syndrome
WANG Houmei, HUANG Lin, XIAO Ziwen
(DepartmentofObstetricsandGynecology,theAffiliatedHospitalofGuizhouMedicalUniversity,Guiyang550004,Guizhou,China)
Objective: To investigate the androgen levels in serum, ovary and adrenal gland in PCOS SD rats. Methods: Female SD rats were randomly divided into control group and test group. The control group was fed with the basic diet food and uncontrolled water; test group was fed with high-fat and high-sugar diet, 5% glucose water, and on 1 to 42 days was given Novolin N (low protamine zinc insulin NPH-Humulin), vastus medialis subcutaneous injection, while on 11 to 22 days was injected with human chorionic gonadotropin, then killed the rats. Observing weight of ovaries and ovarian tissue pathological,then the serum levels of luteinizing hormone(LH), follicle stimulating hormone(FSH), testosterone(T), free-testosterone(FT), dehydroepiandr-Osteronesulfate (DHEA-S) was observed by using ELISA, meanwhile T, FT, DHEA-S levels in ovarian tissue and adrenal tissue were tested. Results: Microscopically, the test group showed the large follicular cystic increased, corpus luteum and follicles at various developmental stage decreased. While the control group showed many corpus luteum and follicles at each development stage, granulosa cells lined with 8-9 layers. These showed the models built successfully. The weight of ovaries, the serum T level, the serum LH level and the ovarian tissue T level of test group were higher than the control group (P<0.05). The results of the serum FSH, FT, DEAH-S comparison between the two groups had no significant difference (P>0.05). The ovarian FT, DHEA-S and the adrenal T, FT, DEAH-S had no significant difference between the test group and the control group (P>0.05); Conclusion: High level serum testosterone is the mainly manifestation of hyperandrogenism, the ovary maybe the major organ to secret it.
polycystic ovary syndrome; ovary; adrenal gland; serum; rats,Sprague-Dawley; hyperandrogenism
贵州省科技厅攻关课题SY[(2011)3021号]
时间:2016-12-15
http://www.cnki.net/kcms/detail/52.1164.R.20161215.1534.019.html
R711.75
A
1000-2707(2016)12-1415-04
10.19367/j.cnki.1000-2707.2016.12.011
**通信作者 E-mail:19763368@qq.com

