维持性血液透析患者的心脏瓣膜钙化发病情况
庞家华, 赵 霞, 万 玮
(南京中医药大学第三附属医院 南京市中医院, 1. 超声心动图室; 2. 肾脏病科, 江苏 南京, 210001)
维持性血液透析患者的心脏瓣膜钙化发病情况
庞家华1, 赵 霞2, 万 玮1
(南京中医药大学第三附属医院 南京市中医院, 1. 超声心动图室; 2. 肾脏病科, 江苏 南京, 210001)
维持性血液透析; 瓣膜钙化; 血磷
终末期肾病(ESRD)是各种病因所致的慢性肾脏疾病(CKD)的最终阶段,心血管疾病是慢性肾脏病患者的主要致死原因,终末期慢性肾病患者心血管疾病的死亡率显著高于非终末期肾病患者,在70岁以下的终末期肾病患者中,每年死于心血管事件者占50%~60%[1]。维持性血液透析(MHD)是目前终末期慢性肾病最有效的治疗方式之一,但易导致患者体内代谢紊乱、细胞因子排泄障碍,代谢所产生的毒素、糖基化终末产物及晚期氧化蛋白产物在体内积聚,并与单核巨噬细胞表面特异性受体结合,分泌大量的黏附分子,并激活核因子κB(NF-κB),分泌大量炎性细胞因子如IL-1、IL-6 及TNF-α等[2-3]。超声心动图作为一种廉价、易获得性以及无放射性损伤的心血管影像学检查手段,可以实时、动态评价心脏瓣膜的钙化情况。本研究探讨终末期慢性肾病患者心脏瓣膜情况,分析引起瓣膜钙化的相关因素,现报告如下。
1 资料与方法
1.1 一般资料
收集2012年6月—2014年6月本院就诊的终末期慢性肾病患者75例,男43例,女32例,年龄45~76岁,平均(59.4±7.6)岁,透析龄6~61个月,中位数34个月。以上患者均符合以下入选条件: ① 年龄大于18周岁; ② 透析时间大于6月; ③ 排除既往有心脑血管疾病、恶性肿瘤、先天性心脏疾病及活动性炎症病变患者等。另选择本院健康体检者75例,其中男39例,女36例,年龄25~79岁,平均(54.5±13.5)岁。每位体检者均无风湿性心脏病、细菌性心内膜炎、甲亢性心脏病、马凡氏综合征等引起的心脏瓣膜病变,肝肾功能及尿常规均正常。本研究入选患者及正常健康者均知情同意,同时获得医院伦理委员会批准。
1.2 透析方法
采用金宝AK95S血液透析机,东丽TS-1.3s聚砜膜透析器,透析器膜面积1.3 s, 透析液流量500 mL/min, 血流量200~350 nR/min, 碳酸氢盐透析液(钠138 mmol/L、钾2.0 mmol/L、钙1.5 mmol/L、镁0.5 mmol/L、碳酸氢根32 mmol/L)。
1.3 观察指标
透析患者透析当天空腹采集静脉血3 mL, 健康对照者同样空腹采血3 mL。采血后将3 mL血标本送本院检验科,应用全自动生化分析仪检测白蛋白(ALB)、血钙(Ca)、血磷(P)、总胆固醇(TC)、高密度脂蛋白(MHDL)、低密度脂蛋白(LDL)、甘油三脂(TG)、血糖、肌酐、C反应蛋白等指标。
1.4 超声心动图检查
采用HP Sono 5500超声诊断仪,探头频率2.5 MHz, 按美国超声心动图学会指南进行经胸超声心动图检查,所获得图像均由本科经验丰富的超声诊断医师在未知患者其他临床数据的情况下评价,符合瓣膜增厚、回声增强、瓣叶活动受限、开放幅度减小诊断为瓣膜钙化[6]。
1.5 统计学分析
以SPSS19.0软件分析,计量资料以均数±标准差表示,组间比较采用两组独立样本t检验。采用多元线性回归分析与心脏瓣膜钙化相关的危险因素。P<0.05为差异有统计学意义。
2 结 果
肾病组中主动脉瓣钙化28例,二尖瓣+主动脉瓣钙化8例,二尖瓣钙化3例,有心脏瓣膜钙化者共39例;健康对照组中主动脉瓣钙化6例,二尖瓣+主动脉瓣钙化1例,二尖瓣钙化2例,有心脏瓣膜钙化者共9例。与健康体检者相比,慢性肾病患者瓣膜钙化率显著升高(P<0.05)。将肾病组中有瓣膜钙化的维持性血液透析患者设为瓣膜钙化组,与无瓣膜钙化患者进行对比分析,结果显示瓣膜钙化组中患者的透析龄、P、iPTH、TC与TG均显著高于无瓣膜钙化组(P<0.05)。见表1。多元线性回归分析表明,与瓣膜钙化相关的危险因素包括患者年龄、低密度脂蛋白、血磷及iPTH(P<0.05)。见表2。
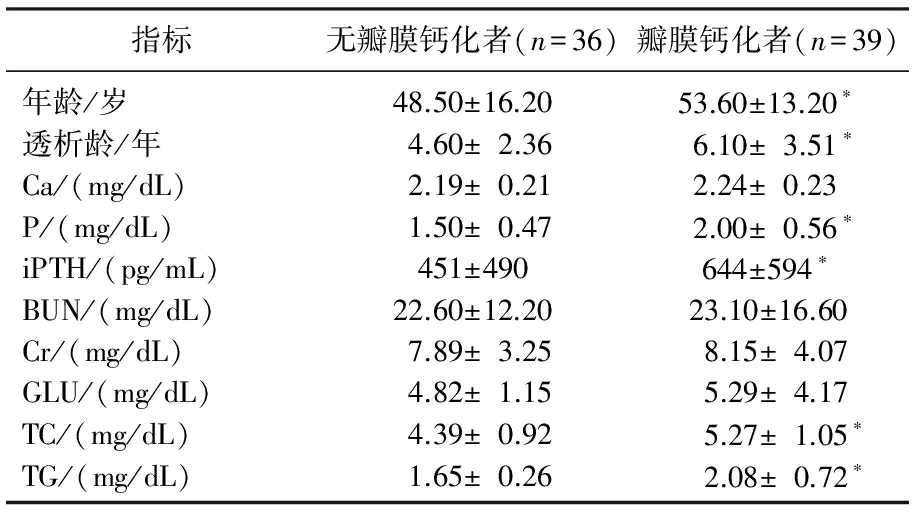
表1 瓣膜钙化组与无瓣膜钙化组血生化指标比较
与无瓣膜钙化者比较, *P<0.05。
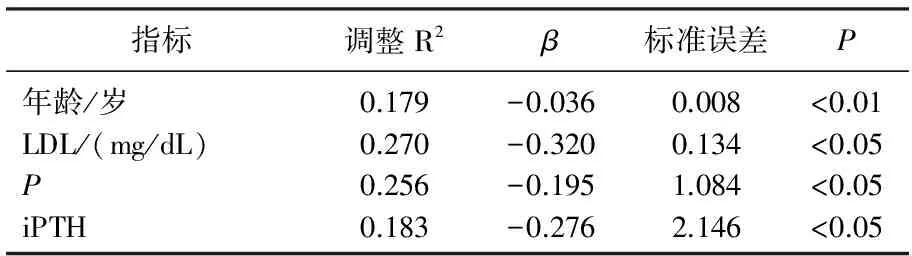
表2 与冠状动脉钙化积分相关的因素分析
3 讨 论
体内抗氧自由基系统与氧自由基产生系统之间的失衡可导致氧自由基损伤和脂质过氧化作用。这些炎症细胞因子及氧化应激在引起MHD患者透析相关心血管事件的过程中起着一定的作用[4-5]。维持性血液透析患者发生血管和心脏瓣膜钙化的概率与正常人相比显著提高,是终末期肾病患者心血管疾病的重要危险因素之一,是心血管事件和死亡的预测指标[6]。
心血管系统钙化是慢性肾病-骨矿物质代谢紊乱患者心血管疾病高发病率和高死亡率的一个可能原因。心血管系统钙化的存在及其严重程度,是心血管事件和死亡率的强烈预测因子。在慢性肾病患者中,瓣膜钙化较普通人群更加普遍和严重,而且已发生钙化的血管其钙化进行的速度较普通人更快。作者通过对比75对慢性肾病患者及健康体检者瓣膜钙化情况充分证明了这一观点。本研究中,慢性肾病患者的瓣膜钙化率显著高于健康体检者,因此对于慢性肾病患者评估瓣膜钙化情况对预测心血管疾病具有非常重要的意义。
本研究发现,将维持性血液透析患者合并瓣膜钙化患者与单纯维持性血液透析患者相比, 2组患者在年龄、透析龄、BUN、Cr、Ca方面无显著差异。然而,合并瓣膜钙化组患者血清透析龄、血清磷、甲状旁腺激素、总胆固醇与三酰甘油均高于正常水平,说明这些因素可能引起维持性血液透析患者心脏瓣膜钙化的形成。通过多元回归进一步分析发现,其与年龄、低密度脂蛋白、血磷及iPTH有关,说明继发性甲状旁腺功能亢进及钙、磷代谢紊乱可能是引起维持性血液透析患者瓣膜钙化的主要因素。
心血管系统钙化的发生和发展是诸多危险因素参与导致的,包括传统的心血管危险因素如高龄、高血压、糖尿病、高脂血症、贫血、营养不良、肥胖、吸烟等。对于需要维持性血液透析治疗的慢性肾病患者,与慢性肾病相关的多种因素也参与了血管的钙化进程,如透析时间,高磷血症、高钙血症、含钙磷结合剂的不当使用、大剂量活性维生素D、过低的骨化三醇水平、甲状旁腺功能亢进或低下、炎症反应、氧化应激以及尿毒症毒素等[7]。此外,慢性肾衰竭患者体内代谢紊乱,细胞因子排泄障碍,体内积聚的代谢所产生的毒素、糖基化终末产物以及晚期氧化蛋白产物与单核巨噬细胞表面特异性受体结合,分泌大量的黏附分子,激活核因子κB(NF-κB), 导致炎性细胞因子如IL-1、IL-6 及TNF-α等大量分泌,进一步促进了瓣膜钙化的形成[8-10]。本研究发现,维持性血液透析患者瓣膜钙化的发生率为52%。通过研究主动脉瓣组织病理以及动物模型发现,主动脉瓣钙化的早期阶段是由氧化的低密度脂蛋白、炎细胞(巨噬细胞、淋巴细胞、肥大细胞)、形成的微钙化灶沉积于内膜下,导致内膜下组织增厚引起的。
[1] Foley R N, Parfrey P S, Sarnak M J. Clinical epidemiology of cardiovascular disease in chronic renal disease[J]. American journal of kidney diseases: the official journal of the National Kidney Foundation, 1998, 32: 112-119.
[2] Kato S, Chmielewski M, Honda H, et al. Aspects of immune dysfunction in end-stage renal disease[J]. Clin J Am Soc Nephrol, 2008, 3(5): 1526-33.
[3] Shahrokh S, Heydarian P, Ahmadi F. Association of Inflammatory Biomarkers with Metabolic Syndrome in Hemodialysis Patients[J]. Ren Fail, 2012, 14: 137-143.[4] Dounousi E, Papavasiliou E, Makedou A, et al. Oxidative stress is progressively enhanced with advancing stages of CKD[J]. Am J Kidney Dis, 2006, 48(5): 752-760.
[5] Karamouzis I, Sarafidis P A, Karamouzis M, et al. Increase in oxidative stress but not in antioxidant capacity with advancing stages of chronic kidney disease[J]. Am J Nephrol, 2008, 28(3): 397-404.
[6] 李学旺. 慢性肾脏病患者的心血管合并症[M]. 北京: 人民卫生出版社, 2011: 161-162.
[7] Lang R M. Recommendations for chamber quantification: a report from the American Society of Echocardiography's Guidelines and Standards Committee and the Chamber Quantification Writing Group, developed in conjunction with the European Association of Echocardiography, a branch of the European Society of Cardiology[J]. Journal of the American Society of Echocardiography: official publication of the American Society of Echocardiography, 2005, 18: 1440-1463.
[8] Mizobuchi M, Towler D, Slatopolsky E. Vascular calcification: the killer of patients with chronic kidney disease[J]. Journal of the American Society of Nephrology, 2009, 20: 1453-1464.
[9] Kaysen G A. The microinflammatory state in uremia: causes and potential consequences[J]. J Am Soc Nephrol, 2001, 12(7): 1549-1557.
[10] Merino A, Nogueras S, Buendía P, et al. Microinflammation and endothelial damage in hemodialysis[J]. Contrib Nephrol, 2008, 161: 83-85.
2016-10-22
R 459.5
A
1672-2353(2016)23-185-02
10.7619/jcmp.201623071

