负载型纳米金催化剂在乙炔选择性加氢反应中的研究进展
李菲菲, 孙 逊, 孙立波 ,郑玉华,韩 春,杨 昕, 祁彩霞*
(1.山东省黄金技术研究中心,烟台大学化学化工学院,山东 烟台 264005;2.烟台大学化学化工学院,山东 烟台 264005)
综述与展望
负载型纳米金催化剂在乙炔选择性加氢反应中的研究进展
李菲菲1, 孙 逊1, 孙立波1,郑玉华1,韩 春1,杨 昕2*, 祁彩霞1*
(1.山东省黄金技术研究中心,烟台大学化学化工学院,山东 烟台 264005;2.烟台大学化学化工学院,山东 烟台 264005)
介绍了乙炔选择性加氢制乙烯催化剂的研究和开发进展。针对负载型纳米金催化剂的发展趋势及其对乙炔加氢反应产物中乙烯的独特选择性,重点对比单金属纳米金催化剂及合金型催化剂的催化性能差异,发现合金型纳米金催化剂具有较高的乙炔转化率和稳定性。影响催化性能的主要因素有纳米粒子的大小及活性组分之间的相互协同作用。分析积炭的形成以及导致催化剂失活的原理。展望低温条件下具有高转化率与高稳定性的合金型纳米金催化剂的应用前景。
催化剂工程;负载型纳米金催化剂;乙炔选择性加氢;乙炔;乙烯
乙烯为全球产量最大的化学品之一,其产量是衡量石油化工发展水平的重要标志。乙烯是制备很多化学产品的基础原料,也是合成各种高聚物的重要单体。我国绝大部分乙烯通过石油脑经高温蒸汽裂解而成[1-2],生产成本高,每吨乙烯需消耗3.2吨石油脑,生产成本1 300美元,是美国和中东的2~2.5倍。经裂解得到的乙烯中含有少量乙炔(裂解炉出口气中乙炔物质的量分数为0.1%~0.5%),影响后续的乙烯聚合反应。例如,在聚烯烃生产过程中,齐格勒-纳塔催化剂很容易因乙烯中乙炔的聚合而堵塞内部孔道或覆盖活性中心,导致催化剂活性降低,得到的聚合产品性能变差。因此,工业用乙烯要求其中乙炔含量必须小于5×10-6。
脱除乙烯中乙炔的方法有溶剂吸收法、选择性加氢法、低温精馏法、乙炔酮沉淀法、氨化法和络合吸收法等[3-5],其中,选择性加氢法是工业上应用最广泛和最有效的方法[6]。催化加氢过程中,乙炔可部分加氢还原为乙烯,也可能被深度加氢还原为乙烷。从原子经济角度考虑,通过控制工艺条件并选用合适的催化剂,生产中可以实现乙炔选择性加氢生成乙烯,达到脱除乙炔和增加乙烯产率的目的。从化学平衡的角度分析,乙炔加氢反应在热力学上接近全部转化。因此,当反应原料中乙炔含量较少和生产规模较大时,采用催化加氢脱炔的方法在工艺操作和经济核算上均比较有利。

1 金催化剂
金被认为是一种不具备催化应用价值的“惰性”贵金属。早在 20世纪 70 年代,Sermon P A等[9]揭示了小尺寸金在加氢反应中的应用潜力。但直到 1987年,Haruta M等[10]发现氧化物负载的纳米金颗粒(<5 nm)对CO低温氧化反应具有极高的催化活性后,金的催化潜力才逐渐受到重视。金不但具有优异的催化氧化活性,而且在诸如丙烯醛加氢[11]、1,3-丁二烯加氢[12]以及α,β-不饱和酮[13]加氢等反应中也表现出较好的催化活性。一般认为,金催化剂的加氢催化活性低于钯催化剂。但金催化剂有一个突出特性,即对单烯烃的形成有100%选择性,主要因为在金表面上炔烃和二烯烃具有比单烯烃更强的吸附能力,导致单烯烃能够很快从金表面脱附,而且至少在反应的第一阶段完成之前不会被重新吸附。这引起研究者的兴趣,尤其是在大量乙烯气流中对乙炔的选择性加氢研究[14-15],重点集中于如何在较低反应温度下提高金的催化性能。Jia J等[16]首次使用单金属金替代钯用于乙炔选择性加氢反应,制备的Au/Al2O3催化剂在(40~250) ℃条件下,乙烯选择性达100%;高于300 ℃时,乙炔转化率100%;并且证明金纳米粒子尺寸在3 nm时具有最高的催化活性。
2008年,Azizi Y等[17]采用直接离子交换法制备了Au/CeO2催化剂,金颗粒尺寸约2 nm,在氢炔体积比为3~60和反应温度(270~400) ℃条件下,对催化剂活性和选择性进行评价,结果表明,反应温度300 ℃时,H2与乙炔体积比选择上述范围任意值,乙烯选择性均达100%。另外,在低于300 ℃时有积炭产生,但对催化剂选择性影响不明显;高于300 ℃时,催化剂迅速失活,乙烯选择性明显降低。Sárkány A等[18]采用溶胶法制备了金粒子尺寸分别为3.7 nm和6.1 nm的Au(Ⅰ)/SiO2和Au(Ⅱ)/SiO2催化剂,并采用沉积-沉淀法制备出金纳米粒子尺寸为3.3 nm的Au/TiO2催化剂进行对比,结果发现,金纳米粒子活性与其尺寸大致满足反比例关系:Au/TiO2>Au(Ⅰ)/SiO2≫Au(Ⅱ)/SiO2;反应温度(227~277) ℃时,乙烯选择性下降,主要由于过度加氢生成乙烷以及氢解生成甲烷所致。相比Au/SiO2催化剂而言,Au/TiO2催化剂易失活且易形成积炭。通过对比TiO2和Au/TiO2催化剂的TPO表征结果发现,积炭的形成主要由Au-Ti3+共同作用促使。Gluhoi A C等[19]研究不同助剂(Li、Ba和Ce的氧化物)的添加对纳米Au/Al2O3催化剂的影响,结果表明,Li2O的存在对乙炔转化率产生促进作用,主要是由于乙炔是酸性气体,而Li2O具有碱性特征,BaO的存在对乙炔的转化率具有抑制作用,但两者对乙烯选择性均无影响。Au/CeO2对乙炔转化率具有明显的促进作用,主要是由于Ce4+可以吸附大量的H2,而经过吸附-脱附的H2对催化剂具有较强的敏感性[20-21]。
我们课题组比较了溶胶法和沉积-沉淀法制备的Au/Al2O3催化剂对乙炔选择性加氢反应的影响,结果如图1所示。由图1可见,相比溶胶法制备的催化剂,沉积-沉淀法制备的Au/Al2O3催化剂上的乙炔转化率较高,主要由于沉积-沉淀法得到的金纳米粒子为3 nm,溶胶法制备的金纳米粒子为5 nm(如图2),表明较小的金纳米粒子更有利于乙炔选择性加氢。
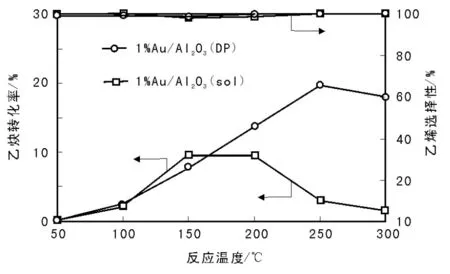
图 1 溶胶法和沉积-沉淀法制备的Au/Al2O3催化剂上乙炔选择性加氢结果Figure 1 Results of selective hydrogenation of acetylene on Au/Al2O3(sol) and catalysts prepared by sol method and deposition precipitation method
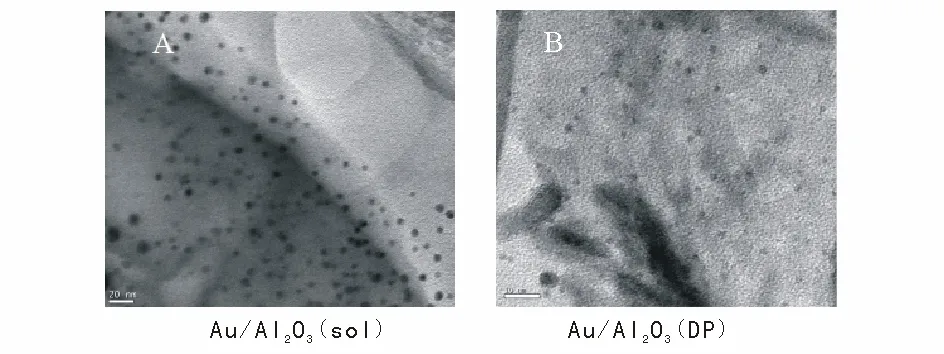
图 2 溶胶法和沉积-沉淀法制备的Au/Al2O3催化剂的TEM照片Figure 2 TEM images of Au/Al2O3 catalysts prepared by sol method and deposition precipitation metho
2 金/钯双金属催化剂
由于金纳米颗粒对乙炔的吸附程度远高于乙烯[25],具有较高的乙烯选择性,但低温下的乙炔转化率很低[19]。为提高低温下的乙炔转化率,具有一定协同作用的双金属催化剂受到关注。Choudhary T V等[26]由[Au2(pph3)6](BF4)2复合物分解制备1%Au/TiO2催化剂,金粒子尺寸为4.6 nm,乙炔加氢反应在180 ℃进行,乙烯选择性90%,失活速率很快。在相同条件下的Pd/TiO2催化剂具有较高转化率,但乙烯选择性较差;而Au-Pd/TiO2催化剂表现较好,相比于Au/TiO2催化剂具有较高的稳定性,相对于Pd/TiO2具有较高的选择性,主要是由于钯和金相互协同作用所致。Sarkany A等[27]将Pd/SiO2催化剂与Pd-Au/SiO2催化剂进行对比研究,发现Pd-Au/SiO2催化剂上乙烯选择性较高且积炭很少,验证了双金属催化剂的优势。Zhang Y等[28]采用化学沉积法制备Au-Pd/SiO2催化剂,可显著增加乙炔转化率和乙烯选择性。这是由于Pd对乙炔的吸附模式发生变化,即从亚乙基对Pd的强吸附转变为π键对Pd的弱吸附,从而避免过度加氢生成乙烷,并从动力学角度证明双金属的协同作用实质上是几何作用而不是电子作用。
PdAu纳米合金催化剂的形貌对催化剂的性能也有不同影响。Ma C等[29]采用在PVA的保护下滴加NaBH4还原剂的方法合成尺寸(30~55) nm的Pd-Au合金纳米花催化剂,并负载于MgAl双层金属氢氧化物上,与PdAu八面体催化剂对比,纳米花形貌的Pd-Au催化剂具有较高的晶体缺陷密度,使该催化剂上乙炔转化率在140 ℃时约95%,而PdAu八面体催化剂上乙炔转化率仅约85%,并且该PdAu纳米花催化剂上乙烯选择性为72%,PdAu八面体催化剂上乙烯选择性仅62%,主要是由于催化剂对乙烯的吸附强度不同所致。由此可以看出,PdAu八面体的乙烯脱附温度相对较高,为(250~260) ℃,更有利于生成副产物乙烷。复杂形貌的协同作用使PdAu纳米花催化剂具有较高选择性,同时该花型PdAu结构分散比较均匀且相邻较远,能够起到阻止PdAu纳米晶体形成的作用。反应48 h,八面体PdAu由于迁移或聚集导致PdAu纳米粒子尺寸明显增大,而PdAu纳米花没有明显的结构变化和团聚现象,对于从晶体结构角度合成多金属催化剂具有指导意义。除此之外,Sarkany A等[30]通过晶种生长法将一定厚度的Pd壳层包覆于5 nm的Au核表面,最后负载于SiO2载体上,制备具有核壳结构的Pdshell-Aucore/SiO2催化剂,并探究作为外壳的Pd厚度(0.12~0.15) nm对丙烯中乙炔催化加氢活性的影响,结果表明,随着Pd核厚度增加,催化剂活性逐渐降低,例如Pd(30)-Au/SiO2的TOF为0.15 s-1,而Pd(80)-Au/SiO2的TOF为0.1 s-1,转化率明显降低。
PdAu双金属催化剂的制备方法对催化性能也有很大影响。Zhang S等[31]以浸渍法将Au沉积于TiO2上,再采用沉积-沉淀法负载Pd进行改性(Au与Pd质量比为14),之后采用低压射频H2对催化剂进行预处理(AuPd-P),与传统热还原处理的催化剂对比发现,乙炔转化率明显提高,乙烯选择性显著降低;而将该催化剂同时进行热还原与低压射频H2预处理(AuPd-P250)却得到相反结果,但转化率和选择性介于传统热还原处理的催化剂与低压射频H2处理催化剂之间。表征数据显示,较高的乙炔转化率是催化剂表面大量的Pd活性位所致,选择性较差则是由于相邻Pd位点的相互接触从而导致乙炔的过度加氢生成乙烷。通过将反应后的催化剂进行DTG表征,表明采用低压射频H2处理催化剂在反应过程中生成的绿油少。
3 其他金属改性的金催化剂
Yang B等[32]发现,Au-Ni催化剂在乙炔加氢方面具有较高的催化活性和选择性,通过将Au、Ag 和 Cu分别掺杂到Ni表面进行活性对比并阐明反应机制,乙烯选择性依次为Au-Ni>Ag-Ni>Cu-Ni。这是由于乙炔在Ni表面具有较强的吸附力,而掺杂Au、Ag和Cu可以减弱乙炔对Ni的吸附能力,增加乙烯选择性。Nikolaev S A等[33]将单金属Au和NiO分别负载于Al2O3、TiO2、ZnO和ZrO2载体上,结果表明,乙烯选择性在84 ℃为95%~100%,两种粒子的大小对乙炔转化率影响截然相反,如NiO粒子尺寸为7 nm时,TOF为(812~1 023) h-1,而NiO粒子尺寸为4 nm时,TOF 降为276 h-1,表明相对较大的NiO粒子更有利于乙炔的选择性加氢。但金纳米粒子为8 nm和2.5 nm时,TOF 分别为(0~28) h-1和36 h-1,再次验证金纳米粒子越小越有利于反应进行。考察双金属NiO/Au在不同载体上的催化性能,结果表明,NiO/Au/Al2O3、NiO/Au/TiO2、NiO/Au/ZnO和NiO/Au/ZrO2催化剂的TOF分别为1 466 h-1、1 147 h-1、563 h-1和 569 h-1。从量子化学角度看,扭曲的3D结构或带正电荷的金易吸附游离的H2或优先吸附乙炔和乙烯混合物中的乙炔。Liu X等[34]使用硅烷偶联剂将金和银还原沉积在SiO2表面,并采用O2等离子体去除硅烷偶联剂,形成尺寸为3.1 nm的金银合金纳米粒子,结果表明,相对于金催化剂,金银合金催化剂在高温下具有较高的催化活性。还验证了相同条件下,相比高温焙烧方法制备的Au-Ag/SiO2-cal催化剂,采用O2等离子体去除硅烷偶联剂制备的Au-Ag/SiO2-OP催化剂具有更好的催化活性,200 ℃时,Au-Ag/SiO2-OP催化剂上乙炔转化率为99%,而Au-Ag/SiO2-cal催化剂上乙炔转化率约75%。考虑到Au-Ag/SiO2-cal(3.05 nm)和Au-Ag/SiO2-OP(3.10 nm)催化剂的纳米粒子尺寸相近,所以Au-Ag/SiO2-OP催化剂催化活性较好可能是O2等离子体的处理使Au-Ag与SiO2催化剂具有更强的相互作用[35]。通过TEM和XRD表征发现,经过干燥、焙烧和O2等离子处理的Au-Ag/SiO2催化剂,金纳米粒子分别为(3.02±0.72) nm、(3.05±0.79) nm和(3.10±0.89) nm,表明银的存在能够有效阻止金催化剂在高温条件下烧结,提高其稳定性。金基催化剂在乙炔选择性加氢反应中的催化性能比较如表1所示。
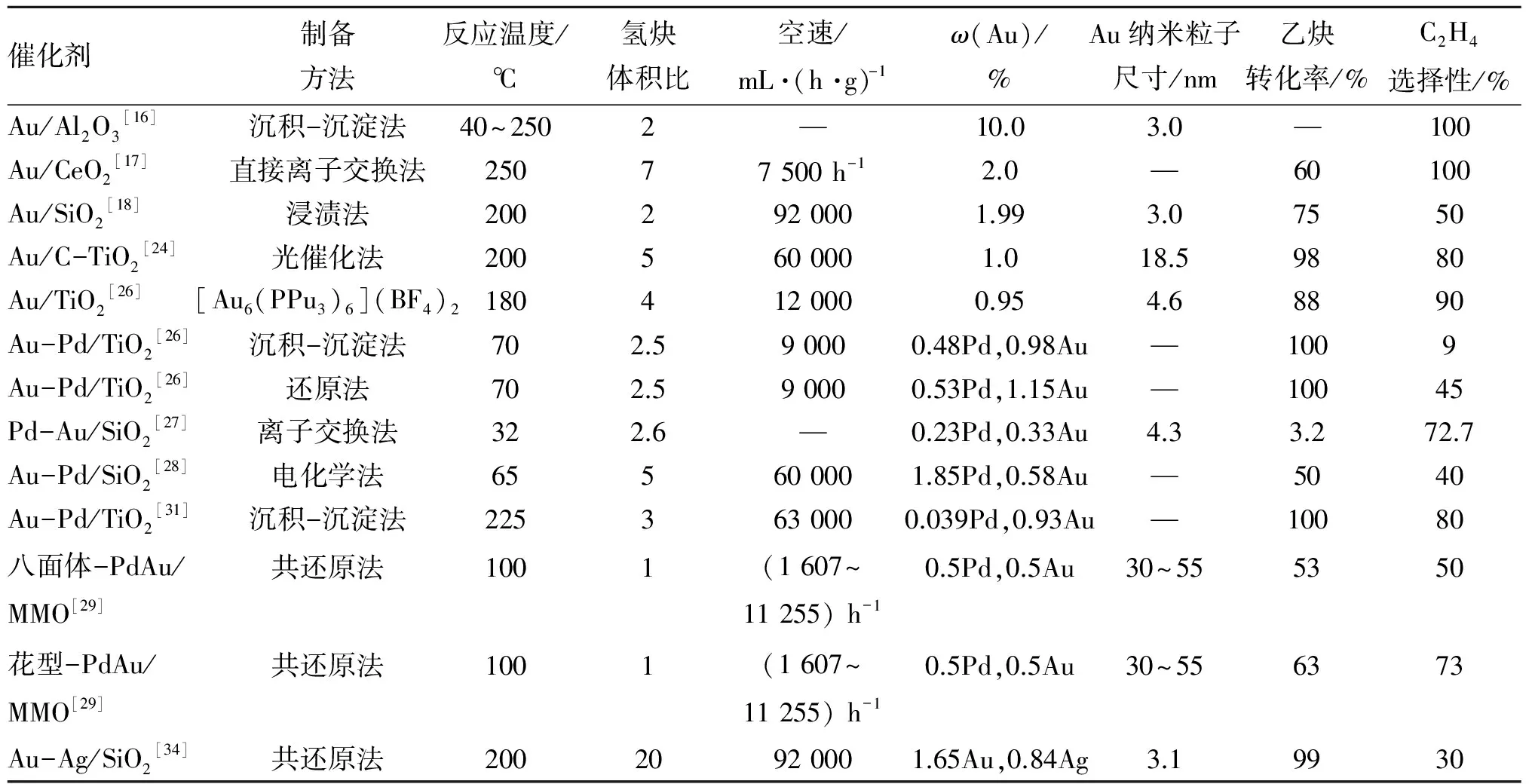
表 1 金基催化剂在乙炔选择性加氢反应中的催化性能比较
4 积炭对金催化剂在乙炔加氢反应的影响
随着反应的进行,金催化剂的催化性能出现逐渐下降甚至失活的趋势,主要是催化剂表面积炭所致。Gluhoi A C等[19]等对乙炔催化加氢的金催化剂进行了失活和再生实验,即将反应后的催化剂在空气中燃烧(最高温度500 ℃),观察CO2脱附情况并再次用于乙炔选择性加氢反应,结果表明,经过高温处理(金纳米粒子为7.1 nm,颗粒相对较大)与未经高温处理的Au/Al2O3催化剂可以看出CO2的脱附温度与金纳米粒子的大小和分散度有密切关系,金纳米粒子越大,CO2脱附温度相对越高。通过对比O2处理前后乙炔转化率可以看出,经过O2处理的催化剂催化性能更加优良。也证实在乙炔加氢过程中催化剂失活主要是由于形成的积炭覆盖催化剂活性位所致,该积炭易于通过燃烧去除,表明金催化剂的失活及再生过程可逆。
还有研究者进行了Au/CeO2[17]、Au/SiO2[18]和Au/TiO2[18]催化剂催化反应后CO2脱附的研究,其中,Au/CeO2催化剂在低于210 ℃形成的积炭虽然可以堵塞催化剂通道,但不会使催化剂中毒,不影响乙烯选择性(仍为100%);并且通过TPO表征可知,积炭位于金属表面或接近于金属的位置。通过对比反应温度对积炭形成的影响(图3)可知,由于两条曲线几乎重合,可以确定在试验范围反应温度对积炭的形成无影响。而该催化剂分别在245 ℃、340 ℃和440 ℃处有脱附峰,代表有3种类型的积炭。文献[27,36-37]认为,位于245 ℃处的脱附峰是由低温下松散的或被捕获的碳氢化合物燃烧而成,该积炭对反应没有影响;345 ℃处的峰是由类似于石墨前驱体的无定型积炭燃烧产生;440 ℃的峰由离子活性位产生的酸性积炭燃烧导致,并附着于催化剂载体上,降低催化剂活性。

图 3 催化剂在V(H2)∶V(C2H2)=5 、(210~400) ℃ 和(30~400) ℃ 条件下反应后的TPO[17]Figure 3 TPO after reaction under the conditions of V(H2)∶V(C2H2)=5 ,(210-400) ℃ and (30-400) ℃[17]
Sárkány A[18]比较了不同大小的金纳米粒子和不同氢炔比对Au(Ⅰ)/SiO2(3.7nm)、Au(Ⅱ)/SiO2(6.1 nm)、Au/TiO2催化剂和单一载体TiO2对积炭形成的影响,相对于Au(Ⅰ)/SiO2催化剂,Au/TiO2催化剂会产生更多积炭,并将Au/TiO2催化剂与TiO2对比,发现Au-Ti3+的相互作用会导致积炭产生。在相同氢炔比条件下对比Au(Ⅰ)/SiO2(3.7 nm)和Au(Ⅱ)/SiO2(6.1 nm)催化剂,发现金纳米粒子大小不同,形成的积炭类型不同。而实验范围氢炔比对积炭的形成没有明显的影响。除此之外,积炭的形成还与催化剂形貌密切相关,将反应后的八面体PdAu催化剂与花型PdAu催化剂进行TPO表征,两种催化剂分别在270 ℃和370 ℃出现峰,意味着具有两种类型的积炭。位于370 ℃的峰主要是由无定型积炭的燃烧引起,该无定型积炭是CxHy结构的石墨前驱物[17],存在严重覆盖活性位点,降低乙炔或H2与活性位点的接触面积,进而降低催化活性。 相对于花型-PdAu/MMO催化剂,八面体-PdAu/MMO催化剂会产生更多积炭,表明催化剂形貌与积炭的形成也有密切关系。
5 结语与展望
负载型金催化剂在乙炔选择性加氢反应中具有良好的催化活性,并可以通过选择适当的载体或加入其他组分改善其性能。基于乙炔加氢反应的纳米Au催化材料的独特优势在于:(1) 拥有大量低配位金原子的小颗粒金能在室温活化氢分子,这将有望实现室温或低温条件下的乙炔选择性加氢;(2) Au纳米颗粒对乙烯具有较弱的吸附能力,在乙炔选择性加氢反应中具有较钯或镍催化剂更高的乙烯选择性。体现出负载型纳米金催化剂在乙炔选择性加氢反应中的巨大应用潜力。
相对于单金属(Pd、Au)催化剂,合金型纳米金催化剂在低温下具有优越的活性和选择性,而且制备工艺简单,比表面积大,在催化化学领域中的地位将日益提高。继续研发在低温下具有高乙炔转化率、高乙烯选择性和稳定性的合金型纳米金催化剂仍然是今后乙炔选择性加氢催化剂发展的重要方向之一;同时,降低金使用量、提高利用率和催化效率也将成为纳米金催化剂研究的重点方向。随着载体材料的不断发展和丰富,可以将载体材料功能化,将会拓展更多的新型纳米金催化材料。总之,对合金型纳米金催化剂研究的深入开展必将给催化加氢领域注入新的活力,促进相关学科的快速发展。
[1]李速延,韩新恩,王志,等.微量乙炔和乙烯加氢催化剂的研制[J].工业催化,2003,11(3):31-34.
Li Suyan,Han Xinen,Wang Zhi,et al.Development of trace acetylene and propylene hydrogenation catalysts[J].Industrial Catalysis,2003,11(3):31-34.
[2]杨春生.我国乙烯工业发展的现状和制约因素[J].中外能源,2006,11(3):12-15.
Yang Chunsheng.Developing status and restrained factors of china ethylene industry[J].Sino-Global Energy,2006,11(3):12-15.
[3] 杨春生.乙烯装置的乙炔脱除技术[J].乙烯工业,1996,8(1):27-44.
[4]邹仁鎏.石油化工裂解原理与技术[M].北京:化学工业出版社,1982.
[5]赵炳义.乙烯生产过程中乙炔的脱除[J].乙烯工业,1994,6(1):15.
[6]Bond G C,Wells P B.The hydrogenation of acetylene:Ⅱ.The reaction of acetylene with hydrogen catalyzed by alumina-supported palladium [J].Journal of Catalysis,1966,5(1):65-73.
[7]Bond G C,Wells P B.The hydrogenation of olefins[J].Advances in Catalysis, 1964,15:92-221.
[8]Sárkány A,Weiss A H,Guczi L.Structure sensitivity of acetylene-ethylene hydrogenation over Pd catalysts[J].Journal of Catalysis,1986,98(2):550-553.
[9]Sermon P A.Hydrogenation of alkenes over supported gold[J].Journal of the Chemical Society Faraday Transactions,1979,75(75):385-394.
[10]Haruta M,Kobayashi T,Sano H,et al.Novel gold catalysts for the oxidation of carbon monoxide at a temperature far below 0 ℃[J].Chemistry Letters,1987,16(2):405- 408.
[11]Mohr C,Hofmeister H,Claus P.The influence of real structure of gold catalysts in the partial hydrogenation of acrolein[J].Journal of Catalysis,2003,213(1):86-94.
[12]Okumura M,Akita T,Haruta M.Hydrogenation of 1,3-butadiene and of crotonaldehyde over highly dispersed Au catalysts[J].Catalysis Today,2002,74(3):265-269.
[13]Milone C,Ingoglia R,Pistone A,et al.Selective hydrogenation of α,β-unsaturated ketones to α,β-unsaturated alcohols on gold-supported catalysts[J].Journal of Catalysis,2004,222(2):348-356.
[14]Hashmi A S K,Hutchings G J.Gold catalysis[J].Angewandte Chemie International Edition,2006,45(47):7896-7936.
[15]仲小慧.乙炔在Cu/SiO2催化剂上选择性加氢性能研[D].大连:大连理工大学,2011.
Zhong Xiaohui.The study of acetylene selective hydrogenation activity on Cu/SiO2catalyst[D].Dalian:Dalian University of Technology,2011.
[16]Jia J,Haraki K,Kondo J N,et al.Selective hydrogenation of acetylene over Au/Al2O3catalyst[J].The Journal of Physical Chemistry B,2000,104(47):11153-11156.
[17]Azizi Y,Petit C,Pitchon V.Formation of polymer-grade ethylene by selective hydrogenation of acetylene over Au/CeO2catalyst[J].Journal of Catalysis,2008,256(2):338- 344.
[18]Sárkány A.Acetylene hydrogenation on SiO2supported gold nanoparticles[J].Reaction Kinetics and Catalysis Letters,2009,96(1):43-54.
[19]Gluhoi A C,Bakker J W,Nieuwenhuys B E.Gold,still a surprising catalyst:selective hydrogenation of acetylene to ethylene over Au nanoparticles[J].Catalysis Today,2010,154(1):13-20.
[20]Bernal S,Calving J J,Cifredo G A,et al.Reversibility of hydrogen chemisorption on a ceria-supported rhodium catalyst[J].Journal of Catalysis,1992,137(1):1-11.
[21]Bernal S,Calvino J J,Cifredo G A,et al.Hydrogen chemisorption on ceria:influence of the oxide surface area and degree of reduction[J].Journal of the Chemical Society Faraday Transactions,1993,89(18):3499-3505.
[22]Yolanda Segura,Nuria Lopez,Javier Perez-Ramirez.Origin of the superior hydrogenation selectivity of gold nanopartieles in alkyne+alkene mixtures:triple-versus double-bond activation[J].Journal of Catalysis,2007,247(2):383-386.
[23]Liu X,Mou C Y,Lee S,et al.Room temperature O2plasma treatment of SiO2supported Au catalysts for selective hydrogenation of acetylene in the presence of large excess of ethylene[J].Journal of Catalysis,2012,285(1):152-159.
[24]Yan X,Wheeler J,Jang B,et al.Stable Au catalysts for selective hydrogenation of acetylene in ethylene[J].Applied Catalysis A:General,2014,487:36-44.
[25]Hashmi A S K,Hutchings G J.Gold catalysis[J].Angewandte Chemie International Edition,2006,45(118):7896-7936.
[26]Choudhary T V,Sivadinarayana C,Datye A K,et al.Acetylene hydrogenation on Au-based catalysts[J].Catalysis Letters,2003,86(1/3):1-8.
[27]Sarkany A,Horvath A,Beck A.Hydrogenation of acetylene over low loaded Pd and Pd-Au/SiO2catalysts[J].Applied Catalysis A:General,2002,229(1):117-125.
[28]Zhang Y,Diao W,Williams C T,et al.Selective hydrogenation of acetylene in excess ethylene using Ag-and Au-Pd/SiO2bimetallic catalysts prepared by electroless deposition[J].Applied Catalysis A:General,2014,469:419-426.
[29]Ma C,Du Y,Feng J,et al.Fabrication of supported PdAu nanoflower catalyst for partial hydrogenation of acetylene[J].Journal of Catalysis,2014,317:263-271.
[30]Sarkany A,Geszti O,Safran G.Preparation of Pdshell-Aucore/SiO2catalyst and catalytic activity for acetylene hydrogenation[J].Applied Catalysis A:General,2008,350(2):157-163.
[31]Zhang S,Chen C Y,Jang B W L,et al.Radio-frequency H2plasma treatment of AuPd/TiO2catalyst for selective hydrogenation of acetylene in excess ethylene[J].Catalysis Today,2015,256:161-169.
[32]Yang B,Burch R,Hardacre C,et al.Origin of the increase of activity and selectivity of nickel doped by Au,Ag,and Cu for acetylene hydrogenation[J].ACS Catalysis,2012,2(6):1027-1032.
[33]Nikolaev S A,Pichugina D A,Mukhamedzyanova D F.Sites for the selective hydrogenation of ethyne to ethene on supported NiO/Au catalysts[J].Gold Bulletin,2012,45(4):221-231.
[34]Liu X,Li Y,Lee J W,et al.Selective hydrogenation of acetylene in excess ethylene over SiO2supported Au-Ag bimetallic catalyst[J].Applied Catalysis A:General,2012,439:8-14.
[35]Jang B,Helleson M,Shi C,et al.Characterization of Al2O3supported nickel catalysts derived from RF non-thermal plasma technology[J].Topics in Catalysis,2008,49(3):145-152.
[36]Maetz P,Touroude R.Modification of surface reactivity by adsorbed species on supported palladium and platinum catalysts during the selective hydrogenation of but-1-yne[J].Applied Catalysis A:General,1997,149(1):189-206.
[37]Guimon C,Auroux A,Romero E,et al.Acetylene hydrogenation over Ni-Si-Al mixed oxides prepared by sol-gel technique[J].Applied Catalysis A:General,2003,251(1):199-214.
Progress in supported nanogold catalyst for selective hydrogenation of acetylene
LiFeifei1,SunXun1,SunLibo1,ZhengYuhua1,HanChun1,YangXin2*,QiCaixia1*
(1.Shandong Applied Research Center of Gold Nanotechnology,School of Chemistry and Chemical Engineering,Yantai University,Yantai 264005,Shandong,China; 2.School of Chemistry and Chemical Engineering,Yantai University,Yantai 264005,Shandong,China)
The advance in research and development of the catalysts for selective hydrogenation of acetylene to ethylene was introduced.Since the supported nanogold catalysts were extensively used in many hydrogenation processes,more particular attention was paid to compare with catalytic performance of monometallic catalyst and nanoalloy Au catalyst in the selective hydrogenation of acetylene,such as nanoalloy Au catalyst had higher acetylene conversion and stability.The main factors affecting the catalytic properties were the size of the nanoparticles and the synergistic effect of the active components.The formation of carbon deposition and the deactivation principle of the catalysts were presented.It is pointed out that the future improvement of nanoalloy Au catalyst for acetylene selective hydrogenation should aimed at high conversion,relative higher selectivity and good adaptability.
catalyst engineering;supported nanogold catalyst;acetylene selective hydrogenation;acetylene;ethylene
TQ426.94;O643.36 Document code: A Article ID: 1008-1143(2016)10-0021-07
2016-06-08;
2016-08-07
李菲菲,1990年生,女,在读硕士研究生,研究方向为负载型纳米金催化剂在乙炔选择性加氢反应中的应用。
杨 昕,男,副教授,硕士研究生导师;祁彩霞,女,教授,硕士研究生导师。
10.3969/j.issn.1008-1143.2016.10.004
TQ426.94;O643.36
A
1008-1143(2016)10-0021-07
doi:10.3969/j.issn.1008-1143.2016.10.004

