液相色谱—串联质谱法测定羊肉中伊维菌素残留
文豪+周绪正+李冰+魏小娟+张继瑜

摘要:为建立以液相色谱-串联质谱检测羊肉中伊维菌素的残留方法,所采用的主要仪器参数为:安捷伦1200-6410液质联用仪,ESI电离源,干燥气温度250 ℃;安捷伦ZORBAX Eclipse Plus C8柱;流动相为乙腈-含0.1%甲酸的 10 mmol/L 乙酸铵水溶液(体积比为90 ∶10),流速0.2 mL/min。样品使用乙腈提取,使用碱性氧化铝固相萃取小柱净化,在10、20、40 μg/kg的添加水平下,羊肌肉组织中伊维菌素的添加回收率为87%、87%、89%,变异系数为4.01%、3.48%、1.14%,方法的定量限为0.5 μg/kg,该方法可用于检测羊肌肉组织中的伊维菌素的药物残留。
关键词:羊肉;伊维菌素;液相色谱-串联质谱;残留
中图分类号: S852.6 文献标志码: A
文章编号:1002-1302(2016)09-0290-03
阿维菌素类(AVMs)药物是由阿维链霉菌产生的一组高效、广谱、安全的大环内酯类抗寄生虫药,国内外广泛应用于包括猪、牛、羊等家畜在内的食品动物中,其中使用最广泛的是伊维菌素[1]。伊维菌素是一种具有神经毒性的化合物,其脂溶性较强,在动物组织中残留时间较长。当伊维菌素残留过量时,可能会给食品安全带来隐患。欧盟、美国和中国等都设定了最高残留限量(MRLs),欧盟伊维菌素的最高限量标准是15 μg/kg,美国和中国是20 μg/kg[2-5]。羊肉营养价值高,纤维细嫩,其所含的主要氨基酸的种类和数量能完全满足人体的需要[6]。因此,随着社会经济的发展,人们出于饮食营养和健康的考虑,肉食类食品结构也逐渐从快速生产的鸡肉、猪肉转向味美、质优、安全、保健的羊肉,根据国家肉羊产业技术研发中心调查,我国已是羊肉生产和消费大国,羊肉生产已成为我国畜牧业发展的支柱产业[7]。目前,国内针对伊维菌素的检测方法主要是参照国标GB/T 21320—2007《动物源食品中阿维菌素类药物残留量的测定》和SN/T 1973—2007《进出口食品中阿维菌素残留量的检测方法》,并没有专门针对羊组织中伊维菌素残留检测的国家标准,所以对羊组织中伊维菌素残留的检测方法进行研究很有必要。本研究应用液相色谱-串联质谱法(HPLC-MS/MS),成功建立了羊肉与羊肝组织中伊维菌素残留的检测方法。
1 材料与方法
1.1 仪器与试剂
安捷伦1200-6410液质联用仪,美国Agilent公司生产;高速匀浆机,江苏省金坛市荣华仪器公司生产;KL512型氮吹仪,北京康林科技有限责任公司生产;湘仪离心机,湘仪公司生产;涡旋振荡器(Heros BIO,RS-2 Shaker);针筒式微孔滤膜过滤器(0.22 μm、有机系),天津津腾试验设备有限公司生产;乙腈、甲酸和乙酸铵均为色谱纯,美国Fisher公司生产;无水硫酸钠为分析纯(650 ℃灼烧4 h生产);试验用水为屈臣氏纯净水;固相萃取SPE柱为碱性氧化铝小柱,美国Sepax公司生产;99.5%伊维菌素标准品,中国食品药品检定研究院提供生产;96.0%内标物多拉菌素(德国Dr Ehrenstorfer GmbH)。
1.2 方法
1.2.1 标准溶液的配制
1.2.1.1 标准储备液的制备 分别准确称取10 mg伊维菌素和多拉菌素标准品用乙腈溶解并稀释,分别配制成100 μg/mL 的标准储备液,置于-20 ℃冰箱中避光保存。
1.2.1.2 标准中间溶液的制备 分别准确吸取1 mL伊维菌素和多拉菌素的标准储备液至100 mL容量瓶中,用乙腈稀释至刻度混匀即得1 μg/mL的混合标准中间溶液,于4 ℃贮藏备用。
1.2.1.3 系列标准工作溶液的制备 用乙腈溶液逐级稀释上述伊维菌素混合标准中间液,配制成浓度不等的系列标准工作溶液,现用现配。
1.2.1.4 基质匹配标准溶液的制备 分别准确量取系列标准工作溶液,依次加入到空白羊肉经提取、净化及浓缩后的样品中,涡旋30 s,制得基质匹配的系列标准溶液。
1.2.2 LC-MS/MS条件
1.2.2.1 质谱条件 电喷雾离子源(ESI),正离子模式,动态多反应监测(dynamic MRM)方式采集,毛细管电压4 kV,碰撞气(N2)流速10 L/min,雾化器压力206.85 kPa,去溶剂气温度200 ℃。伊维菌素与多拉菌素的质谱参数见表1,质谱结果见图1。
1.2.2.2 色谱条件 分析柱为安捷伦ZORBAX Eclipse PlusC8柱;流动相A为乙腈,流动相B为含0.1%甲酸的10 mmol/L 乙酸铵水溶液;流速0.2 mL/min,柱温25 ℃;进样量5 μL。
1.2.3 样品的前处理
1.2.3.1 提取 称取剪碎混匀的新鲜组织2.0 g,置于50 mL 离心管中,加8 mL乙腈,高速匀浆1 min,涡旋振荡2 min,超声5 min,4 000 r/min离心10 min,取上清液至50 mL 离心管。另取1支50 mL离心管加入8 mL乙腈,洗涤匀质刀头10 s,洗涤液移入前1支离心管中,用玻璃棒捣碎残渣,涡旋振荡2 min,超声5 min,4 000 r/min离心10 min,合并上清液,待净化。
1.2.3.2 净化 在碱性氧化铝小柱上平铺2 g无水硫酸钠,使用10 mL乙腈活化,取上述提取液过碱性氧化铝小柱,控制流速1.0~2 mL/min,之后用3 mL乙腈淋洗,收集全部流出液,于50 ℃水浴氮吹至干,用1.0 mL流动相溶解残渣,加入50 μL 1 μg/mL多拉菌素内标液,过0.22 μm有机微孔滤膜后,供HPLC-MS/MS测定。
2 结果与分析
2.1 特异性
从图2可以看出,按以上方法处理羊肌肉空白样品,空白样品在多拉菌素和伊维菌素出峰处无干扰,方法选择性好。
2.2 基质匹配标准曲线的绘制
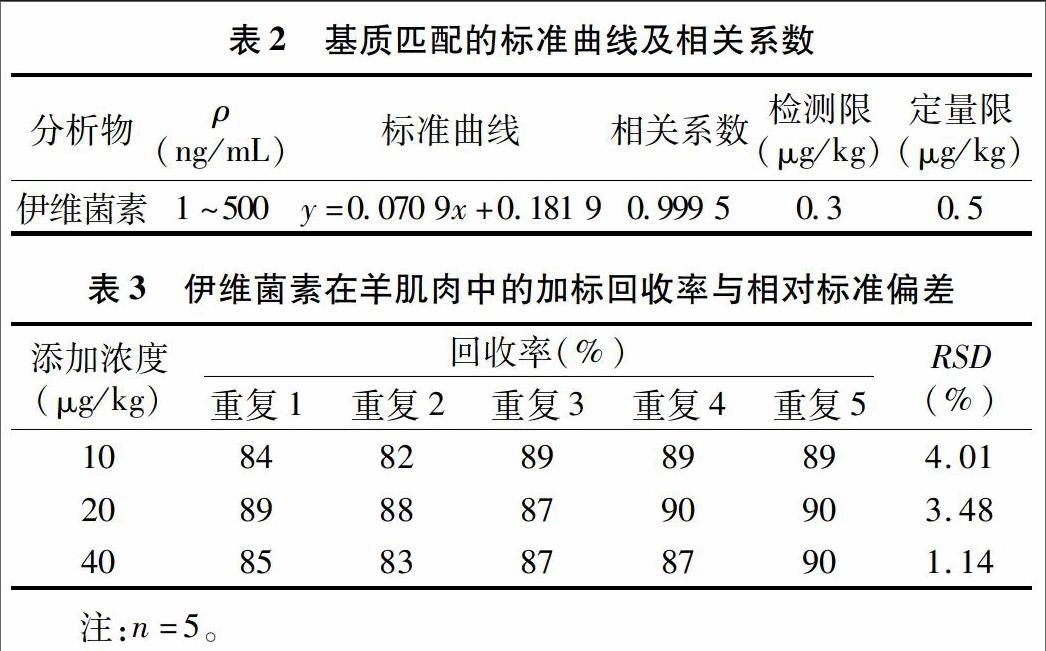
参照国标GB/T 21320—2007《动物源食品中阿维菌素药物残留量的测定》,为补偿基质效应,本试验用空白样品提取液配制标准。吸取标准贮备液,用空白样品提取液稀释成1、5、20、40、80、250、500 ng/mL基质匹配标准溶液,按以上所述仪器条件进行测定。以基质标准溶液浓度(e)为横坐标,伊维菌素特征子离子m/z为307的色谱峰面积与多拉菌素特征子离子m/z为593.3的色谱峰面积的比(I)为纵坐标,用最小二乘法进行线性回归得到标准曲线(表2)。
2.3 添加回收率试验
选取不含伊维菌素本底的羊肉组织样品,进行不同浓度的伊维菌素加标回收试验,添加水平为10、20、40 μg/kg等3个浓度,按以上条件进行分析,得到添加回收率(表3)。
2.4 方法检出限
计算空白组织样品的噪音与对应保留值处的峰面积的比值,以10倍信噪比(S/N>10)所对应的待测物浓度为最低定量限,确定本方法定量限为0.5 μg/kg。以3倍信噪比(S/N>3) 所对应的待测物浓度为检出限,确定本方法检出限为0.3 μg/kg。
3 结论与讨论
3.1 质谱条件的选择
由于质谱检测时较灵敏,各种因素对检测结果影响较大,本试验选用多拉菌素作为内标物,提高检测的准确性。本试验在ESI源正模式下对伊维菌素与多拉菌素标准溶液(1 mg/L)进行全扫描,得到伊维菌素与多拉菌素的[M+NH4]+母离子峰,在流动相中加入甲酸以增强待测物的离子化,加入乙酸铵用来促进[M+NH4]+峰的形成。以该分子离子峰对离子源参数进行优化,使仪器灵敏度达到最高。再对该离子进行二级质谱全扫描,选取二级质谱中没有干扰、信号相对较强的2个特征碎片离子,与其母离子组成2对离子对,对该药物进行定性和定量分析。ESI离子源为软电离方式,伊维菌素在ESI离子源内通常与H+、Na+、NH+4等结合而形成准分子离子峰,其中,[M+Na]+离子结构稳定,若对其进行二级质谱裂解,不易得到碎片离子,且H+、NH+4等可竞相与目标分子结合,从而引起[M+Na]+离子丰度极不稳定[8]。本试验结果显示,离子源去溶剂气体温度对阿维菌素类药物的离子加合物形态有较大的影响。当去溶剂气温度低于250 ℃ 时,离子加合物主要以[M+NH4]+形式存在;当去溶剂气温度高于250 ℃时,[M+Na]+峰的比例迅速升高,当达到350 ℃时,伊维菌素基本以[M+Na]+峰的形式存在。
3.2 色谱条件的选择与优化
由于伊维菌素是一种相对分子质量较高的弱极性化合物,所以选用反相高效液相色谱进行分离较合适[9]。本试验对C8色谱柱进行观察,结果表明,伊维菌素在C8柱上保留相对较强,能完全与杂质分离。由于干燥气温较低,流速越小,其气化越好,所以选定0.2 mL/min为理想流速。在流动相中加入10 mmol/L乙酸铵可有效促进[M+NH4]+母离子的形成,同时在流动相中加入0.1%甲酸可有效增强待测物的离子化,最终选择乙腈 ∶缓冲液(0.1%乙酸+10 mmol/L乙酸铵)=90 ∶10为流动相。
3.3 提取条件与净化条件的选择
伊维菌素是一种脂溶性化合物,参考国内外相关文献资以及GB/T21320—2007《动物源食品中阿维菌素类药物残留量的测定》和SN/T 1973—2007《进出口食品中阿维菌素残留量的检测方法》,伊维菌素的提取选用乙腈作为提取溶剂,亦是如此。乙腈本身对样品中的糖、脂肪和蛋白质的溶解性较小,对蛋白质又有沉淀作用,且乙腈与水可以任意比例混溶,很容易渗透到组织内部,提取效率高,所以试验选用乙腈作为提取溶剂[10]。实验室较常用的净化方法有液-液萃取法和固相萃取法。碱性氧化铝柱对脂肪以及组织内的内源性因子的去除效果很好,操作简便,而且回收率也高,既保证了试验的准确性,又缩短了分析时间,可以满足方法要求,因此,本试验确定用碱性氧化铝柱净化。
本试验建立了一种超高效液相色谱-质谱法检测羊肉组织中伊维菌素残留量的方法。该法专属性强,灵敏度高,简便准确,准确度、精密度均达到了兽药残留检测的要求,所以适用于羊肉组织中伊维菌素的测定。
参考文献:
[1]武志雄,胡江涛,郑卫东,等. 猪肉组织中阿维菌素、伊维菌素残留的高效液相色谱-串联质谱法研究[J]. 四川大学学报:医学版,2010,41(3):523-526.
[2]农业部畜牧兽医局. 农业部发布动物性食品中兽药最高残留限量(续)[J]. 中国兽药杂志,2003,37(4):5-11.
[3]中华人民共和国农业部公告第235号[EB/OL]. [2015-06-30]. http://wenku.baidu.com/link?url=NINFLVw8X2Gqga G5z8jFdXLIXFKlZyGLnjTVE__b31BNib204a6P3 VMGNRH_sz47Qef_uf2GFIArBUhU8aWy-PvSRhregGr_DfCFJbKapz7
[4]European Medicines Agency,Committee for Veterinary Medicinal Products.EMEA/CVMP/915/04-FINAL,ivermectin summary report(5)[EB/OL]. [2015-06-30]. http://www.ema.europa.eu/docs/en_GB/document_library/Maximum_Residue_Limits_-_Report/2009/11/WC500014505.pdf
[5]U.S. food and drug administration.21CFR556.344[EB/OL]. [2015-06-30]. http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?fr=556.344.
[6]康永锋,邹世文,段吴平,等. 超声波-微波辅助提取-高效液相色谱法同时检测羊肉组织中4种非甾体抗炎药物残留[J]. 色谱,2010,28(11):1056-1060.
[7]邹世文. HPLC同时检测多种非甾体抗炎药残留的研究[D]. 上海:上海海洋大学,2011.
[8]赵肖华,曹赵云,牟仁祥,等. 液相色谱-串联质谱法测定蔬菜、水果中5种阿维菌素类药物残留量[J]. 分析测试学报,2012,31(10):1266-1271.
[9]郑卫东,胡江涛,阴文娅,等. 高效液相色谱-串联质谱测定猪肝中阿维菌素、伊维菌素残留[J]. 食品科学,2011,32(4):185-188.
[10]王祖翔,余 杨,孙 莉,等. 离子色谱法测定食品中的无机铵[J]. 食品与机械,2012,28(4):96-99.

