老龙皮多糖分离纯化及糖组成研究
张 红,孙婷婷,王海峰,刘建峰
(1.陕西省中医药研究院,陕西西安710003;2.武警工程大学医院,陕西西安710086)
老龙皮多糖分离纯化及糖组成研究
张红1,孙婷婷1,王海峰2,刘建峰1
(1.陕西省中医药研究院,陕西西安710003;2.武警工程大学医院,陕西西安710086)
目的分离纯化老龙皮多糖,并对其糖组成进行测定。方法采用冷水浸提、75%乙醇沉淀、离子交换和凝胶过滤等方法分离纯化老龙皮多糖,采用PMP衍生法及高效液相色谱法测定其糖组成。结果对老龙皮多糖进行了系统分离,得到5个组分,即LKY1,LKY2,LKY3,LKY4,LKY5,并对含量较高的LKY1和LKY2进行进一步分离和糖组成测定。结论初步分离纯化得到5种均一性多糖,并确定其中两种的糖组成,为老龙皮多糖的结构研究提供了一定的研究基础。
老龙皮;多糖;糖组成
老龙皮为子囊地衣类Ascolichenes茶渍目Lecanorales牛皮叶科Stictaceae肺衣属Lobaria Hoffm植物光肺衣Lobaria kurokauae Yoshim.、裂芽肺衣Lobariaisidiosa Vaim.和网肺衣Lobaria retigera Trev.的干燥叶状地衣体,主要生长于岩石表面、树干基部及树皮上,分布于秦岭北坡等地,是陕西部分地区民间常用中药材,具有利水健脾、祛风止痒的功效,临床主要用于治疗小儿疳积、腹胀等,以及水肿、烫伤、无名肿毒、皮肤瘙痒等[1-9]。多糖类化合物是维持生物体正常生理功能所必须的能量来源,同时也是参与生物体中的各类细胞生物活动的活性物质。因此,多糖类药物的活性与结构研究受到越来越多研究者的关注。老龙皮中含有大量多糖[10],但有关研究报道较少,本课题旨在通过对老龙皮多糖的提取分离纯化及糖组成研究,为老龙皮的开发利用作前期的基础研究工作。
1 仪器与试药
1.1仪器
高速组织捣碎机(上海标准模型厂);T-214型精密电子天平(北京赛多利斯仪器有限公司);Waters 2695型高效液相色谱仪(美国Waters公司);超低温冷冻干燥器(丹麦);Sorvall RC5C plus型高速低温冷冻离心机(美国Sorvall公司)。
1.2试药
老龙皮采自陕西省宝鸡市红河谷地区。经陕西省中医研究院中药鉴定室杨智峰教授鉴定为肺衣属Lobaria Hoffm植物光肺衣Lobaria kurokauae Yoshim.的干燥叶状地衣体。葡萄糖(批号20140630)、葡萄糖醛酸(批号140648-201403)、甘露糖(批号140651-201403)、阿拉伯糖(批号111506-200001)、半乳糖醛酸(批号111646-200301)、鼠李糖(批号111683-20041)、木糖(批号111508-200404)、半乳糖(批号100226-201105)对照品,均购自中国食品药品检定研究院; PMP(sigma公司,批号101337108);Sephadex G-100 (Pharmacia进口分装产品)。磷酸二氢钠、过氧化氢、冰醋酸、苯酚、硫酸钠、正丁醇、氯化钠、浓硫酸、无水乙醇、氢氧化钠等均为分析纯。
2 方法与结果
2.1老龙皮粗多糖(LKY)的提取[11-12]
将400 g老龙皮于烘箱中50℃烘干,粉碎,加冷水浸提2次,每次12 h,提取液过100目纱布,高速离心机离心,过滤,滤液减压浓缩,加入95%乙醇,使含醇量达75%,静置过夜,过滤,取沉淀反复用75%乙醇清洗2~3遍,蒸馏水溶解,采用Sevage法脱蛋白(THMS∶nbutanol=4∶1),置振荡器上震荡20 min,离心,取上清液,再加入Sevage试剂适量,重复操作7~8次,至蛋白完全去除后将样品装入透析袋,对水透析2~3 d,取出,冷冻干燥,得到LKY。
2.2老龙皮多糖的分离纯化
2.2.1离子交换柱层析
称取LKY样品1 g,置试管中,加蒸馏水10 mL溶解,离心,取上清液过离子交换层析柱(填料为DEAE-52,50 cm×6 cm),依次用水和0.05,0.1,0.25,0.5 mol/L NaHCO3溶液洗脱,分部收集流出液。待洗脱完全后,用苯酚-硫酸法在490 nm波长处隔管检测吸光度值,以吸光度值绘制多糖和蛋白的洗脱曲线,并根据洗脱曲线合并各组分,对水透析,减压浓缩,冷干,备用。
2.2.2凝胶过滤柱层析
取上述样品100 mg加蒸馏水2 mL溶解,过G-100凝胶过滤色谱柱进一步分离,以蒸馏水洗脱。
2.2.3分离纯化
取400 g老龙皮药材,粉碎后采用冷水浸提法提取2次,合并提取液,减压浓缩至400 mL,加95%乙醇,使含醇量达75%,静置过夜,过滤。所得沉淀反复用75%乙醇清洗2~3遍,再将沉淀加水100 mL,复溶,Sevage法脱蛋白7~8次,再对流水透析2 d后,取出,冻干,得到黄棕色水提LKY。经采用DEAE-52阴离子交换树脂柱进行分离后得到5个组分:LKY1,LKY2,LKY3,LKY4,LKY5。再取含量较高的LKY1和LKY2,加蒸馏水制成50 g/L的溶液。采用Sephadex G-100凝胶过滤柱(80cm×1.2cm),流动相为蒸馏水,流速为0.6mL/min,每管4 mL,得到LKY1-A和LKY2-A。洗脱曲线图见图1。
2.3单糖组成测定[13]
2.3.1溶液制备
对照品溶液:精密称取阿拉伯糖2.12 mg,甘露糖2.14 mg,半乳糖醛酸2.27 mg,葡萄糖醛酸1.93 mg,半乳糖1.8 mg,木糖1.87 mg,鼠李糖1.85 mg,葡萄糖1.88 mg,分别置5 mL容量瓶中,用蒸馏水配成2 mmol/L的水溶液,制成单糖对照溶液;将单糖对照品各取800 μL,加入0.5 mol/L PMP甲醇溶液800 μL及0.3 mol/L NaOH 800 μL,在QT-2旋涡混合器上震荡10 min;70℃水浴中反应40 min,冷却至室温,加入0.3 mol/L HCl 800 μL进行中和,并加入去离子水1 600 μL稀释混匀。用1 mL氯仿萃取3次,静置分层后吸取上层衍生溶液,用0.45 μm微孔滤膜过滤,备用。
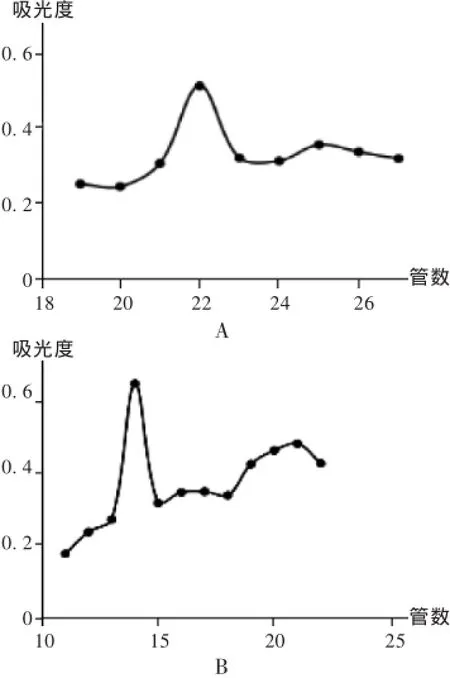
图1 LKY1和LKY2经Sephadex G-100凝胶过滤柱层析的洗脱曲线图
供试品溶液:取样品2 mg,加入1 mL 2 mol/L三氟乙酸在121℃水解2 h,蒸干,加入5 mL氨水溶解。取200 μL与200 μL PMP/甲醇溶液混合,加入200 μL 0.3 mol/L NaOH在QT-2型旋涡混合器上振匀,于70℃水浴锅中加热反应40 min,冷却至室温,再加入200 μL 0.3 mol/L HCl进行中和,加去离子水400 μL,稀释混匀,再用1 mL氯仿萃取3次,静置分层后吸取上层衍生溶液,用0.45 μm微孔滤膜过滤,备用。
2.3.2色谱条件
色谱柱:Diamonsil C18柱(250 mm×4.6 mm,5 μm);流动相:15%乙腈(A)+0.05 mol/L磷酸缓冲液(pH= 6.9,B)-40%乙腈+0.05 mol/L磷酸缓冲液(pH= 6.9),梯度洗脱,见表1;流速:1 mL/min;柱温:25℃。

表1 梯度洗脱条件
2.3.3测定结果
测定结果表明,LKY1-A由甘露糖、半乳糖、阿拉伯糖、半乳糖醛酸组成,相对摩尔比为6∶25∶18∶1; LKY2-A由甘露糖、半乳糖、阿拉伯糖、半乳糖醛酸组成,相对摩尔比为3∶15∶8∶1。色谱图见图2。

图2 高效液相色谱图
3 讨论
老龙皮中含有大量的蛋白质,蛋白质的存在会干扰糖结构检测结果,因此须将蛋白质去除。Sevage法[14]脱蛋白是采用氯仿、正丁醇等有机溶剂使蛋白转变为变性蛋白,进而分离多糖,操作简便,不破坏多糖结构。多糖粗提取多采用冷水浸提、热水提取、加酸提取、加碱提取等方法,采用冷水浸提不会对多糖结构造成破坏,因此本试验采用热水浸提法提取LKY。
离子交换技术是分离多糖的常用技术,可以有效除去多糖中的蛋白质和色素等,并对多糖进行初步分级,本试验中采用DEAE-52对老龙皮多糖进行初分,得到5个组分:LKY1,LKY2,LKY3,LKY4,LKY5。凝胶过滤技术是分离大分子化合物的常用方法,本试验中采用葡聚糖凝胶G-100层析柱对组分LKY1和LKY2进行细分离,分离效果良好,得到两种均一性多糖LKY1-A和LKY2-A。
PMP作为一种重要的衍生化学试剂,可以在温和条件下(70℃,反应30 min)与糖链的还原端发生反应,并且不会导致糖链脱唾液酸化,且产物无立体异构体,并在245 nm波长处有最强紫外吸收。糖链经PMP衍生后,极性减弱,可用高效液相色谱法检测[15],因此采用这种方法测定单糖组成。
综上,对老龙皮多糖进行了系统分离,得到5个组分:LKY1,LKY2,LKY3,LKY4,LKY5,并对含量较高的LKY1和LKY2进行进一步分离,确定其糖组成为:LKY1-A由甘露糖、半乳糖、阿拉伯糖、半乳糖醛酸组成,相对摩尔比为6∶25∶18∶1;LKY2-A由甘露糖、半乳糖、阿拉伯糖、半乳糖醛酸组成,相对摩尔比为3∶15∶8∶1。
[1]李世全.秦岭巴山药物志[M].西安:陕西科学技术出版社,1987:777.
[2]中国药科大学.中药辞海(第一卷)[M].北京:中国医药科技出版社,1993:1 899.
[3]杜远东.老龙皮的药效物质及质量标准研究[D].西安:陕西中医学院,2012.
[4]王晓梅,李健,李宗孝,等.老龙皮提取物的体外抗氧化活性研究[J].现代中医药,2010,30(5):79-80.
[5]尹娜,张琪,牛庆慧,等.中药复方逆转胃癌前病变的临床研究[J].齐鲁医学杂志,2011,26(4):314-315.
[6]王启林,房敏峰,胡正海.太白山药用地衣的种质资源及其化学成分的研究概况[J].中国野生植物资源,2011,30(4):1-6.
[7]史雪.《中华本草》收载具有利水功效药物的药性规律研究[D].青岛:山东中医药大学,2013.
[8]李志东,王慧,张海娟,等.老龙七水提液对兔离体肠平滑肌收缩的影响[J].中国药房,2015,26(4):463-466.
[9]贾萍.指纹图谱与中药质量控制[J].中国药业,2004,13(2):79-80.
[10]靳菊情,丁东宁,边晓丽,等.老龙皮多糖的研究[J].中药材,1997,20(7):355-357.
[11]庹康秀,廖共山,胡仁统,等.可口革囊星虫多糖的提取及含量测定[J].中国药业,2013,22(4):18-19.
[12]张捷,黄荣花,张书华.标准曲线法测定茯神中多糖的含量[J].中国药业,2013,22(16):15-16.
[13]方金红.多糖化学修饰方法的研究进展[J].中国药业,2014,23(19):4-8.
[14]Bradford MM.A rapid,and sensitive method for the quantification of protein using the principle of protein-dye binding[J].Analytical Biochemistry,1976(72):48-54.
[15]李薇,夏晴,孙成荣,等.柱前衍生(PMP)-HPLC法测定不同品种甘草多糖中单糖组成[J].辽宁中医药大学学报,2014,16(1):56-58.
Isolation and Structural Characterization of Polysaccharides from Lobaria Kurokauae Yoshim.
Zhang Hong1,Sun Tingting1,Wang Haifeng2,Liu Jianfeng1
(1.Shaanxi Academy of Traditional Chinese Medicine,Xi'an,Shaanxi,China 710003;2.Engineering University of CAPF,Xi'an,Shaanxi,China710086)
ObjectiveTostudytheisolation,purification,monosaccharidecharacterizationofpolysaccharideobtainedfromLobaria kurokauae Yoshim.MethodsThe polysaccharides was extracted from the Lobaria kurokauae Yoshim.with cold water,75%ethanol precipitation and then purified by DEAE-cellulose ion exchange chromatography and Sephadex G-100 gel filtration chromatography;its monosaccharide composition was detected by PMP-derivative method combined with HPLC.ResultsThe crude polysaccharide(LKY)obtained from Lobaria kurokauae Yoshim.was fractionated into 5 sub-fractions by DEAE-cellulose ion exchange chromatography,designated as:LKY1,LKY2,LKY3,LKY4,LKY5.The polysaccharides,termed LKY1-A and LKY2-A was extracted respectively from LKY1 and LKY2 by Sephadex G-100 gel filtration chromatography.Conclusion5 kinds of polysaccharides are obtained by the preliminary isolation and purification,and the monosaccharide of two of them is confirmed,which provides a foundation for the further structural study of Lobaria kurokauae Yoshim.
Lobaria kurokauae Yoshim.;polysaccharides;monosaccharide composition
TQ461;R284.1;R282.71
A
1006-4931(2016)13-0040-04
张红,博士研究生,副主任药师,研究方向为中药质量标准,(电子信箱)zhanghong919919@ 163.com;刘建峰,大学本科,研究员,研究方向为中药质量标准,本文通讯作者,(电子信箱)13032910828@ 126.com。
2016-02-10;
2016-03-16)

