PFNA-Ⅱ治疗不稳定型股骨转子间骨折的动态有限元研究
姜自伟,虎群盛,黄枫,郑晓辉,赵京涛,周琦石
(广州中医药大学第一附属医院,广州510405)
PFNA-Ⅱ治疗不稳定型股骨转子间骨折的动态有限元研究
姜自伟,虎群盛,黄枫,郑晓辉,赵京涛,周琦石
(广州中医药大学第一附属医院,广州510405)
目的采用有限元方法动态分析亚洲型股骨近端防旋髓内钉(PFNA-Ⅱ)治疗不稳定型股骨转子间骨折后不同阶段的生物力学性能,为临床上合理使用PFNA-Ⅱ提供理论依据。方法 建立PFNA-Ⅱ固定Evans-Jensen Ⅳ型股骨转子间骨折模型,通过调整骨折端的接触关系和去除PFNA-Ⅱ模拟骨折愈合和取出内固定后的情况,利用有限元计算各模型的应力峰值和生物力学稳定性,并与正常股骨模型进行比较。 结果PFNA-Ⅱ固定Evans-Jensen Ⅳ型股骨转子间骨折后的应力集中位于螺旋刀片与主钉的交界部位,骨折愈合后内固定应力峰值上升。取出内固定后股骨颈区域的应力明显上升,骨骼稳定性下降。结论 在股骨转子间骨折愈合后为避免内固定断裂应去除PFNA-Ⅱ,但需要注意防范股骨颈骨折的风险。
股骨转子间骨折;内固定;股骨近端防旋髓内钉;有限元分析
股骨转子间骨折是临床常见骨折,以股骨近端防旋髓内钉(PFNA-Ⅱ)为代表的髓内钉是目前治疗不稳定型股骨转子间骨折的常用方法。在骨折愈合后,大多数的老年患者无需常规取出内固定,但是由于钉尾末端的激惹疼痛、金属过敏等原因,部分患者需要进行内固定取出手术,从而存在股骨颈骨折的风险[1]。2016年1~4月,本研究通过建立PFNA-Ⅱ治疗Evans-Jensen Ⅳ型股骨转子间骨折模型,应用有限元分析的方法了解不稳定型股骨转子间骨折的不同治疗阶段的生物力学变化,为临床治疗提供理论依据。
1 材料与方法
1.1材料 选择1例40岁成人健康男性志愿者,经过X线检查排除股骨病变情况。使用64 排螺旋CT扫描,扫描条件:电压120 kV,扫描电流250 mA,扫描速度0. 875 s /r; 层厚为0. 5 mm,以DICOMG格式保存。所用软件:Mimics 13.0 (Materialise Company,Belgium),Geomagic studio 10. 0(Raindrop Company,USA),Solid work 2010(Dassault Systemes Company,France),Abaqus 6.12.1 ( SIMULIA Company,USA) 。本研究中的内固定及股骨均假设为均质、连续、各向同性的线弹性材料,材料属性赋值参考相关文献[2,3]。
1.2建模方法将DICOMG 格式的CT 数据导入图像处理Mimics 13.0软件,通过阈值分析、像素修补、光滑处理,得到包含骨皮质、骨松质在内的股骨中上段三维模型,输出为STL文件,再导入Geomagic studio 10.0中进行光滑处理网格划分和拟合曲面,以Iges文件输出并导入到Solid work 2010软件中模拟Evans-Jensen Ⅳ型骨折进行截骨。在Solid works 2010 软件中根据辛迪斯公司所提供的PFNA-Ⅱ髓内钉数据尺寸三维虚拟重建出PFNA-Ⅱ三维数字模型,PFNA-Ⅱ螺旋刀片进行仿真重建,忽略远端锁定螺钉的螺纹细节,以圆柱体代替螺纹部分。将股骨模型与PFNA-Ⅱ模型导入Solid works 2010,通过Solid works 2010软件的切割实体、组合、装配操作以及有限元分析软件Abaqus 6.12.1中的装配、接触面关系设置来建立PFNA-Ⅱ治疗Ⅳ型股骨转子间骨折后不同阶段的模型,分别为骨折固定模型、骨折愈合模型、取出PFNA-Ⅱ模型、正常股骨模型。
1.3 边界条件及加载骨折固定模型A的骨折面为完全断裂并接触的关系,参照文献[4]设定骨折端的摩擦系数为0.46;髓内钉主钉、远端锁定螺钉与股骨的接触为绑定;螺旋刀片与骨折近端的关系为绑定;螺旋刀片与骨折远端的摩擦系数为0.3,螺旋刀片与主钉之间的摩擦系数为0.23,滑移形式是有限滑移。骨折愈合模型中,设定PFNA-Ⅱ所有零件与骨骼之间的关系以及螺旋刀片与主钉之间的关系为绑定。骨折愈合模型和取出PFNA-Ⅱ模型的骨折面为绑定关系。在股骨头表面最上端取一个较小的受力面,模拟人在直立状态下的受力情况,将1 000 N的力加到每个点上进行有限元加载。股骨远端底面作为固定端,施加三向平移和三向旋转约束。 观察指标包括应力峰值及位置、位移、股骨颈应力峰值
2 结果
2.1应力峰值及位置随着骨折治疗的时间变化,4种模型的应力峰值及其位置存在显著变化。PFNA-Ⅱ固定骨折模型和骨折愈合模型的应力峰值均位于螺旋刀片与主钉接触区域,当骨折愈合之后内固定的应力峰值上升63.7%。去除PFNA-Ⅱ模型的应力峰值有所下降,但仍然是正常股骨模型D的2.5倍。见表1、图1A~D。

表1 不同模型的应力峰值与位置

图1A 骨折固定模型应力分布云图

图1B 骨折愈合模型应力分布云图
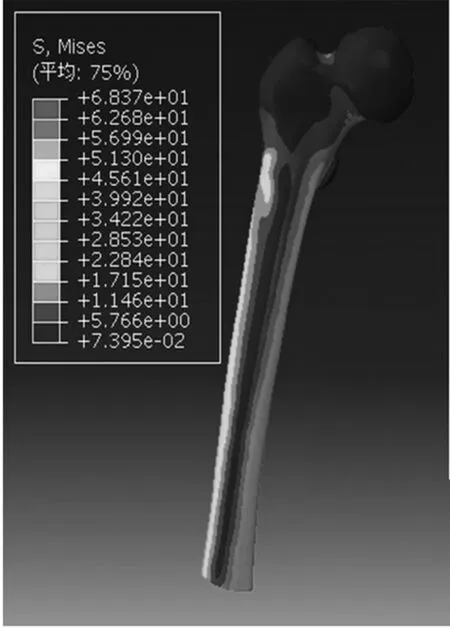
图1C 取出PFNA-Ⅱ模型应力分布云图
2.2位移位移云图中,从股骨头顶部到股骨干,位移量逐渐减小。正常股骨模型的位移最小,稳定性最好。骨折固定模型、骨折愈合模型、取出PFNA-Ⅱ后模型的最大位移分别是正常股骨模型的5.42、
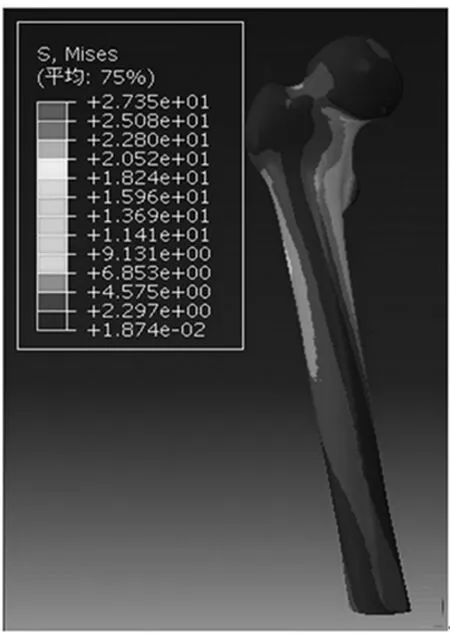
图1D 正常股骨模型应力分布云图
4.21、5.69倍。骨折愈合模型的稳定性优于骨折固定模型和取出PFNA-Ⅱ模型。见图2A~D、图3。

图2A 骨折固定模型位移云图

图2B 骨折愈合模型位移云图

图2C 取出PFNA-Ⅱ模型位移云图

图2D 正常股骨模型位移云图
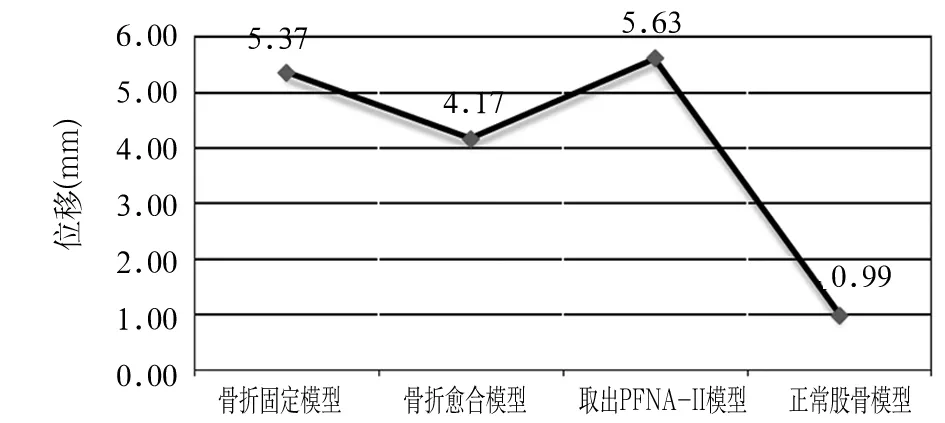
图3 不同模型的位移变化图
2.3股骨颈应力峰值由于PFNA-Ⅱ承担了主要应力,骨折愈合模型的股骨颈区域应力最小。取出PFNA-Ⅱ模型的股骨颈区域的应力较骨折愈合模型上升86.6%,比正常股骨模型大25.5%。比骨折固定模型大42.9%。见图4A~D、图5。

图4A 骨折固定模型股骨颈应力分布云图
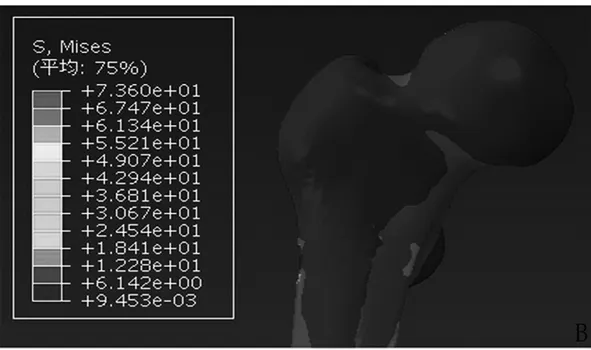
图4B 骨折愈合模型股骨颈应力分布云图

图4C 取出PFNA-IIⅡ模型股骨颈应力分布云图

图4D 正常股骨模型股骨颈应力分布云图
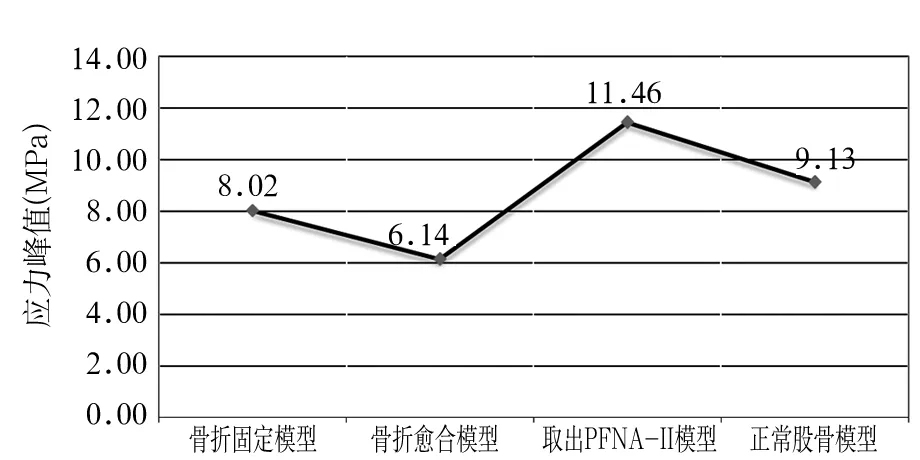
图5 不同模型股骨颈应力峰值变化图
3 讨论
股骨转子间骨折手术治疗的目标在于重建骨骼的稳定性与连续性并坚强固定,促进患者早期负重行走,尽可能减少骨折直接或间接引起的并发症[5]。本文对PFNA-Ⅱ治疗不稳定型股骨转子间骨折后的生物力学情况进行了动态研究和分析,根据临床实际,分别建立了骨折固定模型、骨折愈合模型、内固定取出模型和正常股骨模型。研究表明,PFNA-Ⅱ固定治疗不稳定型股骨转子间骨折可以提供较好的稳定性,在治疗过程中的骨骼与内固定的应力、稳定性存在明显变化。PFNA-Ⅱ固定期间,内固定承担主要应力,应力峰值主要集中在螺旋刀片与主钉的交界处。当骨折愈合之后,由于弹性模量较高,PFNA-Ⅱ同样承担了更多的载荷,且最大应力有上升的趋势。骨折愈合后的应力集中会增加内固定疲劳断裂的风险,同时可能会造成骨折[6,7]。这与之前我们所认为的骨折愈合后应力会通过骨传导降低不一致。由于骨与内固定物存在弹性模量的差异,骨折虽然愈合,髓内钉仍为应力的主要传导者,长期的活动会导致内固定物的疲劳断裂。因此,当股骨转子间骨折骨折愈合后,为避免发生内固定断裂,从生物力学的角度考虑,我们认为活动度大、预期寿命较长的患者有必要取出PFNA-Ⅱ。
目前临床上对于取出内固定后是否需要保护,是否可以有限负重以及何时开始正常活动等问题没有统一的意见[8]。Yoon等[1]研究发现股骨转子间骨折内固定取出术后有9%的患者在1 个月内发生了非外伤性股骨颈骨折。股骨小转子的完整性对于股骨近端的稳定性和患者的功能恢复有重要意义[9]。本研究选取小转子缺损的Evans-Jensen Ⅳ型股骨转子间骨折作为研究对象,结果显示在小转子获得愈合、股骨近端完整性获得重建的情况下,取出PFNA-Ⅱ后存在的钉道空洞仍然会明显降低骨骼稳定性和增加股骨颈的应力集中。
不同的内固定取出后对股骨近端骨质强度的影响存在明显不同,钉道空洞越大,骨骼强度降低也就越明显。Kukla等[10]采用直径12 mm的Gamma钉和直径8 mm的动力髋螺钉对尸体股骨进行处理模拟内固定取出后的骨骼,其中经动力髋螺钉处理后的骨骼强度降低了21.1%, 经Gamma 钉处理后的强度降低了40.9%。 PFNA-Ⅱ的主钉近端直径为16.5 mm,螺旋刀片套筒和杆部直径分别为10.5 mm和9 mm,骨折愈合取出内固定后在股骨近端留下较大的钉道骨质空洞,破坏股骨的力学结构和力学强度。Mahaisavariya等[11]研究发现去除Gamma钉后股骨颈区域的应力明显增加。我们的研究结果与其相符。因此可以认为钉道空洞所导致的稳定性降低和股骨颈局部应力增加是导致骨折愈合取出内固定后出现股骨颈骨折的原因。
综上所述,在PFNA-Ⅱ治疗不稳定型股骨转子间骨折后的不同阶段,骨骼与内固定的应力和稳定性存在明显变化。手术医生应对内固定拆除的指征和原因有所了解,在骨折愈合以后为避免内固定断裂,活动度大、预期寿命较长的患者应取出PFNA-Ⅱ。内固定取出之后在钉道骨结构完全重塑之前需特别防范股骨近端再次骨折的风险。
本研究的不足之处在于股骨转子间骨折的骨折线多不规则,骨折断面之间的接触并不完全,在建立三维有限元模型时仅做了简化处理。在力学加载时,选择了静力分析,忽略了髋部肌肉等其他载荷的影响,故研究结果与临床实际可能存在一定偏差。
[1] Yoon PW, Kwon JE, Yoo JJ, et al. Femoral neck fracture after removal of the compression hip screw from healed intertrochanteric fractures[J]. J Orthop Trauma, 2013,27(12):696-701.
[2] Tada S, Stegaroiu R, Kitamura E, et al. Influence of implant designand bone quality on stress/strain distribution in bone around implants: a 3-dimensional finite element analysis[J]. Int J Oral Maxillofac Impants, 2003,18(3):357-368.
[3] Kobayashi E, Wang TJ, Doi H, et al. Mechanical properties and corrosion resistance of Ti -6Al-7Nb alloy dental castings[J].J Mater Sci Mater Med, 1998,9(10):567-574.
[4] Eberle S, Gerber C, von Oldenburg G, et al. A biomechanical evaluation of orthopaedic implants for hip fractures by finite element analysis and in-vitro tests[J].Proc Inst Mech Eng H, 2010,224(10):1141-1152.
[5] Cadarette SM, Lévesque L, Mamdani M, et al. Comparison of orally administered bisphosphonate drugs in reducing the risk of hip fracture in older adults: a population-based cohort study [J].CMAJ Open,2013,1(3):E97-E105.
[6] Wang L, Zhao F, Han J, et al. Biomechanical study on proximal femoral nail antirotation (PFNA) for intertrochanteric fracture[J]. J Mech Med Biol, 2012,12(4):271-276.
[7] 王丽珍,赵峰,樊瑜波. 新型带锁髓内钉在股骨粗隆间骨折愈合过程中的生物力学研究[J].医用生物力学,2011, 26(4):305-309.
[8] Busam ML, Esther RJ, Obremskey WT.Hardware removal: indications and expectations[J].J Am Acad Orthop Surg, 2006,14(2):113-120.
[9] 吕发明,程国杰,陈平波.等.老年股骨转子间骨折伴小转子移位大于2cm行小转子复位固定对髋关节功能的影响:前瞻随机对照[J].中国组织工程研究与临床康复, 2011, 15(52):9750-9755.
[10] Kukla C, Pichl W, Prokesch R, et al. Femoral neck fracture after removal of the standard gamma interlocking nail: a cadaveric study to determine factors influencing the biomechanical properties of the proximal femur[J]. J Biomech, 2001,34(12):1519-1526.
[11] Mahaisavariya B, Sitthiseripratip K, Suwanprateeb J. Finite elementstudy of the proximal femur with retained trochanteric gamma nail and after removal of nail[J]. Injury, 2006,37(8):778-785.
Dynamic finite element analysis of unstable intertrochanteric fractures fixed with PFNA-Ⅱ
JIANGZiwei,HUQunsheng,HUANGFeng,ZHENGXiaohui,ZHAOJingtao,ZHOUQishi
(TheFirstAffiliatedHospitalofGuangzhouUniversityofChineseMedicine,Guangzhou510405,China)
ObjectiveTo explore the dynamic biomechanical properties of unstable intertrochanteric fracture fixed with proximal femoral nail antirotation Ⅱ(PFNA-Ⅱ) through finite element analysis, and therefore to provide theoretical foundation for clinic application.MethodsFinite element model of Evans IV intertrochanteric fracture fixed by PFNA-Ⅱ was developed. We simulated the conditions of fracture union and internal fixation removal by adjusting the contact relationship of fractures and taking out of PFNA-Ⅱ. Stress peak and biomechanical stability of models were compared with normal femur model through finite element analysis. ResultsThe highest stress concentration area of fixation models was located in the caudal passage of the blade through the nail. After fracture union, the stress of internal fixation increased. After internal fixation was removed, the stress of femoral neck increased significantly and the stability decreased. ConclusionsIn order to avoid internal fixation rupture after fracture union, PFNA-Ⅱ should be removed, meanwhile the risk of femoral neck fracture requires attention.
intertrochanteric fractures; internal fixation; proximal femoral nail antirotation Ⅱ; finite element analysis
广东省自然科学基金项目(2014A030310379);广州市科技计划项目(1563000664)。
姜自伟(1980-), 男 ,副主任中医师,医学博士,主要研究方向为中西医结合治疗骨与关节损伤。E-mail:ainemylyy@163.com
10.3969/j.issn.1002-266X.2016.33.005
R683.42
A
1002-266X(2016)33-0014-05
2016-05-10)

