LiOH·H2O催化合成假性紫罗兰酮的研究
陈隽丹, 唐新阳*(. 箴言中学,湖南 益阳 43000;. 宁乡县第一高级中学,湖南 长沙 40660)
LiOH·H2O催化合成假性紫罗兰酮的研究
陈隽丹1,唐新阳2*
(1. 箴言中学,湖南 益阳 413000;2. 宁乡县第一高级中学,湖南 长沙 410660)
以LiOH·H2O为催化剂,由柠檬醛与丙酮Aldol缩合合成了假性紫罗酮;考查催化剂用量、温度、反应时间、柠檬醛与丙酮配比对反应的影响,以及催化剂的重复使用率。结果表明,最佳工艺条件是n(柠檬醛)/n(丙酮)为1∶7,催化剂用量相对于柠檬醛的60%(mol),反应温度45℃,反应时间6 h,转化率可达96.23%,催化剂可重复使用。
假性紫罗兰酮;柠檬醛;Aldol缩合;LiOH·H2O;丙酮
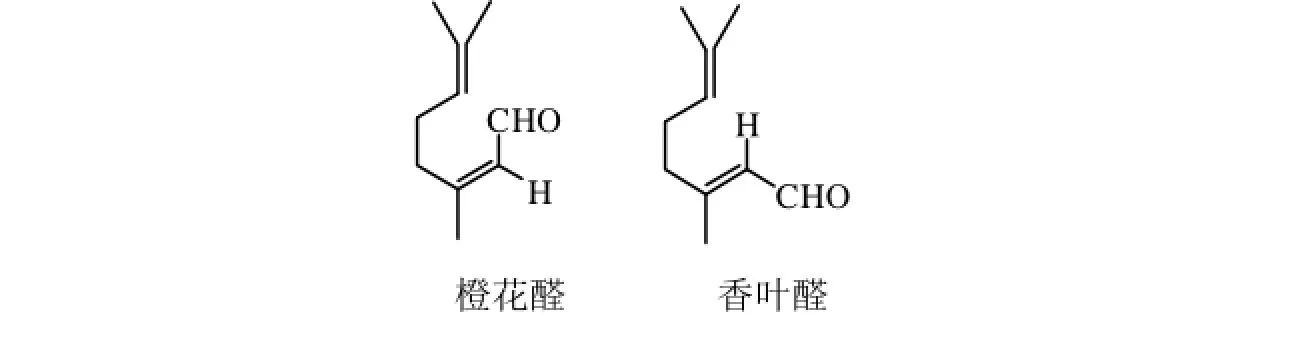
假性紫罗兰酮( C13H20O)是一种重要的有机合成中间体,在香料香精、医药、食品添加剂等有机合成领域占有重要的地位,应用非常广泛;假性紫罗兰酮目前在国内没有形成商业化产品,但随着香料香精及医药行业的发展,对其需求量有望增加。柠檬醛主要来源是山苍子油,我国南方盛产山苍子油,现已建成十万亩的种植基地,可年产山苍子油1 600吨,其中富含75%的柠檬醛,可直接用于假性紫罗兰酮的合成[1-3]。天然柠檬醛是其顺(橙花醛)、反(香叶醛)两种异构体的混合物,其中的反式占80%~90%,顺式仅占10%~20%,如图1所示。目前工业上生产假性紫罗兰酮的一般方法是用柠檬醛与丙酮在NaOH水溶液中发生醇醛缩合反应生成假性紫罗兰酮[4],该反应要求必须严格控制反应的碱性和温度,因为除生成假性紫罗兰酮外,还会发生副反应产生副产品,如平行反应、柠檬醛自身缩合反应、丙酮自身缩合反应等,如图1所示。这吸引学者对催化体系进行改进,如马增欣等[5]用Ba(OH)2·8H2O做催化剂在40℃时反应4 h,蒸馏收率可高达96.3%,Díez V K等[6]用Li/MgO做催化剂,产率可达93%。
主反应:
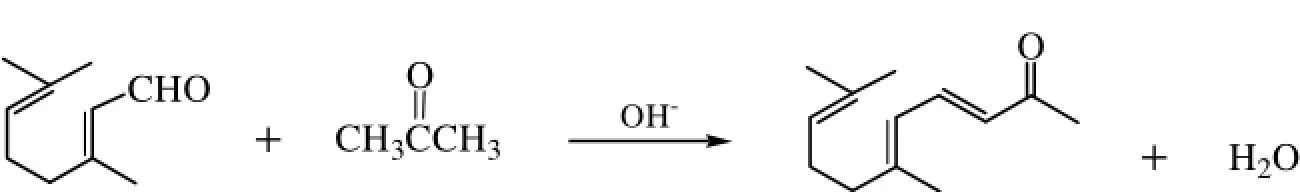
平行反应:
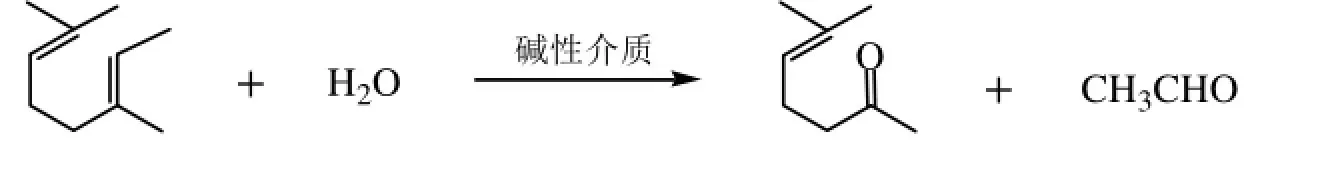
柠檬醛自身缩合

丙酮自身缩合:
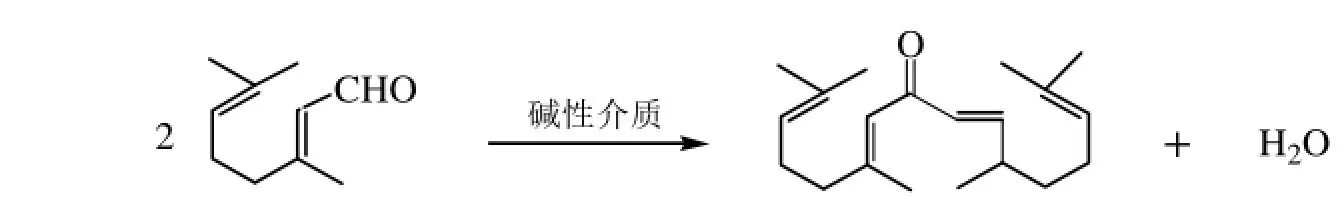
本文利用我国丰富的山苍子生物资源,寻找一种催化效果好、选择性高、可重复使用的催化剂,实验表明,尽管LiOH·H2O具有价格稍贵等不足外,在催化柠檬醛与丙酮缩合生成假性紫罗兰酮的实验中,收到了良好的催化效果。
1 实验
1.1试剂与仪器
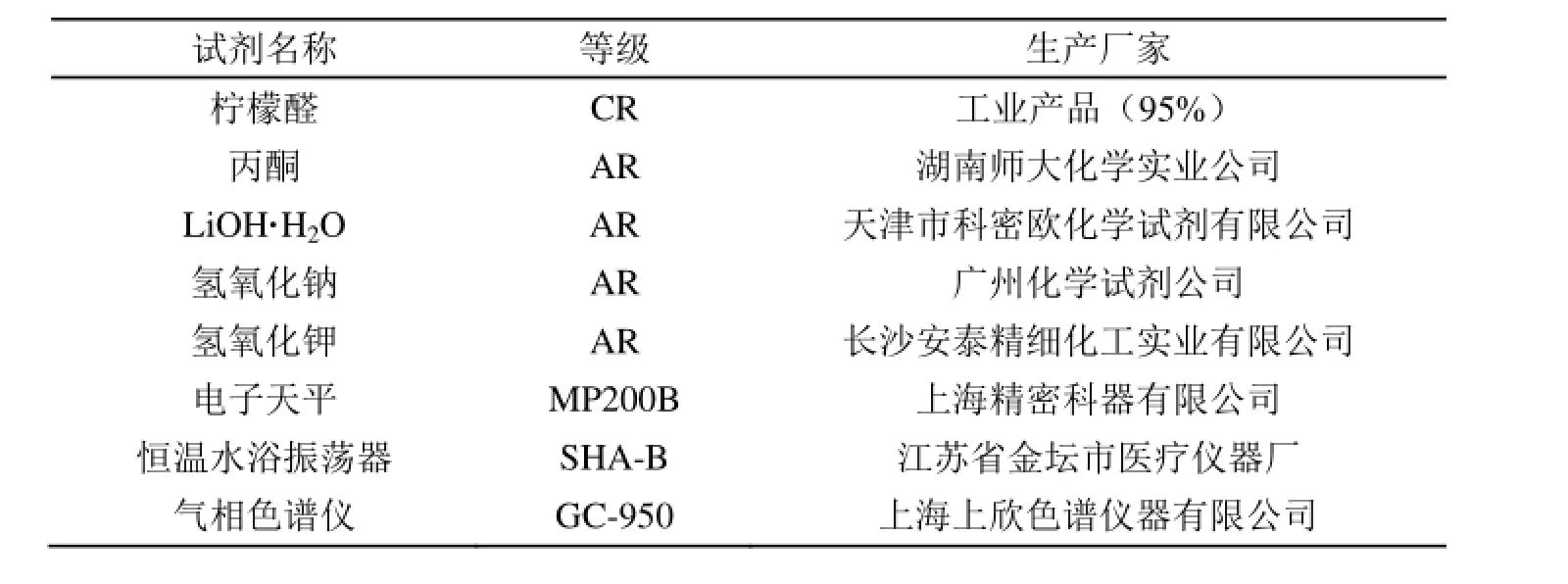
表1 主要实验试剂
1.2LiOH·H2O催化合成假性紫罗兰酮
在锥形瓶中加入一定量的柠檬醛、丙酮和催化剂LiOH·H2O,反应过程中固体LiOH·H2O在体系中有着呈固态,塞紧塞子,放入水浴振荡器中,控制一定温度反应一定时间,每小时取样。用气相色谱检测假柠檬醛的转化率和选择性。
1.3分析测试
样品用上海分析仪器厂1102气相色谱仪分析,OV-17石英毛细管柱(25 m×0.25 mm×0.25µm),FID检测器,以N2为载气,柱温160℃。
2 结果与讨论
2.1反应温度和催化剂用量对反应的影响
考查35℃、38.5℃、45℃下, 不同的LiOH·H2O催化剂用量(相对于柠檬醛)对柠檬醛的转化率的影响,结果如图2~4所示。
图2~4数据表明,在35℃、38.5℃、45℃三种反应温度下,加大催化剂的用量,柠檬醛的转化率有所提高,当催化剂用量相对于柠檬醛物质的量的60%时,结果比较理想。
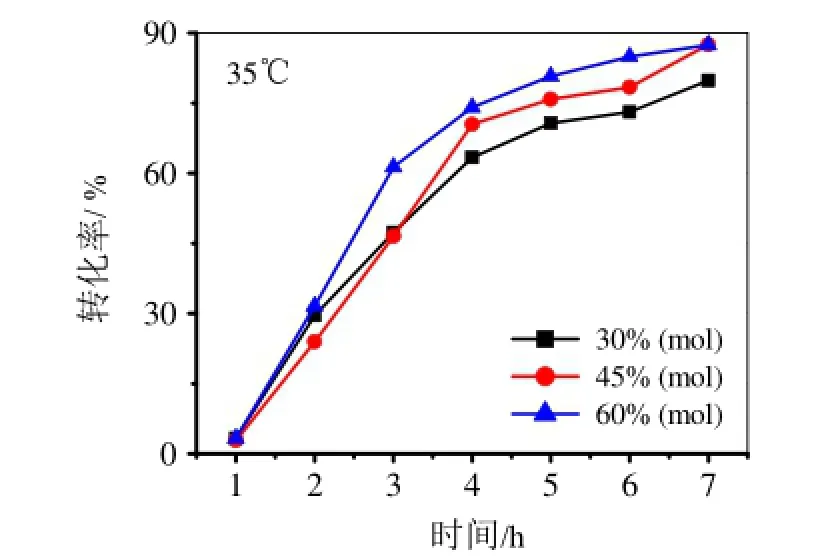
图2 35℃催化剂用量柠檬醛转化率的影响
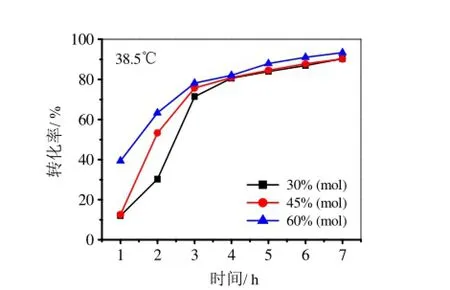
图3 催化剂用量及反应时间对柠檬醛转化率的影响
由图2~4可知,当温度从35℃提高到45℃时,假性紫罗兰酮的产率有很大的提高;在最佳催化剂用量,45℃时,反应6 h,假性紫罗兰酮的产率达到96.23%。
在LiOH·H2O用量为n(柠檬醛)60% mol,反应6 h,考察了不同温度下产物的选择性,结果如表2所示;产物的选择性均大于96%,其中反应温度45℃时,产物选择性为98.03%。
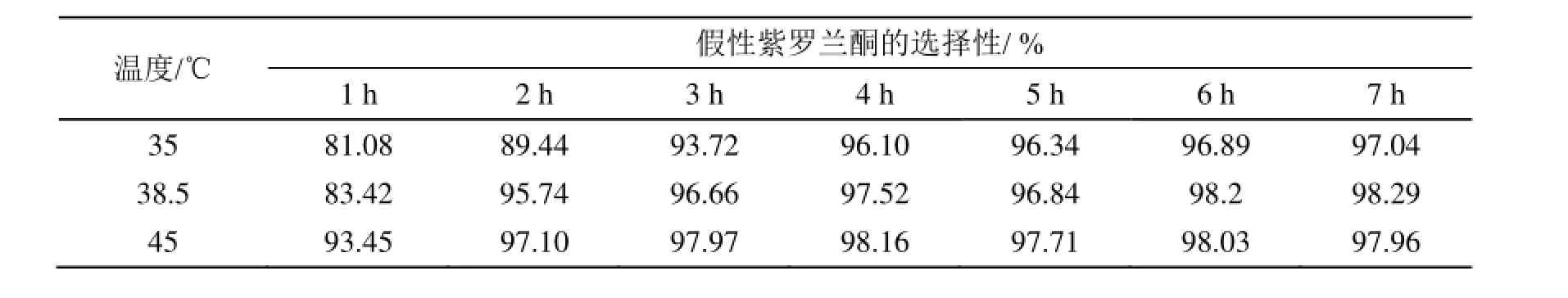
表2 假性紫罗兰酮的选择性
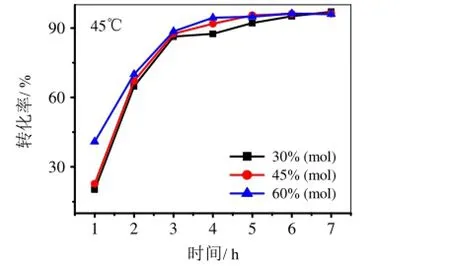
图4 催化剂用量及反应时间对柠檬醛转化率的影响
2.2柠檬醛和丙酮配比对反应的影响
固定反应温度45℃,LiOH·H2O用量为n(柠檬醛)60% mol,改变柠檬醛和丙酮配比(摩尔比),结果如表3所示。结果表明,柠檬醛和丙酮配比对反应也有较大影响,丙酮用量增加,反应速率明显下降,但是丙酮用量过少,反应速率虽快,副反应比较严重;这一类液-固非均相反应中,丙酮与柠檬醛形成完全互溶的均相体系,界面上丙酮和OH-间的可逆反应及界面上进行的缩合反应意味着液-固相平衡和传递过程都不同程度影响着总反应速率,以及所需产品的选择性;当丙酮用量过大时,LiOH·H2O溶解量减少,不利于OH-的形成,同时降低催化剂与反应的接触;故当柠檬醛:丙酮(n/n)=1∶7时最佳,此条件下反应6 h,转化率96.14%,选择性98.57%。
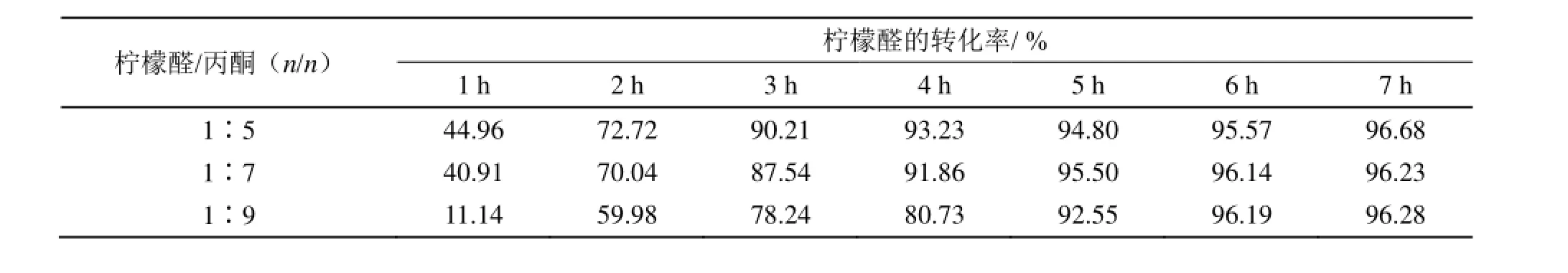
表3 不同配比假性紫罗兰酮产率
2.3催化剂重复使用
倾去液相,用丙酮洗涤三次,干燥,同样的条件下做重复实验考察,得到表4。可以看出LiOH·H2O催化效果没有明显的变化,使用第2次第3次时前1 h的反应速率比初次使用加快,可能是因为反应过程中由于振荡导致LiOH·H2O晶体破碎,表面积增大所致。
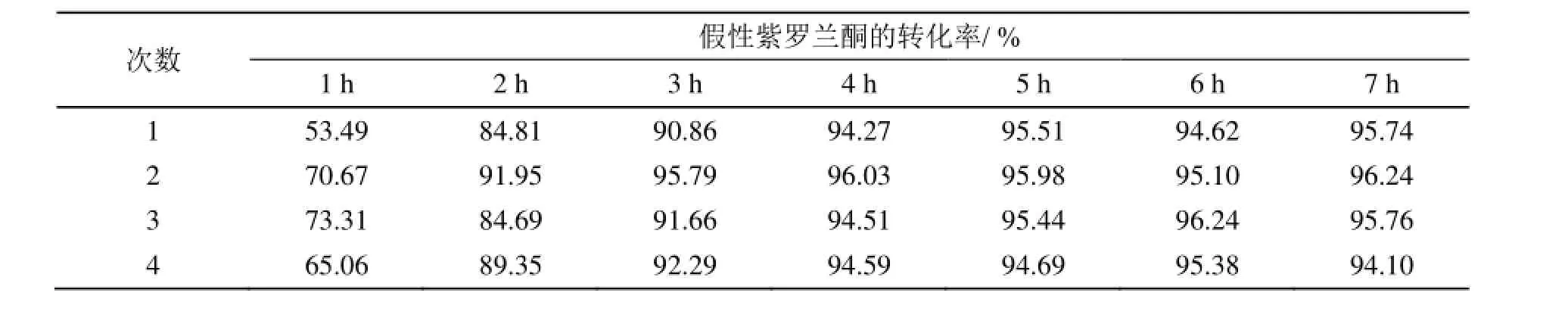
表4 催化剂重复效果

表5 NaOH催化效果
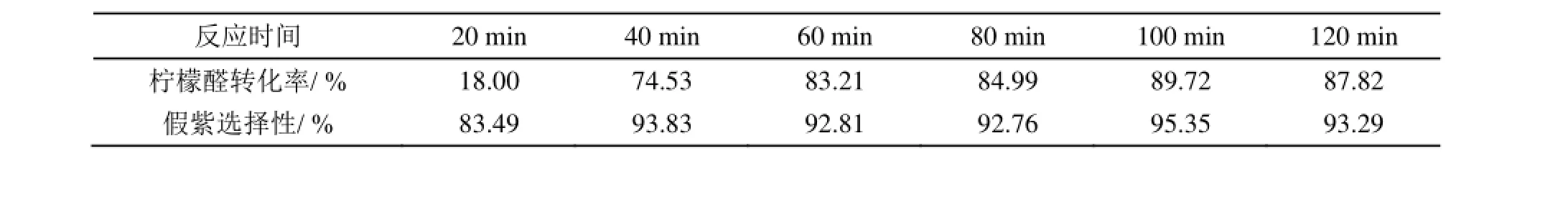
表6 KOH催化效果
2.4NaOH、KOH催化效果对比
在45℃下,催化剂用量相对于柠檬醛60%mol,做了NaOH、KOH对比实验,数据如表5、6所示;NaOH做催化剂时柠檬醛的最高转化率为85.73%,选择性最高为95.51%;KOH做催化剂时柠檬醛的转化率最高为89.72%,选择性最高为95.35%,均低于用LiOH·H2O做催化剂的转化率。两种催化剂在反应终了时均呈浆状不易分离,必须进行中和、水洗等操作;反应液颜色较深,副反应程度严重。
3 结论与展望
本文探讨了反应温度、原料摩尔配比、LiOH·H2O用量等各种反应条件对反应的影响,并就这些条件对反应结果的影响进行了较详细的研究,确定了以上诸因素之间相互关系,确定了合成反应的最佳条件,反应温度45℃,柠檬醛/丙酮=1 : 7,LiOH·H2O用量相对于柠檬醛用量的60% mol。
实验虽然取得了一些进展,但是还是有很多需要改进的地方,虽然在反应过程中流失较少,但是LiOH·H2O价格比较贵,在工业生产中,由于生产量大,其损失也是不容忽视的。在以后的研究工作中,力求寻找一种固载催化剂,降低催化剂的价格和流失率。
[1] 崔志敏, 钟军, 李楠, 等. 直接用山苍子油优化假性紫罗兰酮半合成工艺研究[J]. 江西化工, 1999, 3: 22-24.
[2] 刘晓庚, 陈学恒, 桂衍胜. 由山苍子油合成假性紫罗兰酮和紫罗兰酮的研究[J]. 江西农业大学学报, 1999, 21(1): 32-33.
[3] 黄喜根, 张宁, 黄忠. 由山苍子油合成假性紫罗兰酮的研究[J]. 江西农业大学学报, 2007, 29(2): 12-14.
[4] 黄海水. 假性紫罗兰酮的合成[J]. 应用化学, 1992, 9(4): 81-82.
[5] 马增欣, 郑跃红, 郑玉, 等. 固体碱催化合成假性紫罗兰酮[J]. 天然产物研究与开发. 1997, 9(3): 10-13.
[6] Díez V K, Apesteguía C R, Di Cosimo J I. Aldol condensation of citral with acetone on MgO and alkali-promoted MgO catalysts[J]. Journal of Catalysis, 2006, 240: 235-244.
Study on LiOH·H2O Catalytic Synthesis of Pseudoionone
CHENG Jiu-dan1,TANG Xin-yang2
(1. Proverbs Middle School, Yiyang 413000, China; 2. Ningxiang No.1 High School, Changsha 410660, China)
In this paper, with LiOH·H2O as catalyst, pseudoionone was synthesized by the condensation of citral with acetone. The effects of the amount of catalyst, temperature, reaction time, citral and acetone ratio on the reaction and the catalyst were studied. The optimized conditions were n (citral)/ n (acetone) of 1: 7, the amount of catalyst with respect to 30% (mol) citral, the reaction temperature 45℃, reaction time 6 h, the conversion rate of 96.23%. The catalyst could be reused.
pseudoionone; citral; aldol condensation; LiOH·H2O; acetone
G633.8
A
1009-220X(2016)04-0051-05
10.16560/j.cnki.gzhx.20160417
2016-05-31
陈隽丹(2000~),女,大学预科生;主要从事有机催化的研究。
唐新阳(1978~),男,一级教师;主要从事高中教学和竞赛培训研究。oyzg1790201@163.com

