白及非多糖组分的止血作用及其机制的初步研究
赵菲菲,杨 馨,徐 丹,董 莉,李 靖,王永林,廖尚高
(贵州医科大学 1.药学院、2. 民族药与中药开发应用教育部工程研究中心、3.贵州省药物制剂重点实验室,贵州 贵阳 550004)
白及非多糖组分的止血作用及其机制的初步研究
赵菲菲1,2,杨馨1,3,徐丹1,2,董莉1,3,李靖1,2,王永林1,3,廖尚高1,2
(贵州医科大学 1.药学院、2. 民族药与中药开发应用教育部工程研究中心、3.贵州省药物制剂重点实验室,贵州 贵阳550004)
doi:10.3969/j.issn.1001-1978.2016.08.018
目的明确白及非多糖部分的止血作用,初步了解其止血机制。方法白及95%乙醇提取物上D101大孔树脂,经水洗脱后,用80%乙醇洗脱得到不含多糖的80%乙醇组分(BS-80EE);以小鼠全身肝素化的出血时间(BT)和凝血时间(CT)为指标考察BS-80EE的止血作用;以二磷酸腺苷(ADP)为诱导剂,采用比浊法观察BS-80EE对大鼠体内血小板聚集率的影响;通过考察BS-80EE对大鼠凝血酶时间(TT)、凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)和纤维蛋白原含量(FIB),以及血小板膜糖蛋白P-选择素(P-S)、凝血酶-抗凝血酶复合物(TAT)、纤溶酶原激活物抑制剂-1(PAI-1)、D-二聚体(D-D)的影响,分别从血小板和凝血纤溶系统角度了解BS-80EE的止血机制。结果BS-80EE可剂量依赖性地缩短全身肝素化小鼠的CT和BT(P<0.01或P<0.05);明显促进ADP诱导的大鼠体内血小板聚集作用(P<0.01);明显缩短大鼠的TT值(P<0.01或P<0.05);高剂量组可明显增加FIB含量(P<0.05);中、高剂量组可明显增加P-S、TAT、PAI-1的含量,减少D-D的生成(P<0.01)。BS-80EE虽有缩短大鼠APTT和PT的趋势,但差异均无显著性。结论白及非多糖组分(BS-80EE)具有良好的止血功效,可通过促进血小板聚集和凝血而发挥止血作用。
白及;非多糖组分;止血;血小板聚集;出血时间;凝血时间;作用机制
白及为兰科植物白及[Bletillastriata(Thunb.)Reichb. F.]的干燥块茎,又名甘根、白根、地螺丝等,是《中国药典》收载的常用中药之一,其味苦、甘、涩,性微寒,具有收敛止血、清热利湿、消肿生肌之功效,临床上主要用于咯血、吐血、外伤出血等治疗[1-2]。前期化学研究表明[3-4],白及药材中的化学成分复杂,除含有较多多糖类物质外,还含有大量联苄类、二氢菲类、联苄葡萄糖苷类、菲类等物质,但目前白及止血的化学与药理研究主要集中在白及多糖上,白及非多糖部位的止血作用尚未见报道。本课题组在前期研究中已对白及非多糖组分进行了组分分离、色谱分析和简单体外止血作用评价,发现在大孔树脂色谱柱上去除了强水溶性成分和强亲脂性成分后获得的白及80%乙醇洗脱组分(BS-80EE)中含有大量的非多糖类化合物[5],且家兔体外凝血实验结果表明BS-80EE可以明显缩短家兔体外的凝血时间。但是,由于前期药效学考察方法仅从凝血时间上进行评价,指标单一,不能充分阐明BS-80EE的作用,且其发挥止血作用的止血机制尚不明确。故本文旨在对BS-80EE进行进一步的药效研究,并在此基础上初步探讨其发挥止血作用的机制,为白及的进一步开发奠定实验基础。
1 材料
1.1动物SPF级KM小鼠(♀ ♂各半),体质量20~22 g;SPF级SD大鼠(♀ ♂各半),体质量200~240 g,均由贵州医科大学实验动物饲养中心提供,许可证号:SCXK(黔)2012-0001。实验动物自由摄食饮水,实验前适应性饲养7 d。
1.2药品与试剂白及药材(批号:20150223,产地贵州正安县,等级优级),由贵州医科大学药学院生药学与药用植物学教研室龙庆德副教授鉴定为兰科植物白及Bletillastriata(Thunb.) Reichb. F. 的干燥块茎;云南白药(YNBY)(批号:ZMA1415 20141210,云南白药集团股份有限公司);乙醇为分析纯;羧甲基纤维素钠(CMC-Na)(批号:20150408,成都金山化学试剂有限公司);肝素钠注射液(批号:51506101,江苏万邦生化医药股份有限公司);水合氯醛(批号:20150120,国药集团化学试剂有限公司);二磷酸腺苷(ADP)(批号:91M7002V,Sigma公司);试剂盒凝血酶时间(TT,批号:20101-87B)、凝血酶原时间(PT,批号:20201-59)、活化部分凝血活酶时间(APTT,批号:20301-52)、血浆纤维蛋白原(FIB,批号:20401-63)均购自北京世帝科学仪器公司;凝血酶-抗凝血酶复合物(TAT,批号:20150910)、D-二聚体(D-D,批号:20150911)、纤溶酶原激活物抑制剂-1(PAI-1,批号:20150912)、P-选择素(P-S,批号:20150913)均购自南京建成生物科技有限公司。
1.3仪器LGPABEER 型血小板聚集凝血因子分析仪(北京世帝科学仪器公司);TDL-80-2B台式离心机(上海安亭科学仪器厂);DK-98-ⅡA恒温水浴锅(天津市泰斯特仪器有限公司);酶标仪(上海伯乐生命医学产品有限公司);METTLER AE240十万分之一电子天平(梅特勒-脱利多仪器上海有限公司);DZF-6050真空干燥箱(上海博讯有限公司医疗设备厂);超纯水机(四川沃特尔科技发展有限公司)。
1.4供试品制备
1.4.1阳性对照药云南白药临床用量为每人2 g,实验动物按人临床用量20倍给药,即0.667 g·kg-1。称取云南白药粉末6.67 g加入100 mL 0.5% CMC-Na研磨均匀即得。
1.4.2白及非多糖组分参照文献方法[5],称取白及药材(过40目筛)5 kg,用4倍量体积分数为0.95的乙醇溶液回流提取3次,每次2 h。合并滤液后浓缩至浸膏,浸膏用水溶解后上D101(大孔树脂5.5 cm, 35 cm)柱色谱,依次用水、体积分数为0.8的乙醇溶液、体积分数为0.95乙醇溶液进行洗脱,合并体积分数为0.8的乙醇洗脱液后浓缩至浸膏,真空挥干得白及80%乙醇洗脱物(BS-80EE)690 g(每克相当于生药量7.25 g),计算得率为13.6%,即为白及非多糖组分。白及临床用量为每人15 g,实验动物按人临床用量10倍、20倍、40倍分别作为低剂量、中剂量、高剂量给药,即为2.5、5.0、10.0 g·kg-1。分别称取BS-80EE加入100 mL 0.5% CMC-Na研磨均匀,BS-80EE灌胃量分别是3.4、6.8、1.36 g·kg-1。
1.4.3肝素钠注射液[6]取适量肝素钠注射剂,用生理盐水稀释,配成16 kU·L-1活性浓度,现用现配。
2 方法
2.1全身肝素化小鼠出血时间(BT)的测定[6]取KM小鼠60只(♀ ♂各半),随机分为6组,每组10只。分为空白对照组、肝素化模型组、云南白药组(0.667 g·kg-1)、BS-80EE高(10.0 g·kg-1)、中(5.0 g·kg-1)、低(2.5 g·kg-1)剂量组。各组小鼠每天灌胃给药1次,空白组和模型组分别给予0.5% CMC-Na生理盐水20 mL·kg-1,连续5 d。d 5,灌胃给药60 min后,除空白组外,其余各组均尾静脉注射肝素钠,每只3.2 U,15 min后用手术刀于距小鼠尾尖0.5 cm处割断,待血液自行溢出时开始计时,每隔30 s用滤纸吸附血滴1次,直至血液自然停止(滤纸吸时无血迹)。以人工形成创面到出血停止所经时间作为小鼠出血时间(BT)。
2.2全身肝素化小鼠凝血时间(CT)的测定[6]取KM小鼠60只(♀ ♂各半),随机分为6组,每组10只,分组及给药方法同“2.1”项。于d 5灌胃给药60 min后,除空白组外其余各组均尾静脉注射肝素钠,每只3.2 U,15 min后用内径1 mm,长10 cm的毛细玻璃管从小鼠内眼球后静脉丛取血,待血液充满玻璃管时开始计时,接着每隔30 s折断两端毛细玻璃管(约0.5 cm),并缓慢向左右拉开,观察折断处有无血凝丝出现,从血液充满玻璃管开始至出现血凝丝所经历的时间作为小鼠凝血时间(CT)。
2.3大鼠血小板聚集率的测定取SD大鼠50只(♀ ♂各半),随机分为5组,每组10只。分为空白对照组、云南白药组(0.667 g·kg-1)、BS-80EE高(10.0 g·kg-1)、中(5.0 g·kg-1)、低(2.5 g·kg-1)剂量组。各组大鼠每天灌胃给药1次,空白组给予0.5% CMC-Na生理盐水10 mL·kg-1,连续7 d。d 7,灌胃给药60 min后,腹腔注射100 g·L-1水合氯醛麻醉,使用3.8%枸橼酸钠抗凝真空采血管大鼠腹主动脉釆集血样。将血样800 r·min-1离心10 min,分离上层血浆即得富血小板血浆(PRP),余下部分3 000 r· min-1离心10 min,分离上层血浆即得贫血小板血浆(PPP),用PPP调PRP中血小板的计数为(2~3)×1011·L-1,用PPP调零后,取PRP 290 μL,37℃孵育60 s后,加入终浓度为5 μmol·L-1ADP 10 μL,记录5 min内血小板的最大聚集率。
2.4大鼠TT、PT、APTT、FIB的测定[7]取SD大鼠50只(♀ ♂各半),分组及给药方法同“2.3”项。取枸橼酸抗凝全血,3 000 r· min-1离心10 min,分离上层血浆备用。按血小板聚集凝血因子分析仪操作程序和各指标试剂盒要求分别对TT、PT、APTT 、FIB进行测定。
2.5大鼠TAT、PAI-1、D-D、P-S的测定取SD大鼠50只(♀ ♂各半),分组及给药方法同“2.3”项。取枸橼酸抗凝全血,3 000 r· min-1离心10 min,分离上层血浆备用。按各指标试剂盒的要求进行P-S、TAT、D-D、PAI-1的含量测定。
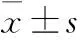
3 结果
3.1BS-80EE对全身肝素化小鼠BT、CT的影响小鼠尾静脉注射肝素钠注射液后,小鼠的BT和CT与空白组相比明显延长(P<0.01),说明小鼠出血模型建模成功。BS-80EE的各剂量组与模型组相比,均能剂量依赖性地缩短全身肝素化小鼠的BT和CT(P<0.01或0.05),且高剂量组的BT与模型组相比缩短率达到77.6%,其BT值趋近于空白组,见Tab 1、Fig 1。
3.2BS-80EE对大鼠血小板聚集率的影响BS-80EE各剂量组与空白组相比,可剂量依赖性地增加ADP诱导的血小板聚集率,且中、高剂量组差异有显著性(P<0.01),促进率分别为20.6%、25.9%,BS-80EE低剂量组对血小板聚集无影响,见Tab 2、Fig 2。
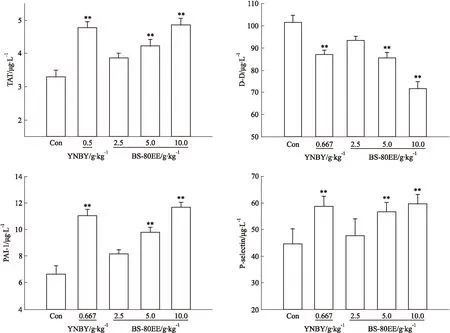
3.3BS-80EE对大鼠TT、PT、APTT、FIB的影响与空白组相比,BS-80EE各剂量组对大鼠PT、APTT没有影响(P>0.05),对TT值有剂量依赖性缩短的作用(P<0.01或0.05),且FIB含量有随着剂量升高而增加的趋势,但除高剂量差异有显著性外(P<0.05),低、中剂量差异均无显著性,见Tab 3。3.4BS-80EE对大鼠血浆中TAT、PAI-1、D-D、P-S的影响灌胃给药后,BS-80EE各剂量组与空白组相比,各组均可剂量依赖性地增加大鼠血浆中的TAT、PAI-1、P-S的含量,减少血浆中D-D的生成,且除低剂量组以外,高、中剂量组差异均具有统计学意义(P<0.01)。见Tab 4、Fig 3。
Fig 1 Effects of different dosages of BS-80EE
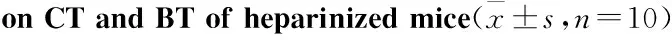
##P<0.01vscontrol;*P<0.05,**P<0.01vsmodel
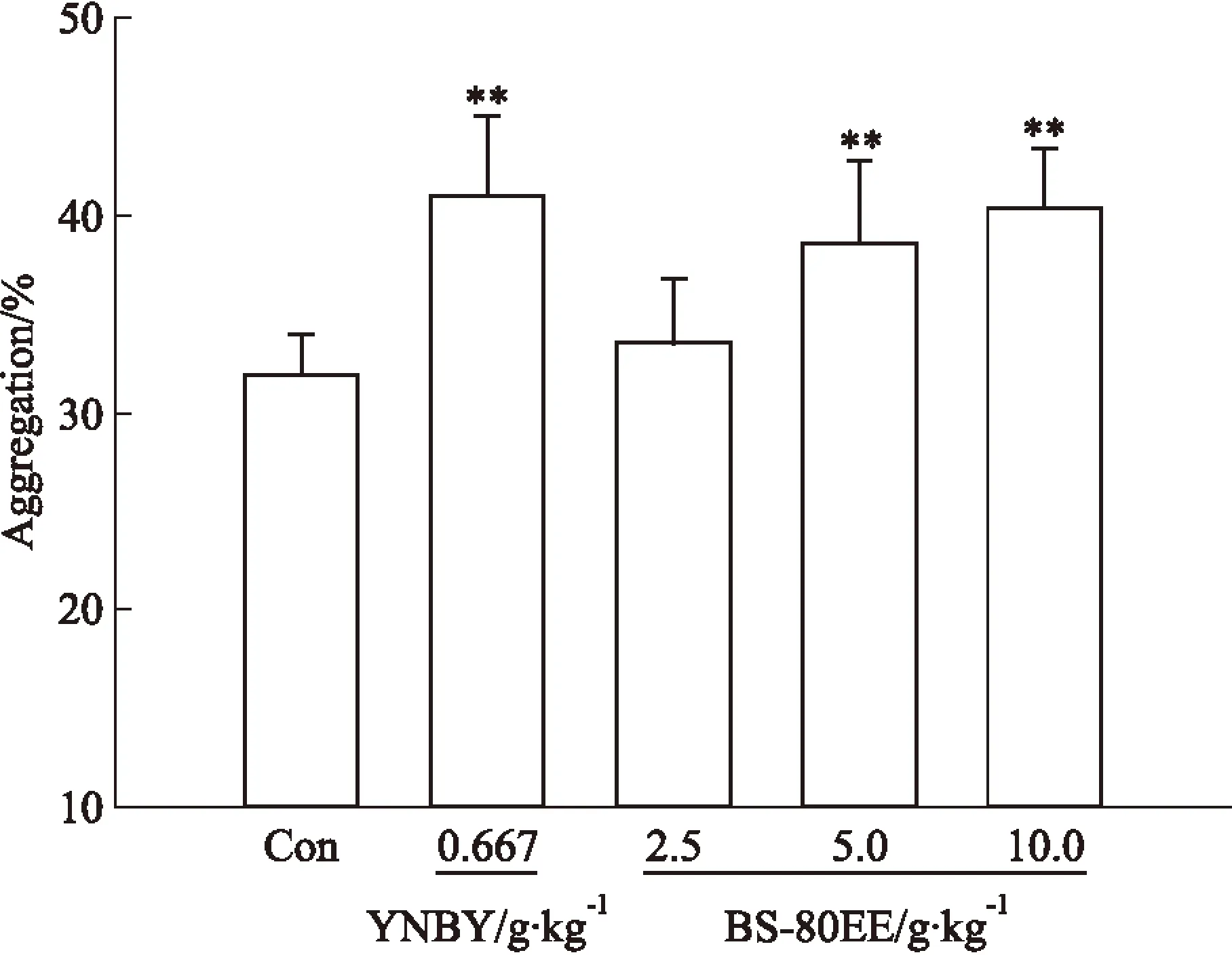
Fig 2 Effects of different dosages from BS-80EE on rat platelet aggregation induced by ±s,n=10)
**P<0.01vscontrol
**P<0.01vscontrol
Tab 1 Effects of different dosages of BS-80EE on CT and BT of heparinized ±s,n=10)
##P<0.01vscontrol;*P<0.05,**P<0.01vsmodel
Tab 2 Effects of different dosages from BS-80EE on rat platelet aggregation induced by ±s,n=10)
**P<0.01vscontrol
4 讨论
《本草汇言》中记载白及具有“敛气、止血、消痈”的功效,目前,临床上大多采用白及粉的形式口服或外用,疗效确切[8]。研究表明,白及多糖是其止血主要药效物质[9],我们前期的药理实验也证实,白及多糖具有良好的体外止血作用[10]。大量的临床实践表明,白及对各种体内出血性疾病(如肺出血等)的疗效比较突出,我们推测白及的非多糖组分可能也具有止血作用,本研究表明,白及非多糖组分同样具有明显的止血作用。
小鼠断尾出血时间(BT)和毛细管凝血时间(CT)实验是一种比较经典的用于止血、促凝血中药的活性筛选方法,可综合反映参与止血过程的各种因素,如血管、血小板、凝血系统等的功能[7,11]。本研究结果表明,BS-80EE对病理性出血小鼠模型有明显的止血药效,且灌胃给予BS-80EE后,采用ADP诱导的大鼠血小板聚集率增加,大鼠血浆中TT值缩短,FIB增加,提示BS-80EE的止血作用可能与促进血小板活化,激活凝血-纤溶系统有关。
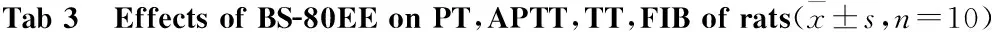
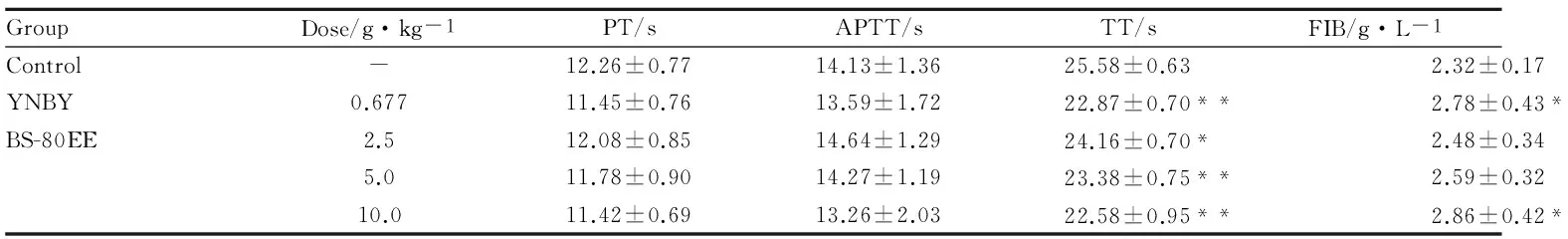
GroupDose/g·kg-1PT/sAPTT/sTT/sFIB/g·L-1Control-12.26±0.7714.13±1.3625.58±0.632.32±0.17YNBY0.67711.45±0.7613.59±1.7222.87±0.70**2.78±0.43*BS-80EE2.512.08±0.8514.64±1.2924.16±0.70*2.48±0.345.011.78±0.9014.27±1.1923.38±0.75**2.59±0.3210.011.42±0.6913.26±2.0322.58±0.95**2.86±0.42*
*P<0.05,**P<0.01vscontrol
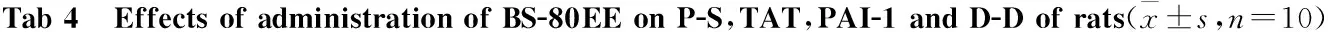

GroupDose/g·kg-1P-S/μg·L-1TAT/μg·L-1PAI-1/μg·L-1D-D/μg·L-1Control-44.58±5.753.28±0.646.62±2.14101.48±9.65YNBY0.66758.71±3.81**4.77±0.61**11.05±1.57**87.03±6.49**BS-80EE2.547.74±6.333.86±0.468.19±1.0293.47±5.165.056.76±3.51**4.21±0.65**9.78±1.19**85.63±7.50**10.059.68±3.47**4.86±0.62**11.71±1.14**71.63±10.17**
**P<0.01vscontrol
凝血酶时间(TT)的变化反映凝血共同途径中纤维蛋白原转化为纤维蛋白时异常抗凝存在与否的特征性指标,由于其作用于凝血过程的最后一步,因而只有纤维蛋白原的浓度和血浆中凝血酶的含量影响TT值的大小[11-12]。凝血酶是凝血级联反应过程中的关键酶,能激活凝血因子Ⅴ、Ⅶ、Ⅺ、Ⅻ等,从而正反馈加速凝血[13]。TAT是体内凝血和抗凝血相互作用的产物,是凝血酶生成的标志物之一,TAT升高,表明凝血酶形成过多,血液呈高凝状态。D-D 是交联纤维蛋白在纤溶酶催化下产生的降解产物,是纤溶系统激活,体内存在继发性纤溶的特异性标志分子之一[14]。PAI-1是体内主要的纤溶活化素抑制物,它可抑制纤溶活化素将纤溶酶原转化为纤溶酶,从而抑制纤溶酶将纤维蛋白(原)转化为纤维蛋白产物[15]。P-S是最具特异的血小板活化的分子标志物,血小板在刺激物的作用下发生变形、黏附、聚集和释放反应与其颗粒膜蛋白P-S表达呈正相关。因此,检测血浆中的TAT、PAI-1、D-D、P-S因子的变化可以在一定程度上反映止血中药发挥止血作用的机制。
本研究显示,给予BS-80EE后,大鼠体内P-S、TAT和PAI-1均增加,D-D减少,结合前面血小板聚集和凝血4项实验结果,提示BS-80EE止血作用可能与血小板、凝血和纤溶功能均有关,并且可以推测其可能通过刺激血小板活化,使血小板聚集作用增强;同时促使凝血共同途径中凝血酶的生成增加,缩短TT值,加速血液的凝固;并抑制纤溶酶原转化为纤溶酶,从而抑制纤溶酶将纤维蛋白转化为纤维蛋白降解产物而发挥止血作用。尽管本文明确了白及非多糖组分止血作用,初步了解了其止血机制,但其发挥药效物质基础仍不明确,因此,有必要对白及非多糖部分的止血物质作用进行进一步的研究,期望能从中发现止血作用突出的化学物质。
(致谢:感谢黄勇教授、徐国波老师等对本论文的悉心指导。感谢龙庆德副教授对白及药材的鉴定。)
[1]国家药典委员会. 中国药典,一部[S].北京:中国医药科技出版社, 2015:103.
[1]Chinese Pharmacopoeia Commission. Pharmacopoeia of the People’s Republic of China[S].Beijing: China Medical Science Press, 2015.Vol I: 103.
[2]张龙霏,胡晶红,张永清.白及药理研究进展[J].中国现代中药,2014,16(1):83-6.
[2]Zhang L F, Hu J H, Zhang Y Q. Research progress on pharmacological action of Bletilla rhizome[J].ModChinMed, 2014, 16(1):83-6.
[3]Feng J Q,Zhang R J. Novel bibenzylderiva-tives from the tubers ofBletillastriata[J].HelvChimActa, 2008, 91(3): 520-34.
[4]Lin Y L, Chen W P. Dihydrophenanthrenes form Bletilla formosana[J].ChemPharmBull,2005,53(9):1111-3.
[5]鄢艳,关焕玉,王爱民,等.黔产白及的化学成分[J].中国实验方剂学,2014,20(18): 57-60.
[5]Yan Y,Guan H Y,Wang A M,et al.Chemical constituents ofBletillaerhizome[J].ChinJExpTraditiMedForm, 2014, 20(18):57-60.
[6]楼彩霞.蒙药阿结炭止血作用及其机制研究[D].北京:中央民族大学,2010.
[6]Lou C X.Study on the hemostatic effect and mechanism of Carbonized Agei[D]. Beijing: Minzu Univ of China, 2010.
[7]王辉,刘刚,罗顺德.莲心碱对血小板聚集、凝血功能和血栓形成的影响[J].中国药理学通报, 2010,26(6): 768-72.
[7]Wang H, Liu G, Luo S D. Effect of liensinine on platelet aggregation and coagulability and thrombotic activity[J].ChinPharmacolBull, 2010, 26(6):768-72.
[8]徐思清. 白及的止血作用及其临床应用[J].内蒙古中医药, 2014, 33(31): 94.
[8]Xu S Q.Study on the hemostatic effect ofBletillastriataand its clinical application[J].NeiMongolJTraditChinMed, 2014, 33(31): 94.
[9]吕洪乐,张同华, 李倩.白及多糖药理作用的研究进展[J].中国药房,2015, 26(28):4014-6.
[9]Lyu H L, Zhang T H, Li Q.Research progress on pharmacological action ofBletillastriatapolysaccharide[J].ChinaPharm, 2015, 26(28):4014-6.
[10]鄢艳. 白及止血药效物质基础及多指标质量控制研究[D].贵阳:贵州医科大学,2013.
[10]Yan Y.Studies on the hemostatic material basis and multi-marker quality control method ofBletillastriata[D].Guiyang:Guizhou Medical University,2013.
[11]沈涛.独一味止血作用及机制的研究及其活性部位的提取分离[D].兰州:兰州大学,2006.
[11]Shen T.Study on the hemostatic effect and mechanism of lamiophlomisrotata(benth.) kudo and extraction of the effective compositions[D].Lanzhou: Lanzhou University, 2006.
[12]郭月芳,谢炜,王玉梅, 等.聚乙二醇化降纤酶对血小板聚集和凝血功能的影响[J].中国药理学通报,2011,27(4):512-5.
[12]Guo Y F, Xie W, Wang Y M, et al.Effects of PEGylated defibrase on platelet aggregation and coagulability activity[J].ChinPharmacolBull,2011,27(4):512-5.
[13]黄远铿,肖百全,欧慧瑜,等.新型止血材料纤维蛋白贴的止血作用研究[J]. 中国药理学通报,2013,29(8):1140-5.
[13]Huang Y K, Xiao B Q, Ou H Y, et al.Stypticity study of Fibrin Patch made of new homeostatic materials[J].ChinPharmacolBull, 2013,29(8):1140-5.
[14]美合日阿依·伊萨克,马虎,周文婷,等. 维药榅桲多糖抗血栓作用及其机制研究[J].中国药理学通报,2015,26(6): 768-72.
[14]Isak Mihray, Ma H, Zhou W T, et al. Anti-thrombotic effect of polysaccharide of cydoniaoblonga mill and mechamism[J].ChinPharmacolBull, 2015,26(6): 768-72.
[15]毛春芹,曾莉,陆兔林,等.川芎嗪纳米喷雾剂对大鼠腹腔粘连相关因子和纤溶系统影响的实验研究[J]. 中国药理学通报,2012,28(1):118-23.
[15]Mao C Q, Zeng L, Lu T L,et al. Effects of ligustrazinenano spray on celiac adhession related factors and fibrinolysis system in rats[J].ChinPharmacolBull,2012, 28(1):118-23.
Hemostatic effect and mechanism of a non-polysaccharide fraction ofBletillastriata
ZHAO Fei-fei1,2,YANG Xin1,3,XU Dan1,2,DONG Li1,3,LI Jing1,2,WANG Yong-lin1,3,LIAO Shang-gao1,2
[1.SchoolofPharmacy, 2.EngineeringResearchCenterfortheDevelopmentandApplicationofEthnicMedicineandTCM(MinistryofEducation), 3.GuizhouProvincialKeyLaboratoryofPharmaceutics,GuizhouMedicalUniversity,Guiyang550004,China]
AimTo understand the hemostatic effect of a non-polysaccharide fraction ofBletillastriata(BS-80EE) and to clarify its mechanism of action.MethodsThe non-polysaccharide fraction(BS-80EE) was prepared by passing the 95% ethanol extract ofBletillastriatathrough a D101 macroporous resin column eluted first with water and then with 80% ethanol. Bleeding time(BT) and clotting time(CT) of heparinized mice were employed as indicators for evaluating the hemostatic effect of BS-80EE.The mechanism of action was investigated through observing the effect of BS-80EE on platelet aggregation induced by adenosine diphosphate(ADP) in rats with nephelometry and testing the effect of BS-80EE on the thrombin time(TT), prothrombin time(PT), activated partial thromboplastin time(APTT), fibrinogen(FIB), P-selectin(P-S),thrombin-antithrombin complex(TAT), D-dimer(D-D) and plasminogen activator inhibitor-1(PAI-1) .ResultsBS-80EE significantly shortened the CT and BT(P<0.01 or 0.05) of heparin mice in a dose-dependent manner; groups of all doses significantly reduced the rat TT(P<0.01 or 0.05),and the high-dose group significantly increased the FIB content(P<0.05); the mid-dose group and high-dose groups of BS-80EE significantly increased the contents of P-S,TAT and PAI-1, while reduced the D-D production in rats(P<0.01); although dose-dependent reductions of APTT and PT were observed for each treatmentgroup, no significance was observed.ConclusionBS-80EE possess pronounced hemostatic effect by promoting platelet aggregation and coagulation.
Bletillastriata; non-polysaccharide fraction;hemostasis; platelet aggregation;bleeding time; coagulation time; mechanism
2016-03-21,
2016-04-30
国家自然科学基金资助项目(No 81360636,81460630)
赵菲菲(1991-),女,硕士生,研究方向:中药药效物质基础及作用机制,E-mail:775928773@qq.com;
廖尚高(1972-),男,博士,教授,硕士生导师,研究方向:天然药物化学、中草药药效物质基础及药物开发,通讯作者,E-mail:lshangg@163.com
A
1001-1978(2016)08-1121-06
R-332;R284.1;R331.124;R446.11;R973.1
网络出版时间:2016-7-19 10:43网络出版地址:http://www.cnki.net/kcms/detail/34.1086.R.20160719.1043.036.html

