粉防己煮散和饮片煎剂有效成分煎出率变化的比较
冀德富,诸葛增楠,梁超,王雪剑,裴妙荣
(山西中医学院,山西太原030024)
粉防己煮散和饮片煎剂有效成分煎出率变化的比较
冀德富,诸葛增楠,梁超,王雪剑,裴妙荣
(山西中医学院,山西太原030024)
目的:比较粉防己煮散与其传统饮片汤剂在煎煮过程中有效成分的含量变化。方法:对粉防己煮散和其传统饮片汤剂中有效成分总生物碱和浸膏得率进行比较研究。结果:不同时间点粉防己煮散中的总生物碱含量及出膏率均高于粉防己饮片煎液。结论:粉防己饮片制成煮散,可提高药材使用率,节省药材资源,为创新中药饮片的应用形式提供了新思路。
粉防己煮散;粉防己饮片;总生物碱;含量测定
粉防己(Stephania tetrandra S.Moore)又称汉防己、白木香、土防己等,系防己科千金藤属植物,其药用部位为根,质坚实,富粉性,性寒、味苦,归膀胱、肺经,主产于浙江、安徽、湖北、湖南、江西等地,具有祛风止痛,利水消肿等功效,临床常用于治疗风湿痹痛、水肿脚气、小便不利、湿疹疮毒、高血压等疾病[1-3]。粉防己中含有的化学成分较为复杂,主要是生物碱、黄酮、挥发油、多糖等,其中的生物碱类成分为其主要药效物质。中药煮散是指将中药材粉碎成一定粒度与水共煎,去渣取汁或带渣服用的中药液体制剂。它保持了传统汤剂的煎煮过程和疗效,能够很好地适应病情需要、随证加减,具有传统汤剂吸收快、疗效高的优点[4-5]。中药煮散历史悠久,源于先秦,定名于唐,鼎盛于宋,延续至今。通过将药材粉碎,制成煮散,有利于提高药材生物利用度,减少药材使用量,具有省材省时之特点[6-9]。本实验在传统中药煮散理论指导下,以粉防己为研究对象,比较其粉末和饮片在煎煮过程中主要药效成分总生物碱的含量变化,旨在为后续开发新型中药饮片的形式奠定良好基础。
1 实验材料
1.1 实验仪器
UV1601型紫外可见分光光度计(北京瑞利分析仪器有限公司);AB-135S十万分之一电子天平(METTLER梅特勒公司),FA2104型电子分析天平(上海第二分析仪器厂);BGZ-76型电热鼓风干燥箱。
1.2 药物与试剂
粉防己饮片购于安国市万联中药饮片有限公司,经山西中医学院牛燕珍老师鉴定为正品;粉防己碱对照品(批号AS 518-23-1)购于成都思科华生物技术有限公司;溴甲酚绿试液(精密称取溴甲酚绿0.05 g,邻苯二甲酸氢钾1 g,用0.2moL/L氢氧化钠溶液6mL溶解,加水稀释至100mL,即得)、0.5moL/LNaOH(精密称取2 g NaOH,加水溶解定容于100mL容量瓶中,即得)、0.2moL/LNaOH(精密称取0.4 g NaOH,加水溶解定容于50mL容量瓶中,即得)、0.5 moL/L盐酸(精密移取4.2mL的浓盐酸于100mL容量瓶中,加水定容即得);氯仿等为分析纯,水为蒸馏水。
2 方法与结果
2.1 煮散和饮片煎剂的制备
2.1.1 煮散的制备精密称取粉防己最粗粉(即通过1号药筛但不能通过2号药筛的颗粒)各5 g,共6份,无纺布袋包裹,加水100mL浸泡20min后进行煎煮,分别在煮沸10min、20min、30min、45min、60min、90min后过滤,滤液定容于100mL容量瓶中,即得不同时间点的煮散样品液M1~6。
2.1.2 饮片煎剂的制备精密称取粉防己饮片各5 g,共6份,包裹、浸泡、煎煮方式同2.1.1项,煎液定容于100mL容量瓶中,即得不同时间点的饮片煎剂样品液N1~6。
2.2 粉防己煮散和饮片煎剂不同时间点总生物碱煎出率
2.2.1 对照品溶液的制备精密称取粉防己碱对照品4.06mg,加氯仿溶解定容于10mL量瓶中,摇匀,即得0.406mg/mL的对照品溶液。
2.2.2 供试品溶液的制备精密吸取M3样品液10 mL水浴蒸干,用0.5moL/L盐酸10mL溶解,过滤至分液漏斗中,用氯仿萃取3次,每次5mL,弃去氯仿层。酸水层用0.5 moL/L氢氧化钠调节pH至10,接着用氯仿萃取3次,每次5mL,合并氯仿层并水浴挥干至小体积,转移至10mL量瓶中,少量多次润洗,定容至刻度。精密移取5 mL于分液漏斗中,加溴甲酚绿试液5 mL,充分振摇使分层,静置40min,收集氯仿层于10 mL量瓶中,加氯仿定容,即得供试品溶液。同法制得试剂空白溶液。
2.2.3 最大吸收波长的确定吸取“2.2.1”项下粉防己碱对照品溶液1mL,置10mL量瓶中,氯仿定容。再移取上述溶液5mL于分液漏斗中,精密加溴甲酚绿试液5mL,充分振摇使分层,静置40min,收集氯仿层于10mL量瓶中,氯仿定容至刻度。以不加对照品液及样品液的三氯甲烷作空白,用紫外分光光度计在300~800 nm的范围内进行扫描,波长扫描图见图1,结果表明对照品溶液在416 nm处有最大吸收。对供试品进行同样的紫外光谱扫描,结果显示在(416±2)nm处有最大吸收,波长扫描图见图2,因此确定416 nm为测定波长。
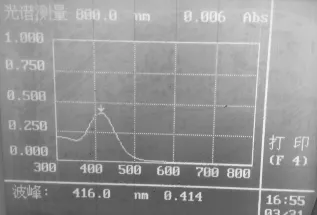
图1 粉防己对照品显色液扫描图
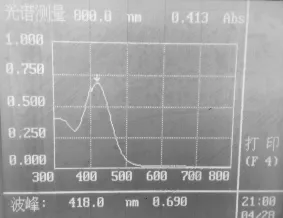
图2 供试品显色液扫描图
2.2.4 标准曲线的绘制分别精密移取对照品溶液0.2mL,0.4mL,0.6mL,0.8mL,1.0mL,1.2mL,置10mL量瓶中,氯仿定容。再分别移取上述溶液5mL于分液漏斗中,精密加溴甲酚绿试液5 mL,充分振摇使分层,静置40min,分取氯仿层于10mL量瓶中,氯仿定容至刻度,即得浓度分别为4.06μg/mL,8.12μg/mL,12.18μg/mL,16.24μg/mL,20.30μg/mL,24.36μg/mL的对照品溶液。以相应的试剂为空白,于416 nm波长处测定吸光度。以吸光度(Y)为纵坐标,粉防己碱含量(X)为横坐标,绘制标准曲线,计算回归方程为Y=0.029 1X+0.266 4(R=0.999 6)。结果表明,粉防己碱在4.06μg/mL~24.36μg/mL范围内与吸光度呈良好的线性关系。
2.2.5 精密度试验精密移取“2.2.1”项下粉防己碱对照品溶液(0.406mg/mL)1mL,按“2.2.4”项下方法测定吸光度,结果吸光度的RSD为0.15%(n=6),表明仪器精密度良好。
2.2.6 稳定性试验精密移取M3样品6 mL,按“2.2.2”项下方法制备供试品溶液,按“2.2.4”项下方法测定吸光度,依法显色后于0、20 min、40 min、60 min、75 min、90 min测定吸光度。结果随着时间的延长吸光度值减小,但减小的幅度不大,RSD为2.23%(n=6),表明样品液显色后在1.5 h内稳定。
2.2.7 重复性试验精密移取M3样品6 mL,按“2.2.2”项下方法平行制备6份供试品溶液,测定吸光度值,计算总生物碱的煎出率,结果总生物碱的平均煎出率为0.478 mg/g,RSD为2.37%(n= 6),表明本方法重复性良好。
2.2.8 回收率试验精密移取M3样品6份,每份3 mL(含总生物碱0.478mg/g),每份分别加入粉防己碱对照品溶液(40.60μg/mL)3 mL,按“2.2.2”项下方法平行制备6份供试品溶液,测定吸光度值,计算回收率,结果回收率分别为96.21%、95.72%、97.13%、95.79%、98.18%、96.15%,平均回收率为96.53%,RSD为1.96%。
2.2.9 样品测定分别精密移取粉防己煮散及饮片煎剂不同时间点的样品溶液M1~6和N1~6各10 mL,按“2.2.2项下的方法制备显色液,测定吸光度值,计算不同时间点煎液中总生物碱的煎出率,结果见表1。
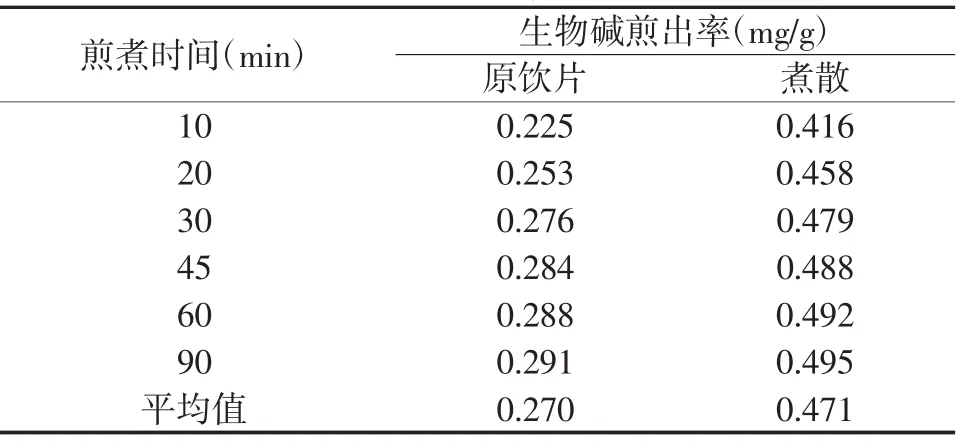
表1 煎煮不同时间总生物碱的煎出测定结果
结果表明,不同时间点粉防己煮散的总生物碱煎出量均高于粉防己原饮片煎液,粉防己煮散的总生物碱平均煎出量是原饮片的1.74倍。
2.3 样品出膏率的测定
精密移取粉防己饮片及煮散不同时间点的样品溶液M1~6和N1~6各20mL,分别置已恒重的蒸发皿中水浴蒸干,于105℃烘箱中干燥3 h,取出后置干燥器中冷却30min后,迅速精密称定质量,计算浸膏得率,结果见表2。
结果表明,不同时间点粉防己煮散的总煎出物的煎出率均高于粉防己原饮片煎液,粉防己煮散的总煎出物平均煎出量是原饮片的1.61倍。
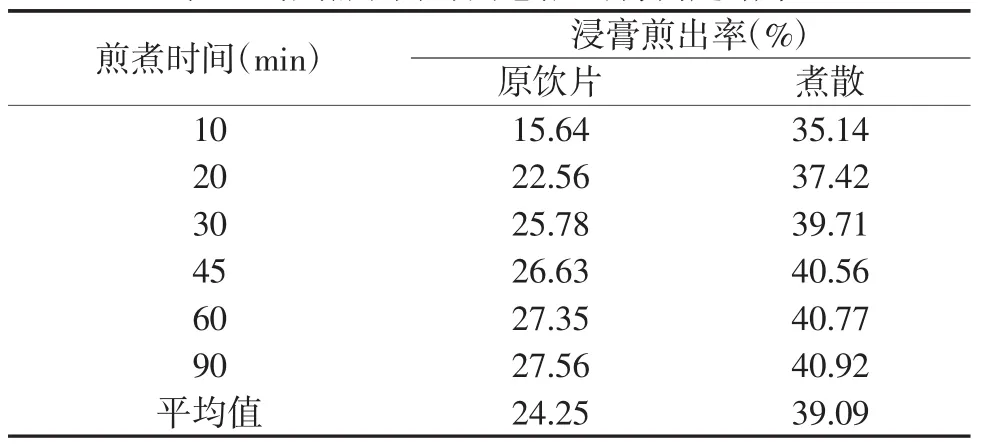
表2 煎煮不同时间总煎出物测定结果
3 讨论
根据扩散定律,扩散速度即单位时间内扩散物质(药材成分)的量与扩散表面积成正比,与扩散物质的粒子半径成反比,颗粒越小,表面积越大,与浸出溶媒的接触面愈大,扩散物质的量也就愈多。因此,同等的煎煮条件,煮散剂的煎出率会高于传统饮片汤剂[10]。预实验时我们曾对粉防己不同粉碎粒度的粉末即最粗粉(10目)、粗粉(24目)、中粉(65目)和细粉(80~100目)均进行了煎煮考察,结果发现将药材粉碎成最粗粉时,经测定,煎液中总生物碱的煎出率不及粗粉、中粉和细粉煎出液中的高,但是用粗粉、中粉和细粉制备的煮散,煎出液黏度较大,过滤难度加大,且药材粉碎的细,需要较大的能耗和设备,药材损失量亦增大,故本文选择制备粉防己煮散的药材粉碎粒度为最粗粉。
通过对比研究粉防己煮散与原饮片不同时间点指标成分总生物碱和浸膏煎出量的差异,进一步证实了应用中药煮散具有煎出率高,节省药材,煎煮时间短,节省能源等优势。提倡建立煮散标准化研究,如确定适宜煮散的入煎药材、药材粒度、规范生产、包装储存、控制质量等,发展煮散实用性,为解决当下中药材资源匮乏、药价偏高等问题提供良好的途径。
[1]嵇远洋,张水冰.防己的临床应用及肾毒性概述[J].新中医,2003,35(8):74-75.
[2]国家药典委员会.中华人民共和国药典[S].北京:中国医药科技出版社,2015:149-150.
[3]钟赣生.中药学[M].北京:中国中医药出版社,2012:173-174.
[4]穆兰澄,曹京梅,李冀湘,等.中药煮散的历史沿革与现代研究概述[J].中国实验方剂学杂志,2008,14(7):74-75.
[5]江泳,冯欣,杨殿兴,等.对中药煮散剂现状的认识与思考[J].四川中医,2010,28(5):69-71.
[6]丁青龙,李莹,丁舒,等.中药生药颗粒剂与传统饮片及免煎颗粒临床疗效比较研究[J].吉林中医药,2008,28(7):530.
[7]张晓平,薛秋红,王婉钢,等.复方芪丹袋煮散治疗脑出血后遗症56例临床研究[J].中医杂志,2001,42(12):727-728.
[8]沙汉玲,李艳华.消银1号煮散剂治疗银屑病120例[J].湖北中医杂志,2000,22(10):24.
[9]陈金月,王力宁,刘倩,等.实验与数学计算结合建立麻杏二陈煮散剂量换算公式[J].时珍国医国药,2013,24(2):407-408.
[10]穆兰澄,牟稽征,何怡,等.复方煮散与传统饮片汤剂煎出率的比较[J].辽宁中医药大学学报,2012,14(3):211-212.
(编辑:张世霞)
Com parison of active ingredient content changes between Stephania tetrandra S.M oore powder and decoction pieces of Stephania tetrandra S.M oore in the process of decoction
JiDefu,Zhuge Zengnan,Liang Chao,Wang Xuejian,PeiMiaorong
(ShanxiCollege of Traditional Chinese Medicine,Taiyuan Shanxi030024)
Objective:To compare the content of active ingredients between Stephania tetrandra S.Moore powder and decoction pieces of Stephania tetrandra S.Moore in the process of decoction.Methods:The UV method was used for the determination of the content of total alkaloid changes in Stephania tetrandra S.Moore powder and decoction pieces of Stephania tetrandra S.Moore at various decoction time.The comparative studies of active ingredients extract rate and dry extract rate weremade.Results:The content of total alkaloid and dry extract rate in Stephania tetrandra S.Moore powder were both greatlymore than those in decoction pieces of Stephania tetrandra S.Moore.Conclusion:Stephania tetrandra S. Mooremade from powder can savematerial,which providesapplication form of traditional Chinesemedicinewith innovative ideas.
powder-decocting of Stephania tetrandra S.Moore;decoction pieces of Stephania tetrandra S.Moore;total alkaloid;determination of content
R285
A
1671-0258(2016)06-0019-03
冀德富,硕士,讲师,E-mail:jdfaaa@126.com
裴妙荣,教授,博士生导师,E-mail:peimr602@163.com

