颈椎康热融压敏胶贴质量控制研究
康阿龙,王卫峰,汤迎爽
(1.解放军第四五一医院,西安 710054;2.陕西省中医药研究院中药研究所,西安 710003;3.解放军第三二三医院,西安 710054)
Study on the quality control method for Jingzhuikang Plaster based on hot-melt pressure sensitive adhesives
颈椎康热融压敏胶贴质量控制研究
康阿龙1,王卫峰2,汤迎爽3*
(1.解放军第四五一医院,西安710054;2.陕西省中医药研究院中药研究所,西安710003;3.解放军第三二三医院,西安710054)
摘要:目的 建立颈椎康热融压敏胶贴的质量检测方法。方法 采用专属性薄层色谱法鉴定方中4味主药;高效液相色谱法检测该药中的主要指标成分葛根素含量。色谱条件:色谱柱:Diamonsil C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水(25∶75);流速:1.0 mL·min-1;检测波长:250 nm;柱温:室温。结果 薄层鉴别斑点清晰,分离效果良好,空白无干扰;葛根素含量在0.101 6~1.101 6 μg范围内线性关系符合要求(r=0.999 7),方法加样回收率为100.4%,RSD为2.17%(n=6)。结论 经研究建立的方法,可作为该药的质量检测手段。
关键词:葛根素;颈椎康热融压敏胶贴;质量标准; HPLC;TLC
Study on the quality control method for Jingzhuikang Plaster based on hot-melt pressure sensitive adhesives
颈椎病是以颈椎退行性改变为基础的一种临床常见病、多发病[1],近年来,有逐年增多和年轻化的趋势[2],颈椎康贴作为传统膏药在民间习用多年,我们应用现代制剂技术[3-4],将其研制成一种以SIS为骨架材料的热熔压敏胶贴。该方由葛根、肉桂、杜仲、当归、山茱萸、花椒等11味中药组成,具有温里散寒、散风止痛的功效,用于治疗风湿瘀阻所致颈椎疼痛、颈项僵硬、肩背酸痛、头晕等症状,疗效确切。为控制其质量,按照药品注册要求,本文建立了4味主药的薄层鉴别方法,色谱斑点清晰,阴性无干扰;建立的HPLC法检测指标成分葛根素含量,操作简便,重复性好。
1仪器与试药
1.1仪器高效液相色谱仪(2690型泵,996型PDA紫外可见检测器,VP化学工作站,Waters 公司)。电子分析天平(北京赛多利斯天平有限公司,型号:BT25S,d=0.01 mg;BS210S,d=0.1 mg)。
1.2试药葛根素对照品(供含量测定用,批号100752-200912),杜仲对照药材(TLC用,批号121202-201103),当归对照药材(TLC用,批号120927-201315),熊果酸对照品(供含量测定用,批号110742-201421),山茱萸对照药材(TLC用,批号121495-201303),葛根对照药材(TLC用,批号121551-201103),均购自中国食品药品检定研究院;颈椎康贴(规格:每贴2 g,陕西安和医药科技有限公司生产,批号:20130308,20131201,20131209)。HPLC测定试剂为色谱纯;其他提取处理试剂为分析纯。
2方法与结果
2.1薄层色谱鉴别2.1.1杜仲的薄层鉴别 取本品2贴,揭去背衬,剪碎,置于具塞锥形瓶中,加无水乙醇50 mL,放置30 min,超声提取30 min,滤过并浓缩至约2 mL,即为供试品溶液。另取杜仲对照样品1 g,采用与供试品相同的方法处理,得对照药材溶液,再按照处方比例称取所有药材(除去杜仲),按照样品制备方法制得空白样品,按照供试品溶液制备过程处理得到空白对照溶液。依照现行版《中国药典》TLC实验法,分别吸取供试品溶液、空白对照溶液各10 μL和对照药材溶液5 μL,分别点于同一含CMCNa的硅胶G板上,展开剂:正己烷-乙酸乙酯(9∶2),取出晾干后,在紫外光灯(365 nm)下观察。供试品色谱中,在与对照药材相应位置,显一致的荧光斑点,空白对照溶液未显相同斑点,说明空白不存在干扰。见图1。
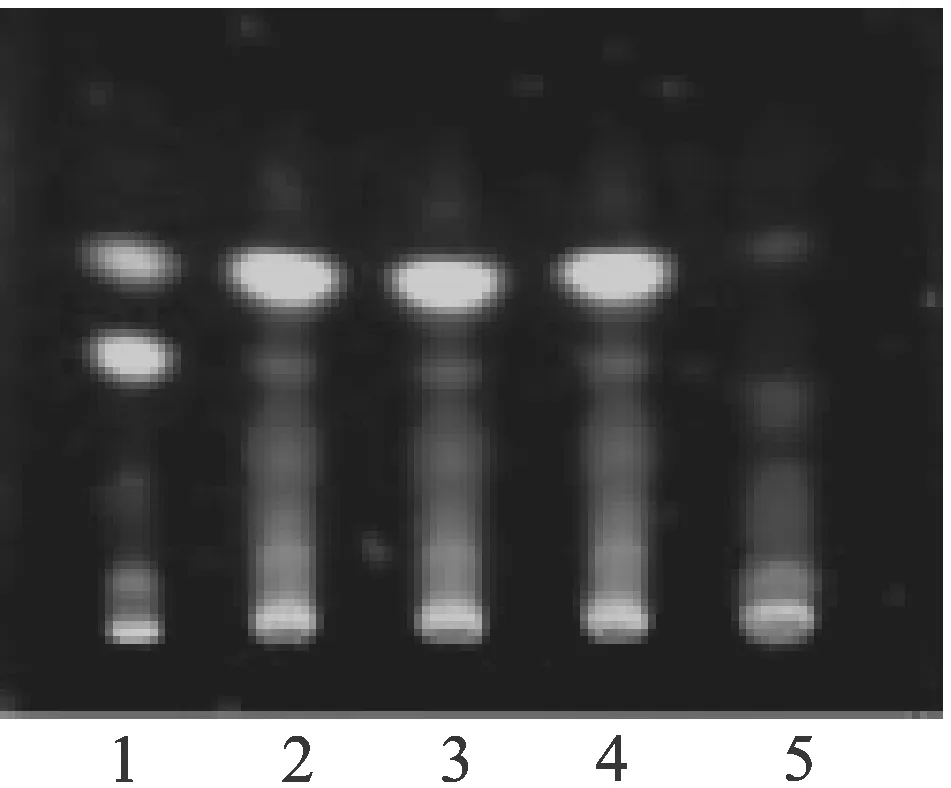
图1 杜仲TLC图
1.杜仲药材;2~4.供试品;5.阴性对照
Fig.1 TLC ofEucommiaecortex
1.Eucommiaecortex;2-4.test sample;5.negative control
2.1.2当归的薄层鉴别 取本品2贴,揭去背衬,剪碎,置于锥形瓶中,加乙醚40 mL,静置30 min,超声处理10 min,离心,上清液自然挥干,残留物用1 mL乙醇溶解,即为供试品溶液。另取当归对照药材样品1 g,采用与供试品相同的方法处理,得对照药材液,再按处方比例称取所有药材(除当归),按照样品制备方法制得空白样品,继续按照供试品溶液制备过程处理得空白对照溶液。依照现行版《中国药典》TLC实验法,分别吸取供试品溶液、空白对照溶液各10 μL和对照药材溶液5 μL,分别点于同一含CMCNa的硅胶G板上,展开剂-正己烷-乙酸乙酯(4∶1),取出晾干后,在紫外光灯(365 nm)下观察。供试品色谱在与对照药材相应的位置,显一致的荧光斑点,空白对照溶液未显相同斑点,说明空白不存在干扰。见图2。

图2 当归TLC图
1.当归药材;2~4.供试品;5.阴性对照
Fig.2 TLC ofAngelicaesinensisradix1.Angelicaesinensisradix;2-4.test sample;5.negative control
2.1.3山茱萸的薄层鉴别 取本品2贴,揭去背衬,剪碎,置于锥形瓶中,加乙酸乙酯20 mL,静置30 min,超声提取15 min,滤过并蒸干,残留物用1 mL无水乙醇溶解,即得供试液。将熊果酸对照品用无水乙醇溶解制成质量浓度为1 mg·mL-1的对照品溶液;取山茱萸对照药材1 g,采用与供试品相同方法处理,得对照药材溶液;再取除山茱萸外处方其余所有药材,按照样品制备方法制得阴性样品,再按照供试品处理方法制得空白对照溶液。依照现行版《中国药典》TLC实验法,吸取对照品溶液、对照药材溶液各5 μL和供试品溶液及空白对照溶液各10 μL,分别点于同一含CMCNa的硅胶G板上,展开剂:甲苯-乙酸乙酯-甲酸(20∶2.5∶0.5),取出晾干后,喷适量体积分数为10%的硫酸乙醇溶液,热风吹至斑点显色。供试品色谱图中,与对照品、对照药材色谱对应位置,显示一致的斑点,空白对照液未显相同斑点,说明空白不存在干扰。见图3。

图3 山茱萸TLC图
1.熊果酸对照液;2.山茱萸对照药材液;3~5.供试液;6.空白对照液
Fig.3 TLC ofCornifructus1.malol control;2.Cornifructus;3-5.test sample;6.negative control
2.1.4葛根的薄层鉴别 取本品2贴,揭去背衬,剪碎,置于三角瓶中,加入30 mL乙酸乙酯,放置30 min,超声提取20 min,滤过并蒸干,残留物用1 mL甲醇溶解,即得供试品溶液。采用与供试品相同的方法处理制得对照药材溶液,将适量葛根素用适量甲醇溶解制成质量浓度为1 mg·mL-1的对照品溶液,再按处方比例称取所有药材(除去葛根),按样品制备方法制得空白样品,再按供试液制备过程制成空白对照溶液。依照现行版《中国药典》TLC实验法,分别吸取对照品溶液2 μL、对照药材溶液、供试品溶液及空白对照溶液各5 μL,分别点于同一含CMCNa的硅胶G板上,展开剂:氯仿-甲醇-水(7∶2.5∶0.25),取出晾干后,用氨蒸汽熏蒸30 min,挥去氨气,在紫外光灯(365 nm)下观察。供试品色谱中,在与对照品及对照药材色谱相同位置,显示一致的荧光斑点,而空白对照溶液未显相同斑点,说明空白不存在干扰。见图4。
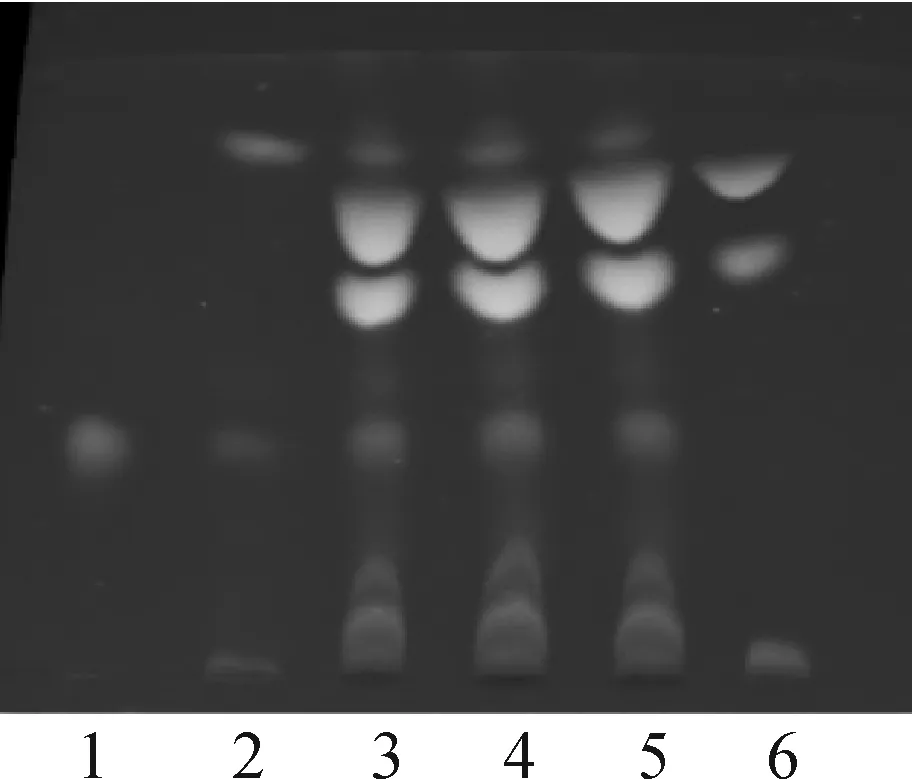
图4 葛根TLC图
1.葛根素对照品液;2.葛根对照药材液;3~5.供试液;6.空白对照液
Fig.4 TLC ofPuerariaeradix1.puerarin control;2.Puerariaeradix;3-5.test sample;6.negative control
2.2含量测定
2.2.1色谱条件 色谱柱:Diamonsil C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水(25∶75);流速:1.0 mL·min-1;检测波长:250 nm;柱温:室温;进样量:10 μL。 以葛根素色谱峰计算,理论塔板数应不低于4 000。
2.2.2实验用溶液的制备(1)对照品溶液:精密称取葛根素对照品12.7 mg,置于25 mL量瓶中,加体积分数为30%的乙醇至刻度,摇匀,作为对照品储备溶液。(2)供试品溶液:取本品,揭去背衬,剪碎,取4 g,精密称定,放入具塞锥形瓶中,精密吸取体积分数为30%的乙醇溶液50 mL加入,密塞,精密称定,回流提取30 min,冷却后,再次精密称定,减失质量用体积分数为30%的乙醇补足,混匀,量取适量提取液,以4 000 r·min-1离心处理5 min,取上清液,用0.45 μm微孔滤膜滤过,取续滤液,即得。(3)阴性对照溶液:取除葛根外处方中其余所有药材,按照样品制备方法制得葛根空白试样,再以供试品溶液制备过程制成葛根阴性对照液。
2.2.3系统适用性及干扰性实验 精密抽取2.2.2项下3种溶液各10 μL,注入液相色谱仪中,按照2.2.1 项下色谱条件进样测定。结果显示,颈椎康热融压敏贴供试液色谱与葛根素对照液色谱峰在相同位置有相应的色谱峰,而阴性对照溶液在相应位置无吸收峰,表明阴性无干扰,葛根素保留时间约为28 min,分离度大于1.5,结果见图5。
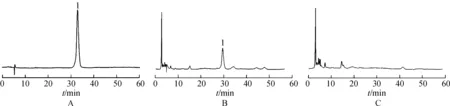
图5 颈椎贴HPLC图
A.对照品溶液;B.供试品溶液;C.阴性对照溶液;1.葛根素
Fig.5 HPLC chromatograms of Jingzhuikang Plaster
A.reference substance;B.test sample;C.negative control;1.puerarin
2.2.4线性关系考察 精密称取葛根素对照品12.7 mg,置于25 mL量瓶中,加体积分数为30%的乙醇至刻度,摇匀,再精密量取1.0 mL上述溶液,置于10 mL量瓶中,加体积分数为30%的乙醇溶液至刻度,混匀,制得含葛根素0.050 8 mg·mL-1的溶液,作为对照品溶液;分别精密吸取2,4,8,12,16和20 μL,注入液相色谱仪,测定峰面积,并以峰面积对进样量进行回归,得回归方程:Y=6 511 614.25X-71 358.54,r=0.999 7,线性范围为0.101 6~1.101 6 μg。
2.2.5精密度实验 精密抽取葛根素对照品溶液10 μL,依次进样6次,分别测得葛根素的峰面积。结果RSD为0.97%,仪器精密度符合规定。
2.2.6稳定性实验 将同一批号(20130308)供试品溶液,放置0,2,4,6,8和10 h,在不同时间各抽取10 μL,进样,注入液相色谱仪,测定其峰面积,结果RSD为0.79%,在10 h内稳定性良好。
2.2.7重复性实验 取同一批号(20130308)样品6份,揭去背衬,剪碎,每份样品4.0 g,精密称定质量,置于具塞锥形瓶中,精密加入体积分数为30%的乙醇溶液50 mL,密塞,精密称定,回流提取30 min,放冷,再精密称定,用体积分数为30%的乙醇溶液补足减失质量,混匀,抽取适量提取液,以4 000 r·min-1离心5 min,取上清液,用0.45 μm微孔滤膜滤过,精密吸取续滤液10 μL,注入液相色谱仪,测定葛根素含量,结果平均含量为0.462 0 mg·g-1,RSD为0.95%(n=6),结果表明重复性良好。
2.2.8加样回收率实验精密称取葛根素对照品10.16 mg,置于25 mL量瓶中,加体积分数为30%的乙醇溶液至刻度,摇匀,配制成1 mL含葛根素0.406 4 mg 的对照品溶液。另精密称取已知含量(0.462 mg·g-1)的样品共6份,每份约2 g,置于具塞锥形瓶中,分别加入质量浓度为0.406 4 mg·mL-1的葛根素对照品溶液2.5 mL,以供试品溶液制备过程制得加样回收供试品溶液,分别精密抽取10 μL,注入液相色谱仪,测定,结果见表1。结果表明,葛根素平均回收率为100.4%,RSD为2.17%。
表1葛根素回收率实验结果
Tab.1 Results of phenol recovery tests
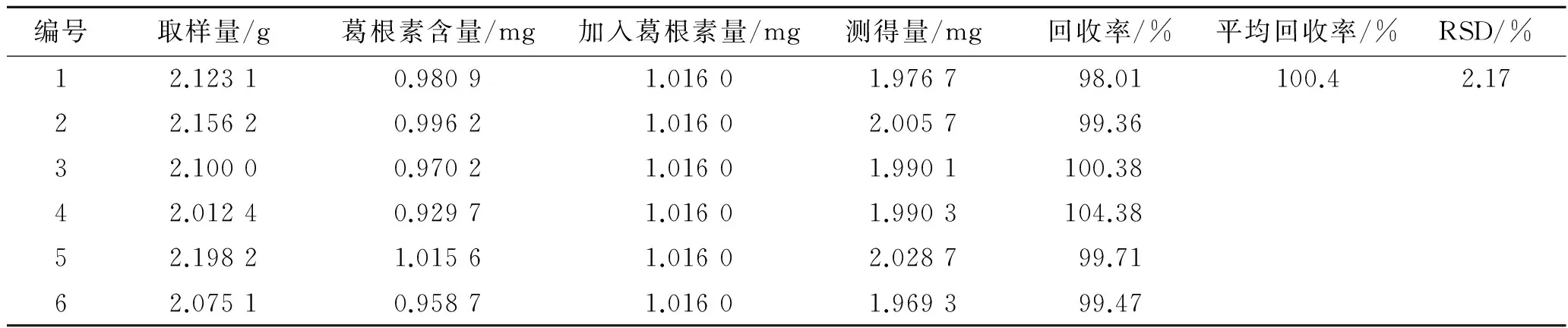
(n=6)
2.2.9样品测定 分别精密称取3批中试样品4 g,按照2.2.6项下制备过程制备供试品液,按照2.2.1项下色谱条件进样检测,结果批号20130308,20131201和20131209的3批贴剂中葛根素含量分别为:0.460,0.475和0.468 mg·g-1。2.2.10含量限度 根据3批中试样品中葛根素含量,结合药材的含量限度[5],制备过程的转移率,确定其限度为含葛根以葛根素(C21H20O9)计不得少于0.3 mg·g-1。
3讨论
该制剂属外用贴膏剂,赋型剂为压敏胶,参考文献[6]选用硅藻土分散除胶,但效果不理想,后采用不加硅藻土,直接剪碎,用有机溶剂浸泡,再经超声或加热回流即可提取出指标成分,且胶质未被提出,对样品鉴别或测定没有影响。
杜仲主要含木脂素类、萜类、黄酮类、酚酸类成分[7],现行药典中没有收载杜仲的TLC法,文献报道[8-9]的鉴别方法主要以京尼平苷、松脂醇二葡萄糖苷等木脂素成分为对照,操作复杂,色谱效果不佳,本文建立的鉴别方法,以杜仲对照药材为对照,主要提取其萜类等脂溶性成分,操作简便,色谱斑点清晰,分离度好,可为其他含杜仲制剂的鉴别提供参考。
葛根素含量及限度标准存在一定差异[10-13],现行版药典中葛根药材含量限度规定为不少于2.4%,葛根芩连丸中葛根素含量限度为4.5 mg·g-1,经计算,其限度仅为理论值(1 000÷300×2.4%=79.92 mg·g-1)的5.6%,无法发挥控制其质量的作用,有必要对其提取转移率进行研究。而梗心舒胶囊中葛根素限度却定得太高[14],实际值为61.4 mg·粒-1,限度定为不少于60 mg·粒-1,实际生产样品很难合格。合理的含量限度的确定,需参考药材提取或粉碎过程中的实际转移率[15],还需考虑实际样品所测成分的稳定性,本文综合考虑了两方面因素,一是3批样品实测平均值0.468 mg·g-1,二是工艺研究中葛根素在粉碎提取等加工过程中的转移率(84%)。计算:0.015 g×1 000×0.024×0.83=0.302 4 mg·g-1,暂定限度为不少于0.30 mg·g-1。是实测结果的64.1%(0.30 mg·g-1÷0.468 mg·g-1×100%=64.1%),与实测结果相符,可有效控制其质量。
参考文献:
[1]黄明亮.中医内治法治疗颈椎病研究简况[J].实用中医内科杂志,2014,28(5):181-183.
[2]王慧芳,程少丹,徐洪亮,等.颈椎病中医综合治疗进展[J].实用疼痛学杂志,2014,10(1):68-71.
[3]闫小平,郑蕊,官仕杰,等.伤湿止痛热熔压敏贴膏质量标准研究[J]. 中国实验方剂学杂志,2012,18(6):66-68.[4]霍宁波,汪晴.几种中药浸膏压敏胶贴片的研究[J]. 中医外治杂志,2006,15(2):3-6.
[5]国家药典委员会.中国药典2010年版[S]. 一部.北京:中国医药科技出版社,2010:312-313.
[6]颜晓航,薛玉梅. 小儿健脾贴膏质量标准研究[J].中国药业,2011,20(23):26-27.
[7]马博,张媛,张达义,等.杜仲的化学成分及其药理作用研究进展[J].西部中医药,2013,26(12):153-157.
[8]宣振华,刘毅.杜仲壮骨丸中杜仲的薄层鉴别研究[J].维吾尔医药,2013,14(6):223.
[9]刘玲,鲍家科.杜仲药材薄层色谱鉴别研究[J].中国民族民间医药,2014,23(2):8-9.
[10]李新中,趣韶,苏世奇.对2000年版《中国药典》(一部)中部分中成药含量限度的商榷[J].中国药房,2001,12(12):762.
[11]毕见福,孙桂明.对《中国药典》中药有效成分含量测定的商榷[J].中国药品标准,2013,14(6):411-414.
[12]冯维希,胡虹,张爱丽,等.HPLC法测定云台山葛根不同部位葛根素的含量[J].西北药学杂志,2007,22(3):110-111.
[13]耿庆光,宇建华,林英旭,等.HPLC法测定野葛中葛根素含量的不确定度分析[J].西北药学杂志,2007,22(3):9-11.
[14]肖志强,杨建刚,王天,等.HPLC法测定梗心舒胶囊中葛根素的含量[J].陕西中医,2014,35(2):228-229.
[15]杨建冬,李存金,陈厚平,等.维C银翘片中绿原酸含量限度的制定与探讨[J].江西中医学院学报,2006,18(3):46-47.
作者简介:康阿龙,男,主任药师
*通信作者:汤迎爽,女,副主任药师
doi:10.3969/j.issn.1004-2407.2016.04.010
中图分类号:R284
文献标志码:A
文章编号:1004-2407(2016)04-0360-04
(收稿日期:2015-09-15)
KANG Along1,WANG Weifeng2,TANG Yingshuang3*
(1.The Hospital 451 of PLA, Xi′an 710054,China;2.Institute of Chinese Medicine,Shaanxi Provincial Institute of Traditional Chinese Medicine,Xi′an 710003,China;3.The Hospital 323 of PLA,Xi′an 710054,China)
Abstract:ObjectiveTo establish a quality standard for Jingzhuikang Plasterbased on hot-melt pressure sensitive adhesives. MethodsEucommiae cortex,Angelicae sinensis radix,Corni fructus and puerariae radix were identified by TLC. The content of puerarin in Jingzhuikang Plaster was determined by HPLC.Diamonsil C18(250 mm×4.6 mm,5 μm) column was used.The mobile phase consisted of methanol-water(25∶75) at normal flow rate.The detection wavelength was set at 250 nm. ResultsThe spots in TLC were clear.Puerarin showed a good linear relationship within the range of 0.101 6-1.101 6 μg(r=0.999 7).The average recovery was 100.4%,and the RSD was 2.17%(n=6). ConclusionThe established methods can be used for Jingzhuikang Plaster quality control.
Key words:puerarin;Jingzhuikang Plaster based on hot-melt pressure sensitive adhesives;quality control; HPLC;TLC

