重组人血管内皮抑素联合化疗治疗中晚期非小细胞肺癌的临床观察
王加保 唐成武 冯文明湖州师范学院附属第一人民医院外科,浙江湖州 313000
重组人血管内皮抑素联合化疗治疗中晚期非小细胞肺癌的临床观察
王加保唐成武▲冯文明
湖州师范学院附属第一人民医院外科,浙江湖州313000
[摘要]目的观察重组人血管内皮抑素(恩度)对中晚期非小细胞肺癌的疗效。 方法 回顾性分析2008年5月~2011年5月间我院65例中晚期非小细胞肺癌临床资料。其中GP组32例接受GP方案化疗[(吉西他滨1000 mg/m2,d1+d8)、顺铂(20 mg/m2,d1~5)];联合组33例在GP方案基础上同时加用恩度(15 mg/d,d1~14)。两组患者均接受4~6周期化疗。观察比较两组患者近期疗效、功能状态评分、不良反应及生存率。结果联合组近期疗效明显优于GP组(P=0.0390),联合组总有效率明显优于GP组(P=0.0467);两组在不良反应方面无明显差异,均无化疗相关性死亡病例发生;化疗结束3个月后联合组KPS评分明显优于GP组[(91.52±11.25)vs(85.74±10.97),(P= 0.0401)];GP组3年生存率21.88%,联合组3年生存率27.27%,联合组明显高于GP组(P=0.0425)。 结论恩度联合GP方案化疗治疗晚期非小细胞肺癌可明显提高临床疗效,提高生存率,且耐受性好,值得临床推广应用。
[关键词]非小细胞肺癌;化疗;重组人血管内皮抑素;生存率
近年来在全世界范围内肺癌每年的发病率都处于恶性肿瘤的首位,对人类的健康和生命产生了严重的威胁。在全部的肺癌患者中,非小细胞肺癌占80%左右[1,2],由于非小细胞肺癌的早期临床表现并不明显,很难在早期诊断发现,因此在就诊时已经是中晚期,甚至失去手术机会,所以现阶段中晚期非小细胞肺癌的首选治疗方法仍然是化疗[3]。但迄今为止,化疗有效率还不尽如人意,近年来有学者发现重组人血管内皮抑素可有效地抑制肿瘤血管的生成,并逐渐成为目前恶性肿瘤治疗的新策略[4]。本研究采用重组人血管内皮抑素(恩度)联合GP方案化疗(吉西他滨和顺铂)联合治疗中晚期非小细胞肺癌,取得显著的效果,现报道如下。
▲通讯作者
1 资料与方法
1.1一般资料
选取2008年5月~2011年5月65例肺癌患者,纳入标准:①非小细胞肺癌经临床病理诊断成立,未接受任何放化疗或抗肿瘤治疗;②临床分期处于Ⅲb~Ⅳ的患者;③功能状态评分(KPS)≥70分;④化疗结束后存活期>3个月。排除标准:有严重器官功能障碍的患者。其中男48例,女17例;年龄56~78岁。两组患者的一般资料、吸烟史、所接受的化疗周期数、病理类型和肿瘤分期等方面差异无统计学意义(P>0.05),具有可比性。见表1。
1.2治疗方法
根据化疗方案将患者分两组:GP组32例接受GP方案化疗[吉西他滨(江苏豪森药业股份有限公司,规格:200 mg/支,国药准字H20030104;顺铂(江苏南京制药厂有限公司,规格:20 mg/(20 mL·支),国药准字H20030675)][(吉西他滨1000 mg/m2,d1+d8)、顺铂(20 mg/m2,d1~5)];联合组33例在GP方案基础上同时加用恩度(15 mg/d,d1~14)[山东先声麦得津生物制药有限公司,规格:15 mg/(3 mL·支),国药准字S20050088],两组患者均接受4~6周期化疗,每3周为1个周期。化疗期间给予止吐止痛等对症支持治疗,观察记录不良反应发生情况。根据NCI化疗反应评价标准将化疗不良反应分为4度:1度为轻度不良反应,2度为中度不良反应,3度为严重不良反应,4度为危及生命的不良反应。如发生3度以上不良反应,下一次化疗可最多推迟3个星期,直到患者恢复,且中性粒细胞计数超过1.5×109/L、血小板计数超过100×109/L。如出现化疗相关的严重的心脏或神经中枢不良反应或3~4度过敏反应则化疗终止。
1.3化疗有效率判定标准及随访
化疗有效率根据RECIST标准[5]进行评估。完全缓解(CR):病灶完全消失状态持续4周以上;部分缓解(PR):病灶的最大径减小>30%状态持续4周以上;病情稳定(SD):介于PR和PD之间;病情进展(PD):病灶最大径增加≥20%,或出现肺内转移或者全身转移。总有效率(RR)=(CR+PR)/总例数×100%。患者结束化疗后均每月接受随访,直至死亡,比较两组长期生存率。评估比较化疗前及化疗结束3个月后的KPS评分,KPS评分标准:正常,无症状和体征100分;能进行正常活动,有轻微症状和体征90分;勉强可进行正常活动,有一些症状或体征80分;生活可自理,但不能维持正常生活工作70分;生活能大部分自理,但偶尔需要别人帮助60分;常需人照料50分;生活不能自理,需要特别照顾和帮助40分;生活严重不能自理30分;病重,需要住院和积极的支持治疗20分;重危,临近死亡10分;死亡0分。得分越高,健康状况越好;得分越低,健康状况越差[6]。
1.4统计学方法
采用SPSS20.0统计学软件对数据进行处理,计量数据以均数±标准差(±s)表示,组间两两比较采用q检验;计数资料用Χ2检验,等级资料采用Ridit分析;生存分析采用Kaplan-Meier法进行检验。P<0.05为差异有统计学意义。
2 结果
2.1两组患者近期疗效比较
GP组CR、PR、SD和PD分别有1、18、11和2例,联合组则分别有3、24、5和1例,联合组明显优于GP组(P=0.0390),GP组的RR为59.38%,联合组的RR为81.82%,两组比较差异有统计学意义(P=0.0467)。见表2。

表2 两组患者近期疗效比较[n(%)]
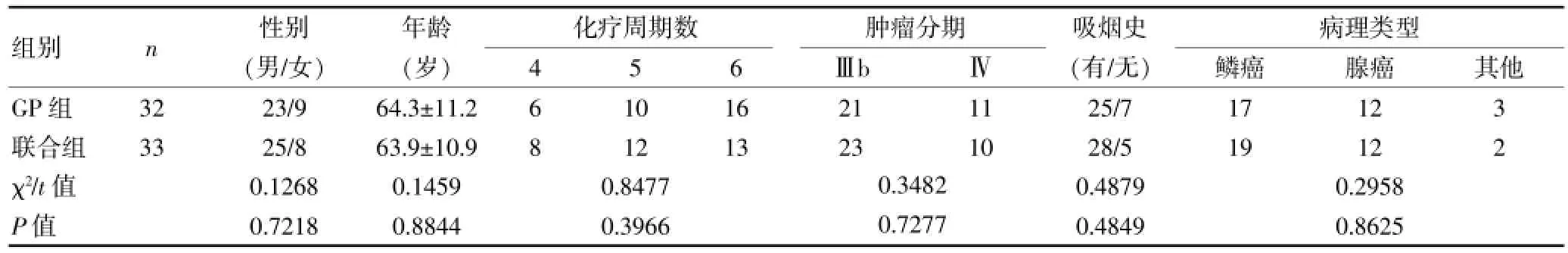
表1 两组患者的临床资料比较
2.2两组患者不良反应比较
两组均无化疗相关性死亡病例发生。两组在化疗后均有不同数量的患者出现白细胞减少、血小板减少、贫血、恶心呕吐和肝肾毒性等不良反应,但两组在不良反应方面比较差异无统计学意义。见表3。
2.3两组患者KPS评分比较
两组患者在化疗前KPS评分无明显差异[(80.95± 11.34)vs(80.42±10.75);t=0.1933,P=0.8474],化疗结束3个月后再次评估KPS评分发现GP组KPS评分为(85.74±10.97)分,较化疗前有所提高,但差异无统计学意义(t=1.9594,P=0.0546);化疗结束3个月后联合组KPS评分为(91.52±11.25)分,明显高于化疗前(t= 3.8013,P=0.0003)及GP组(t=2.0964,P=0.0401)。见表4。
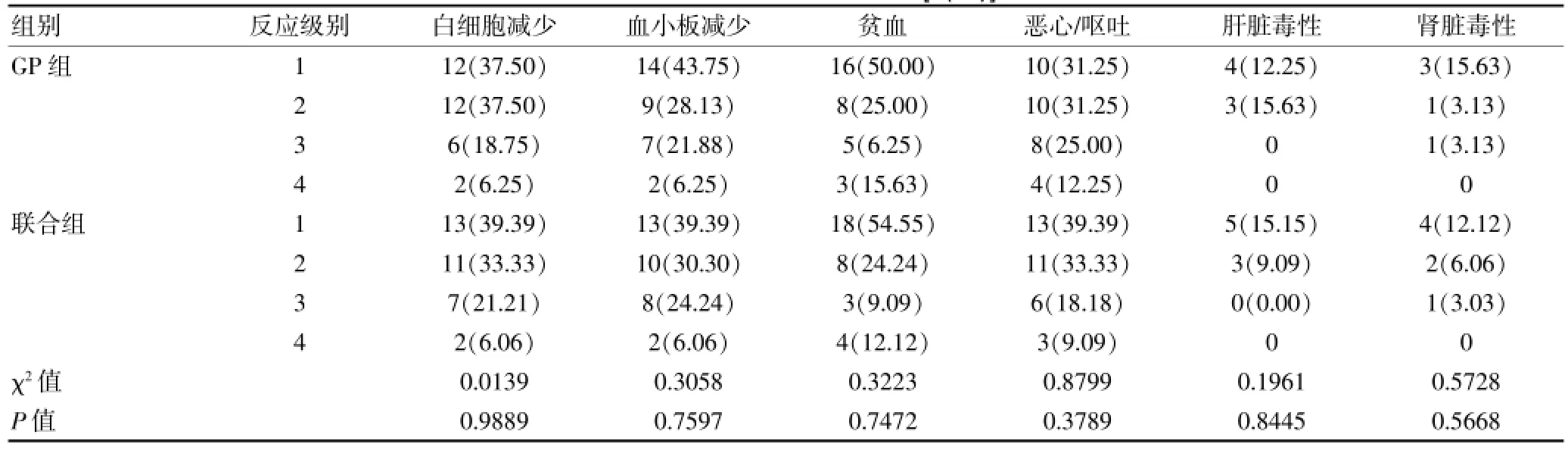
表3 两组患者不良反应的比较[n(%)]
表4 两组患者KPS评分比较(±s)
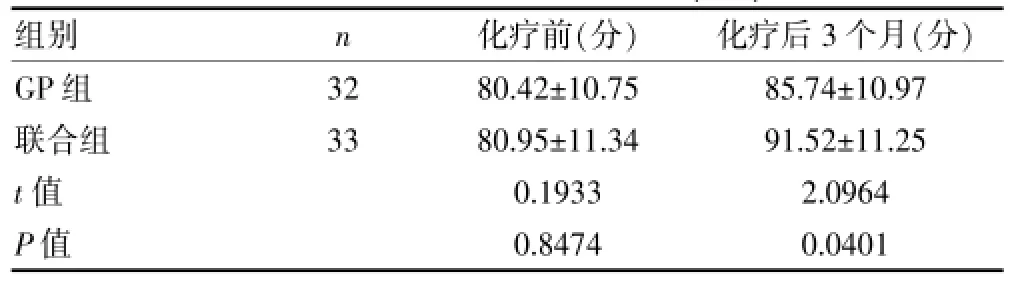
表4 两组患者KPS评分比较(±s)
组别 n 化疗前(分) 化疗后3个月(分)GP组联合组t值P值32 33 80.42±10.75 80.95±11.34 0.1933 0.8474 85.74±10.97 91.52±11.25 2.0964 0.0401
2.4两组患者3年生存率比较
GP组3年内有25例死亡,生存率为21.88%,而联合组3年内有24例死亡,生存率为27.27%,生存分析提示联合组3年生存率明显高于GP组(P=0.0425)。见图1。
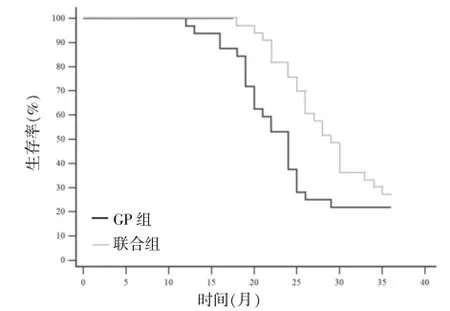
图1 两组患者3年生存率比较
3 讨论
由于对非小细胞肺癌的早期诊断很有难度,所以在确诊时一般已处于晚期,并可能已经发生了转移,无法通过手术进行根治性治疗,故化疗成为其最好的选择。但是迄今为止,单药化疗方案治疗有效率仅仅在40%~50%[7,8],即使多药联合的化疗方案有效率也仅在60%左右[9],均无法令人满意。自1971年“肿瘤血管生成”理论被提出来以后,肿瘤治疗研究热点逐渐转移到针对肿瘤新生血管的靶向化疗[10,11]。随后ECOG 4599研究证实,贝伐单抗联合化疗治疗6周期并维持至进展,能显著延长晚期非小细胞肺癌患者平均生存期,改善化疗疗效。贝伐单抗和血管内皮抑素已被公认为是当前最具代表性的抗肿瘤新生血管形成的靶向药物[12,13]。
重组人血管内皮抑素(恩度)是一款由我国自主研究发明的新型抗肿瘤新生血管形成的靶向药物,其羧基末端与细胞外基质胶原具有高度同源性,是一个多靶点血管内皮抑制剂。恩度能通过下调血管内皮细胞一氧化氮(NO)合成酶的激活、抑制VEGF介导的信号转导和bcl-2/bcl-XL、bad的表达及促进血管内皮细胞凋亡等多种途径阻断肿瘤新生血管的形成,从而使肿瘤处于乏血状态来起到抑制肿瘤细胞生长的作用。还有研究表明恩度能够显著下调骨桥蛋白的表达,进而诱导前基质金属蛋白酶(MMP)-2、基质金属蛋白酶(MMP)-9的表达下降,抑制肿瘤转移[14,15]。恩度作为血管内皮抑素,本身无细胞毒效应,但其与化疗药物具有良好的协同作用,体外实验结果显示,本品对人微血管内皮细胞株HHEC的迁移、Tube形成有抑制作用,并能明显抑制鸡胚尿囊膜血管生成,提示本品具有一定的体外抗血管生成作用[16-18]。体内实验结果显示,本品对鼠肿瘤模型(S180肉瘤、H22肝癌)、人异种移植肿瘤(SPC-A4肺腺癌、SGC7901胃癌、Hela宫颈癌、SMMC-7721和Bel7402肝癌)有抑瘤作用,并且在既往研究中恩度显示了对多种肿瘤均具有良好的疗效[19,20]。
本研究中,我们发现恩度联合GP方案化疗,可明显提高近期疗效,改善总有效率,3年生存率为27.27%明显高于GP组的21.88%(P=0.0425),且未增加不良反应的发生率。其主要作用机制可能是[21,22]:①抑制肺癌细胞的血管内皮生长因子表达,促进血管内皮细胞凋亡;②使肺癌新生血管有序化,促使化疗药物有效地进入肿瘤组织,增强化疗疗效;③减少肺癌的营养及氧的供应,抑制肿瘤的生长,从而有效控制肺癌的进展。
本研究通过探讨恩度联合GP方案化疗治疗晚期非小细胞肺癌的临床疗效,结果表明,联合治疗能显著提高化疗疗效、提高3年生存率,与单纯化疗比较差异显著,同时不增加不良反应发生率,因此恩度联合GP方案化疗治疗晚期非小细胞肺癌是一种安全高效的治疗方式,值得临床广泛应用。
[参考文献]
[1]Enders F,Geisenberger C,Jungk C,et al.Prognostic factors and long-term survival in surgically treated brain metastases from non-small cell lung cancer[J].Clinical Neurology and Neurosurgery,2016,142:72-80.
[2]Jin XR,Ye M,Cai ZZ,et al.Standardized transbronchial needle aspiration procedure for intrathoracic lymph node staging of non-small cell lung cancer[J].Journal of Thoracic Disease,2015,7(Suppl 4):S266-271.
[3]Shi Y,Sun Y.Medical management of lung cancer:Experience in China[J].Thoracic Cancer,2015,6(1):10-16.
[4]Zhang FL,Gao EY,Shu RB,et al.Human recombinant endostatin combined with cisplatin based doublets in treating patients with advanced NSCLC and evaluation by CT perfusion imaging[J].Asian Pacific Journal of Cancer Prevention:APJCP,2015,16(15):6765-6768.
[5]Zhou Y,Xie PM,Dong C,et al.Prospective clinical study of pre-operative SIB-IMRT in preparing surgical boundary of extremity soft tissue sarcoma[J].European Review for Medical and Pharmacological Sciences,2015,19(24):4738-4750.
[6]Nie X,Liu D,Li Q,et al.Predicting chemotherapy toxicity in older adults with lung cancer[J].Journal of Geriatric Oncology,2013,4(4):334-339.
[7]Engel J,Lategahn J,Rauh D.Hope and Disappointment:Covalent inhibitors to overcome drug resistance in nonsmall cell lung cancer[J].ACS Medicinal Chemistry Letters,2016,7(1):2-5.
[8]Miao J,Zhang W,Hu X,et al.Clinical evaluation of postoperative chemotherapy based on genetic testing in patients with stageⅢA non-small cell lung cancer[J].Thoracic Cancer,2016,7(1):44-49.
[9]Zhang Q,Qin N,Wang J,et al.Crizotinib versus platinum-based double-agent chemotherapy as the first line treatment in advanced anaplastic lymphoma kinase-positive lung adenocarcinoma[J].Thoracic Cancer,2016,7(1):3-8.
[10]Al-Husein B,Abdalla M,Trepte M,et al.Antiangiogenic therapy for cancer:An update[J].Pharmacotherapy,2012,32(12):1095-1111.
[11]Ahluwalia A,Jones MK,Matysiak-Budnik T,et al.VEGF andcoloncancergrowthbeyondangiogenesis:Does VEGF directly mediate colon cancer growth via a nonangiogenic mechanism?[J].Current Pharmaceutical Design,2014,20(7):1041-1044
[12]Yazdi MH,Faramarzi MA,Nikfar S,et al.A comprehensive review of clinical trials on EGFR inhibitors such as cetuximab and panitumumab as monotherapy and in combination for treatment of metastatic colorectal cancer[J]. Avicenna Journal of Medical Biotechnology,2015,7(4):134-144.
[13]Jiang X,Ding M,Qiao Y,et al.Recombinant human endostatin combined with radiotherapy in the treatment of brain metastases of non-small cell lung cancer[J].Clinical&Translational Oncology:Official Publication of the Federation of Spanish Oncology Societies and of the National Cancer Institute of Mexico,2014,16(7):630-636.
[14]Arjaans M,Schroder CP,Oosting SF,et al.VEGF pathway targeting agents,vessel normalization and tumor drug uptake:From bench to bedside[J].Oncotarget,2016.
[15]Jiang XD,Ding MH,Qiao Y,et al.Study on lung cancer cells expressing VEGFR2 and the impact on the effect of RHES combined with radiotherapy in the treatment of brain metastases[J].Clinical Lung Cancer,2014,15(2):e23-29.
[16]Bao Y,Peng F,Zhou QC,et al.Phase II trial of recombinant human endostatin in combination with concurrent chemoradiotherapy in patients with stage III non-smallcell lung cancer[J].Radiotherapy and Oncology:Journal of the European Society for Therapeutic Radiology and Oncology,2015,114(2):161-166.
[17]Jiang X,Guan W,Li M,et al.Endostatin combined with platinum-based chemo-radiotherapy for advanced nonsmall cell lung cancer[J].Cell Biochemistry and Biophysics,2015,71(2):571-577.
[18]Masters GA,Temin S,Azzoli CG,et al.Systemic therapy for stage IV non-small-cell lung cancer:American society of clinical oncology clinical practice guideline update[J]. Journal of Clinical Oncology:Official Journal of the American Society of Clinical Oncology,2015,33(30):3488-3515.
[19]Wang J,Xiao J,Wei X,et al.Circulating endothelial cells and tumor blood volume as predictors in lung cancer[J].Cancer Science,2013,104(4):445-452.
[20]Rong B,Yang S,Li W,et al.Systematic review and metaanalysis of Endostar(rh-endostatin)combined with chemotherapy versus chemotherapy alone for treating advanced non-small cell lung cancer[J].World Journal of Surgical Oncology,2012,10:170.
[21]Dingemans AM,Groen HJ,Herder GJ,et al.A randomized phase II study comparing paclitaxel-carboplatinbevacizumab with or without nitroglycerin patches in patients with stage IV nonsquamous nonsmall-cell lung cancer:NVALT12(NCT01171170)dagger[J].Annals of Oncology:Official Journal of the European Society for Medical Oncology/ESMO,2015,26(11):2286-2293.
[22]Sacco PC,Maione P,Rossi A,et al.New antiangiogenetic therapy beyond bevacizumab in the treatment of advanced non small cell lung cancer[J].Current Pharmaceutical Design,2015,21(32):4763-4772.
[中图分类号]R734.2
[文献标识码]B
[文章编号]1673-9701(2016)13-0105-04
[基金项目]国家自然青年基金资助项目(81501830)
收稿日期:(2016-01-22)
Effect of recombinant human endostain combined with chemotherapy on advanced non-small cell lung cancer
WANG JiabaoTANG ChengwuFENG Wenming
Department of Surgery,the First People's Hospital Affiliated to Huzhou University Medical College,Huzhou313000,China
[Abstract]Objective To investigate the effect of recombinant human endostain combined with chemotherapy on advanced non-small cell lung cancer.Methods Medical documents of 65 patients with advanced non-small cell lung cancer during May 2008 and May 2011were retrospectively reviewed.Patients were divided into GP group and combination group.In GP group,32 patients received Gemcitabine(1000 mg/m2on d1 and d8)and cisplatin(20 mg/m2d1-5)by intravenous injection.While in combination group,33 patients received additional recombinant human endostain (15 mg/d,d1-14)by intravenous injection concurrently with the same chemotherapy as GP group.Patients accepted chemotherapy every 3 weeks for 4-6 cycles.Short-term response rate,long-term survival,KPS score and adverse effects were compared.Results Significantly higher short-term response rate(P=0.0390)and RR(P=0.0467)were found in combination group.No chemotherapy-related death was observed.No significant difference was found in adverse effects between two groups.KPS score of combination group was significantly better than that of GP group(91.52±11.25 vs 85.74±10.97,P=0.0401).Combination group was found to have a significantly higher 3-year survival probability than GP group(27.27%vs 21.88%,P=0.0425).Conclusion The combination of recombinant human endostain and GP chemotherapy lead to a better short-term RR and a higher 3-year survival probability without increasing adverse effects.
[Key words]Non-small cell lung cancer;Chemotherapy;Recombinant human endostain;Survival probability

