野皂荚多糖胶与黄原胶复配增效作用研究
刘彦涛,李晓利,韩明会,孙达锋,张卫明,蒋建新*
(1. 北京林业大学 材料科学与技术学院,林业生物质材料与能源教育部工程研究中心,北京 100083;2. 南京野生植物综合利用研究院,江苏 南京 210042)
野皂荚多糖胶与黄原胶复配增效作用研究
刘彦涛1,李晓利1,韩明会1,孙达锋2,张卫明2,蒋建新1*
(1. 北京林业大学 材料科学与技术学院,林业生物质材料与能源教育部工程研究中心,北京 100083;2. 南京野生植物综合利用研究院,江苏 南京 210042)
摘要野皂荚多糖胶是一种从豆科皂荚属的灌木或小乔木野皂荚豆分离得到的半乳甘露聚糖胶,按照不同配比、浓度、温度、电解质种类配制野皂荚多糖胶与黄原胶的复配胶液,通过凝胶强度测定仪比较其复配胶液凝胶强度的变化情况。结果表明,野皂荚多糖胶和黄原胶通过分子间缠绕或者分子间次级键的相互作用使其形成凝胶,协同增效凝胶的最优工艺条件为:野皂荚多糖胶与黄原胶复配质量比为6∶4,总胶浓度2%,60 ℃水浴中加热30 min,凝胶强度达到100.5 g/cm2。加入氯化钾、氯化钠、磷酸二氢钾、氢氧化钾能显著提高复配胶液的凝胶强度。
关键词野皂荚多糖胶;黄原胶;复配胶液;凝胶强度
野皂荚豆胶又称胡里豆胶,来源于豆科皂荚属的灌木或者小乔木野皂荚豆的胚乳部分。野皂荚多糖胶属于半乳甘露聚糖大分子,其主链是由β-(1→4)-苷键连接的D-吡喃甘露糖组成,D-半乳糖以侧链形式通过α-(1→6)-苷键连接到主链中的甘露糖上[1-2]。野皂荚多糖胶与瓜尔多糖胶、胡卢巴多糖胶的性能相似,可作为增稠剂、稳定剂、粘合剂应用于石油、食品和纺织印染等行业。由于多糖胶精细结构上的差异,初步流变性质研究表明,野皂荚多糖胶能与黄原胶水溶液复配形成凝胶。
黄原胶是野油菜黄单孢菌分泌于胞外的中性水溶性多糖。由“五糖重复单元”构成的大分子多糖,每个单元由D-葡萄糖、D-甘露糖、D-葡萄糖醛酸、乙酸以及丙酮酸相互连接而成。它是水溶性生物高分子聚合物,其微观结构中侧链与主链间通过氢键结合形成双螺旋结构,并以多重螺旋聚合体状态存在,侧链葡萄糖醛酸基带负电荷[3]。尽管黄原胶溶液可以产生很高的特性粘度,呈现弱凝胶的性质,但是在任意浓度和温度下黄原胶均不能形成真正的凝胶等[4],但是在黄原胶中加入其它物质,利用复配胶的协同增效作用,其凝胶强度将会有很大的改善[5]。黄原胶能使多糖胶具有好的凝胶强度,这样不但使得产品有较好的强度,弹性,使成型后的产品不易变形,外观美观,表面柔滑而有光泽,而且也具更好的口感[6]。电解质对黄原胶流变性质影响以及黄原胶与多糖胶的复配研究已有较多报道[7-8],而很少有关野皂荚多糖胶与黄原胶的复配研究。野皂荚多糖胶林业行业标准(LY/T 2390—2014)于2014年12月正式实施,本文重点研究了不同配比、浓度、加热温度、水合时间以及电解质等加入量等条件下凝胶强度的变化,以期为野皂荚多糖胶与黄原胶复配胶体在食品工业上的应用提供参考依据。
1材料与方法
1.1材料与试剂
野皂荚多糖胶由河北涉县羟乙基龙胶厂提供,黄原胶为市售食品级,其余试剂如乙醇、KCl、NaCl、KOH、KH2PO4等均为分析纯。
1.2仪器与设备
冻力凝胶强度测定仪(JS-Ⅱ,天津市旭阳仪器设备有限公司),分析天平(上海分析仪器公司),恒温磁力搅拌器(江苏省金坛市美特仪器制造有限公司),机械搅拌器(上海飞云生物科技有限公司)等。
1.3实验方法
1.3.1复配胶液的配制方法
按照配方称取一定量的野皂荚多糖胶与黄原胶胶粉,加入2 mL无水乙醇使其充分分散,混合均匀后,加入定量的去离子水,恒温磁力搅拌水合,30 min后,分装小瓶,用保鲜膜封口,置于4 ℃冰箱中冷藏并静置24 h,使其凝胶强度稳定[9]。
1.3.2凝胶强度的测定方法
采用JS-II型冻力测定仪测定凝胶强度,首先要开机预热30 min,深度设置为10 mm,速度设置2 mm/s,模式设置保持。冻力凝胶强度值调零,将试样放置在测试圆盘上,并调整测试圆盘的高度,按启动键开始测试,读取凝胶强度值。
1.3.3野皂荚多糖胶与黄原胶凝胶不同质量比的复配胶液凝胶强度
以野皂荚多糖胶与黄原胶质量比为10∶0,9∶1,8∶2,7∶3,6∶4,5∶5,4∶6配成1%和2%的溶液,在60 ℃的水浴中加热30 min,取出并分别移入3个冻力瓶中,做3个平行,并迅速用冷水冷却,在4 ℃冰箱中放置24 h,用冻力测定仪测定其凝胶强度[10-11]。
1.3.4浓度对野皂荚多糖胶与黄原胶复配胶液凝胶强度的影响
按照最优质量比分别配制0.5%、1%、1.5%、2%、2.5%、3%浓度的复配胶液,在60 ℃的水浴中加热30 min,取出倒入3个测试瓶中,用冷水冷却,在4℃冰箱中放置24 h,测定其凝胶强度。
1.3.5温度对野皂荚多糖胶与黄原胶复配胶液凝胶强度的影响
按照最优质量比配制2%的复配胶液,机械搅拌水合均匀,分别在50 ℃、60 ℃、70 ℃、80 ℃的条件下加热30 min,取出分装在3个测试瓶中,然后在冷水中迅速冷却,在4 ℃冰箱中放置24 h,测定其凝胶强度。
1.3.6电解质及非盐类物质对野皂荚多糖胶与黄原胶复配胶液凝胶强度的影响
以最优质量比配制2%的复配胶液,在胶液中分别加入0.3%的氯化钾、氯化钠、氢氧化钾、氢氧化钠、磷酸二氢钾、磷酸二氢钠、柠檬酸钠、蔗糖。机械搅拌水合均匀,在60 ℃水浴中加热30 min,取出分装在3个测试瓶中,冷水中迅速冷却,在4 ℃冰箱中放置24 h,测定其凝胶强度[12]。
以最优质量比配成2%的复配胶液,在胶液中分别加入0.1%、0.3%、0.5%的电解质等,机械搅拌水合均匀,在60 ℃水浴中加热30 min,取出分装在3个冻力瓶中,冷水中迅速冷却,在4 ℃冰箱中放置24 h,测定其凝胶强度。
2结果与分析
2.1野皂荚多糖胶与黄原胶不同质量比复配胶液的凝胶强度
野皂荚多糖胶与黄原胶复配胶液的凝胶强度随着黄原胶的加入量的增加逐渐增大,当凝胶强度达到最大值时,继续增加黄原胶的比例,其凝胶强度反而呈下降趋势。原因是黄原胶属于双螺旋状的结构,随着黄原胶加入量的增加,其所占比例的增加,这样由于分子间缠绕或者分子次级键的相互作用使凝胶强度得到提高。然而,当分子缠绕达到饱和后,继续增加黄原胶所占比例,分子之间不仅不会再相互缠绕,反而因为自身带有负电荷而相互排斥,这样使得分子之间的距离增大,分子之间次级键的作用力减弱,从而使凝胶强度有所下降。图1表明,野皂荚多糖胶与黄原胶的最优复配质量比是6∶4,其中,2%浓度的复配胶液的最大凝胶强度达到100.5 g/cm2。
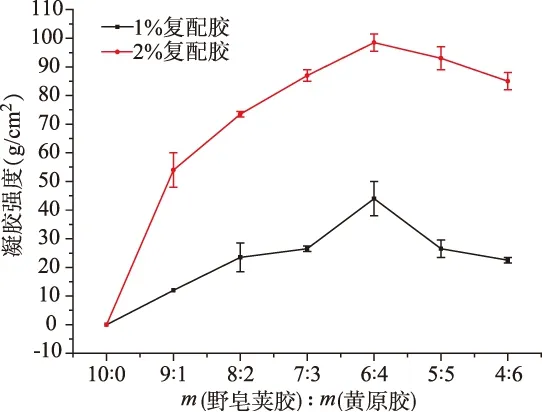
图1 野皂荚多糖胶与黄原胶不同质量
2.2浓度对野皂荚多糖胶与黄原胶复配胶液凝胶强度的影响
随着野皂荚多糖胶与黄原胶复配胶液浓度的增加,其凝胶强度逐渐增大。原因是随着复配胶液浓度的增加,其结合水的能力增加,单个分子的体积会增大,从而分子与分子之间形成更加紧密的网状结构,使其凝胶强度不断增加。但是在一定的振荡力下,高浓度的凝胶更容易发生断裂。因此,较优的复配胶液浓度为1.5%~2.5%(图2)。
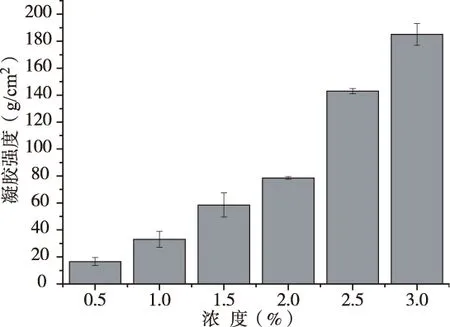
图2 浓度对野皂荚多糖胶与黄原胶复配胶液
2.3温度对野皂荚多糖胶与黄原胶复配胶液凝胶强度的影响
在2%胶液浓度下,随着温度的升高,复配胶液的凝胶强度逐渐下降(图3)。原因是随着溶液温度的提高,胶粒分子之间运动加剧,黄原胶分子的构象发生转变,由原来有序的双螺旋结构变成一种无序的状态,这样使其主链暴露在外边,主链上键活性比较小,这样与其他分子的结合的机会就会减少。另外,在高温条件下,黄原胶会与溶液中的溶解氧发生自由基氧化还原反应,使其在高温条件下降解,进一步减少了与其它分子结合的机会,从而使得其凝胶强度下降[13]。因为氧是黄原胶发生自由基氧化还原反应的主要原因,因此加入抗氧剂可提高黄原胶的热稳定性[14]。实验还表明,当胶液浓度低于1.5%时,复配胶液在低于60 ℃时不能形成稳定的凝胶(数据未给出)[15],因此以下实验选用的复配胶液温度为60 ℃。
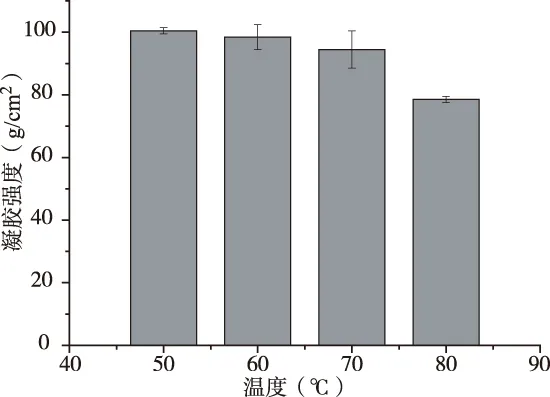
图3 温度对野皂荚多糖胶与黄原胶复配胶液
2.4电解质及非盐物质对野皂荚多糖胶与黄原胶复配胶液凝胶强度的影响
复配胶液中加入氯化钾、氯化钠、磷酸二氢钾、氢氧化钾对其凝胶强度有明显提高,加入柠檬酸钠、蔗糖、磷酸二氢钠后,其凝胶强度虽然有所提高,但是效果不显著,加入氢氧化钠后,其凝胶强度反而有所下降(图4)。原因可能是加入氯化钾、氯化钠、磷酸二氢钾、氢氧化钾后降低了黄原胶三糖侧链上的羧基阴离子之间的静电排斥作用,使黄原胶的结构从无序状态变成有规则的螺旋状结构,加入电解质,使得侧链间的静电排斥作用降低,使得侧链和氢键盘绕在野皂荚多糖胶骨架上,从而增加了分子之间的胶连情况,稳定了黄原胶的规则构象,分子间更容易积聚,进而提高了凝胶强度[16-17]。氢氧化钠在加入后会局部受热不均匀,从而导致其凝胶强度有所下降。
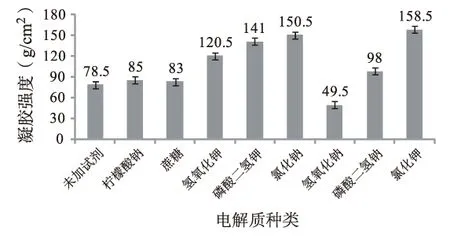
图4电解质及非盐物质对野皂荚多糖胶
随着氯化钾、氯化钠加入量的增加,复配胶液的凝胶强度有所提高(图5)。盐作为一种强电解质,水中解离出阴阳离子,对黄原胶分子与水分子之间的相互作用产生一定的影响。另外,随着加入的试剂浓度的增加,高浓度的盐能够增加溶液的渗透压,这样黄原胶分子会吸附盐中的离子,使得黄原胶分子颗粒在一定程度上被伸展,使其体积增大,增加黄原胶与分子结合的机会,从而使其强度在一定程度上有所提高[18]。然而随着磷酸二氢钾、氢氧化钾加入量的增加,复配胶液的凝胶强度有所下降。
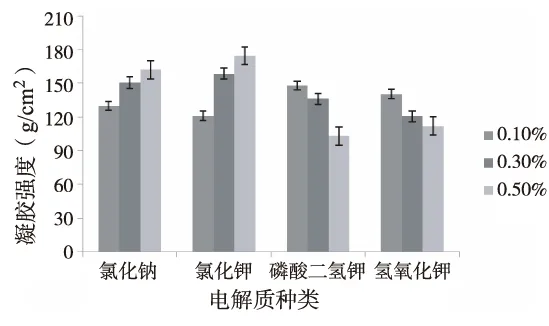
图5 试剂添加量对野皂荚多糖胶与黄原胶复配
3结论
(1)将野皂荚多糖胶与黄原胶分别以不同质量比共混配制成胶液,其凝胶强度随着黄原胶所占比例增加逐渐增大,当凝胶强度达到最大值,再继续增加黄原胶的比例时,其凝胶强度反而降低。野皂荚多糖胶与黄原胶最佳复配质量比为6∶4,在50 ℃下,2%浓度的复配胶液最大凝胶强度达到100.5 g/cm2。
(2)随着野皂荚多糖胶与黄原胶复配胶液浓度的增加,其凝胶强度逐渐增大,较优的复配胶液浓度为1.5%~2.5%。随着温度的升高,复配胶液的凝胶强度逐渐下降;温度低于60 ℃时,低浓度的复配胶不能形成凝胶。
(3)野皂荚多糖胶与黄原胶复配胶液中添加一定量的氯化钾、氯化钠、磷酸氢二钾、氢氧化钾等试剂能明显改变复配胶液的凝胶强度,氯化钾、氯化钠的添加与凝胶强度是正相关,磷酸二氢钠、氢氧化钾的添加与凝胶强度是负相关,而柠檬酸钠、蔗糖、磷酸二氢钠等的添加对凝胶强度影响不明显。
参考文献:
[1]蒋建新,菅红磊,张卫明,等. 野皂荚胚乳细胞多糖胶破壁释放过程研究[J] . 北京林业大学学报, 2009,31 (S1):71-76.
[2]蒋建新,朱莉伟,徐嘉生. 野皂荚豆胶的研究[J]. 林产化学与工业,2000,20(4):59-62.
[3]何飞燕,林华. 黄原胶结构、性能以及在食品加工中的应用[J]. 广西职业技术学院学报,2009,2 (5):1-4.
[4]胡建国,赵玲,戴干策. 黄原胶水溶液的流变性能[J]. 华东理工大学学报(自然科学版),2011,37(1):16-19.
[5]黄来发,洪文生. 食品增稠剂 [M]. 北京:中国轻工业出版社,2000:238-244.
[6]于保淼,徐焱春,熊洪录,等. 以黄原胶为改良剂的复配胶魔芋豆腐的制备[J]. 食品科技,2014,39(01):65-69.
[7]王元兰,李忠海,魏玉. 电解质及非电解质对κ-卡拉胶凝胶强度的影响研究[J]. 食品科技,2009,34(3):220-222.
[9]宁应之,杨永利,李春,等. 皂荚胶与黄原胶复配胶的流变性研究[J]. 食品科学,2005,26(12):34-36.
[10]朱慧,吴伟都,潘永明,等. 黄原胶与阴离子瓜尔胶复配溶液的流变特性研究[J]. 中国食品学报,2014,14(5):55-62.
[11]张雅媛,洪雁,顾正彪,等. 玉米淀粉与黄原胶复配体系流变和凝胶特性分析[J]. 农业工程学报,2011,27(9):357-362.
[12]朱姝宾,李龙伟,王念祥,等. 黄原胶与结冷胶复配在面条加工中的应用研究[J]. 湖南农业科学,2010(19):92-94.
[13]杨永利,丁兰,张继,等.槐豆胶及与黄原胶复配胶耐盐稳定性研究[J]. 西北师范大学学报(自然科学版),2001,37(2):70-72.
[14]刘波,李丹丹,李汴生,等. 软糖用κ-卡拉胶与明胶溶液及其复配液的表观粘度研究[J]. 现代食品科技,2012,28(11):1466-1470.
[15]吴乐,徐同台,潘小镛. 黄原胶高温稳定性的影响因素[J]. 钻井液与完井2011,28(6):77-80.
[16]雷鸣,卢晓黎,陈正纲,等. 黄原胶在低浓度时的流变特性及影响因素研究[J]. 食品科学,2000,21(12):16-18.
[17]黄金城,颜梦婷,曾华斌,等. 盐对玉米淀粉-黄原胶复配体系的影响[J]. 农产品加工(学刊),2013,(7):22-24.
[18]李言郡,朱慧,吴伟都,等. 一价阳离子对黄原胶溶液流变特性的影响研究[J]. 中国食品添加剂,2012(3):77-81.
[19]蔡旭冉,顾正彪,洪雁,等. 盐对马铃薯淀粉及马铃薯淀粉-黄原胶复配体系特性的影响[J]. 食品科学,2012,33(9):1-5.
Synergistic Gel Strength betweenGleditsiamicrophyllaPolysaccharide and Xanthan Gum
Liu Yantao1, Li Xiaoli1, Han Minghui1, Sun Dafeng2, Zhang Weiming2, Jiang Jianxin1*
(1.College of Material Science and Technology, MOE Engineering Research Center of Forestry Biomass Materials and Bioenergy, Beijing Forestry University, Beijing 100083, China;2. Nanjing Institute for Comprehensive Utilization of Wild Plants, Nanjing 210042, China)
AbstractGleditsiamicrophyllapolysaccharide gum is a kind of galactomannan gum extracted from the seeds ofGleditsiamicrophyllabean. Prepared complex gums ofGleditsiamicrophyllapolysaccharide gum and xanthan gum by the ratio, concentration, temperature, cation type and amounts of different cation, Synergistic gel strength changes of complex gums were observed by synergistic gel tester. Results were as follows:Gleditsiamicrophyllapolysaccharide gum and xanthan gum formed gel by the intermolecular entanglement or intermolecular interactions, and the optimization conditions for synergistic gel was: the complex ratio ofGleditsiamicrophyllapolysaccharide gum and xanthan gum 6∶4(m/m); total gum concentration 2%; water bath for 30 min at 60 ℃; the synergistic gel strength reached 100.5 g/cm2. Potassium chloride, sodium chloride, potassium dihydrogen phosphate, potassium hydroxide can significantly increase the synergistic gel strength of complex gums.
Key wordsGleditsiamicrophyllapolysaccharide; xanthan gum; complex gums; synergistic gel strength
doi:10.3969/j.issn.1006-9690.2016.03.003
收稿日期:2015-11-18
基金项目:国家自然科学基金项目(31270624);大学生创新计划(201510022034);“十二五”国家科技支撑计划课题(2012BAD36B01)。
作者简介:刘彦涛(1991—), 男, 硕士研究生,主要从事多糖利用研究。 *通讯作者:蒋建新,教授,博士生导师,研究领域为林产化工及生物质能源。E-mail:jiangjx@bjfu.edu.cn
中图分类号:TQ432.9
文献标识码:A
文章编号:1006-9690(2016)03-0004-04

